Похожие презентации:
Основы органической химии, углеводороды
1.
2.
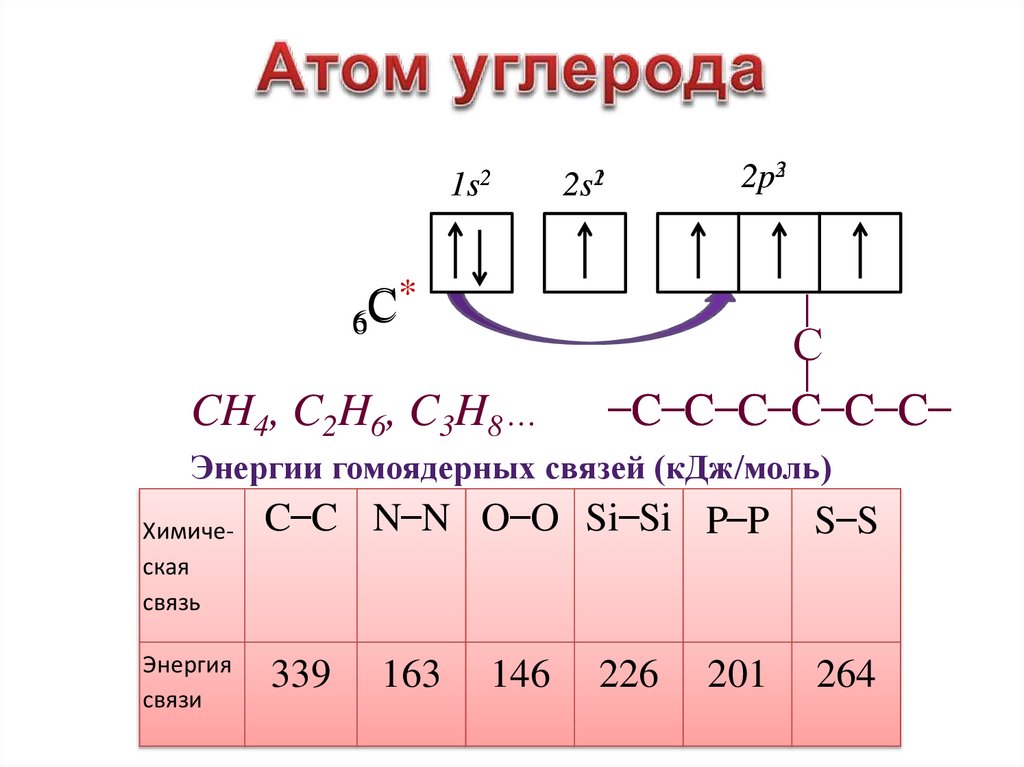
1s2*
С
6
CH4, C2H6, C3H8…
2p32
2s12
С
̶C̶C̶C̶C̶C̶C̶
Энергии гомоядерных связей (кДж/моль)
Химическая
связь
Энергия
связи
C ̶ C N ̶ N O ̶ O Si ̶ Si P ̶ P
S̶S
339
264
163
146
226
201
3.
Органическая химия изучает углеводороды и ихфункциональные производные.
Углеводороды (гидриды углерода) – сложные
вещества, состоящие только из атомов углерода и
водорода.
СCl
СН44
тетрахлорметан
метан
Cl
Cl
Cl
Cl
Путем замещения Н- и С-атомов на другие атомы или
группы атомов из углеводородов можно получить любое
органическое производное.
4.
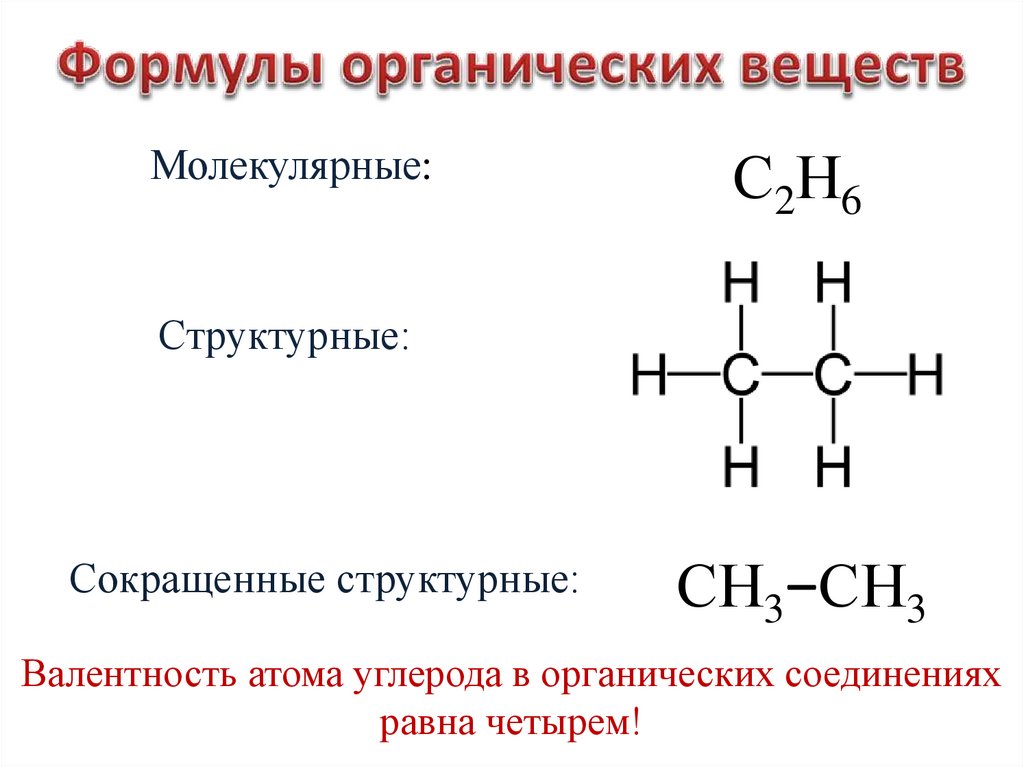
Молекулярные:С 2Н 6
Структурные:
Сокращенные структурные:
СН3−СН3
Валентность атома углерода в органических соединениях
равна четырем!
5.
1. Атомы в молекулах соединены между собой в определенномпорядке теории
химическими
связями
согласно
их валентности.
Следствие
строения:
каждое
органическое
соединение
2. Свойства
определяются
не только
качественным и
должно
иметьвещества
только одну
структурную
формулу.
количественным
составом, но веществ
и его строением,
а также
Изомерия
–
существование
с
одинаковым
взаимным влиянием
атомов.но обладающих различными
молекулярным
составом,
свойствами.
3. Строение молекул может быть установлено на основе
изучения их химических свойств.
С8Н18
СН3−СН2−СН2−СН 2−СН2−СН2−СН 2−СН3
н-октан
СН3
СН3− С− СН2 − СН − СН3
СН3
изооктан
СН3
6.
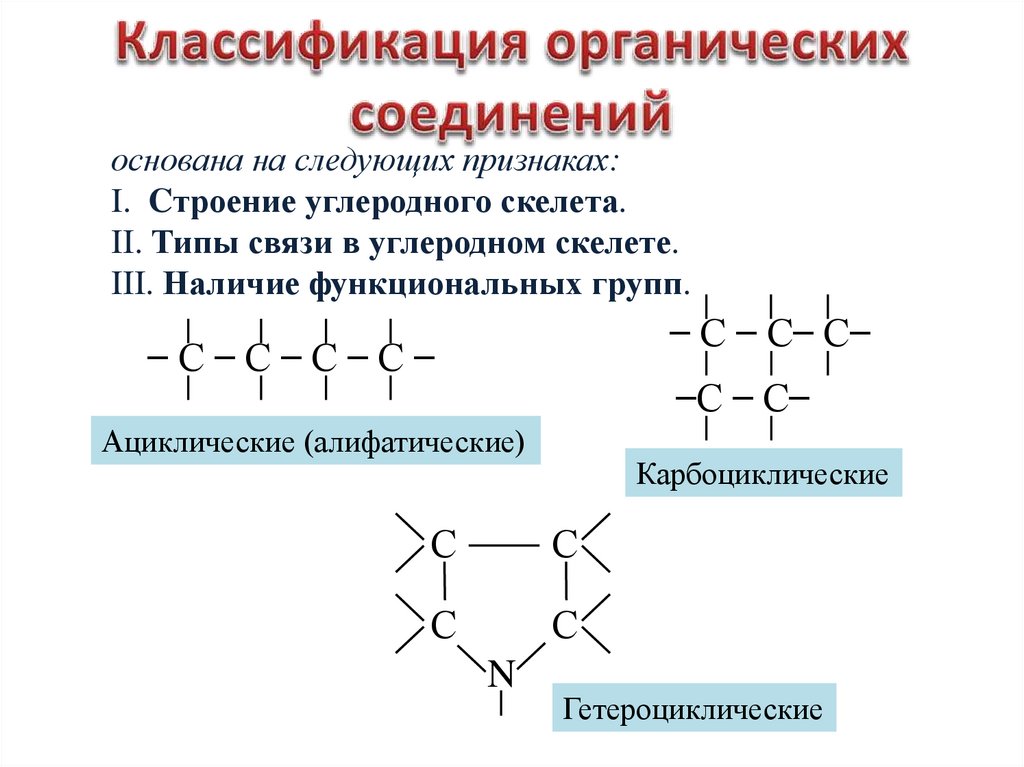
основана на следующих признаках:I. Cтроение углеродного скелета.
II. Типы связи в углеродном скелете.
III. Наличие функциональных групп.
̶ С ̶ С̶ С̶
̶ С ̶ С ̶ С ̶ С ̶
̶С ̶ С̶
Ациклические (алифатические)
Карбоциклические
С
С
С
С
N
Гетероциклические
7.
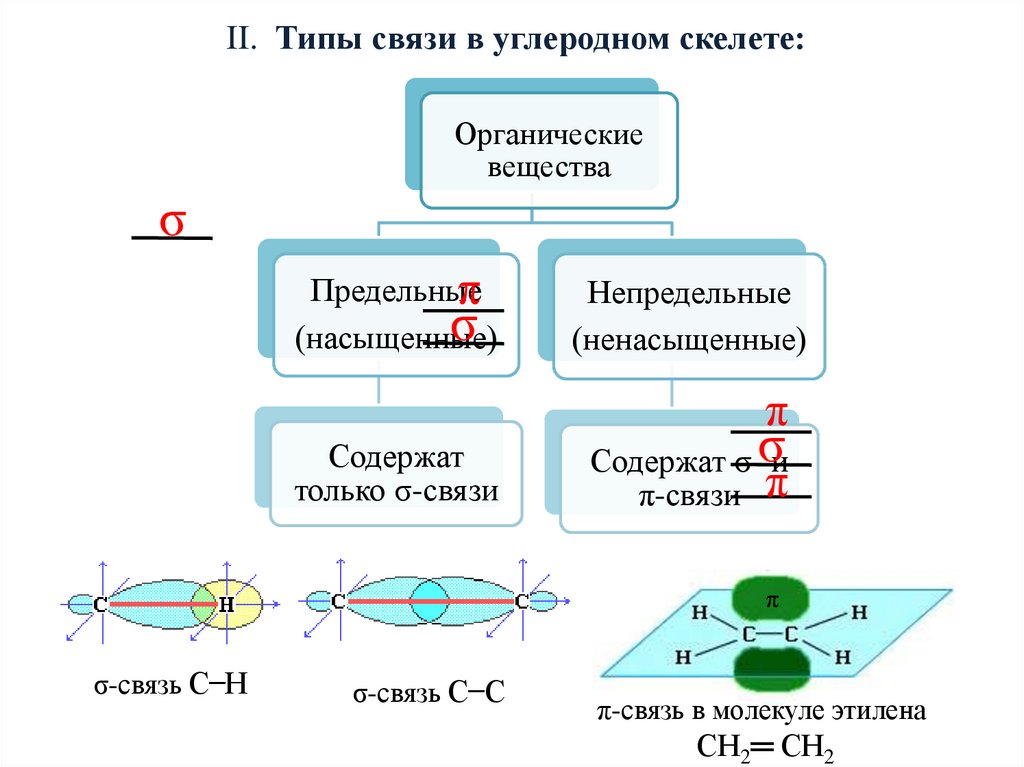
II. Типы связи в углеродном скелете:Органические
вещества
σ
Предельные
π
σ
(насыщенные)
Непредельные
(ненасыщенные)
π
Содержат
только σ-связи
Содержат σ-σи
π-связи π
π
σ-связь С ̶ Н
σ-связь С ̶ С
π-связь в молекуле этилена
СН2═ СН2
8.
III. Наличие функциональных группФункциональная группа – это атом или группа
атомов
неуглеводородного
характера,
которые
определяют химические свойства и принадлежность
соединения к определенному классу.
Углеводородный радикал R–частица с неспаренным
электроном, например СН3 ̶ метил, С2Н5 ̶ этил и т. д.
9.
Функциональнаягруппа
Название класса
Общая формула
класса, примеры
Hal-(F-,Cl-,Br-,I-)
Галоген
Галогенпроизводные
R ̶ Hal
̶ OH
Гидроксильная
Спирты, фенолы
R ̶ OH
O
С=O
Альдегиды
R̶C
H
Карбонильная
Кетоны
R ̶ C ̶ R’
O
O
̶C
OH
Карбоксильная
O
Карбоновые кислоты
R̶C
OH
10.
Гомологи метана CnH2n+2Название
алкана
CH
образуют
4
соединения, сходные по строению и 1.Метан
свойствам,
но
количеством групп -СН2-. 2.Этан
Отдельные
СН3 отличающиеся
– СН3
представители такого ряда называются «гомологами».
СН3 – СН2 – СН3
3. Пропан
СН3– СН2 – СН2 –СН3
4. Бутан
СН3– СН2 – СН2 – СН2 – СН3
5. Пентан
СН3– СН2 – СН2 – СН2 – СН2 – СН3
6. Гексан
СН3– СН2 – СН2 – СН2 – СН2 – СН2 – СН3
7. Гептан
СН3– СН2 – СН2 – СН2 – СН2 – СН2 – СН2 – СН3
8. Октан
СН3– СН2 – СН2 – СН2 – СН2 – СН2 – СН2 – СН2 – СН3
9. Нонан
СН3– СН2 – СН2 – СН2 – СН2 – СН2 – СН2 – СН2 – СН2 – СН3
10. Декан
11.
По правилам заместительной номенклатуры ИЮПАК молекулыорганического соединения рассматриваются как продукты замещения
атомов Н в молекулах углеводородов на другие атомы или группы
(заместители). Названия выражают с помощью сложных слов,
включающих:
1) обозначение основных углеродных цепей Сn: С1 – мет, С2 – эт,
С3 – проп, и т. д.;
2) обозначение боковых цепей –углеводородных радикалов с
помощью суффикса -ил- (метил, этил, пропил, бензил и др.);
3) обозначение характера связи между атомами: ан – ординарная,
ен – двойная, ин – тройная;
4) обозначение характеристических групп с помощью приставок или
суффиксов (окси или ол – ОН);
5) умножающие приставки –ди, – три, –тетра, –пента и т. д.;
6) локанты – цифры или буквы;
7) разделительные знаки – дефисы, запятые, скобки.
Одно название соответствует только одной формуле!
12.
СН3СН2= С − СН = СН2
СН3− С− СН2 − СН − СН3
СН3
СН3
СН3
изооктан
изопрен
2 –метилбутадиен-1,3
2,2,4 -триметилпентан
СН2 − СН2
ОН
ОН
этиленгликоль
этандиол-1,2
13.
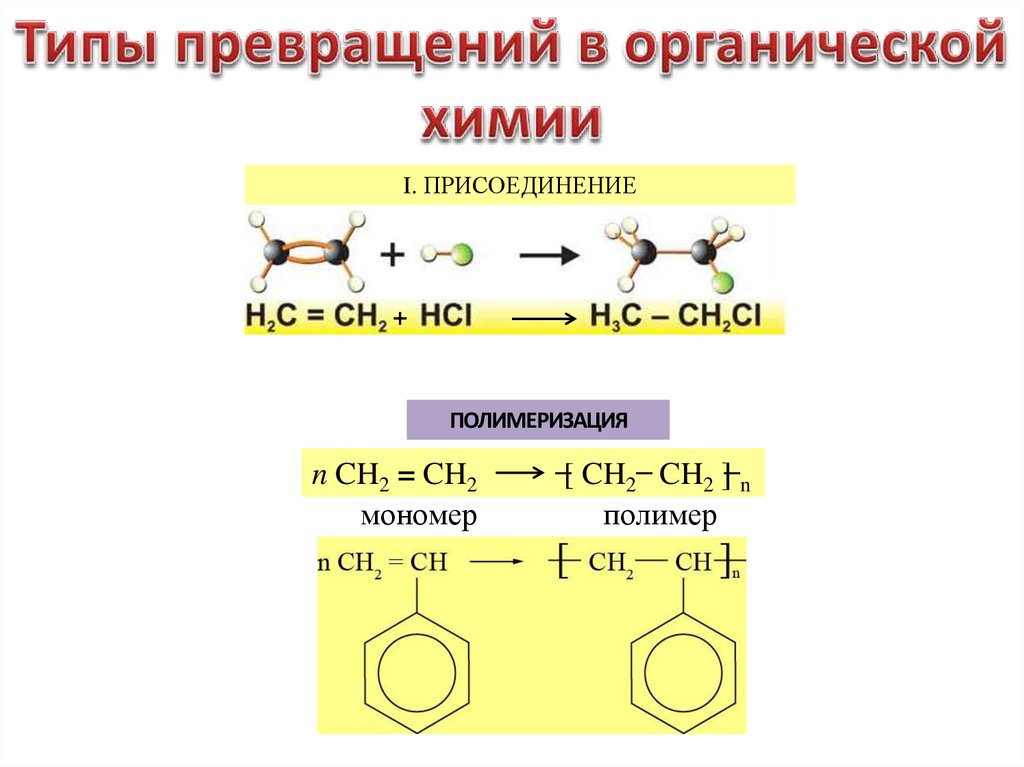
I. ПРИСОЕДИНЕНИЕ+
ПОЛИМЕРИЗАЦИЯ
n CH2 = CH2
мономер
̶[ CH2 ̶ CH2 ]̶ n
полимер
14.
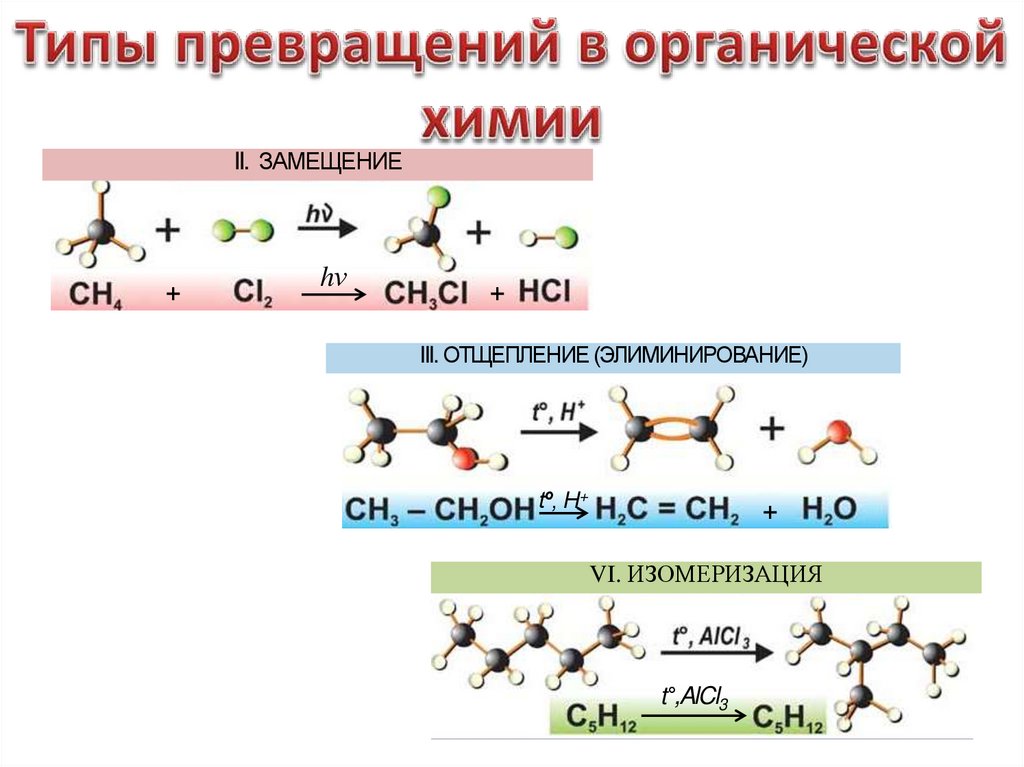
II. ЗАМЕЩЕНИЕ+
hν
+
III. ОТЩЕПЛЕНИЕ (ЭЛИМИНИРОВАНИЕ)
tº, H+
+
VI. ИЗОМЕРИЗАЦИЯ
t°,AlCl3
15.
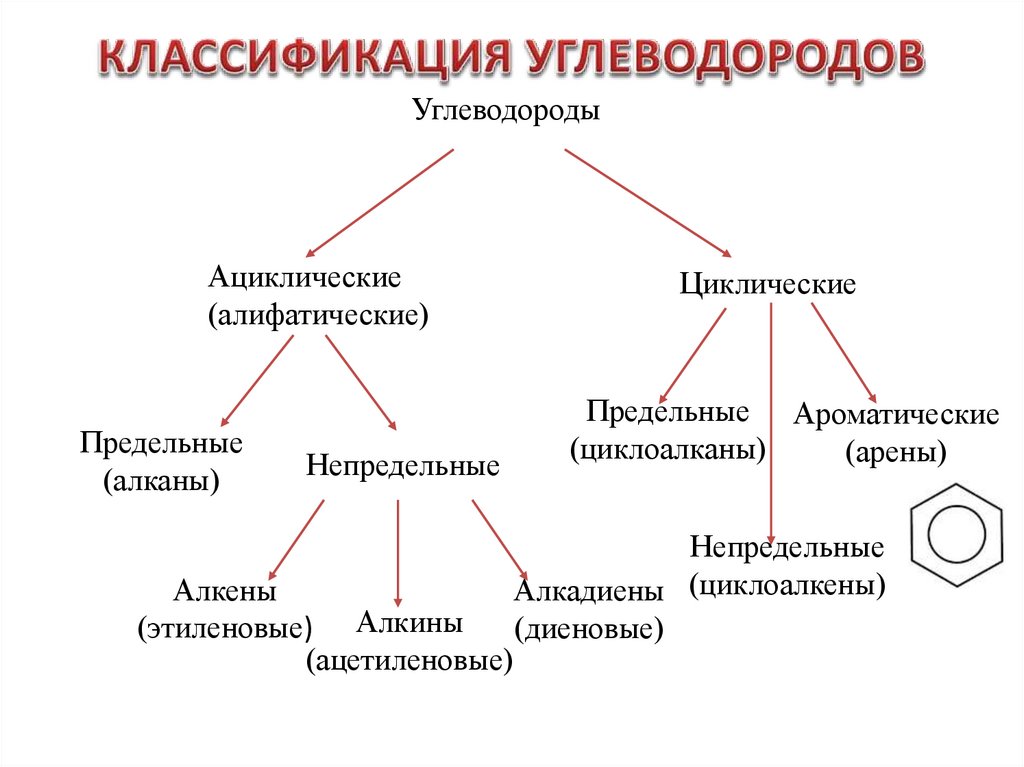
УглеводородыАциклические
(алифатические)
Предельные
(алканы)
Непредельные
Алкены
(этиленовые) Алкины
(ацетиленовые)
Циклические
Предельные Ароматические
(циклоалканы)
(арены)
Непредельные
Алкадиены (циклоалкены)
(диеновые)
16.
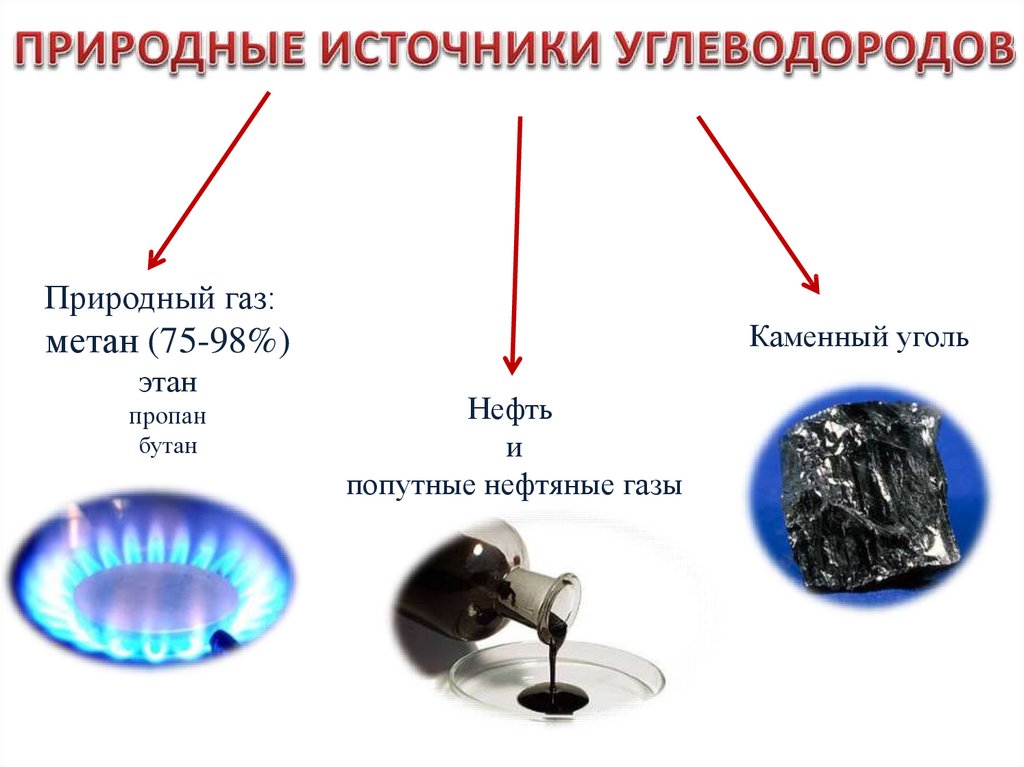
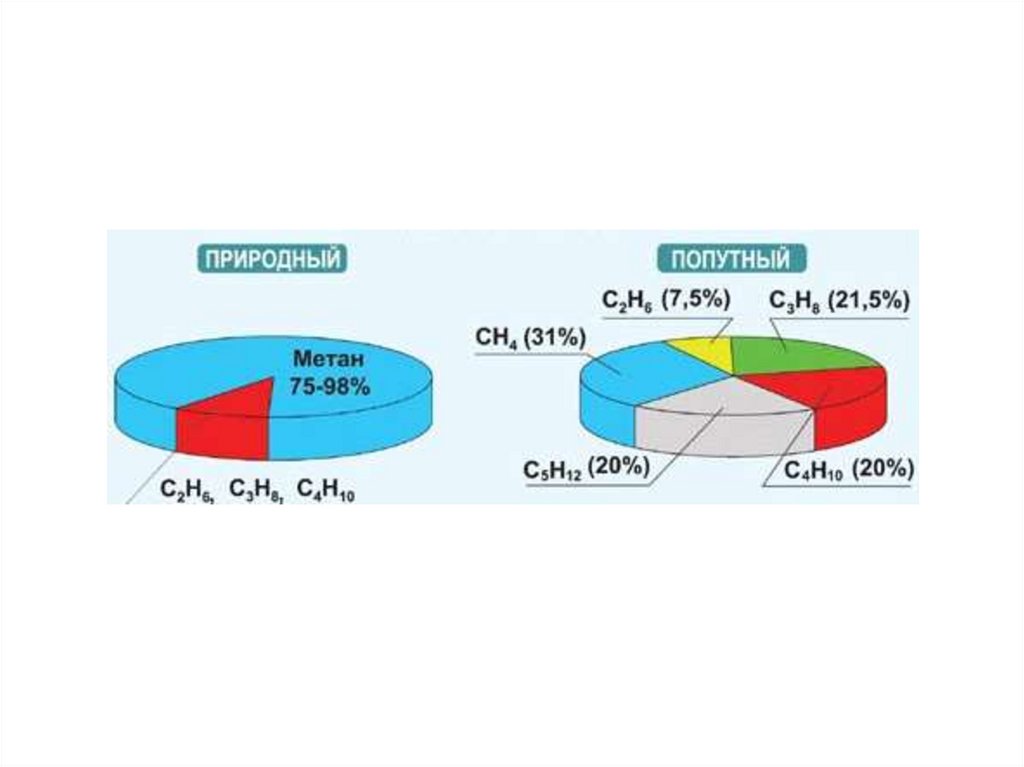
Природный газ:Каменный уголь
метан (75-98%)
этан
пропан
бутан
Нефть
и
попутные нефтяные газы
17.
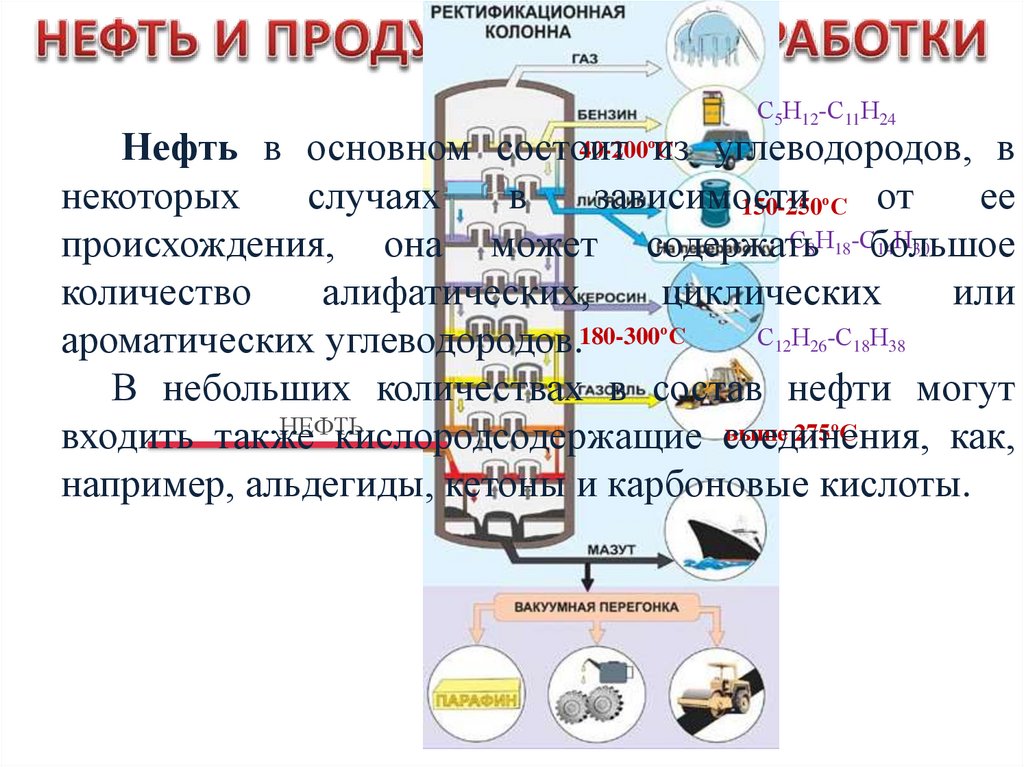
С5Н12-С11Н2440-200ºС
Нефть в основном состоит
из углеводородов, в
некоторых
случаях
в
зависимости
ее
150-250ºС от
С8Н18-Сбольшое
14Н30
происхождения, она может содержать
количество
алифатических,
циклических
или
С12Н26-С18Н38
ароматических углеводородов.180-300ºС
В небольших количествах в состав нефти могут
НЕФТЬ
выше 275ºС
входить также
кислородсодержащие соединения,
как,
например, альдегиды, кетоны и карбоновые кислоты.
18.
19.
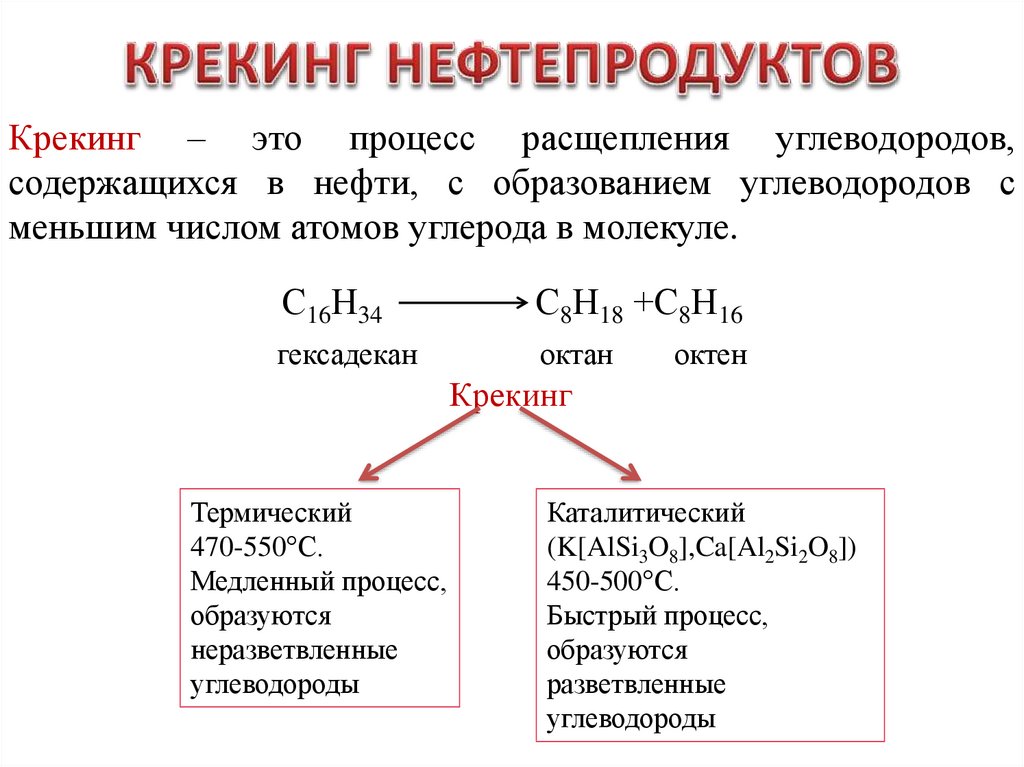
Крекинг – это процесс расщепления углеводородов,содержащихся в нефти, с образованием углеводородов с
меньшим числом атомов углерода в молекуле.
С16Н34
С8Н18 +С8Н16
гексадекан
октан
октен
Крекинг
Термический
470-550°С.
Медленный процесс,
образуются
неразветвленные
углеводороды
Каталитический
(K[AlSi3O8],Ca[Al2Si2O8])
450-500°С.
Быстрый процесс,
образуются
разветвленные
углеводороды
20.
Октановое числоОктановое число – Название
процентное содержание
изооктана в смеси с
углеводорода
н-гептаном, которая по своим антидетонационным свойствам
н-Бутан
91,0
эквивалентна испытуемому
бензину.
Изобутан
99,0
Гептан нормального строения: СН3 – (СН2)5 – СН3
н-Пентан
61,7
Октановое число - 0
Пентен-1
77,1
2-Метилбутан
90,3
СН3
2,2,3-Триметилбутан
101,0
− СН − СН3
2-Метилбутен-1 СН3− С− СН281,9
2-Метилбутен-2
СН3
СН3
84,7
Изооктан 111,6
Октановое
число - разветвление
100
Повышению октанового числа
способствуют
цепи,
наличие двойной связи и появление ароматического кольца, а также
введение антидетонационных добавок: СН3–О–С(СН3)3, Pb(C2H5)4,
Fe(C2H5)2, Mn(CO)3(C2H5), [Ni(CO)(C2H5)]2.
Бензол
21.
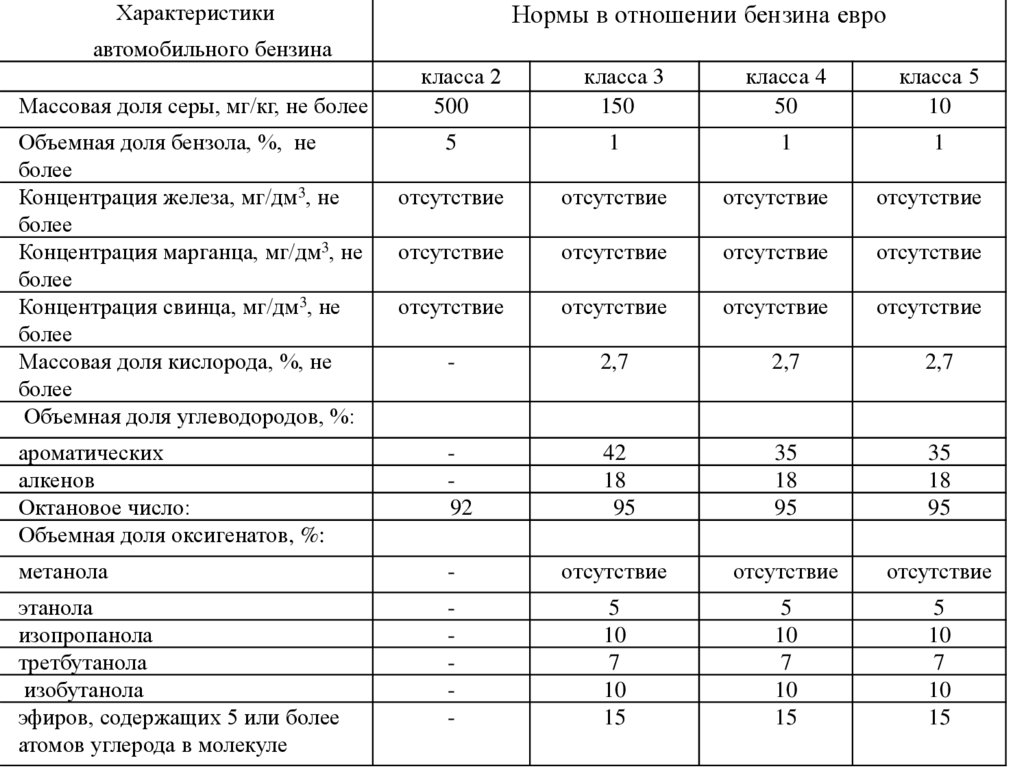
ХарактеристикиНормы в отношении бензина евро
автомобильного бензина
Массовая доля серы, мг/кг, не более
Объемная доля бензола, %, не
более
Концентрация железа, мг/дм3, не
более
Концентрация марганца, мг/дм3, не
более
Концентрация свинца, мг/дм3, не
более
Массовая доля кислорода, %, не
более
Объемная доля углеводородов, %:
класса 2
500
класса 3
150
класса 4
50
класса 5
10
1
1
5
1
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
отсутствие
-
2,7
2,7
2,7
ароматических
алкенов
Октановое число:
Объемная доля оксигенатов, %:
92
42
18
95
35
18
95
35
18
95
метанола
-
отсутствие
отсутствие
отсутствие
этанола
изопропанола
третбутанола
изобутанола
эфиров, содержащих 5 или более
атомов углерода в молекуле
-
5
10
7
10
15
5
10
7
10
15
5
10
7
10
15










 Химия
Химия








