Похожие презентации:
Азотная кислота и ее свойства
1. Тема: «Азотная кислота и ее свойства»
ТЕМА: «АЗОТНАЯ КИСЛОТА И ЕЕСВОЙСТВА»
2. Задание № 1 Запишите формулу соединения азота и его название на основании физических свойств
ЗАДАНИЕ № 1ЗАПИШИТЕ ФОРМУЛУ СОЕДИНЕНИЯ АЗОТА
И ЕГО НАЗВАНИЕ НА ОСНОВАНИИ
ФИЗИЧЕСКИХ СВОЙСТВ
Бесцветный газ с характерным
резким запахом, хорошо
растворим в воде, легче воздуха.
NH3 - аммиак
3. Задание № 2 Расположите соединения азота в порядке возрастания степеней окисления.
ЗАДАНИЕ № 2РАСПОЛОЖИТЕ СОЕДИНЕНИЯ АЗОТА
В ПОРЯДКЕ ВОЗРАСТАНИЯ
СТЕПЕНЕЙ ОКИСЛЕНИЯ.
N2, NH3, KNO3, NO, HNO2.
-3
0
+2
+3
+5
NH3, N2, NO, HNO2, KNO3.
4. АЗОТНАЯ КИСЛОТА и ее свойства
5. I. Физические свойства азотной кислоты
I. ФИЗИЧЕСКИЕ СВОЙСТВААЗОТНОЙ КИСЛОТЫ
Агрегатное состояние – жидкость;
Цвет – отсутствует;
Запах – едкий, кислотный;
Растворимость в воде – хорошая;
«Дымит» на воздухе;
«Особые приметы»:
при хранении на свету разлагается, приобретая
желтоватый оттенок:
4HNO3=4NO2 + O2 + 2H2O
6.
7. III. Химические свойства HNO3
III. ХИМИЧЕСКИЕ СВОЙСТВА HNO3Химические
свойства
Общие с другими
кислотами
Специфические
8. III. Химические свойства HNO3
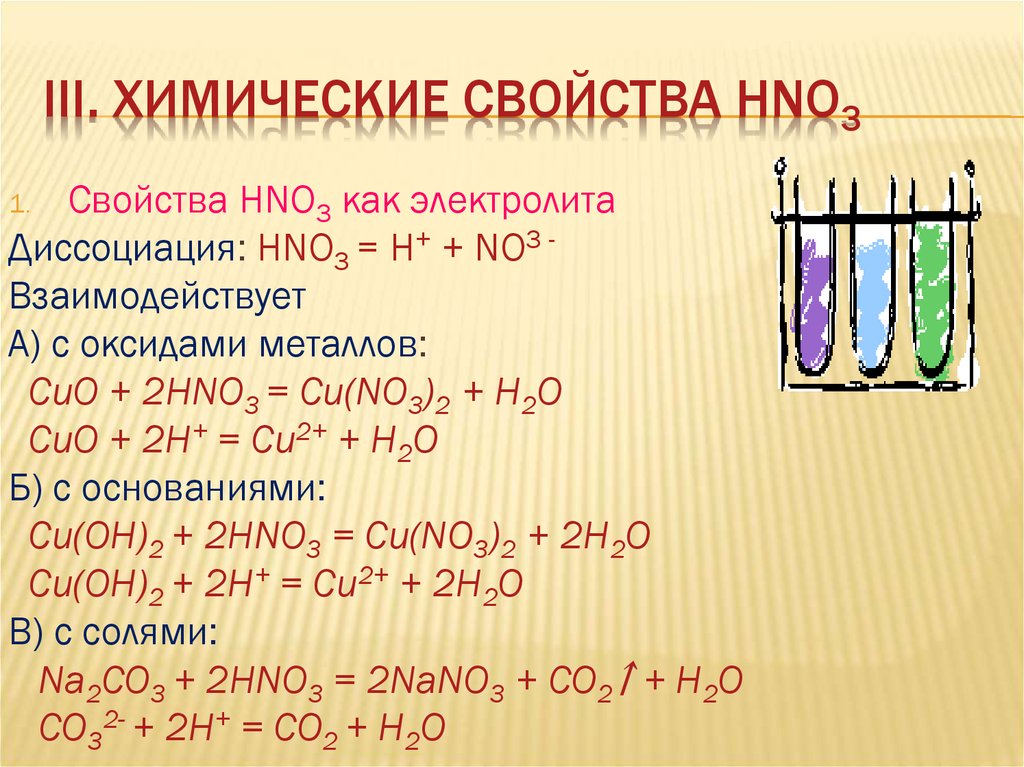
III. ХИМИЧЕСКИЕ СВОЙСТВА HNO3Свойства HNO3 как электролита
Диссоциация: HNO3 = H+ + NO3 Взаимодействует
А) с оксидами металлов:
CuO + 2HNO3 = Cu(NO3)2 + H2O
CuO + 2H+ = Cu2+ + H2O
Б) с основаниями:
Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + 2H2O
В) с солями:
Na2CO3 + 2HNO3 = 2NaNO3 + CO2 + H2O
CO32- + 2H+ = CO2 + H2O
1.
9.
Концентрированнаякислота
HNO3 > 60%
Разбавленная
кислота
HNO3 от 30 % до
60%
Очень
разбавленная
кислота
HNO3 < 30%
Активные
Li - Zn
NO, NO2
NO2, N2
N2 O
NН3
Соли аммония
Средней
активности
Cr - Sn
Не реагируют
(пассивируют)
NO, NO2
N2 O, NН3
NO, NO2
N2 O, NН3
Малоактивные
Pb - Ag
NO2
NO
Благородные
Au, Pt
-
-
-
-
10. III. Химические свойства HNO3
III. ХИМИЧЕСКИЕ СВОЙСТВА HNO32. Окислительные свойства
Взаимодействует с металлами:
K Ca Na Mg Al Zn Cr Fe Pb H2 Cu Hg Ag Au
Ме + HNO3 → Me(NO3)n + H2O + NxOy
Cu + 4HNO3(конц) = Cu(NO3)2 + 2H2O + 2NO2
3Cu + 8HNO3(разб) = 3Cu(NO3)2 + 4H2O + 2NO
Me + HNO3 = Me(NO3)2 + H2
11. Действие на органические вещества
ДЕЙСТВИЕ НА ОРГАНИЧЕСКИЕ ВЕЩЕСТВА•Белки при взаимодействии с
концентрированной азотной кислотой
разрушаются и приобретают жёлтую
окраску .
•Под действием азотной кислоты
воспламеняются бумага, масло, древесина,
уголь.
12. IV. Применение азотной кислоты
IV. ПРИМЕНЕНИЕ АЗОТНОЙ КИСЛОТЫHNO3









 Химия
Химия








