Похожие презентации:
Процессы окисления
1. ПРОЦЕССЫ ОКИСЛЕНИЯ
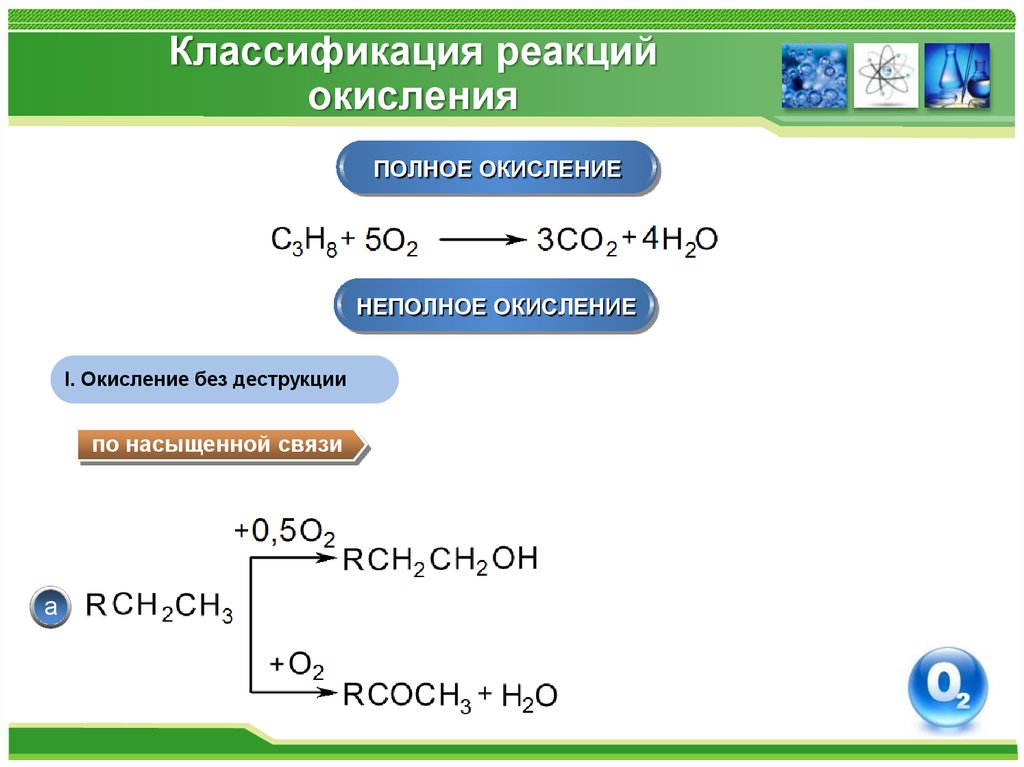
2. Классификация реакций окисления
ПОЛНОЕ ОКИСЛЕНИЕНЕПОЛНОЕ ОКИСЛЕНИЕ
I. Окисление без деструкции
по насыщенной связи
а
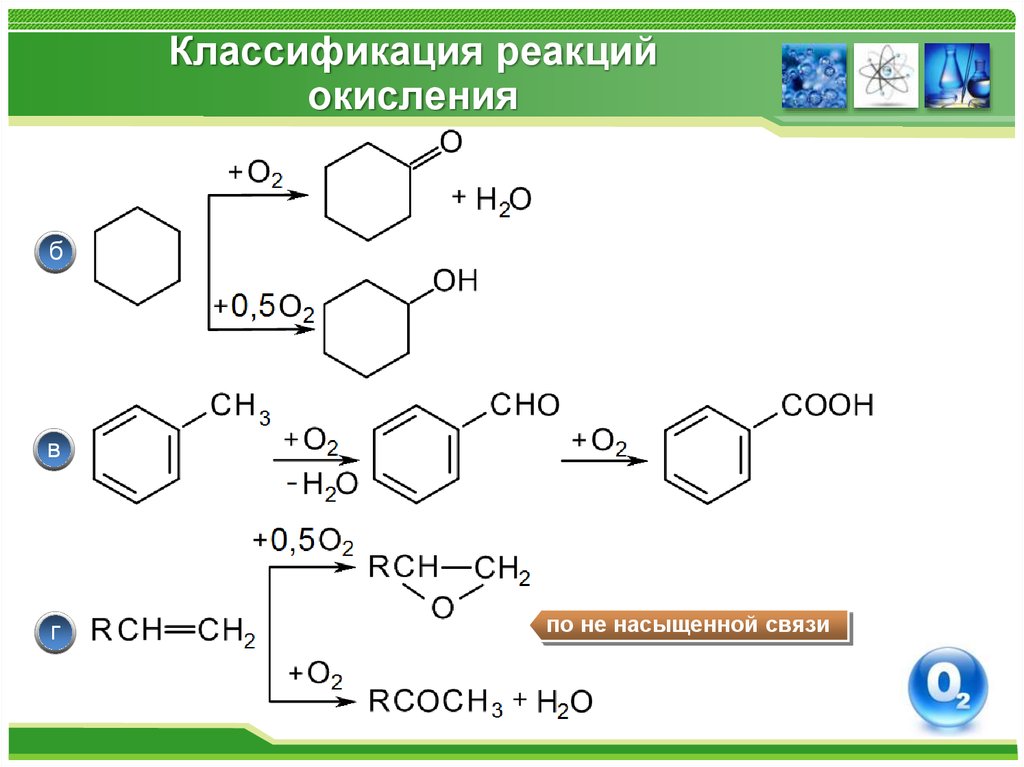
3. Классификация реакций окисления
бв
г
по не насыщенной связи
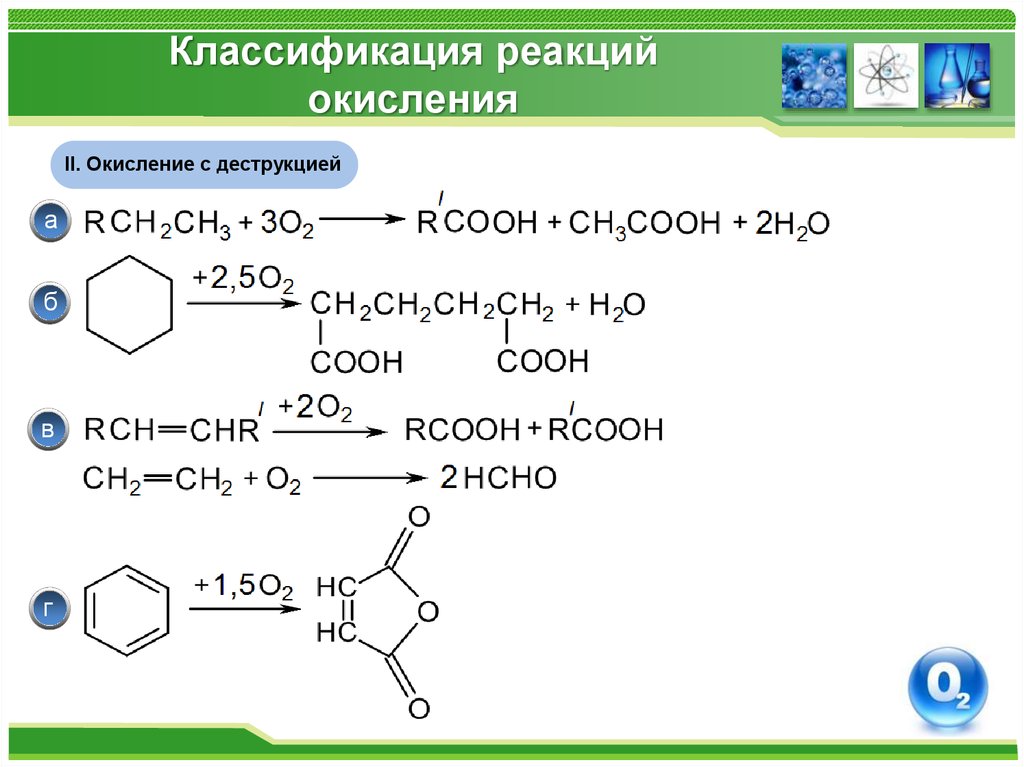
4. Классификация реакций окисления
II. Окисление с деструкциейа
б
в
г
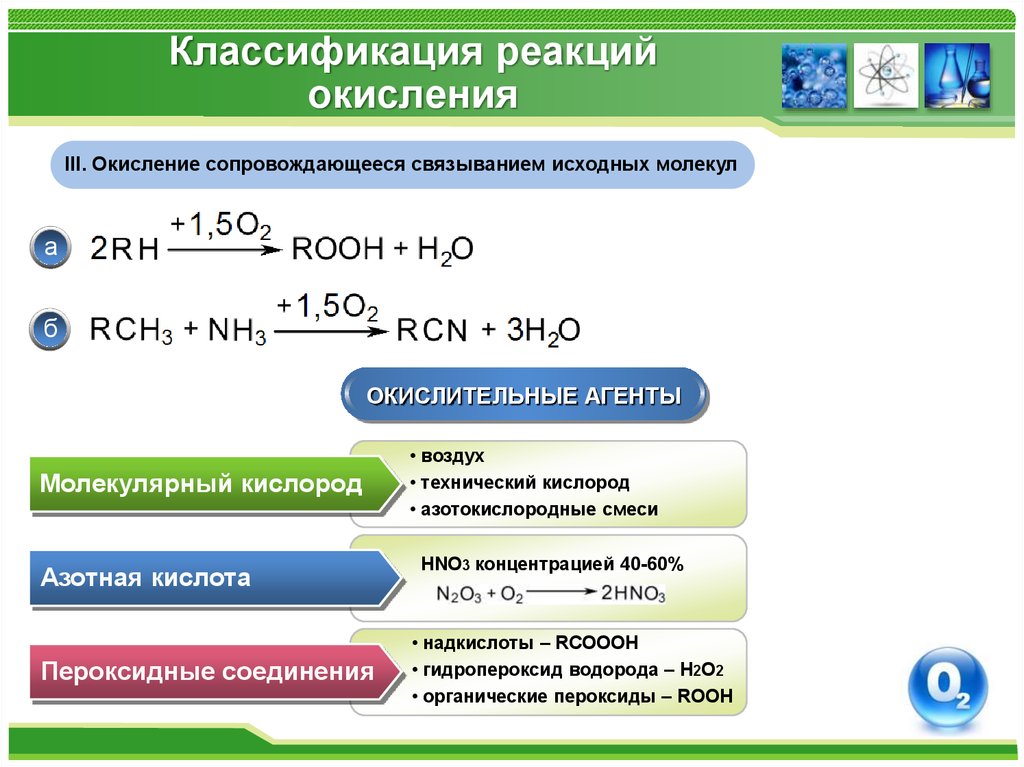
5. Классификация реакций окисления
III. Окисление сопровождающееся связыванием исходных молекула
б
ОКИСЛИТЕЛЬНЫЕ АГЕНТЫ
Молекулярный кислород
Азотная кислота
Пероксидные соединения
• воздух
• технический кислород
• азотокислородные смеси
HNO3 концентрацией 40-60%
• надкислоты – RCOOOH
• гидропероксид водорода – H2O2
• органические пероксиды – ROOH
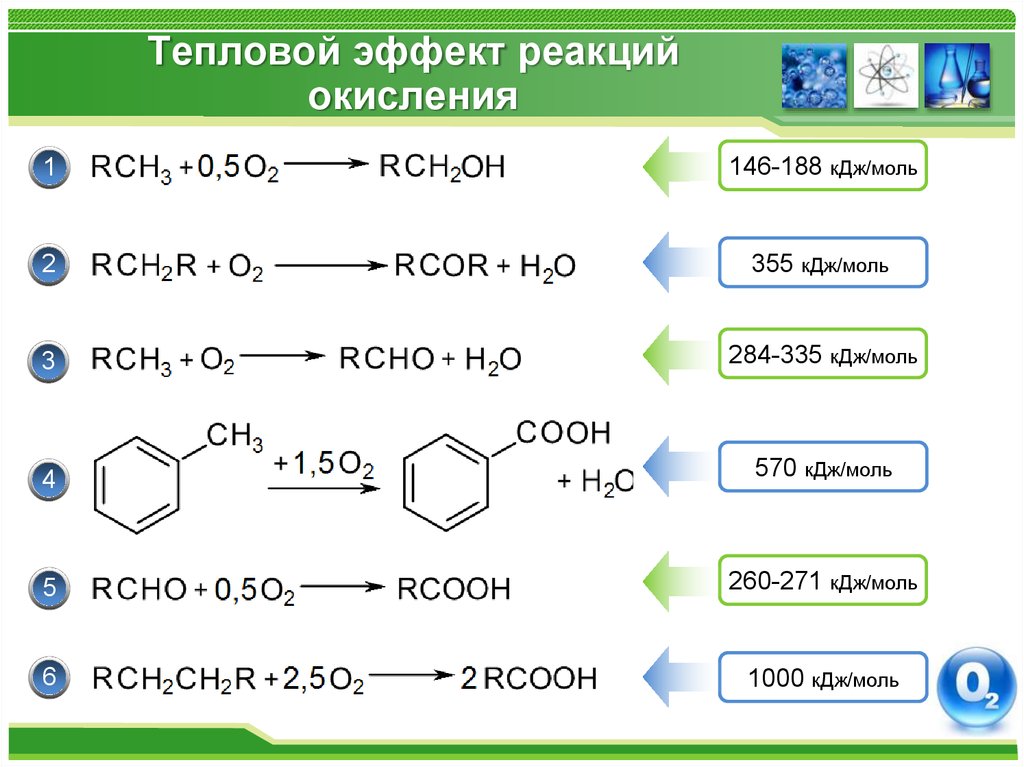
6. Тепловой эффект реакций окисления
1146-188 кДж/моль
2
355 кДж/моль
3
284-335 кДж/моль
4
570 кДж/моль
5
260-271 кДж/моль
6
1000 кДж/моль
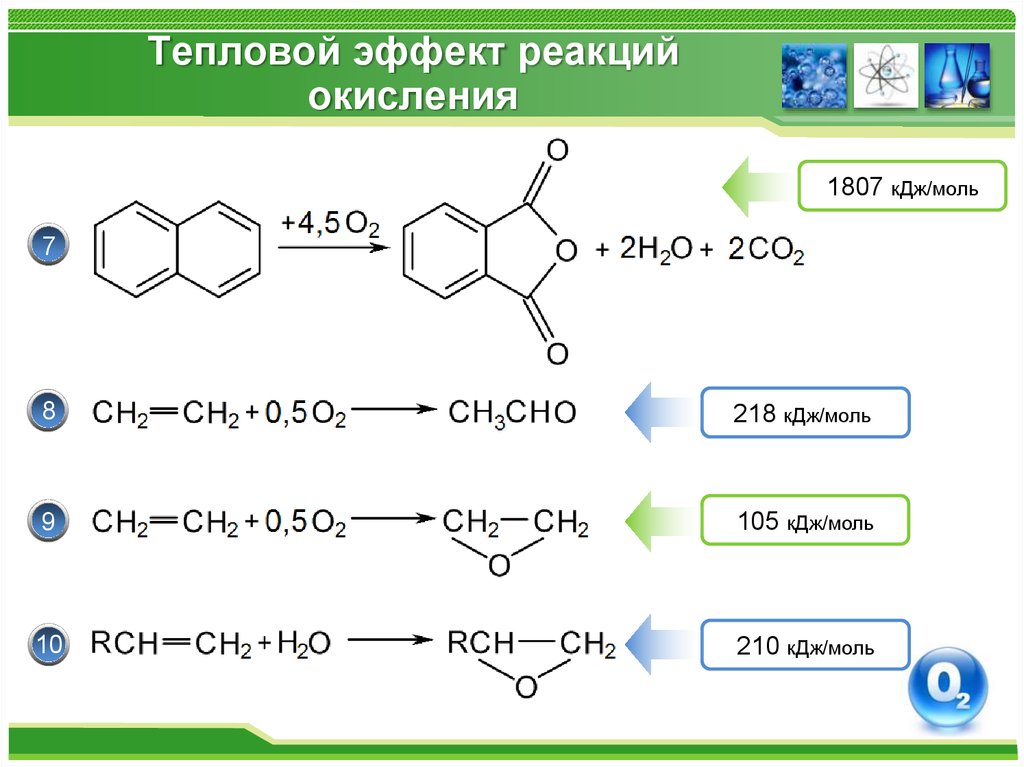
7. Тепловой эффект реакций окисления
1807 кДж/моль7
8
218 кДж/моль
9
105 кДж/моль
10
210 кДж/моль
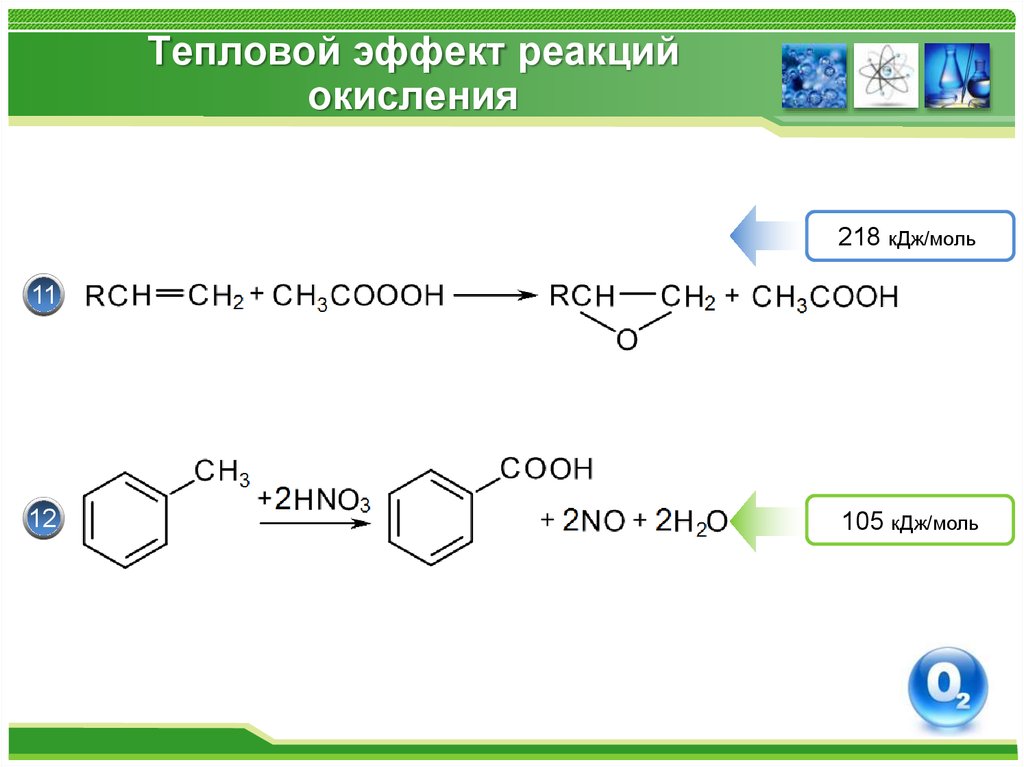
8. Тепловой эффект реакций окисления
218 кДж/моль11
12
105 кДж/моль
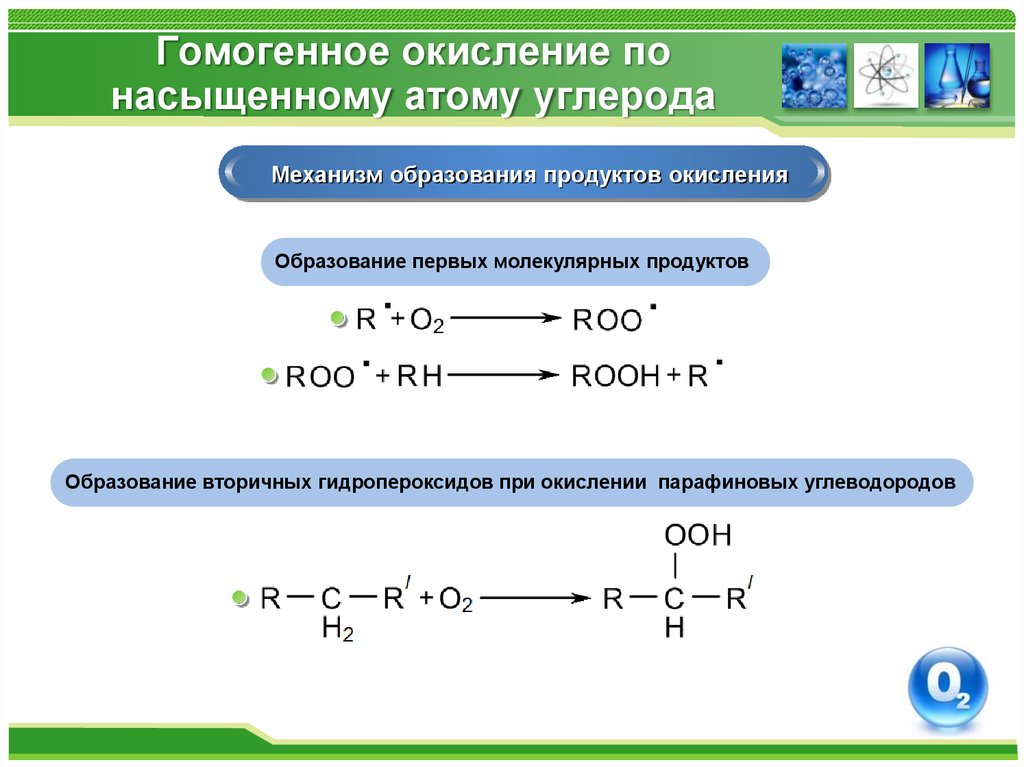
9. Гомогенное окисление по насыщенному атому углерода
Механизм образования продуктов окисленияОбразование первых молекулярных продуктов
Образование вторичных гидропероксидов при окислении парафиновых углеводородов
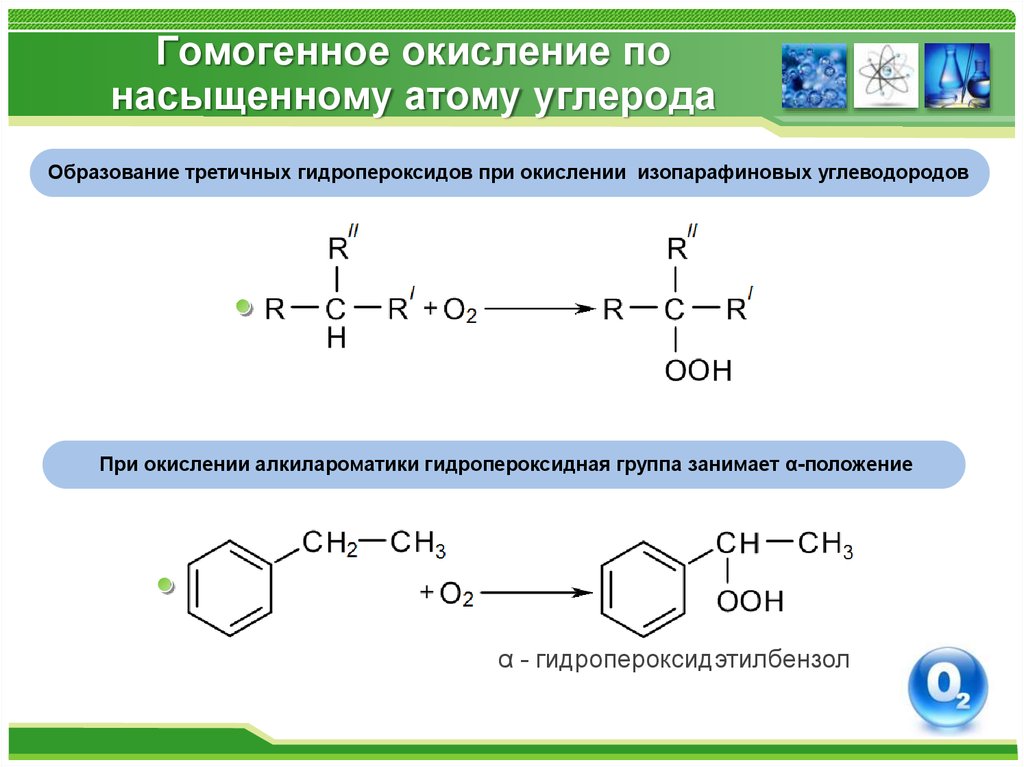
10. Гомогенное окисление по насыщенному атому углерода
Образование третичных гидропероксидов при окислении изопарафиновых углеводородовПри окислении алкилароматики гидропероксидная группа занимает α-положение
α - гидропероксидэтилбензол
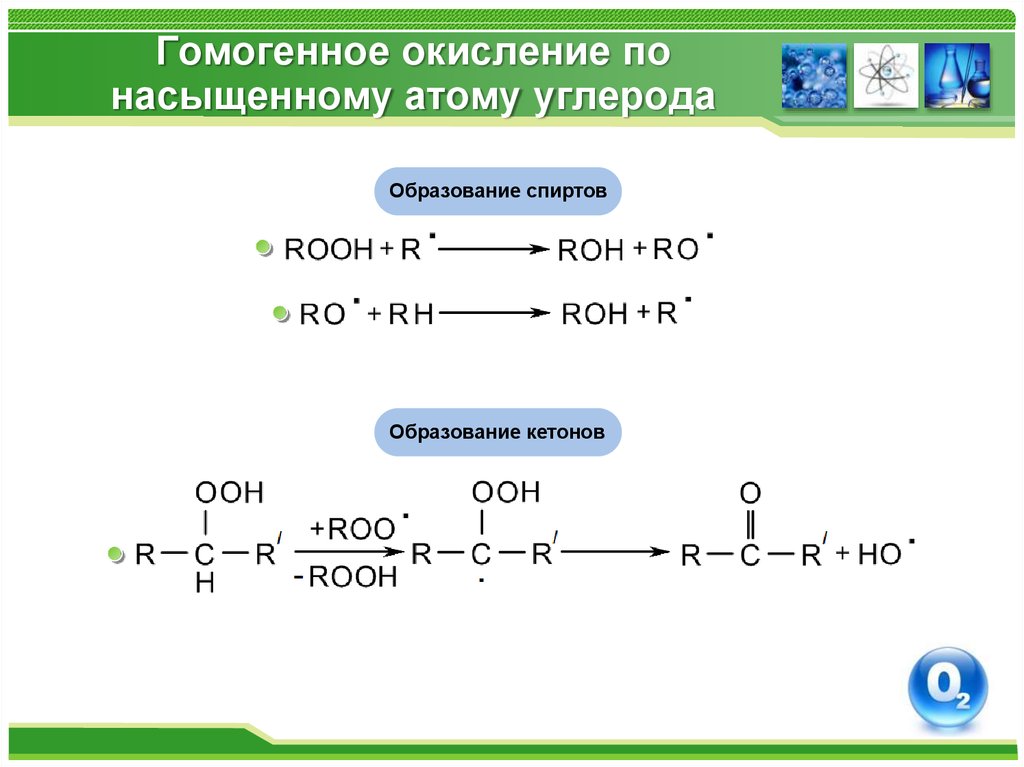
11. Гомогенное окисление по насыщенному атому углерода
Образование спиртовОбразование кетонов
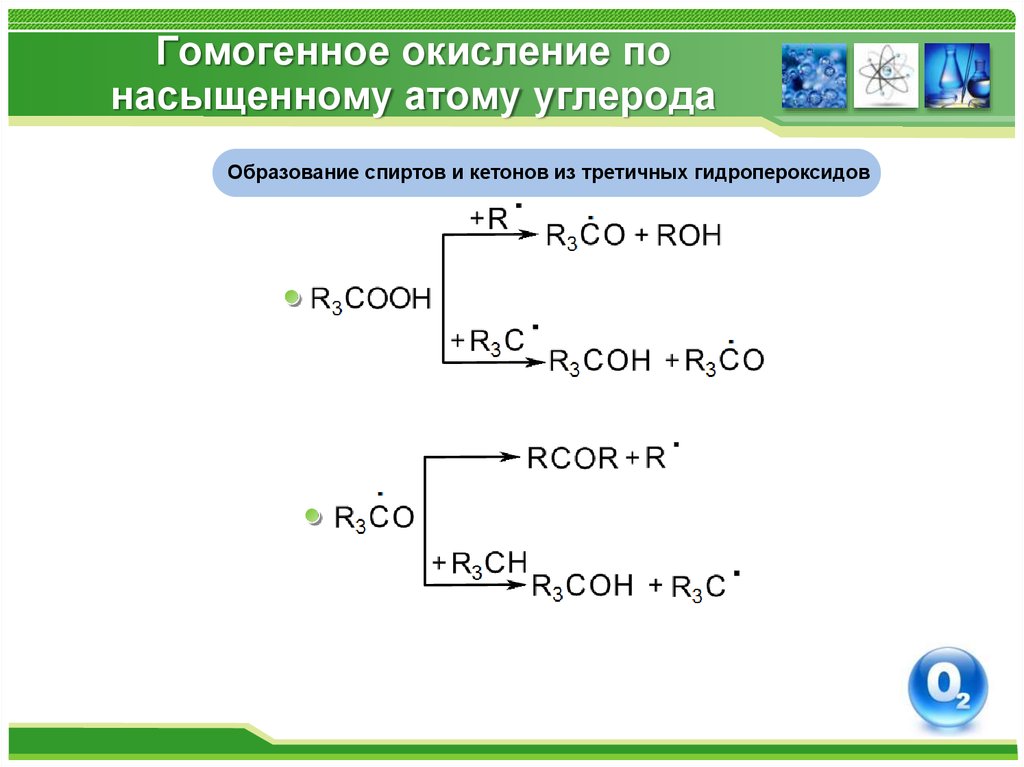
12. Гомогенное окисление по насыщенному атому углерода
Образование спиртов и кетонов из третичных гидропероксидов13. Гомогенное окисление по насыщенному атому углерода
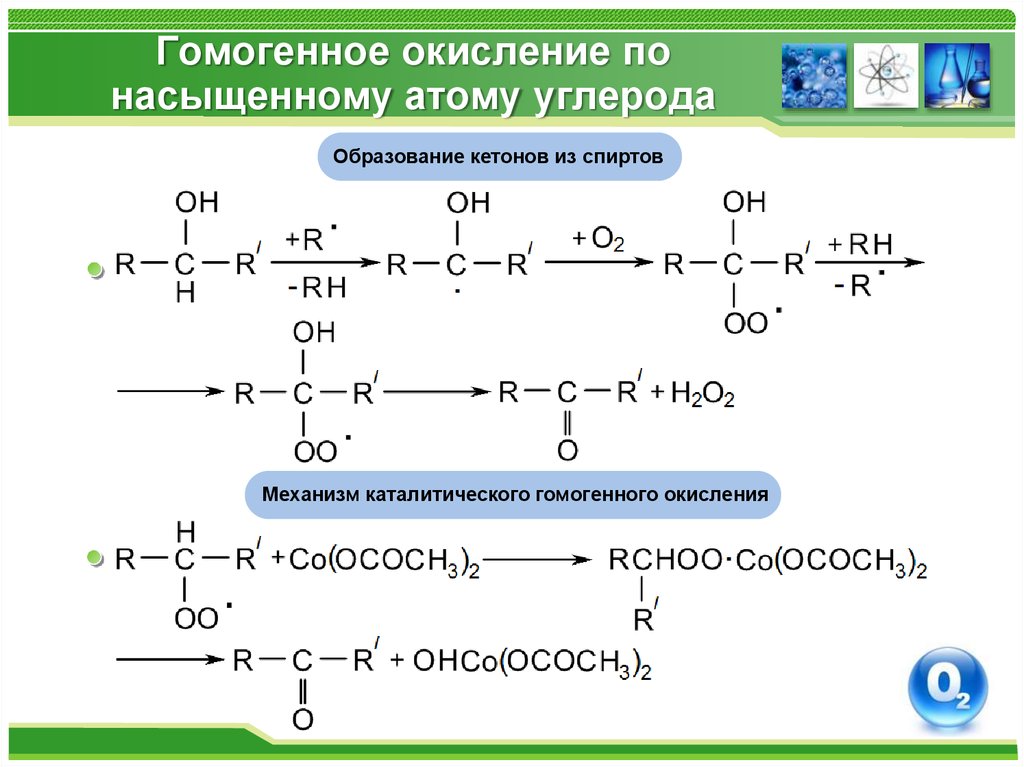
Образование кетонов из спиртовМеханизм каталитического гомогенного окисления
14. Гомогенное окисление по насыщенному атому углерода
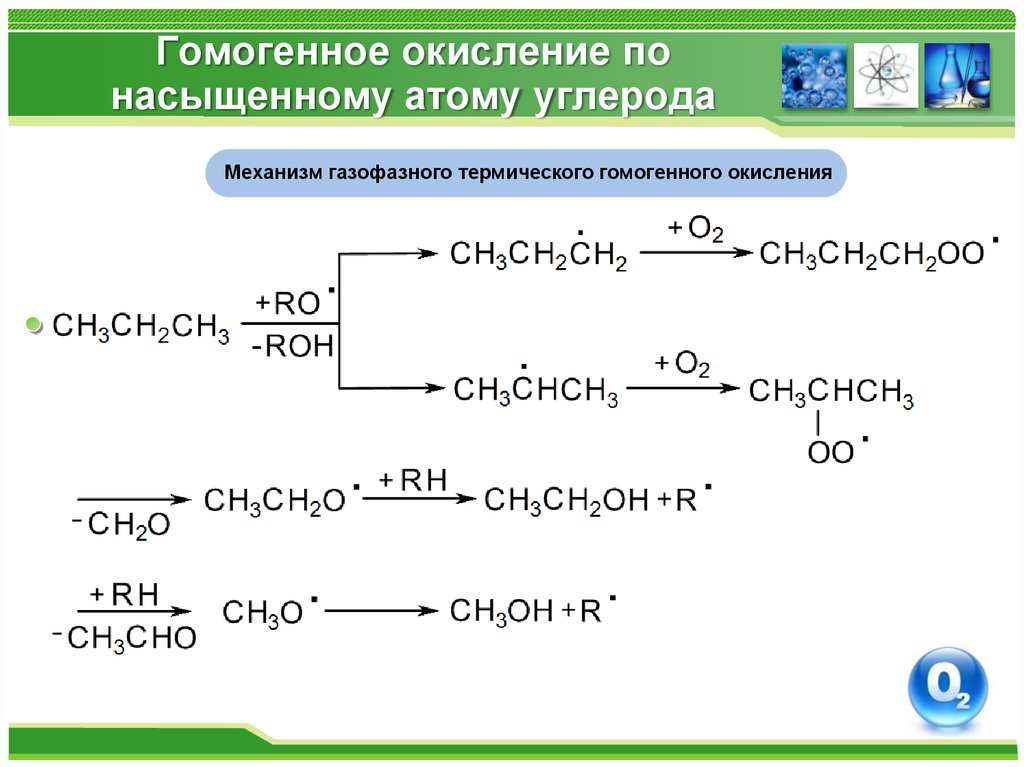
Механизм газофазного термического гомогенного окисления15. Гомогенное окисление по насыщенному атому углерода
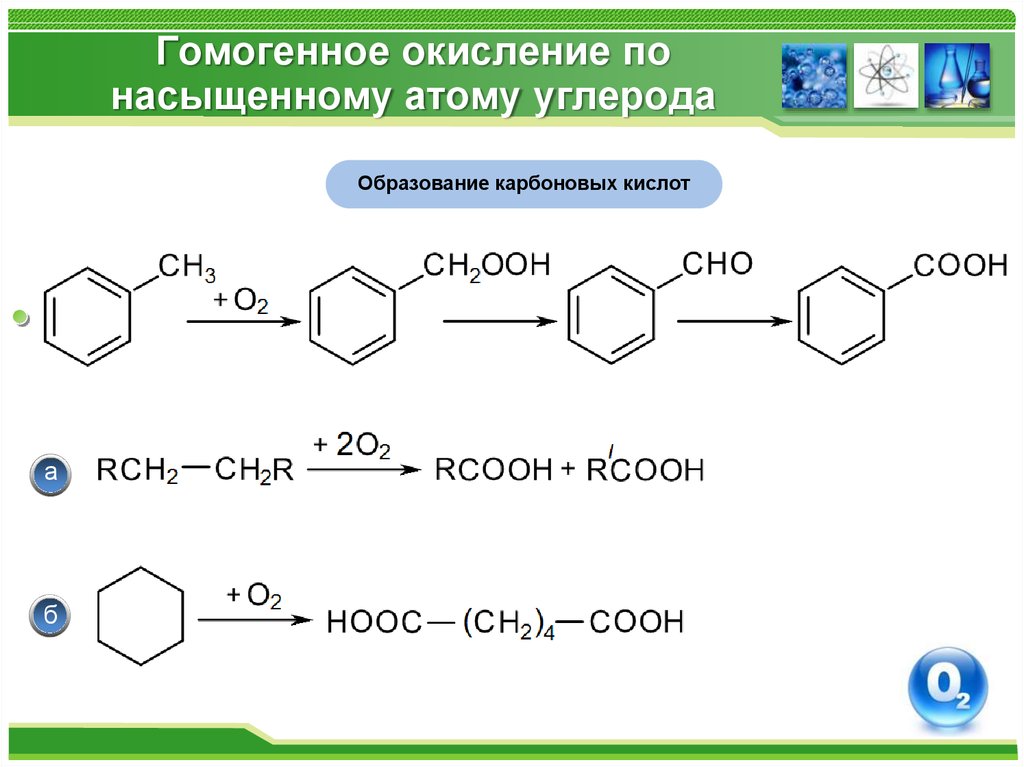
Образование карбоновых кислота
б
16. Гомогенное окисление по насыщенному атому углерода
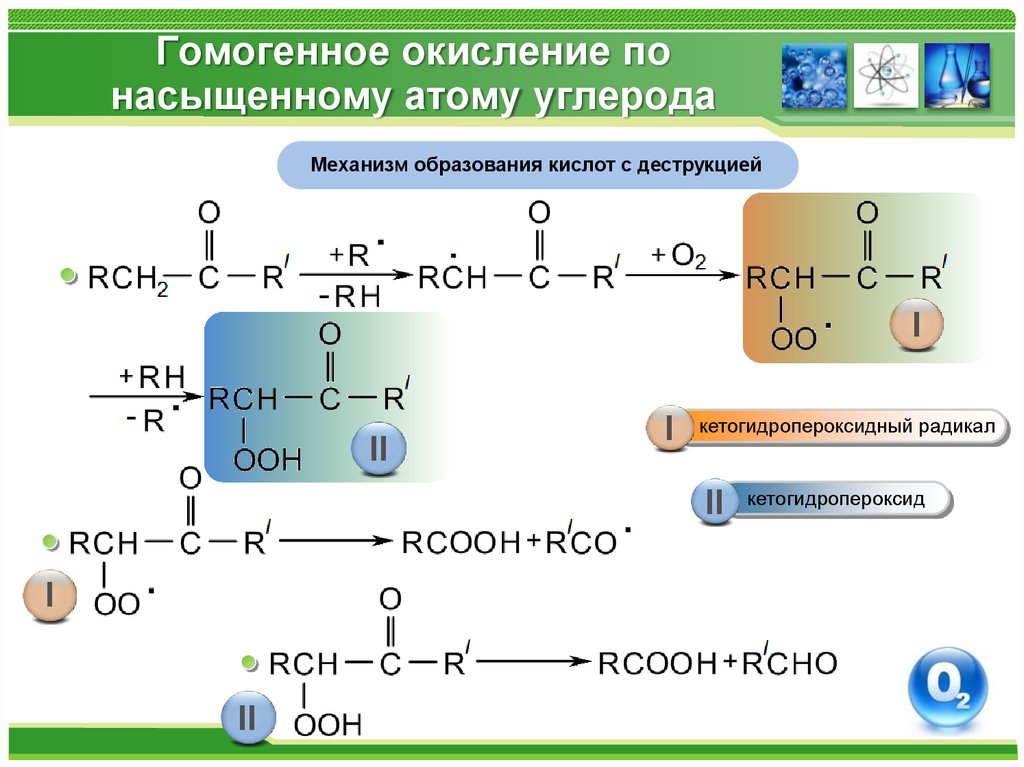
Механизм образования кислот с деструкциейI
II
I
кетогидропероксидный радикал
II
I
II
кетогидропероксид
17. Гомогенное окисление по насыщенному атому углерода
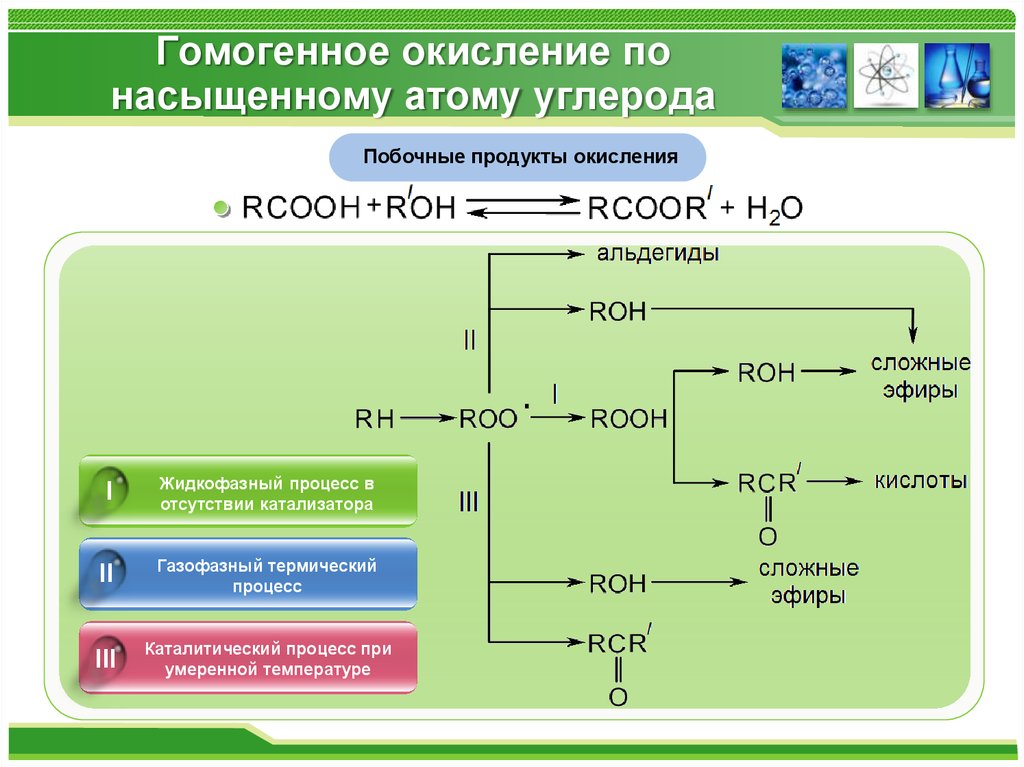
Побочные продукты окисленияI
Жидкофазный процесс в
отсутствии катализатора
II
Газофазный термический
процесс
III
Каталитический процесс при
умеренной температуре
18. Гомогенное окисление по насыщенному атому углерода
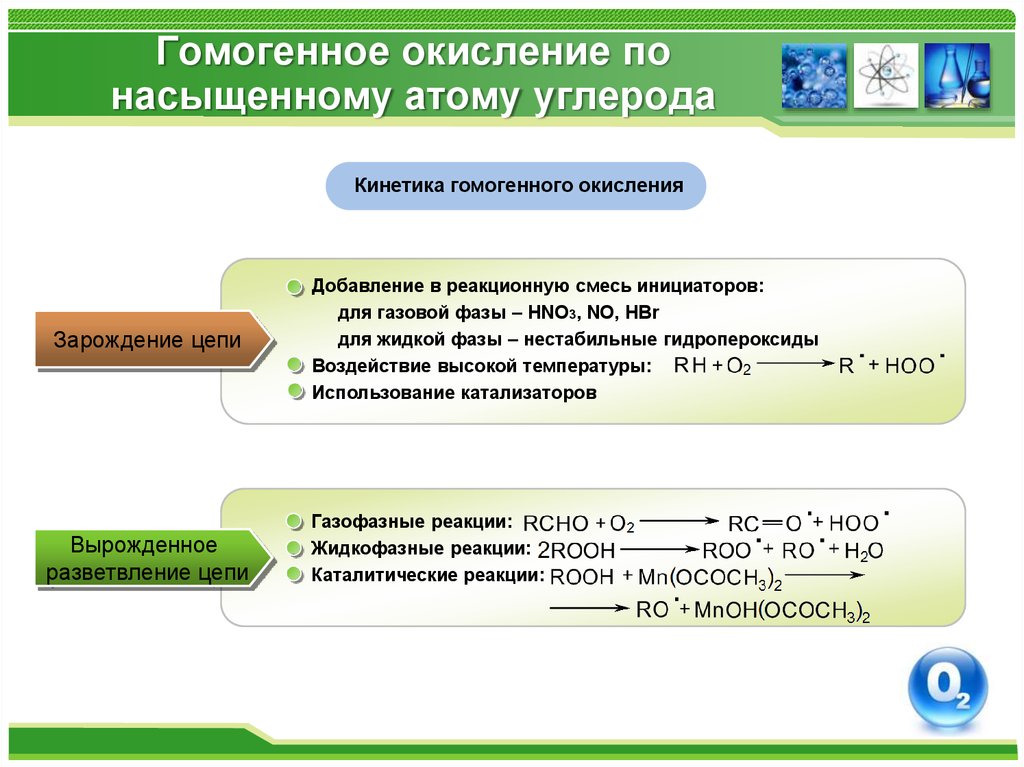
Кинетика гомогенного окисленияЗарождение цепи
Вырожденное
разветвление цепи
Добавление в реакционную смесь инициаторов:
для газовой фазы – HNO3, NO, HBr
для жидкой фазы – нестабильные гидропероксиды
Воздействие высокой температуры:
Использование катализаторов
Газофазные реакции:
Жидкофазные реакции:
Каталитические реакции:
19. Гомогенное окисление по насыщенному атому углерода
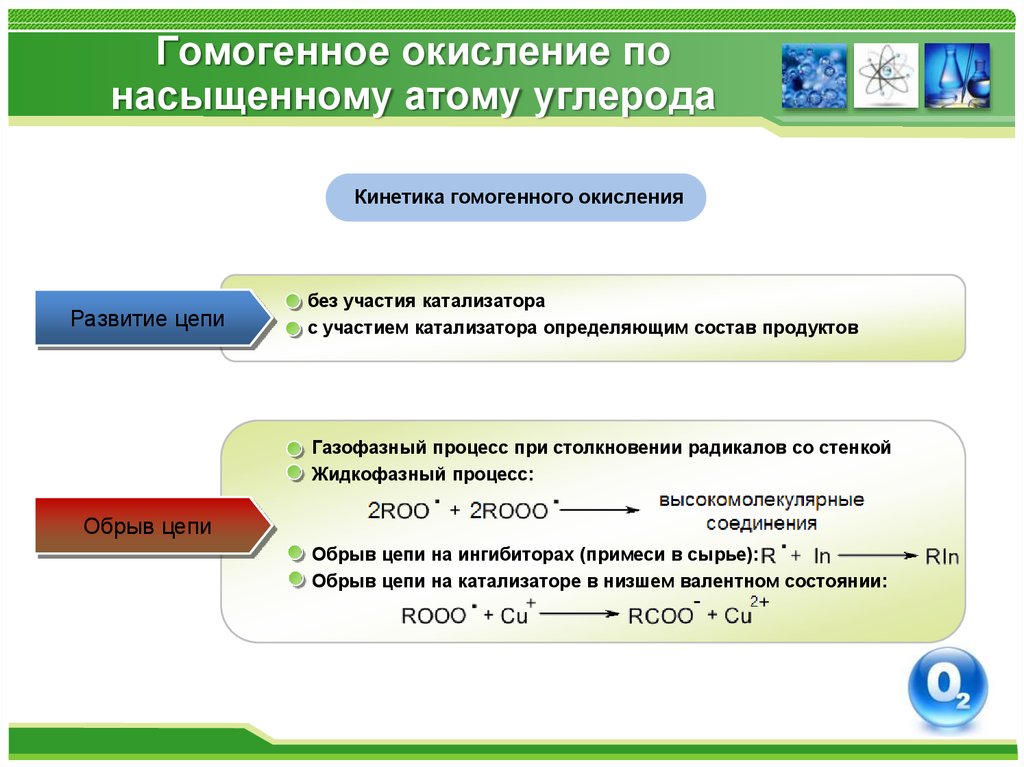
Кинетика гомогенного окисленияРазвитие цепи
без участия катализатора
с участием катализатора определяющим состав продуктов
Газофазный процесс при столкновении радикалов со стенкой
Жидкофазный процесс:
Обрыв цепи
Обрыв цепи на ингибиторах (примеси в сырье):
Обрыв цепи на катализаторе в низшем валентном состоянии:
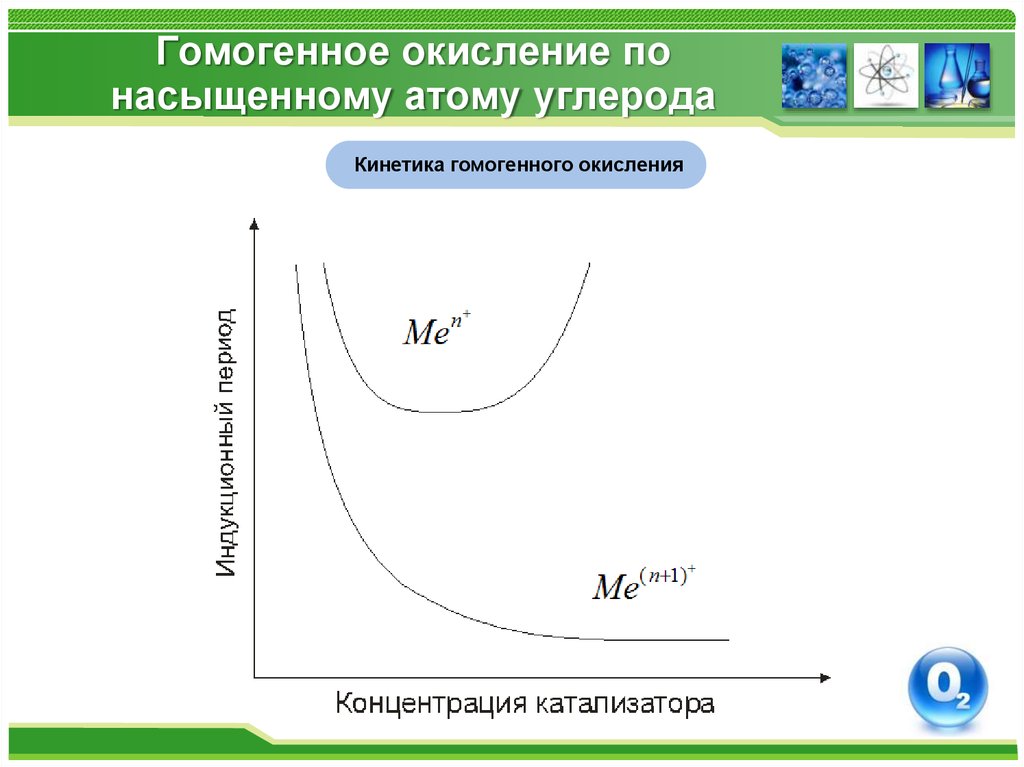
20. Гомогенное окисление по насыщенному атому углерода
Кинетика гомогенного окисления21. Гомогенное окисление по насыщенному атому углерода
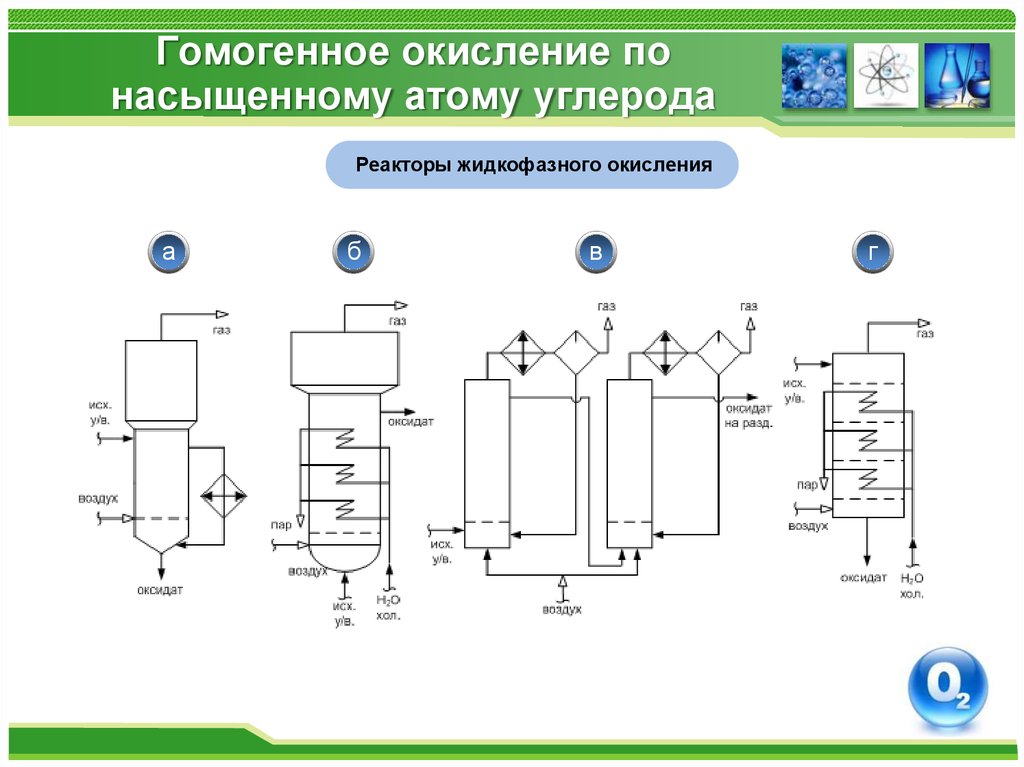
Реакторы жидкофазного окисленияа
б
в
г
22. Гомогенное окисление по насыщенному атому углерода
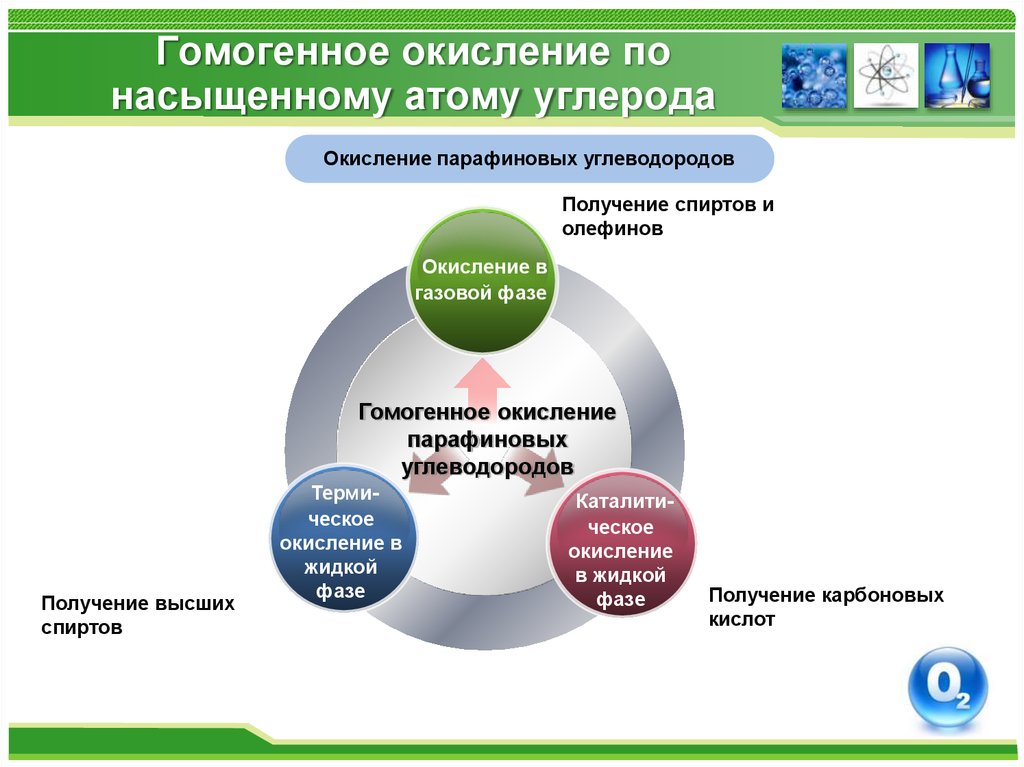
Окисление парафиновых углеводородовПолучение спиртов и
олефинов
Окисление в
газовой фазе
Гомогенное окисление
парафиновых
углеводородов
Получение высших
спиртов
Термическое
окисление в
жидкой
фазе
Каталитическое
окисление
в жидкой
фазе
Получение карбоновых
кислот
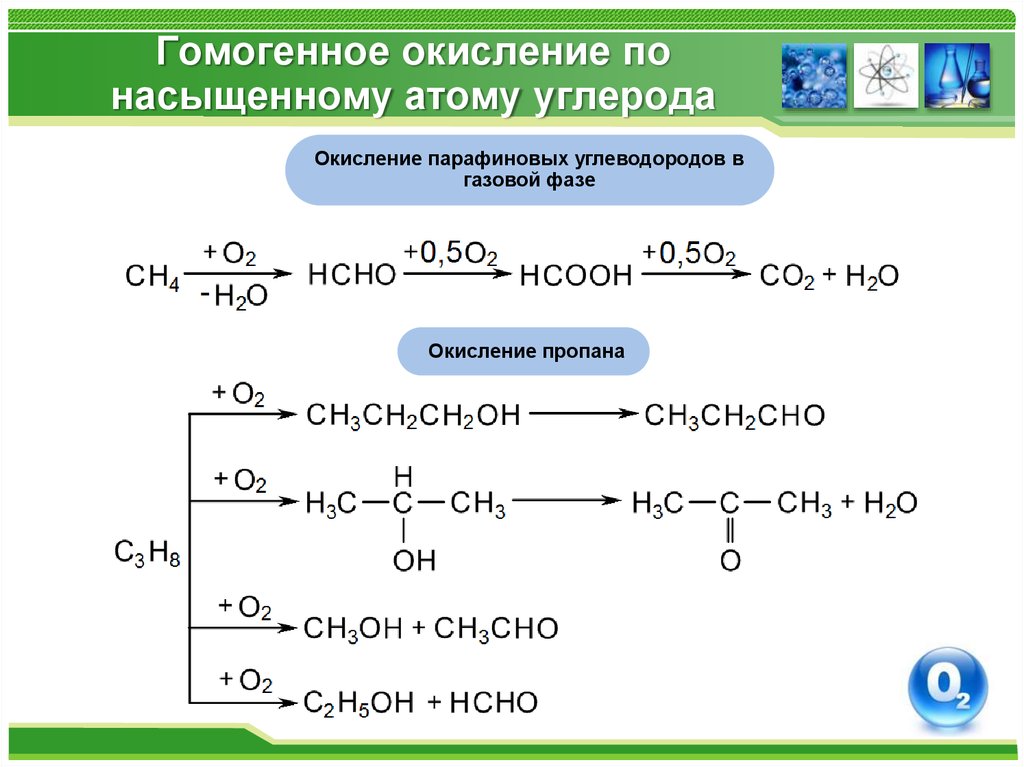
23. Гомогенное окисление по насыщенному атому углерода
Окисление парафиновых углеводородов вгазовой фазе
Окисление пропана
24. Гомогенное окисление по насыщенному атому углерода
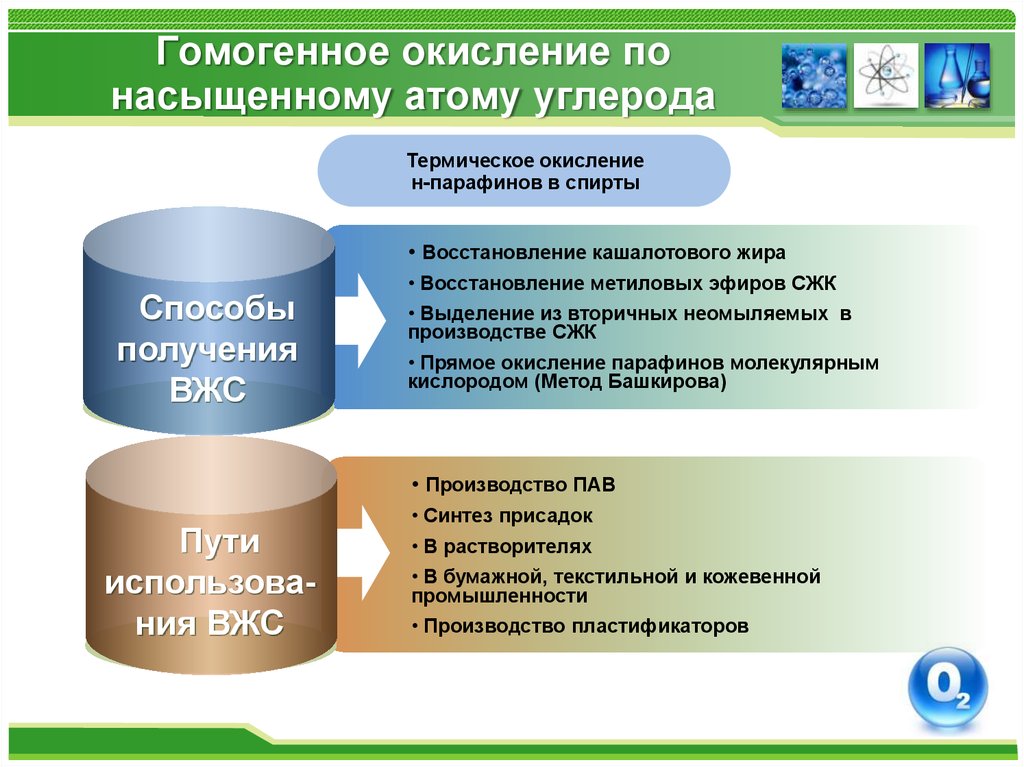
Термическое окислениен-парафинов в спирты
• Восстановление кашалотового жира
Способы
получения
ВЖС
• Восстановление метиловых эфиров СЖК
• Выделение из вторичных неомыляемых в
производстве СЖК
• Прямое окисление парафинов молекулярным
кислородом (Метод Башкирова)
• Производство ПАВ
Пути
использования ВЖС
• Синтез присадок
• В растворителях
• В бумажной, текстильной и кожевенной
промышленности
• Производство пластификаторов
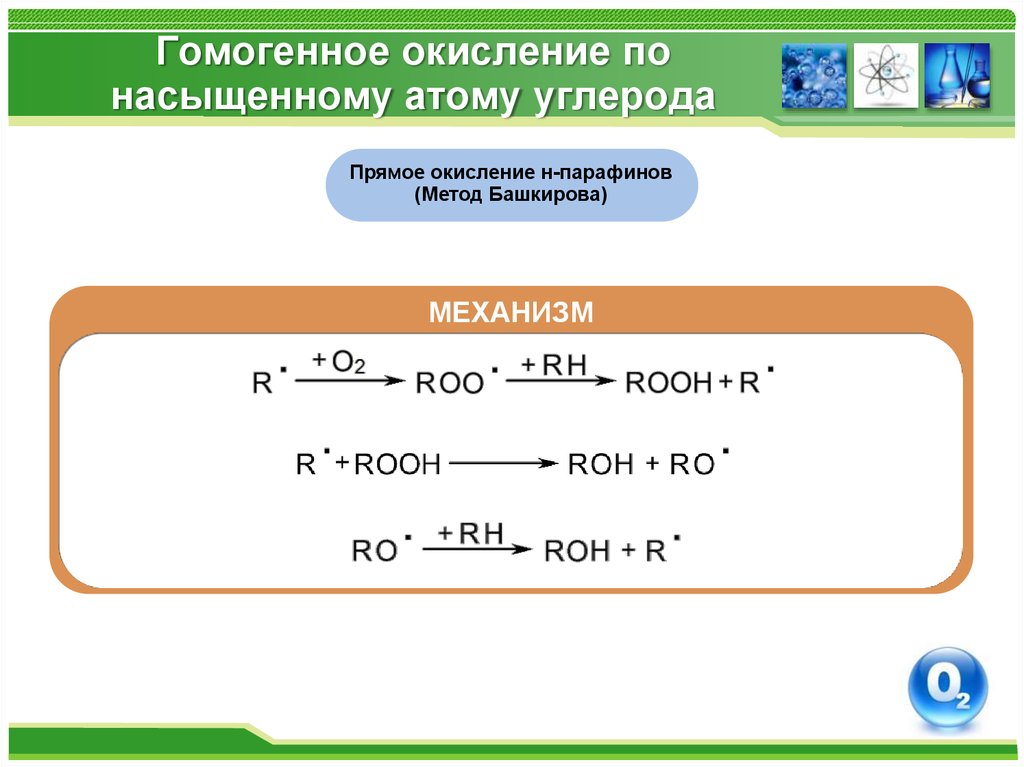
25. Гомогенное окисление по насыщенному атому углерода
Прямое окисление н-парафинов(Метод Башкирова)
МЕХАНИЗМ
26. Гомогенное окисление по насыщенному атому углерода
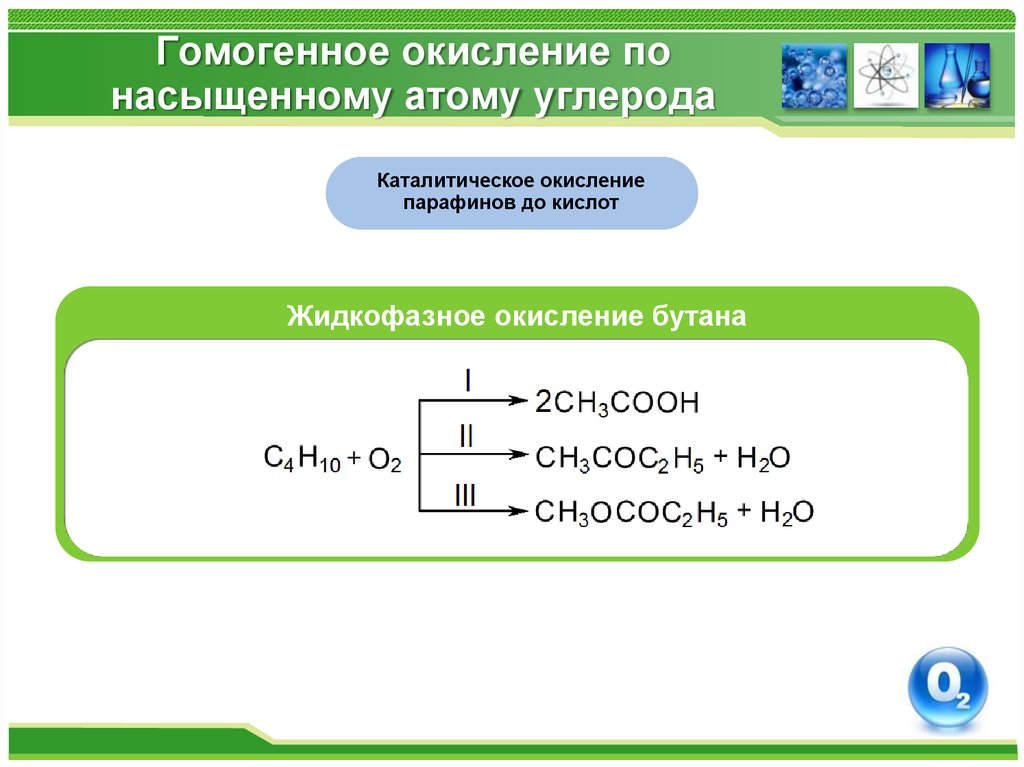
Каталитическое окислениепарафинов до кислот
Жидкофазное окисление бутана
27. Гомогенное окисление по насыщенному атому углерода
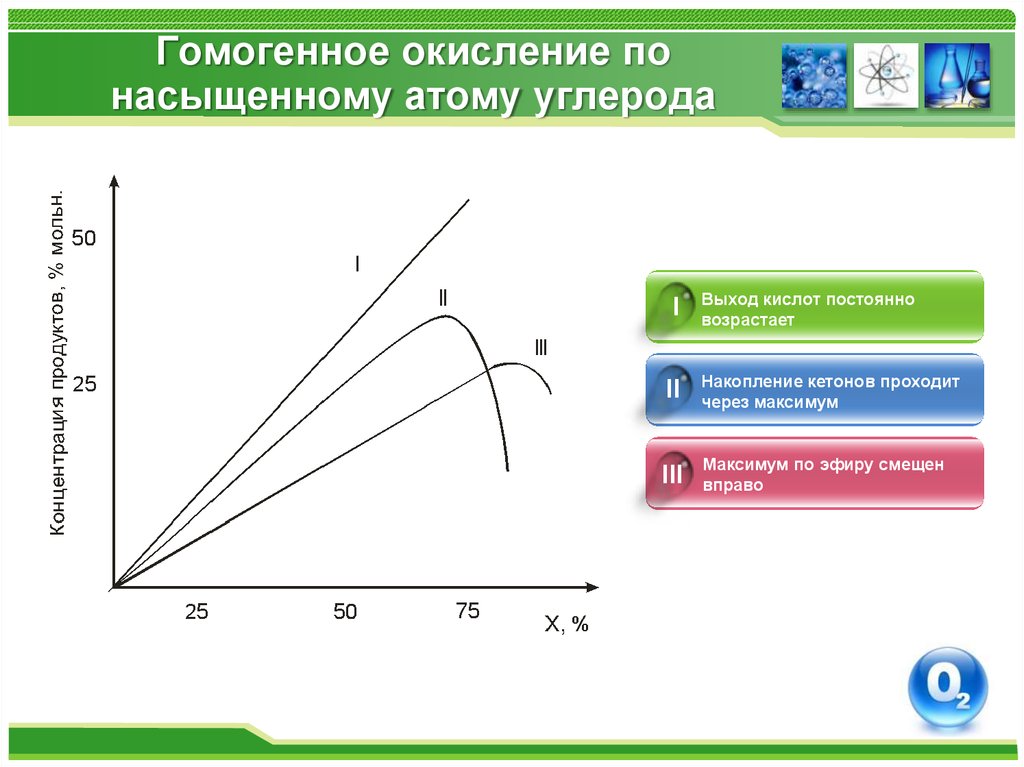
IВыход кислот постоянно
возрастает
II
Накопление кетонов проходит
через максимум
III
Максимум по эфиру смещен
вправо
28. Гомогенное окисление по насыщенному атому углерода
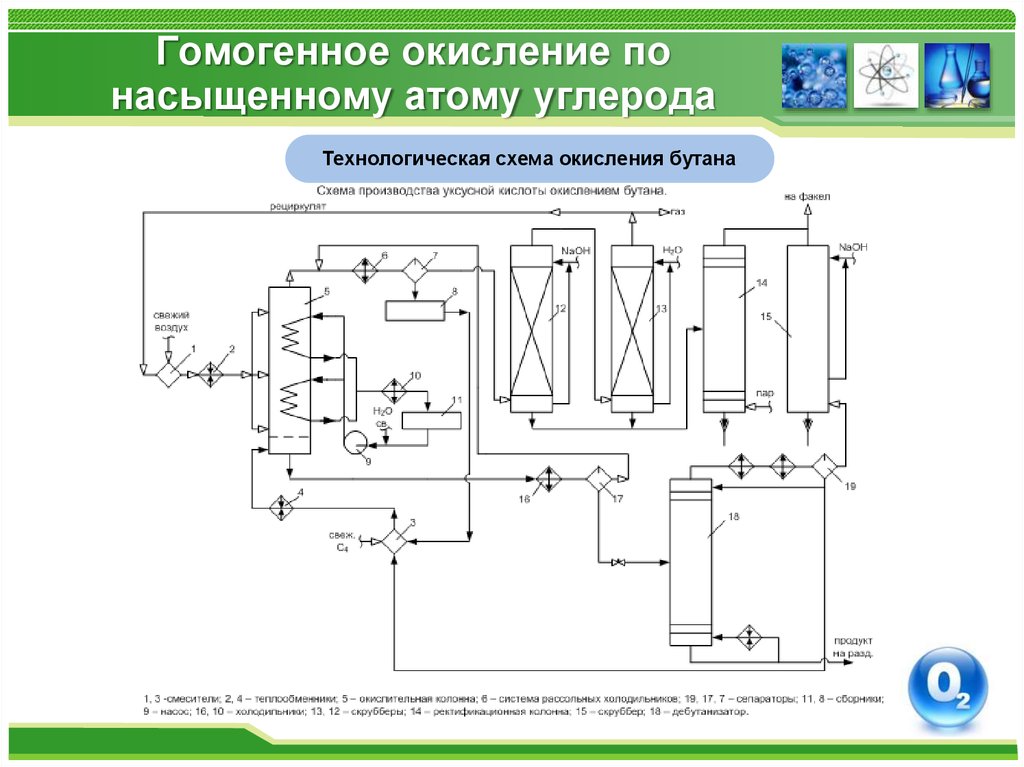
Технологическая схема окисления бутанаЖидкофазное окисление бутана
29. Гомогенное окисление по насыщенному атому углерода
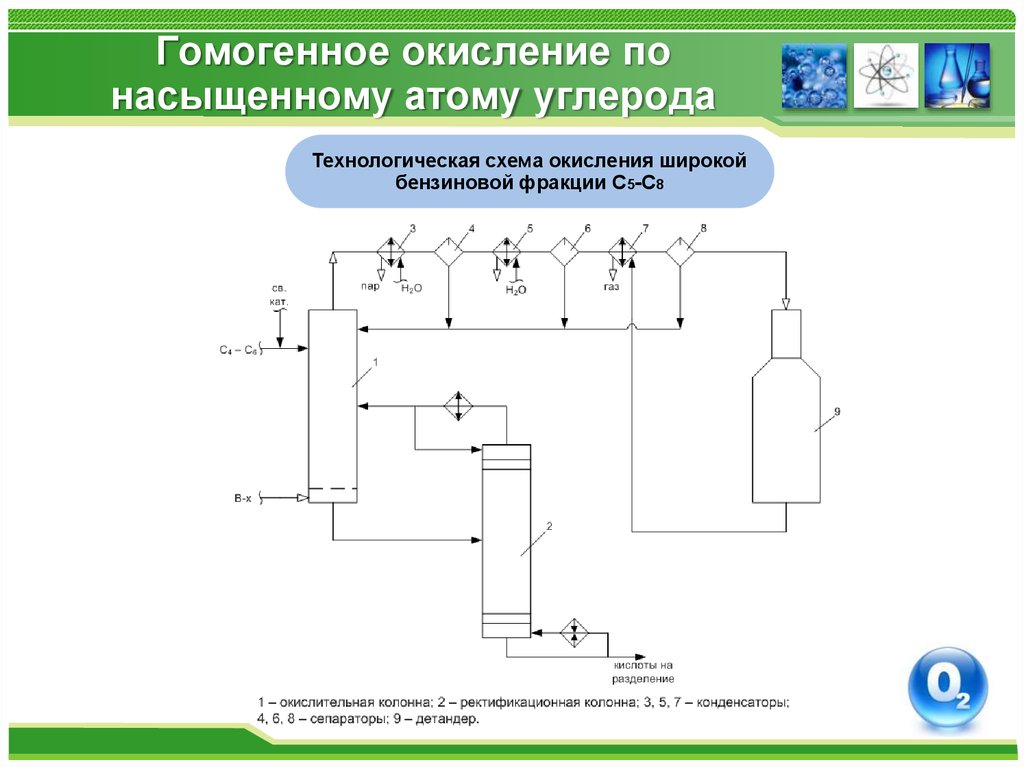
Технологическая схема окисления широкойбензиновой фракции С5-С8
Жидкофазное окисление бутана
30. Гомогенное окисление по насыщенному атому углерода
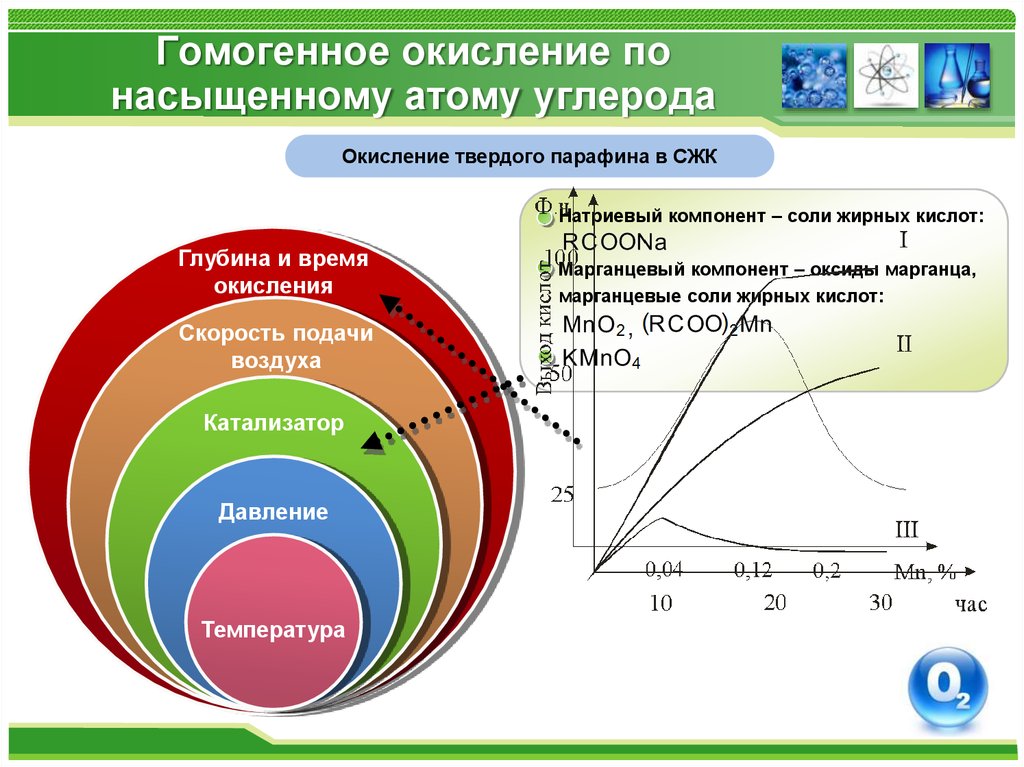
Окисление твердого парафина в СЖКНатриевый компонент – соли жирных кислот:
Глубина и время
окисления
Скорость подачи
воздуха
Катализатор
Давление
Температура
Марганцевый компонент – оксиды марганца,
марганцевые соли жирных кислот:
31. Гомогенное окисление по насыщенному атому углерода
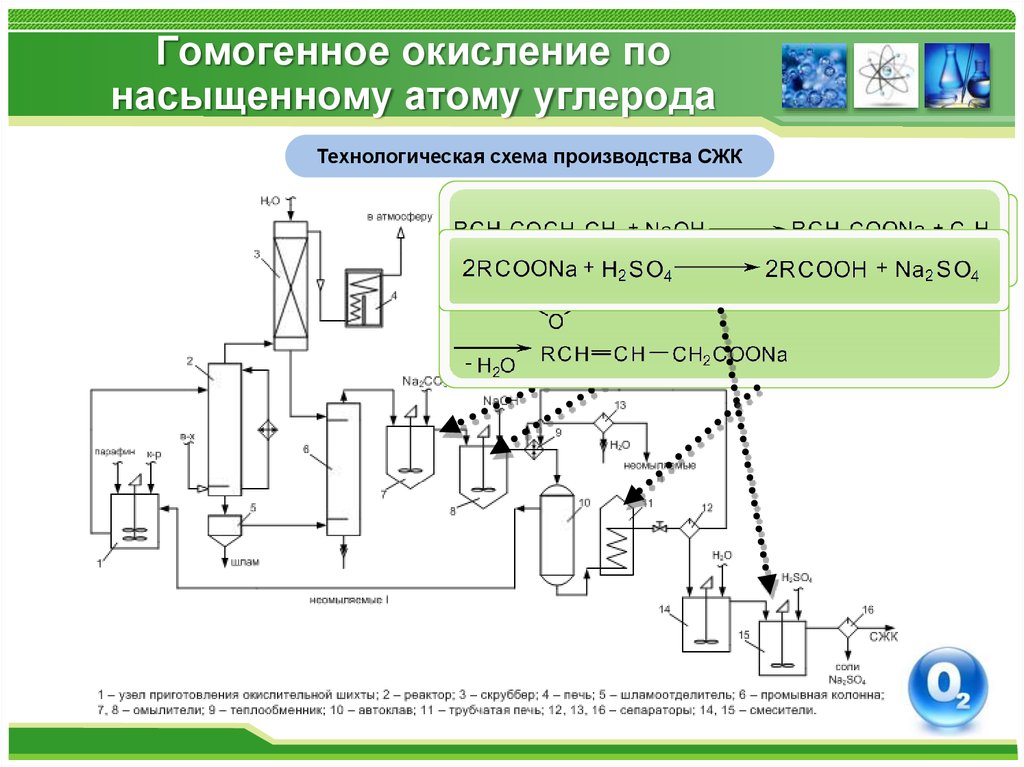
Технологическая схема производства СЖК32. Гомогенное окисление по насыщенному атому углерода
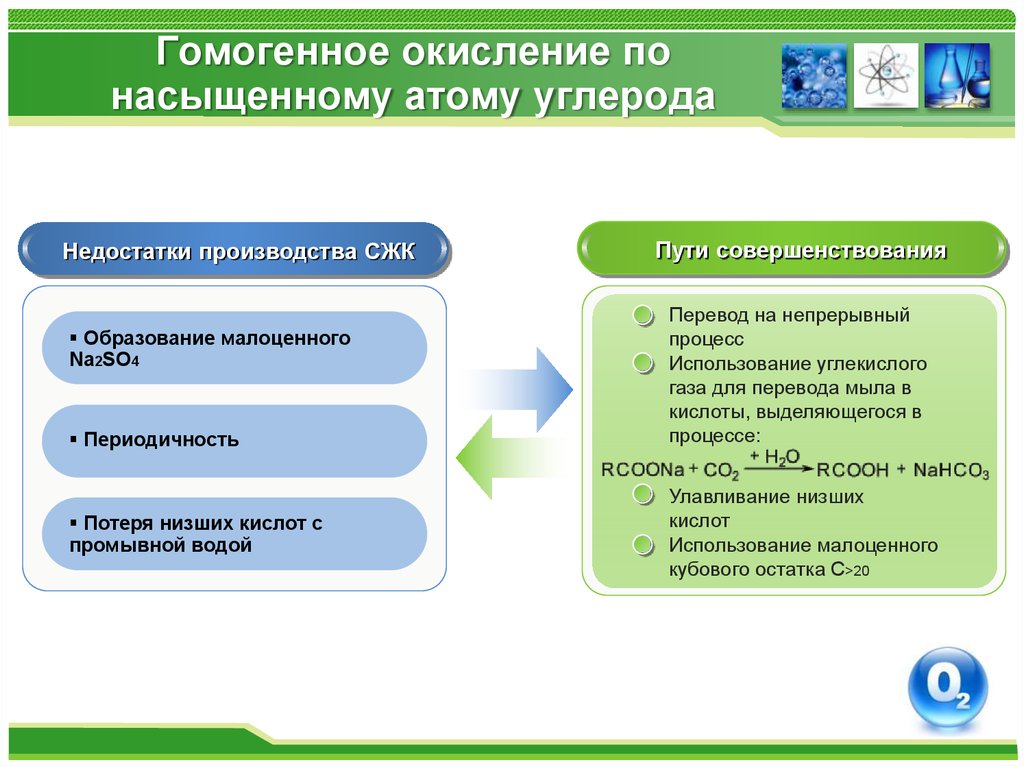
Недостатки производства СЖКОбразование малоценного
Na2SO4
Периодичность
Потеря низших кислот с
промывной водой
Пути совершенствования
Перевод на непрерывный
процесс
Использование углекислого
газа для перевода мыла в
кислоты, выделяющегося в
процессе:
Улавливание низших
кислот
Использование малоценного
кубового остатка С>20
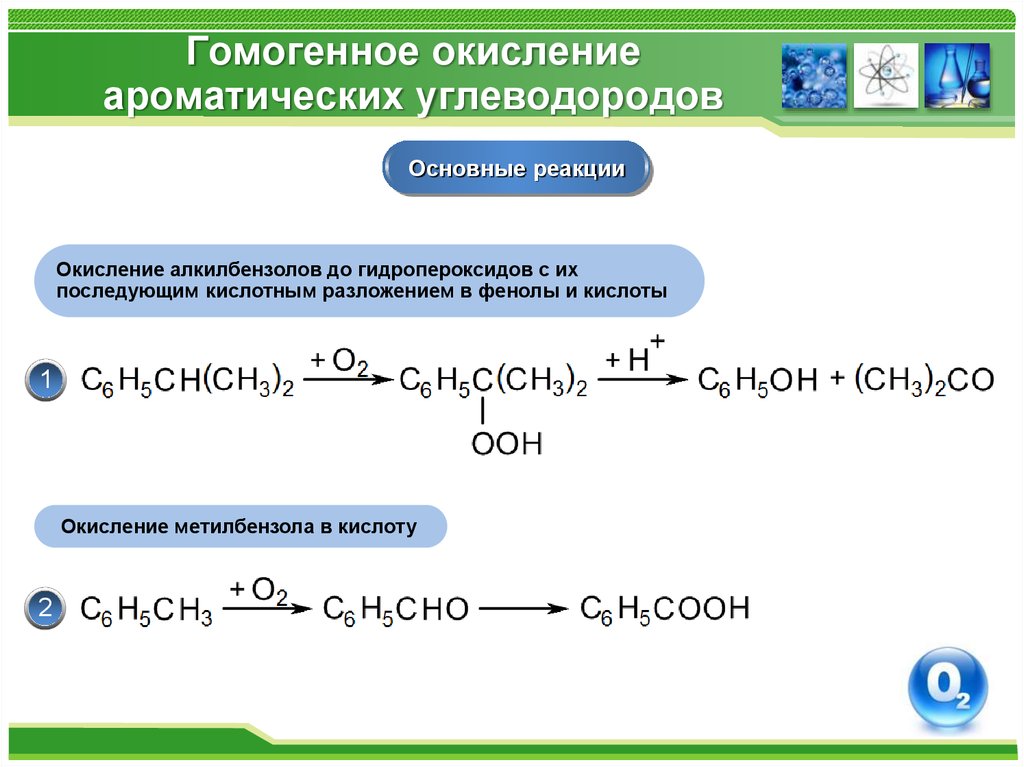
33. Гомогенное окисление ароматических углеводородов
Основные реакцииОкисление алкилбензолов до гидропероксидов с их
последующим кислотным разложением в фенолы и кислоты
1
Окисление метилбензола в кислоту
2
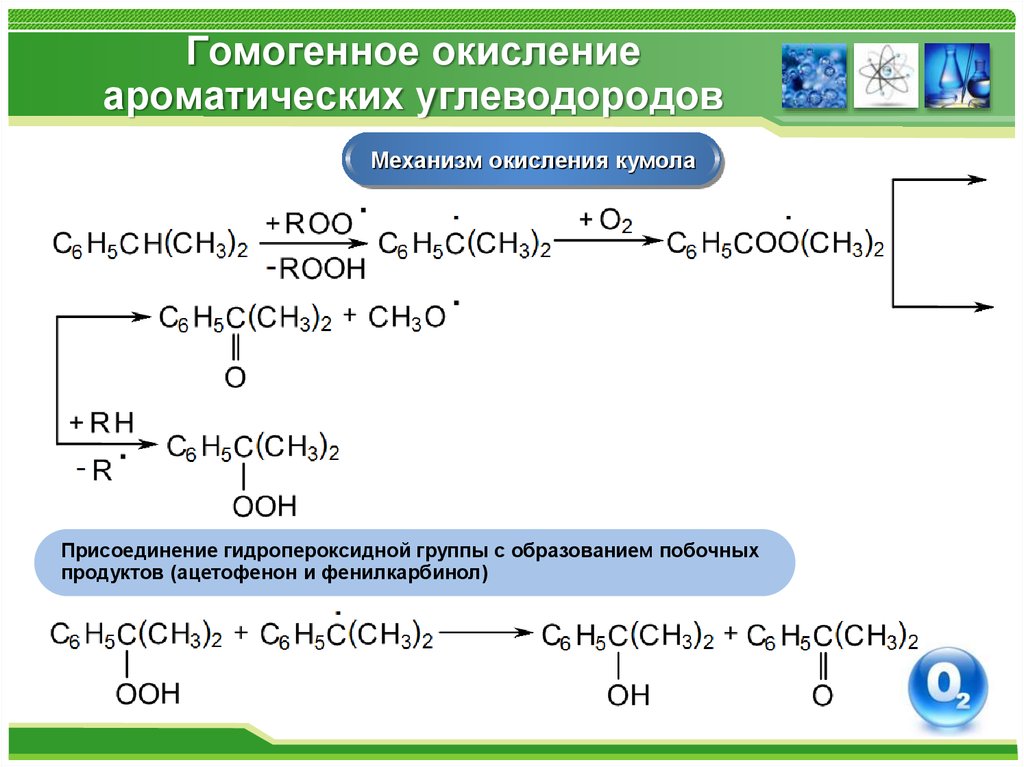
34. Гомогенное окисление ароматических углеводородов
Механизм окисления кумолаПрисоединение гидропероксидной группы с образованием побочных
продуктов (ацетофенон и фенилкарбинол)
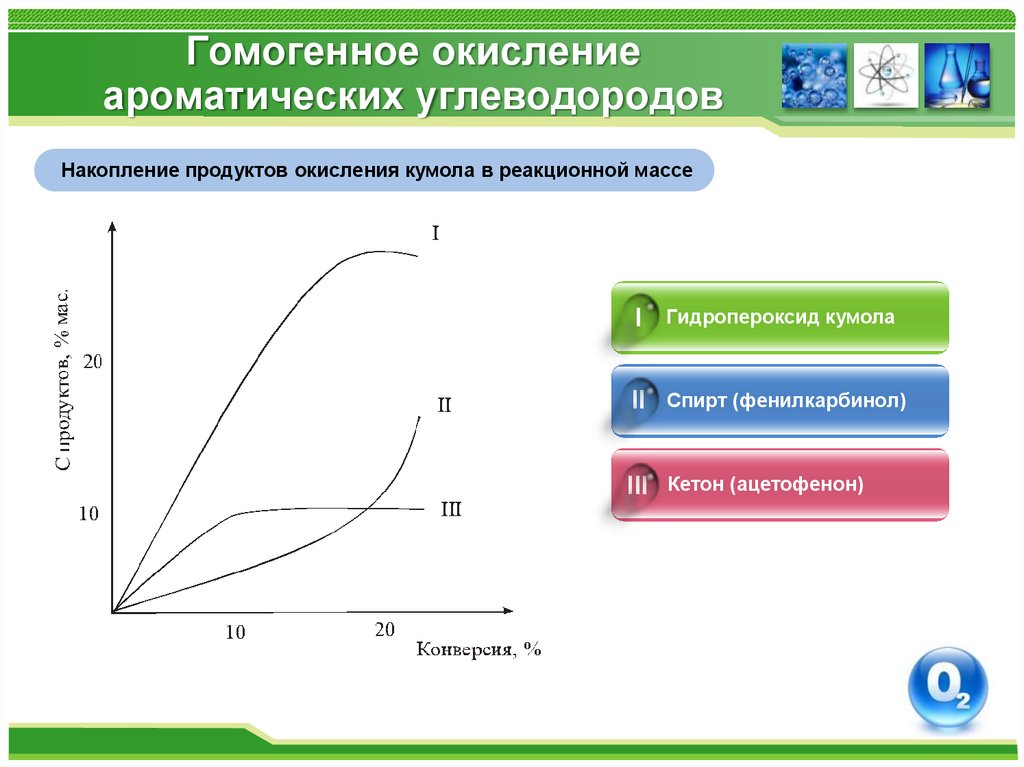
35. Гомогенное окисление ароматических углеводородов
Накопление продуктов окисления кумола в реакционной массеI
Гидропероксид кумола
II
Спирт (фенилкарбинол)
III
Кетон (ацетофенон)
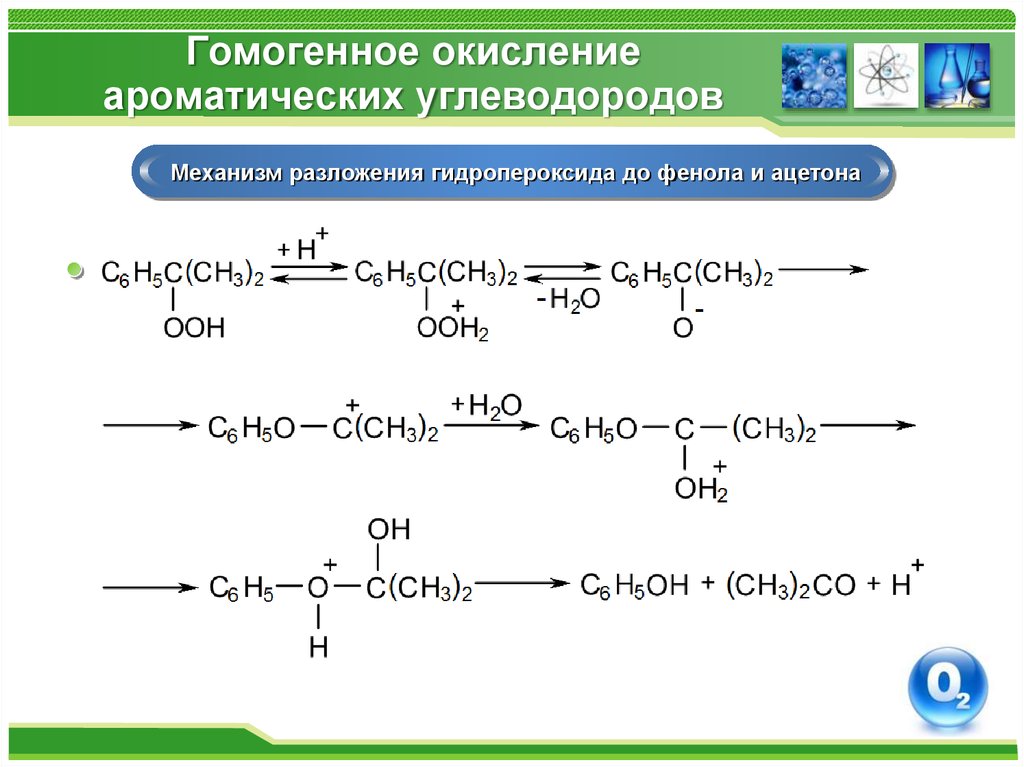
36. Гомогенное окисление ароматических углеводородов
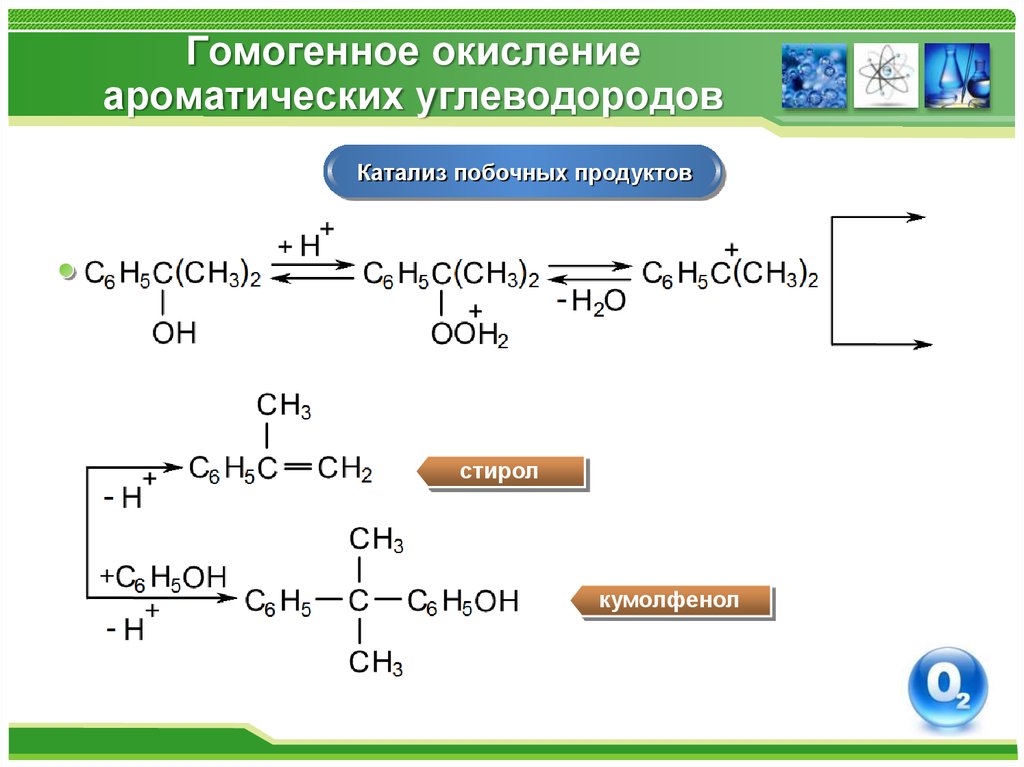
Механизм разложения гидропероксида до фенола и ацетона37. Гомогенное окисление ароматических углеводородов
Катализ побочных продуктовстирол
кумолфенол
38. Гомогенное окисление ароматических углеводородов
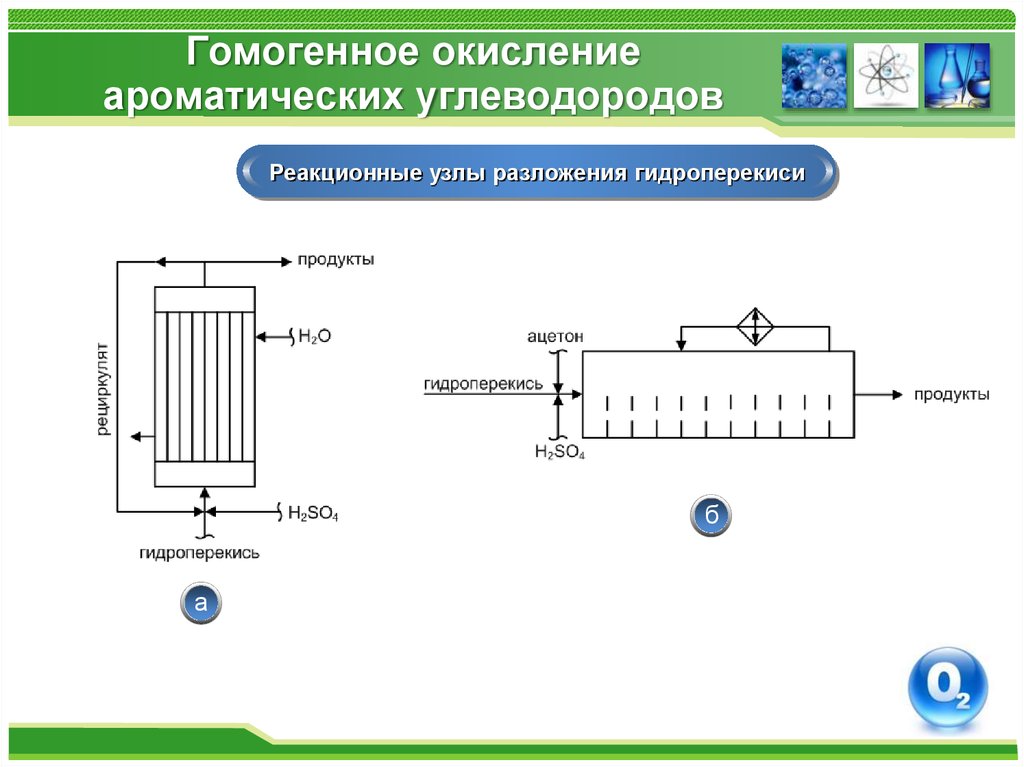
Реакционные узлы разложения гидроперекисиб
а
39. Гомогенное окисление ароматических углеводородов
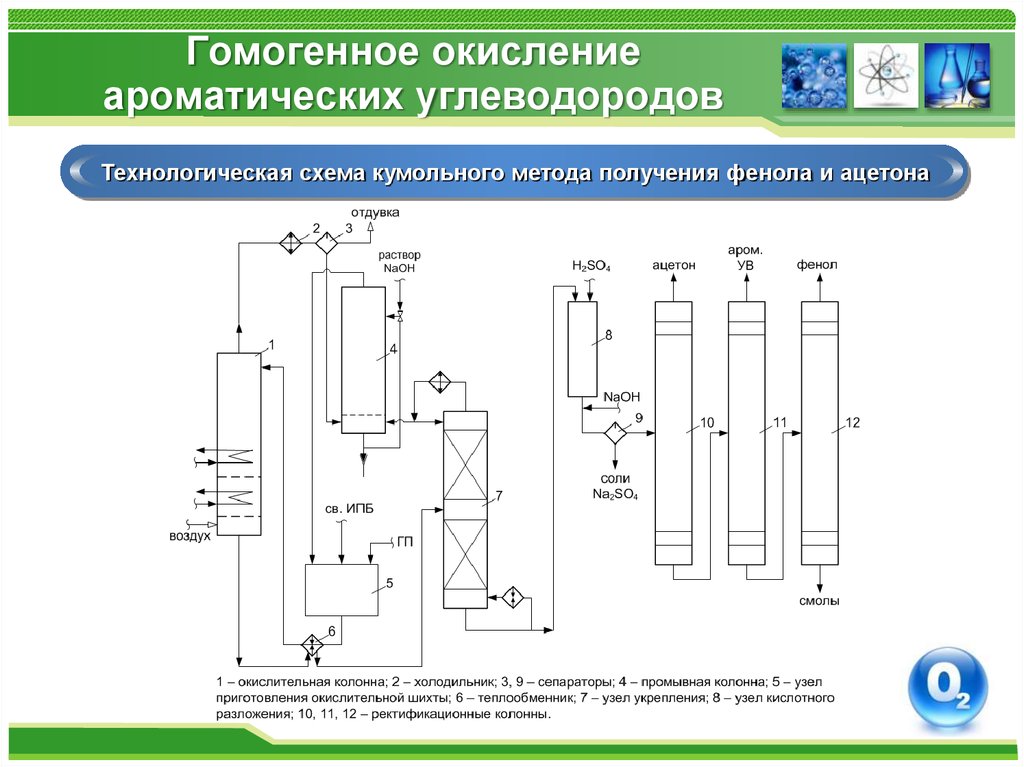
Технологическая схема кумольного метода получения фенола и ацетона40. Гомогенное окисление ароматических углеводородов
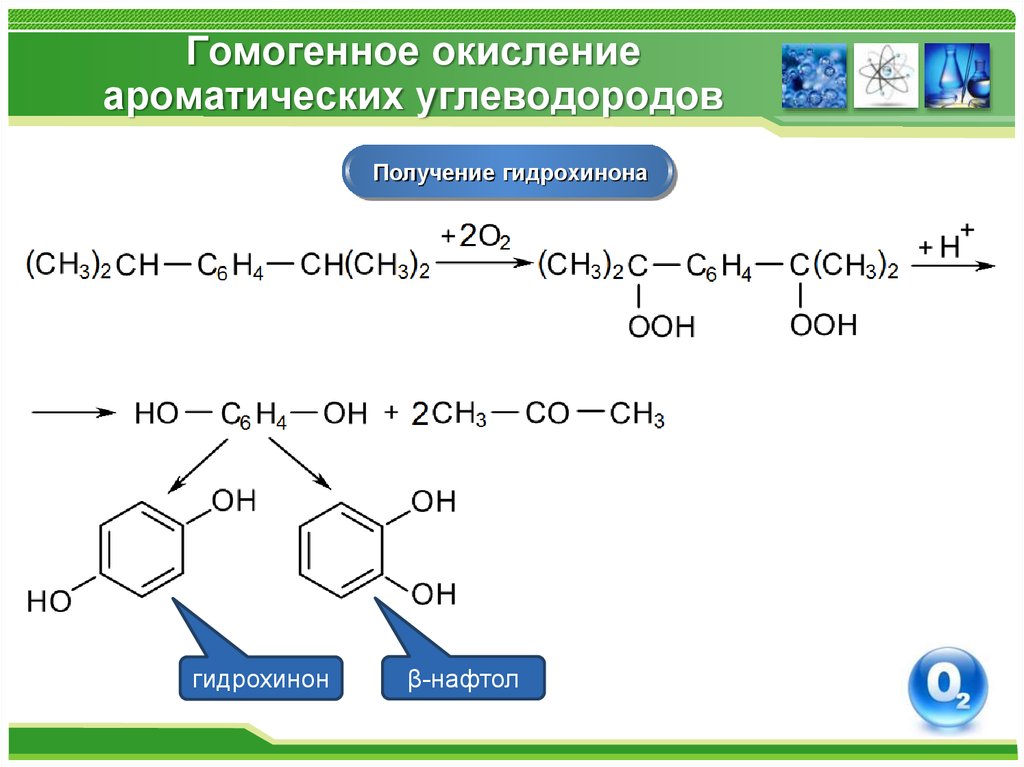
Получение гидрохинонагидрохинон
β-нафтол
41. Гомогенное окисление ароматических углеводородов
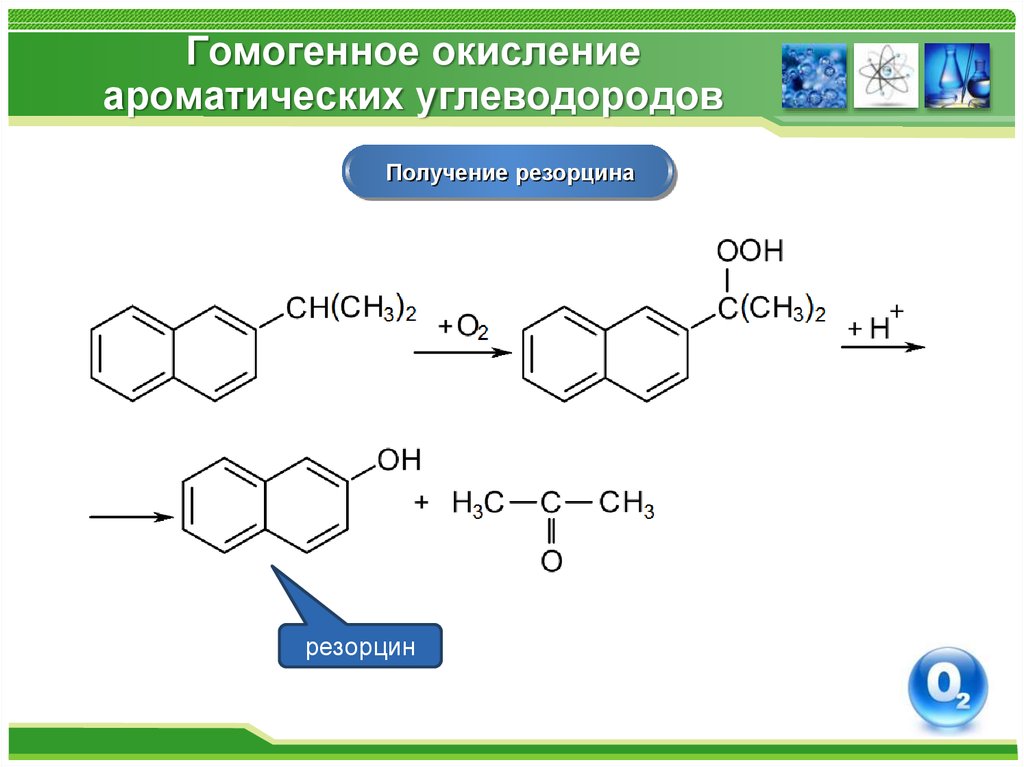
Получение резорцинарезорцин
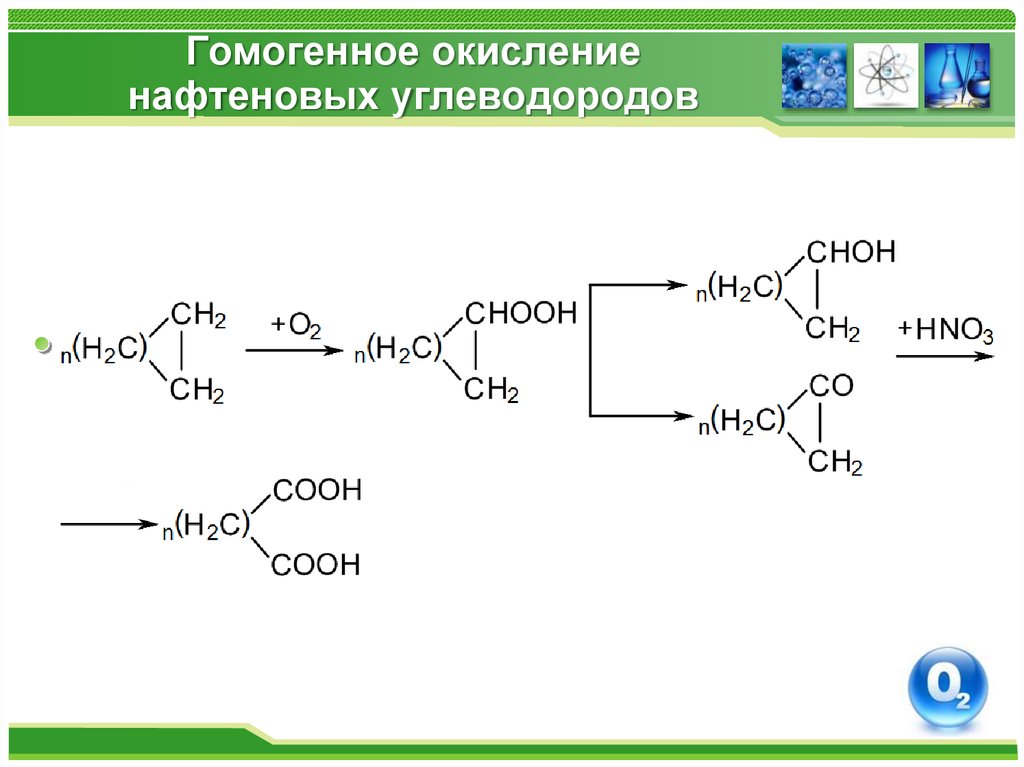
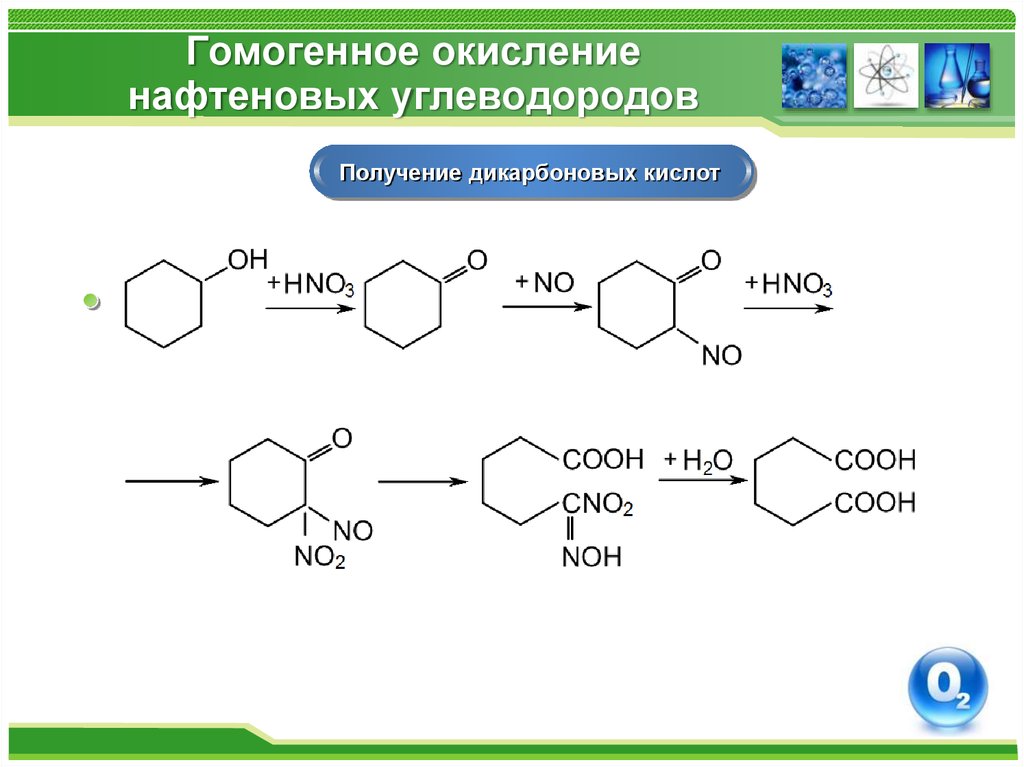
42. Гомогенное окисление нафтеновых углеводородов
43. Гомогенное окисление нафтеновых углеводородов
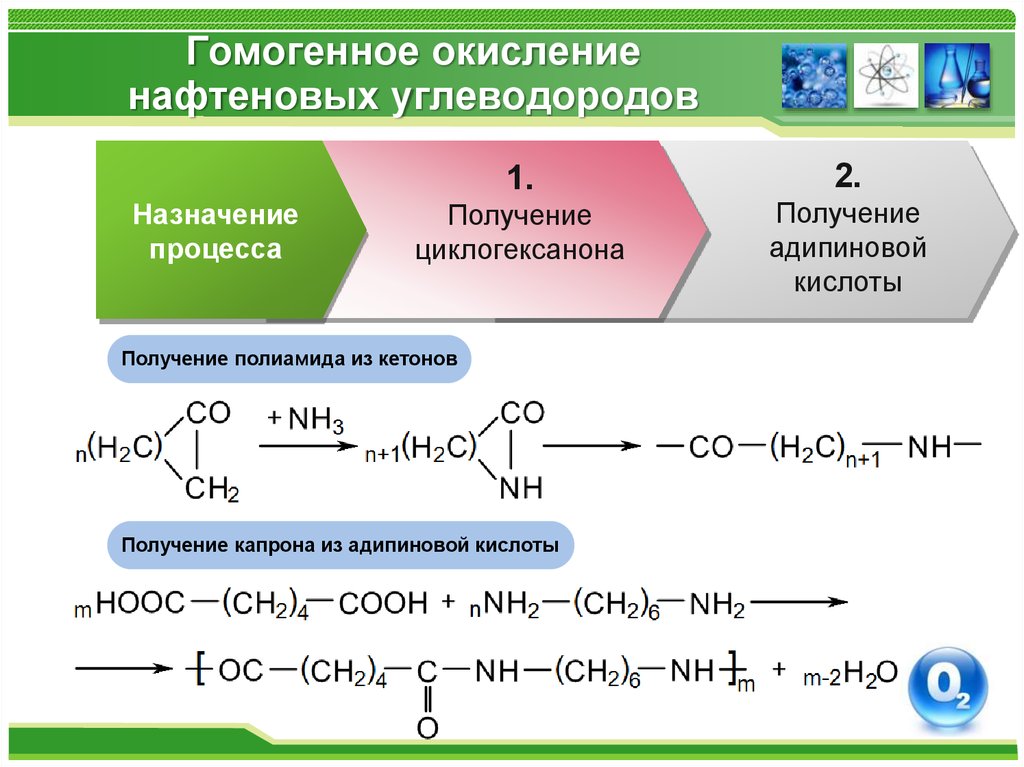
Назначениепроцесса
1.
2.
Получение
циклогексанона
Получение
адипиновой
кислоты
Получение полиамида из кетонов
Получение капрона из адипиновой кислоты
44. Гомогенное окисление нафтеновых углеводородов
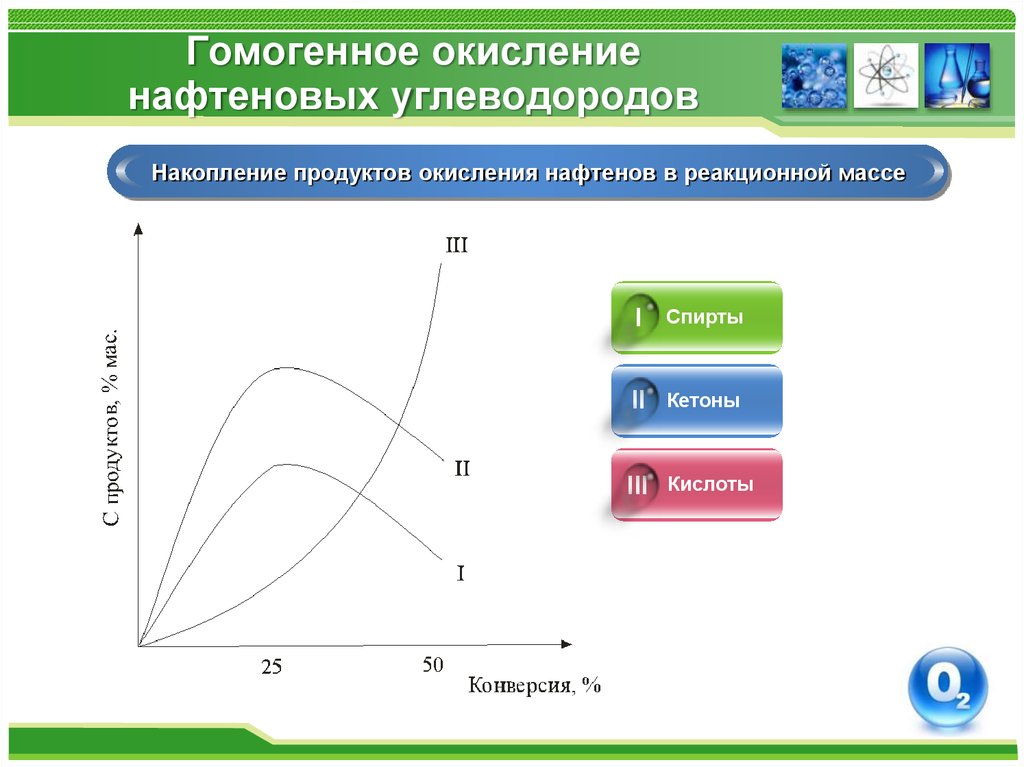
Накопление продуктов окисления нафтенов в реакционной массеI
Спирты
II
Кетоны
III
Кислоты
45. Гомогенное окисление нафтеновых углеводородов
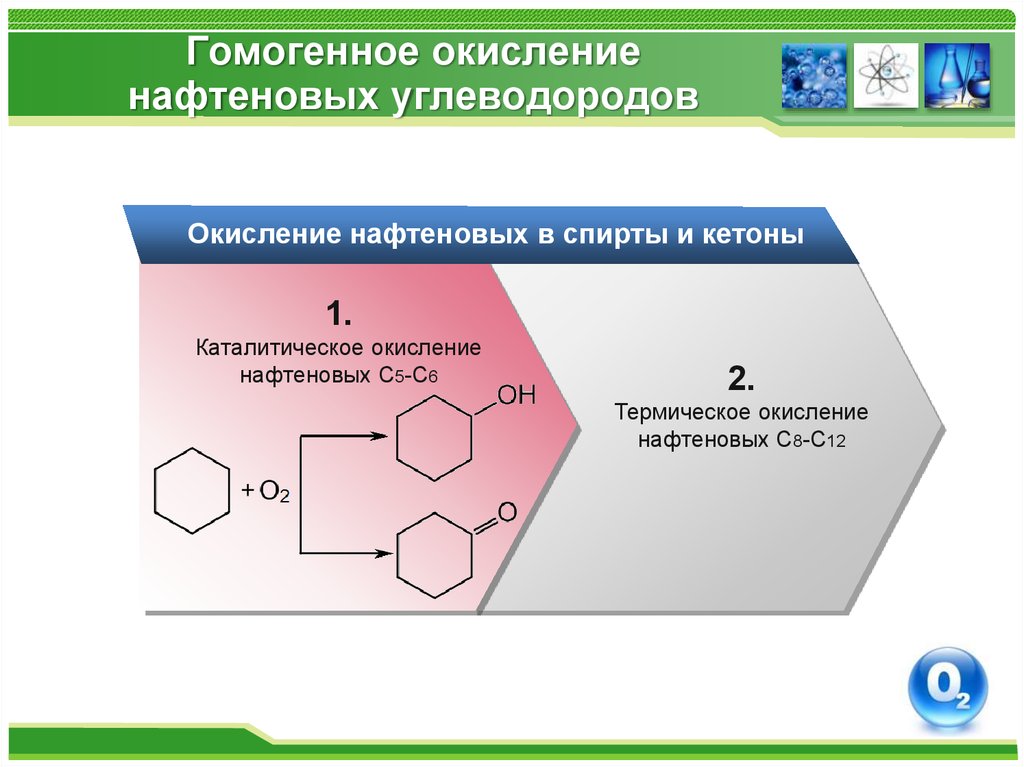
Окисление нафтеновых в спирты и кетоны1.
Каталитическое окисление
нафтеновых С5-С6
2.
Термическое окисление
нафтеновых С8-С12
46. Гомогенное окисление нафтеновых углеводородов
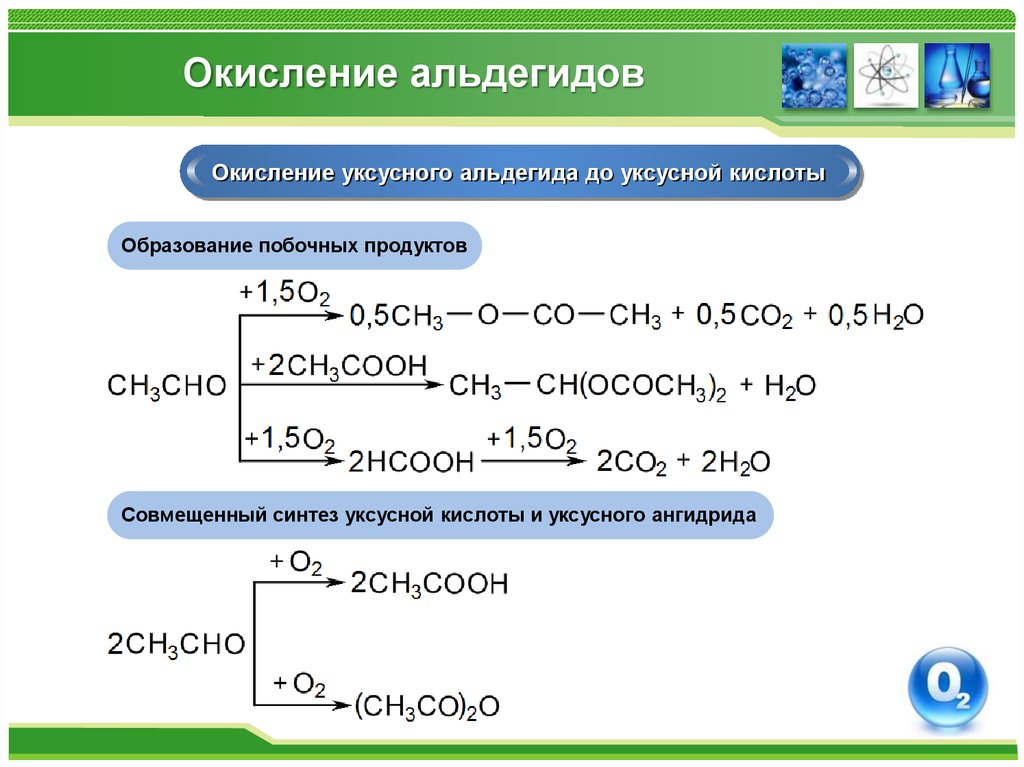
Получение дикарбоновых кислот47. Окисление альдегидов
Окисление уксусного альдегида до уксусной кислотыОбразование побочных продуктов
Совмещенный синтез уксусной кислоты и уксусного ангидрида
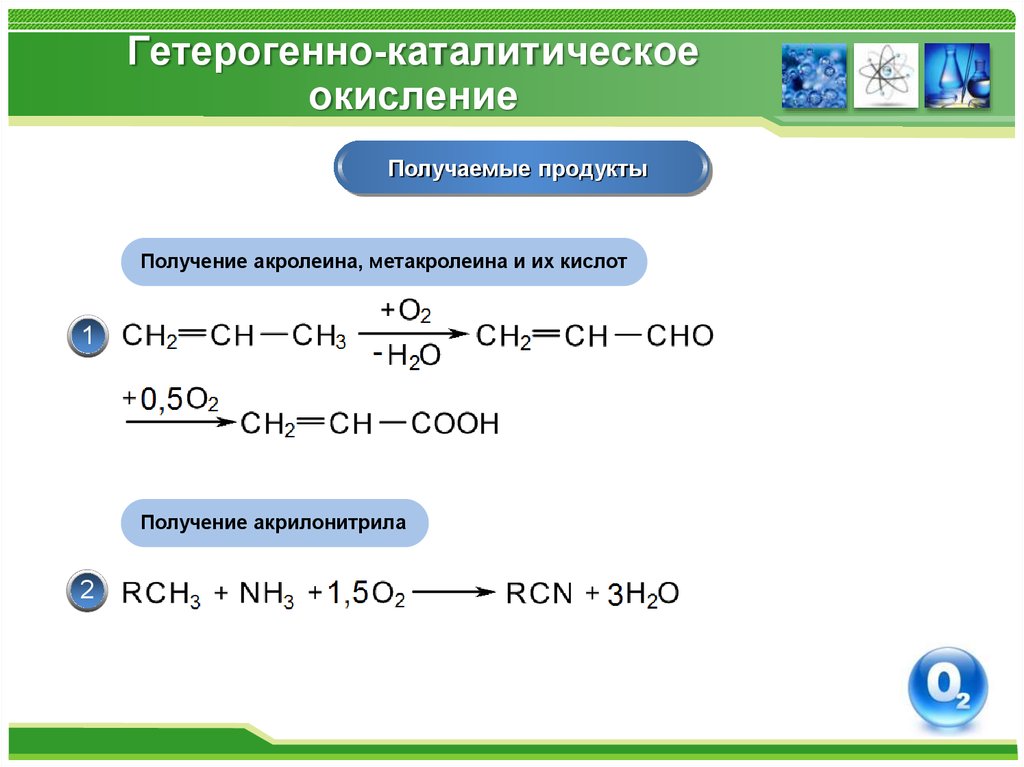
48. Гетерогенно-каталитическое окисление
Получаемые продуктыПолучение акролеина, метакролеина и их кислот
1
Получение акрилонитрила
2
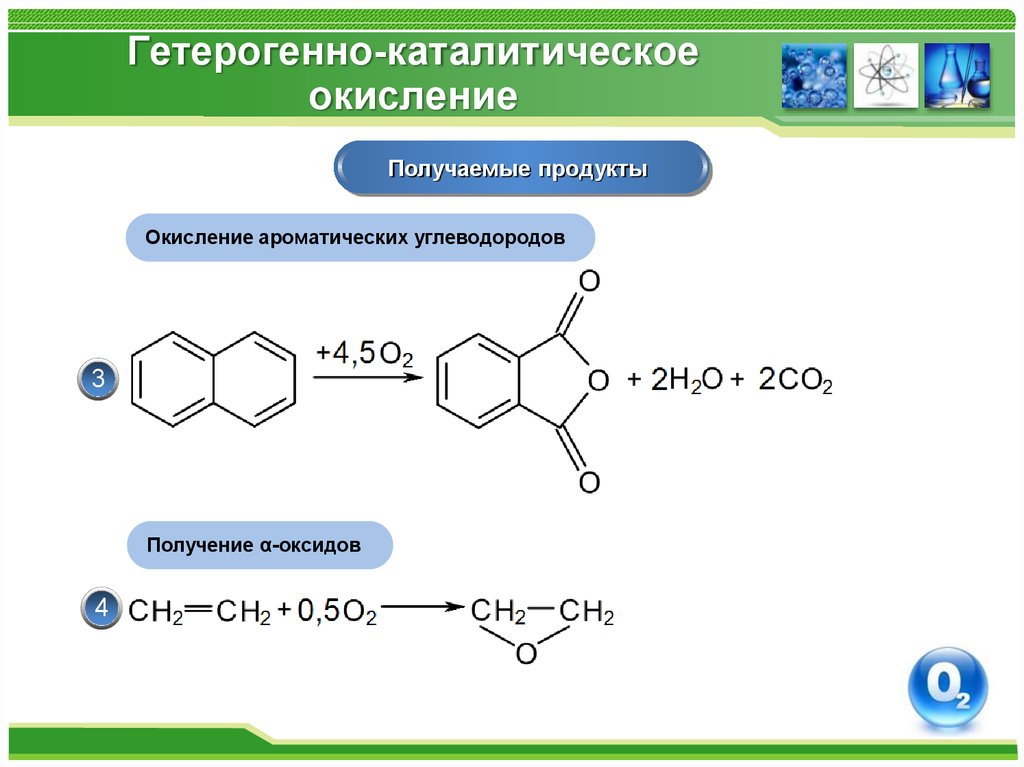
49. Гетерогенно-каталитическое окисление
Получаемые продуктыОкисление ароматических углеводородов
3
Получение α-оксидов
4
50. Гетерогенно-каталитическое окисление
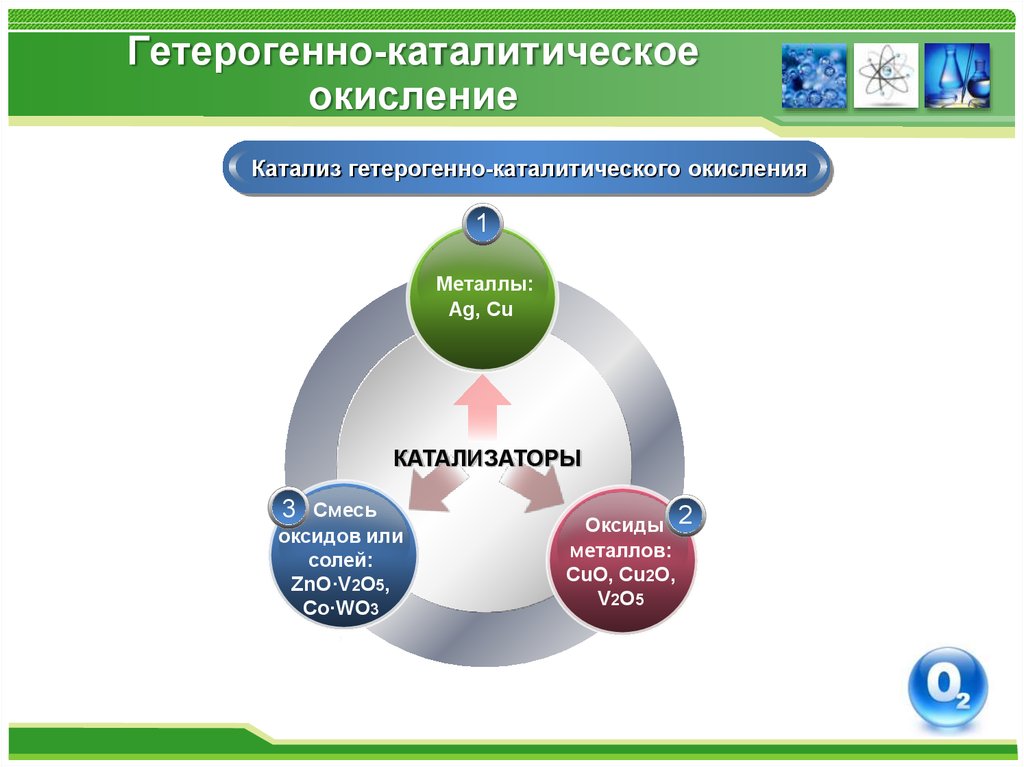
Катализ гетерогенно-каталитического окисления1
Металлы:
Ag, Cu
КАТАЛИЗАТОРЫ
Смесь
оксидов или
солей:
ZnO·V2O5,
Co·WO3
,
3
Оксиды 2
металлов:
CuO, Cu2O,
V2O5
51. Гетерогенно-каталитическое окисление
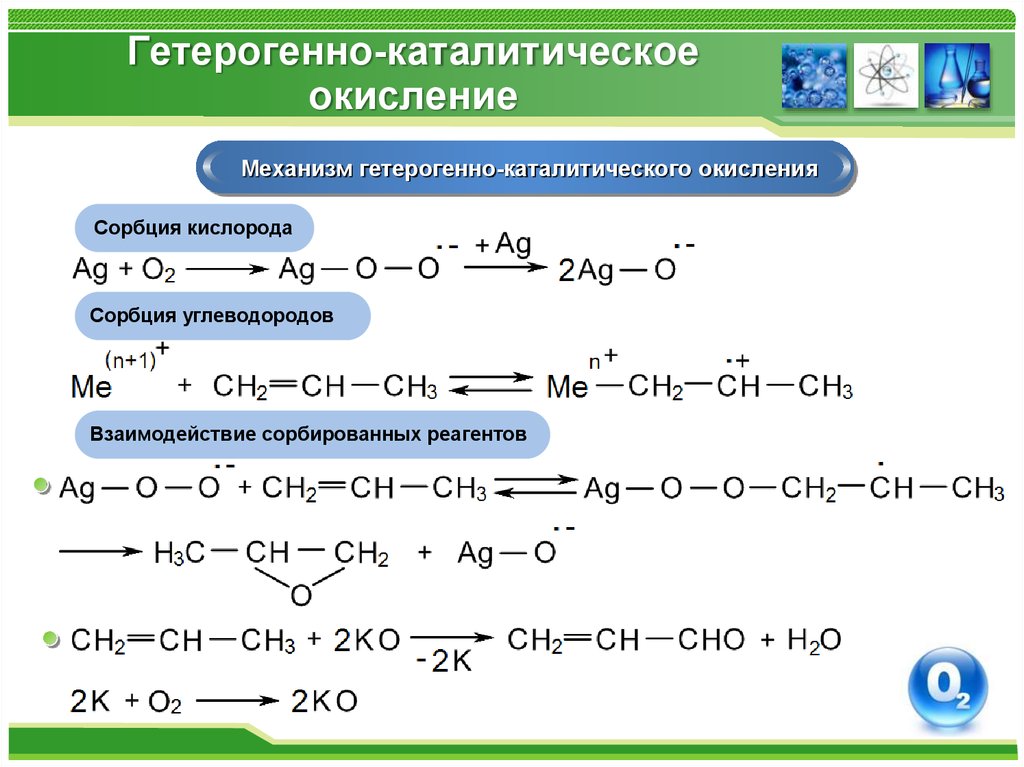
Механизм гетерогенно-каталитического окисленияСорбция кислорода
Сорбция углеводородов
Взаимодействие сорбированных реагентов
52. Гетерогенно-каталитическое окисление
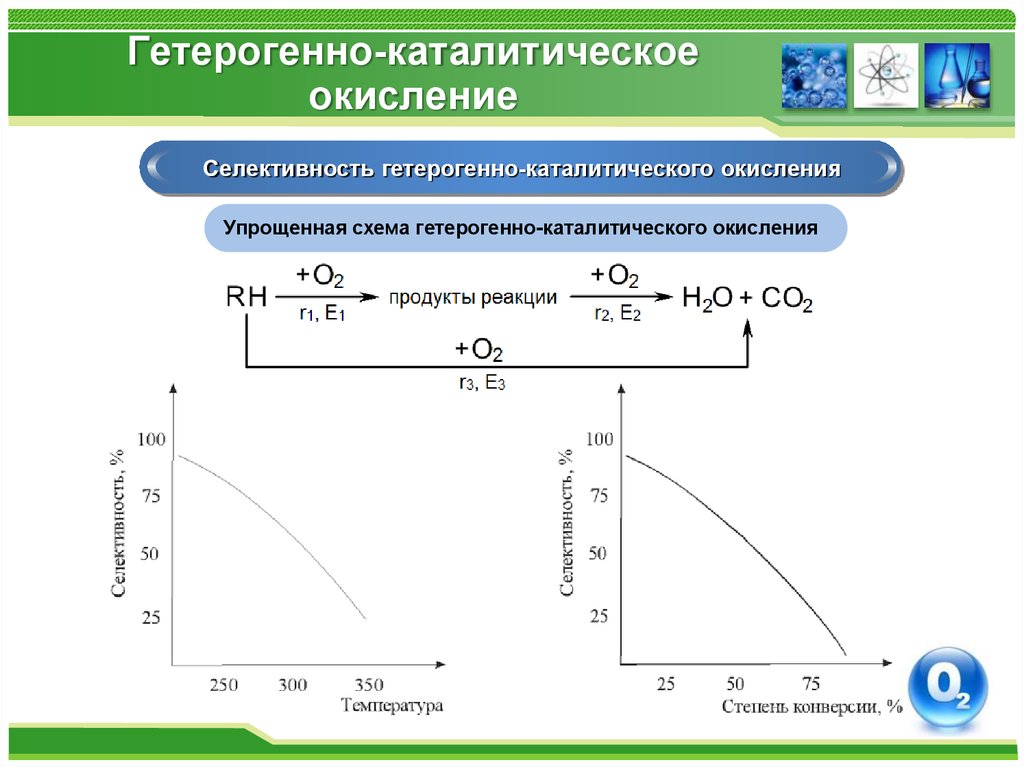
Селективность гетерогенно-каталитического окисленияУпрощенная схема гетерогенно-каталитического окисления
53. Гетерогенно-каталитическое окисление
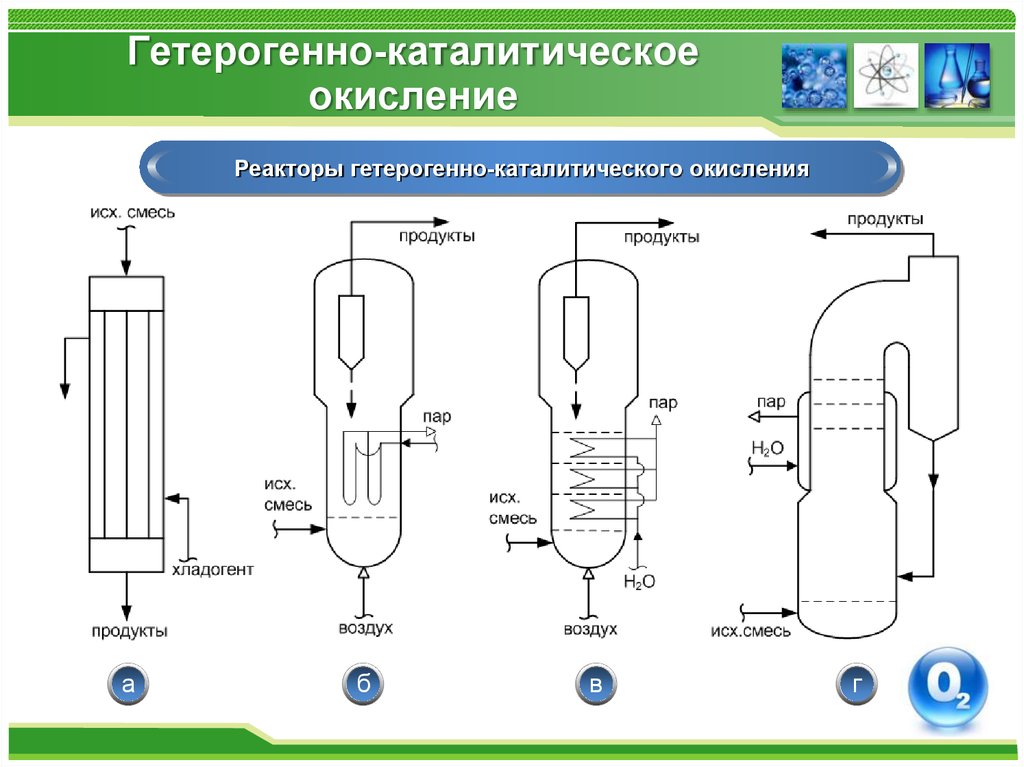
Реакторы гетерогенно-каталитического окисленияа
б
в
г
54. Гетерогенно-каталитическое окисление
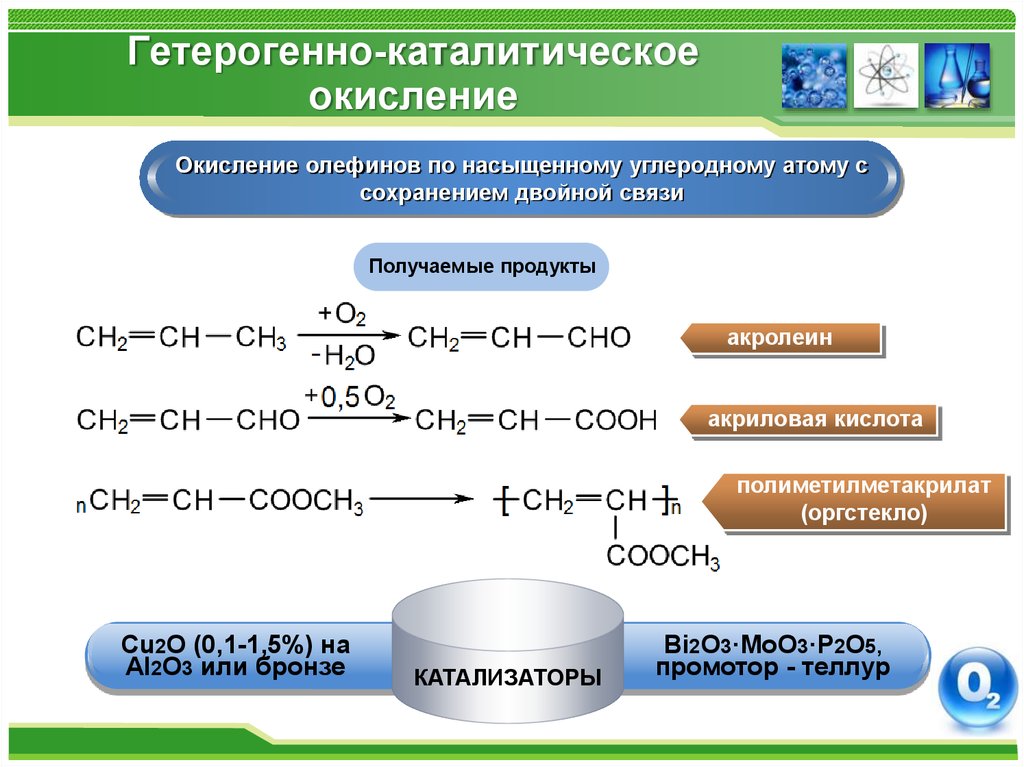
Окисление олефинов по насыщенному углеродному атому ссохранением двойной связи
Получаемые продукты
акролеин
акриловая кислота
полиметилметакрилат
(оргстекло)
Cu2O (0,1-1,5%) на
Al2O3 или бронзе
КАТАЛИЗАТОРЫ
Bi2O3·MoO3·P2O5,
промотор - теллур
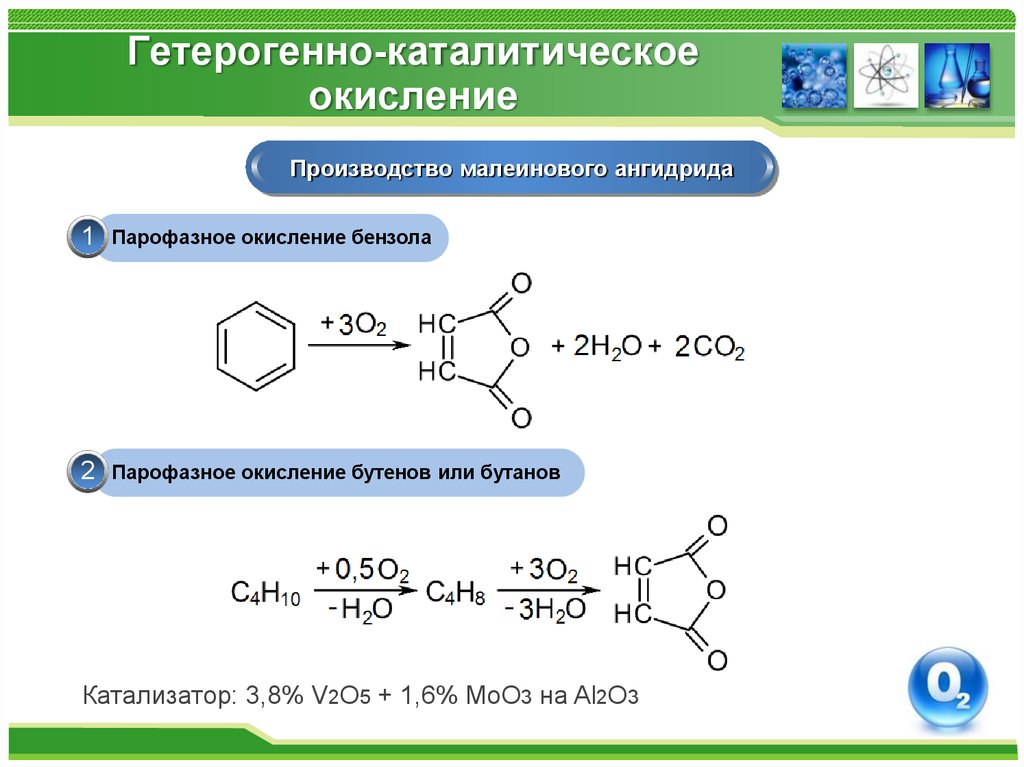
55. Гетерогенно-каталитическое окисление
Производство малеинового ангидрида1
Парофазное окисление бензола
2
Парофазное окисление бутенов или бутанов
Катализатор: 3,8% V2O5 + 1,6% MoO3 на Al2O3
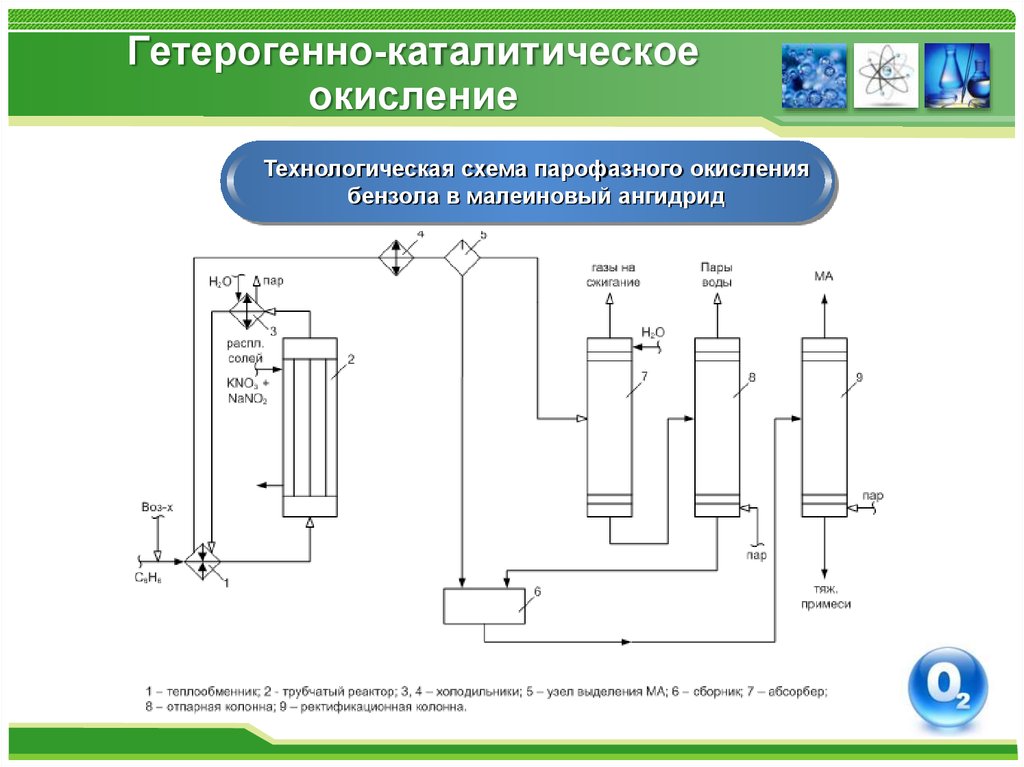
56. Гетерогенно-каталитическое окисление
Технологическая схема парофазного окислениябензола в малеиновый ангидрид
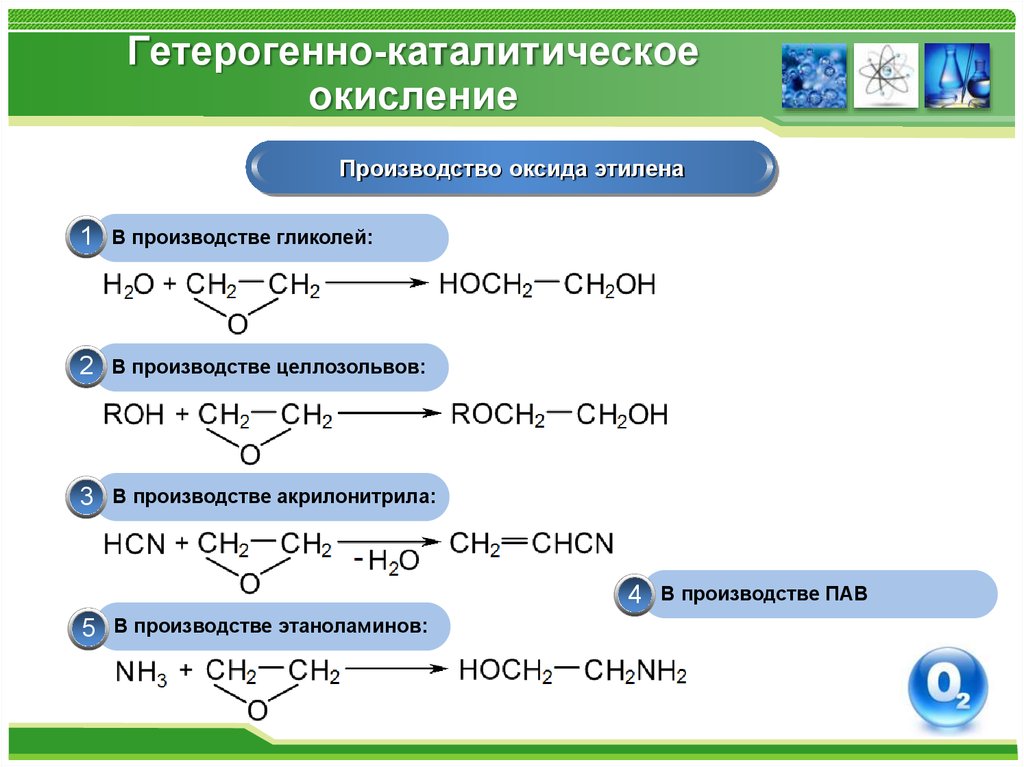
57. Гетерогенно-каталитическое окисление
Производство оксида этилена1
В производстве гликолей:
2
В производстве целлозольвов:
3
В производстве акрилонитрила:
4
5
В производстве этаноламинов:
В производстве ПАВ
58. Гетерогенно-каталитическое окисление
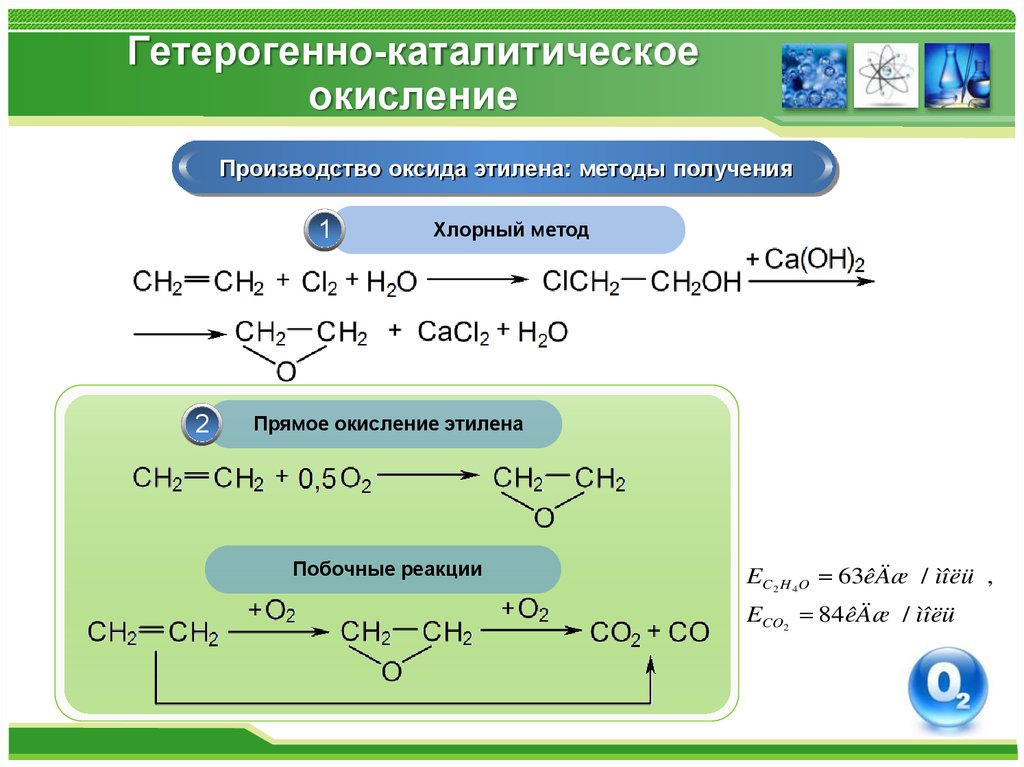
Производство оксида этилена: методы получения1
2
Хлорный метод
Прямое окисление этилена
Побочные реакции
EC2 H 4O 63êÄæ / ìîëü ,
ECO2 84êÄæ / ìîëü
59. Гетерогенно-каталитическое окисление
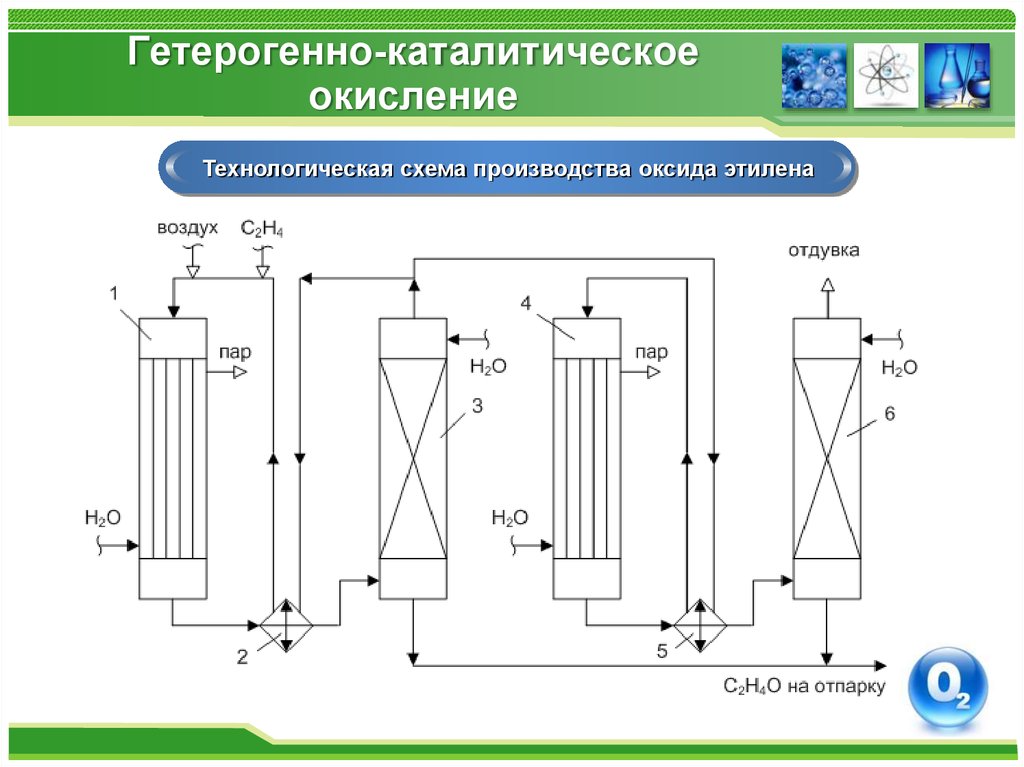
Технологическая схема производства оксида этилена60. Синтезы на основе оксида углерода
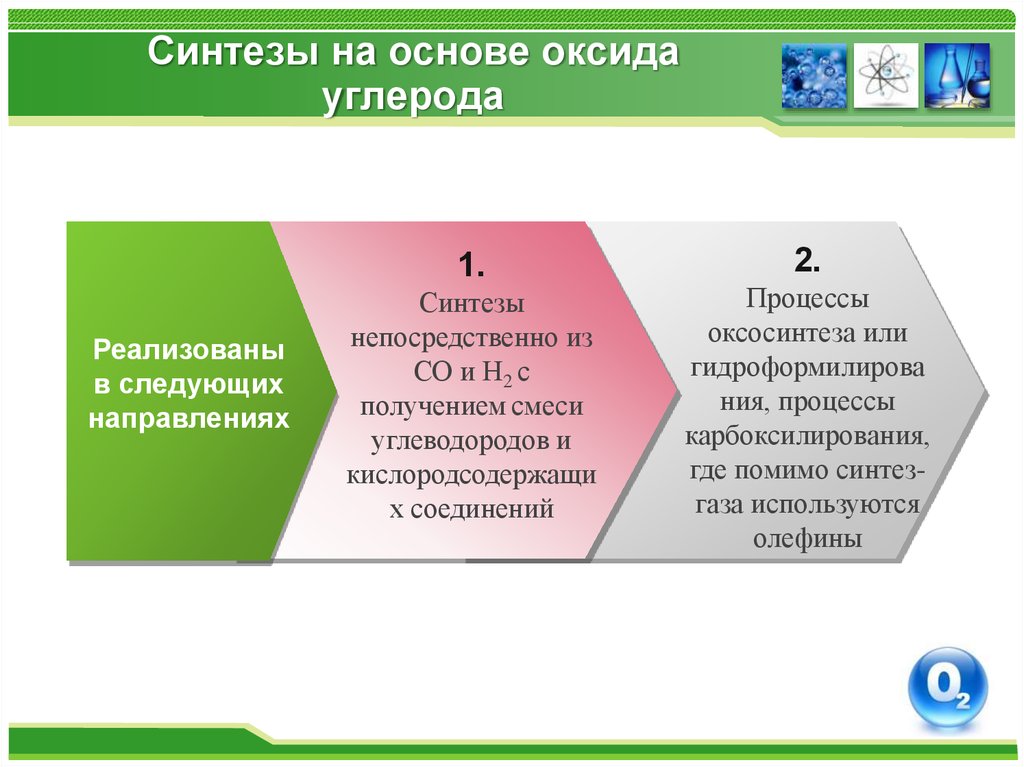
1.Реализованы
в следующих
направлениях
Синтезы
непосредственно из
СО и Н2 с
получением смеси
углеводородов и
кислородсодержащи
х соединений
2.
Процессы
оксосинтеза или
гидроформилирова
ния, процессы
карбоксилирования,
где помимо синтезгаза используются
олефины
61. Синтезы на основе оксида углерода
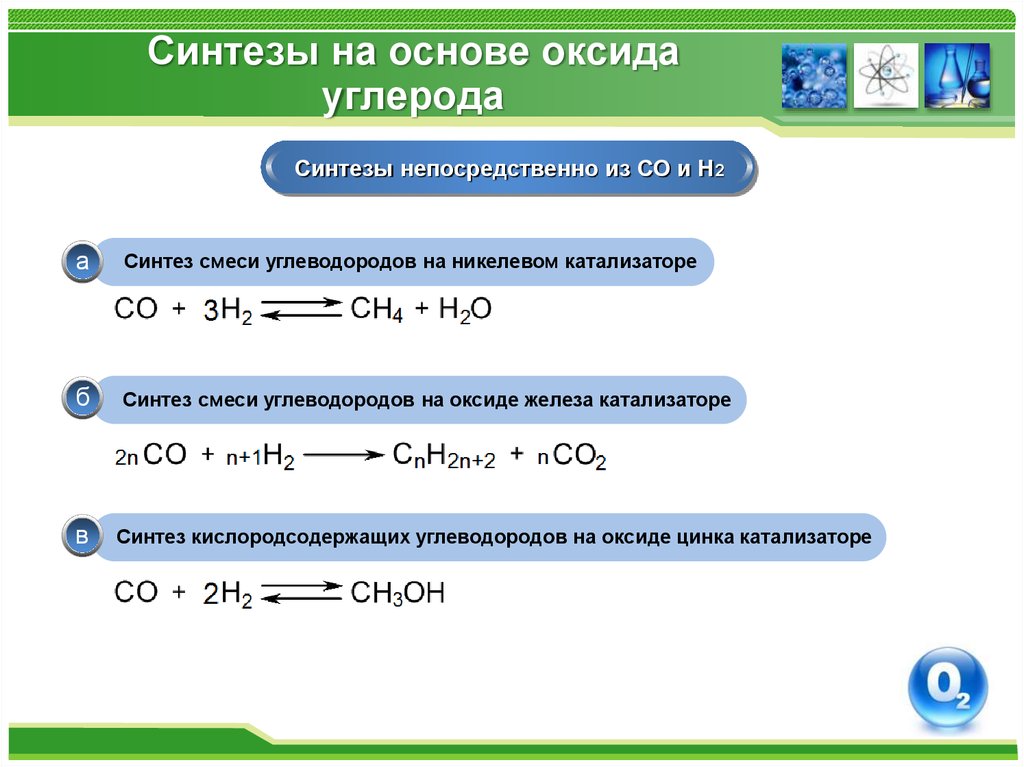
Синтезы непосредственно из СО и Н2а
Синтез смеси углеводородов на никелевом катализаторе
б
Синтез смеси углеводородов на оксиде железа катализаторе
в
Синтез кислородсодержащих углеводородов на оксиде цинка катализаторе
62. Синтезы на основе оксида углерода
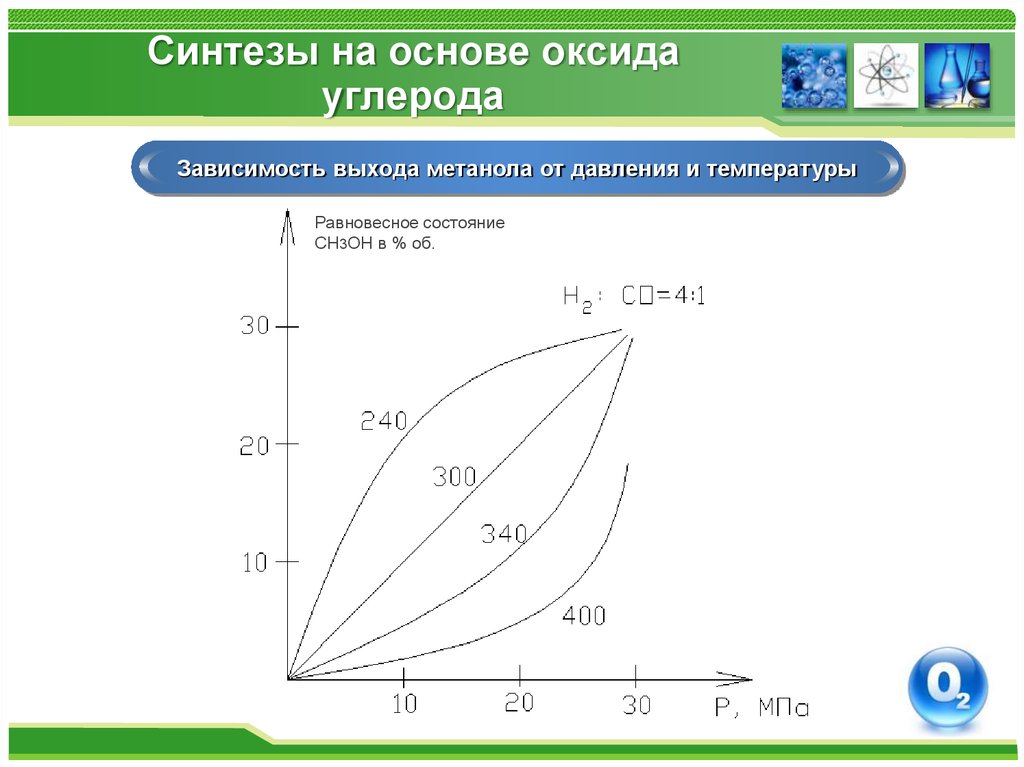
Зависимость выхода метанола от давления и температурыРавновесное состояние
СН3ОН в % об.
63. Синтезы на основе оксида углерода
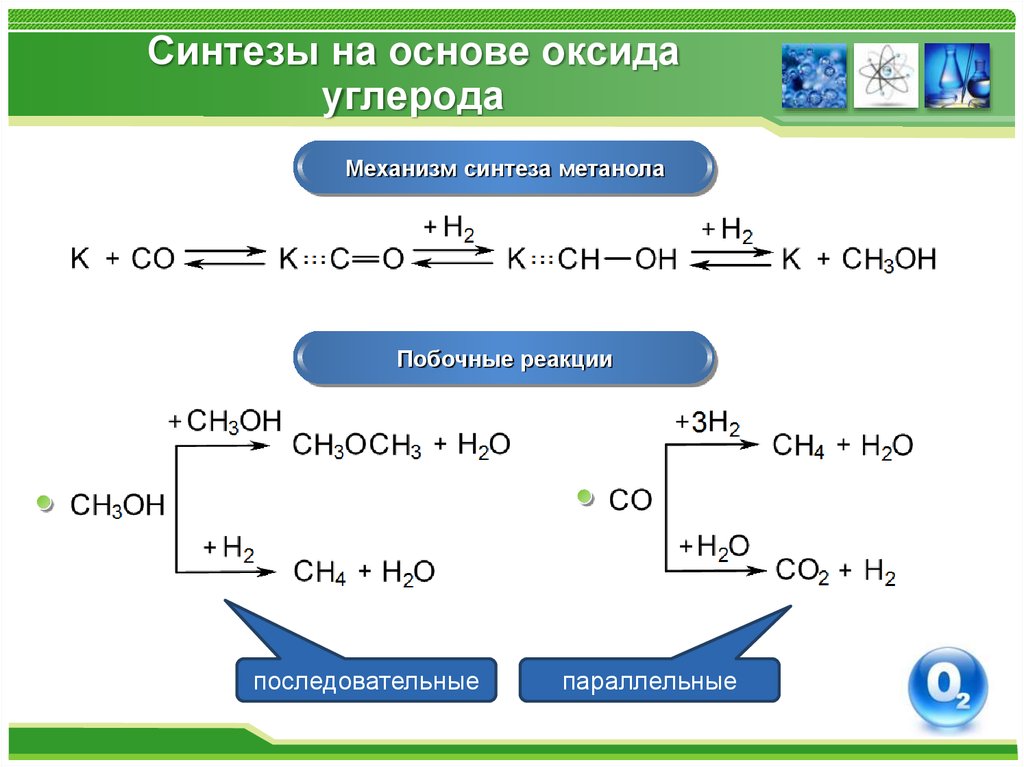
Механизм синтеза метанолаПобочные реакции
последовательные
параллельные
64. Синтезы на основе оксида углерода
Считается, что метанол получается в реакционнойзоне не из СО, а из СО2, который образуется при
взаимодействии с водой которая выделяется из
метанола:
65. Синтезы на основе оксида углерода
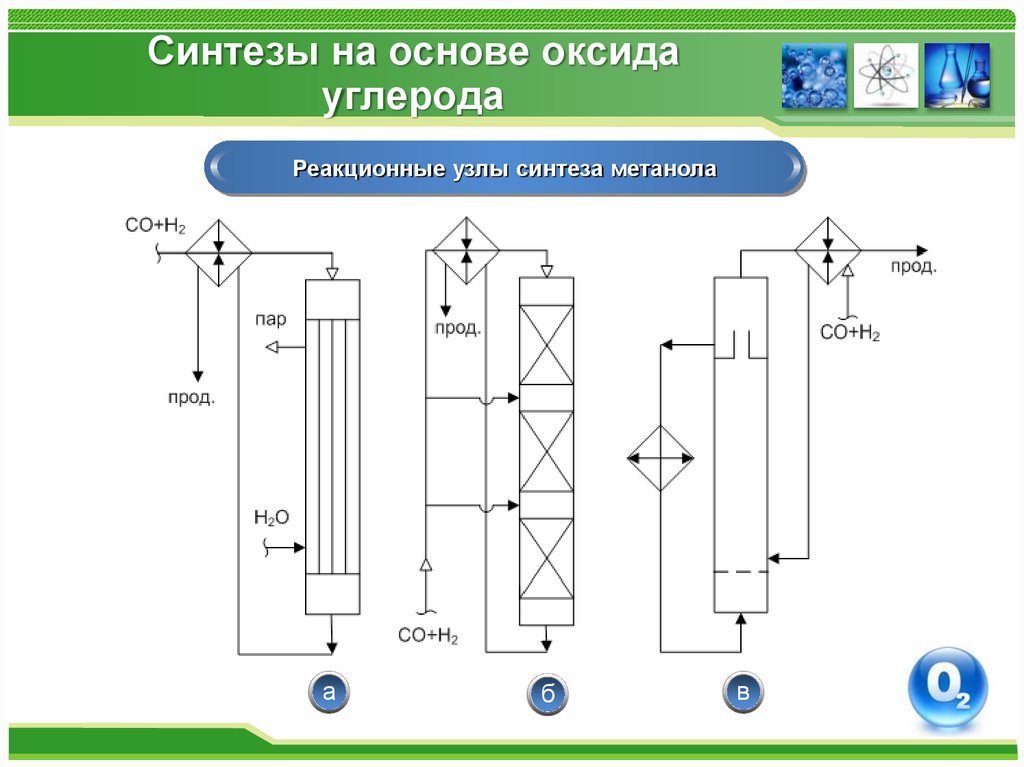
Реакционные узлы синтеза метанолаа
б
в
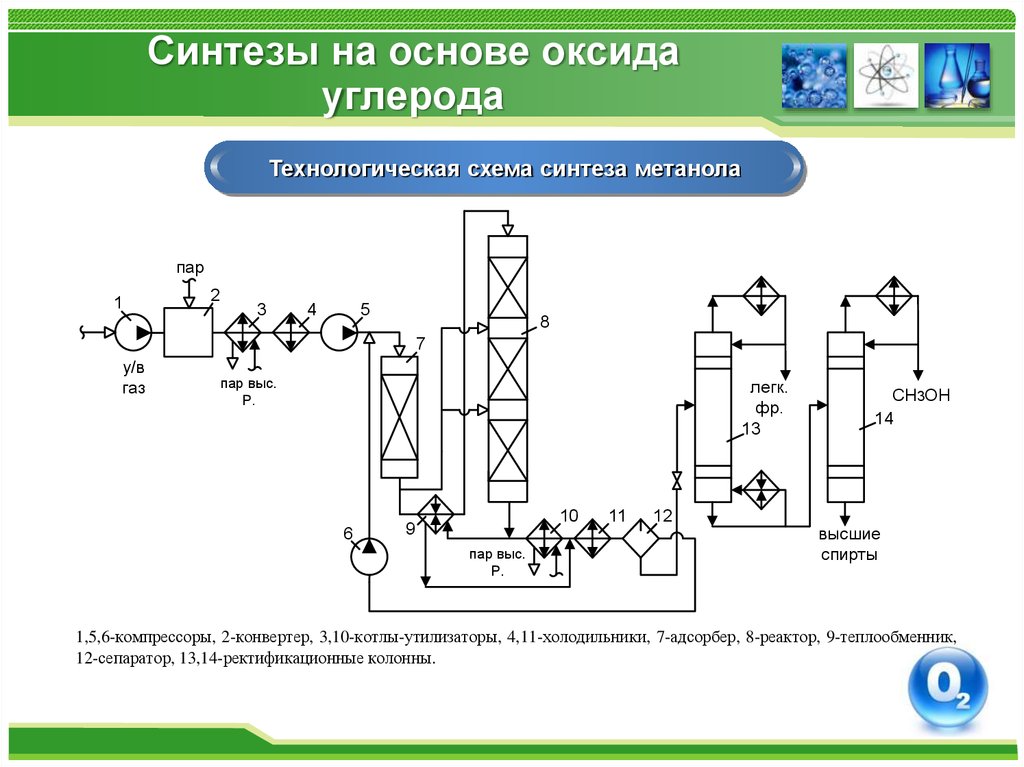
66. Синтезы на основе оксида углерода
Технологическая схема синтеза метанолапар
1
2
3
4
5
8
7
у/в
газ
пар выс.
Р.
легк.
фр.
13
6
10
9
пар выс.
Р.
11
12
СН3ОН
14
высшие
спирты
1,5,6-компрессоры, 2-конвертер, 3,10-котлы-утилизаторы, 4,11-холодильники, 7-адсорбер, 8-реактор, 9-теплообменник,
12-сепаратор, 13,14-ректификационные колонны.
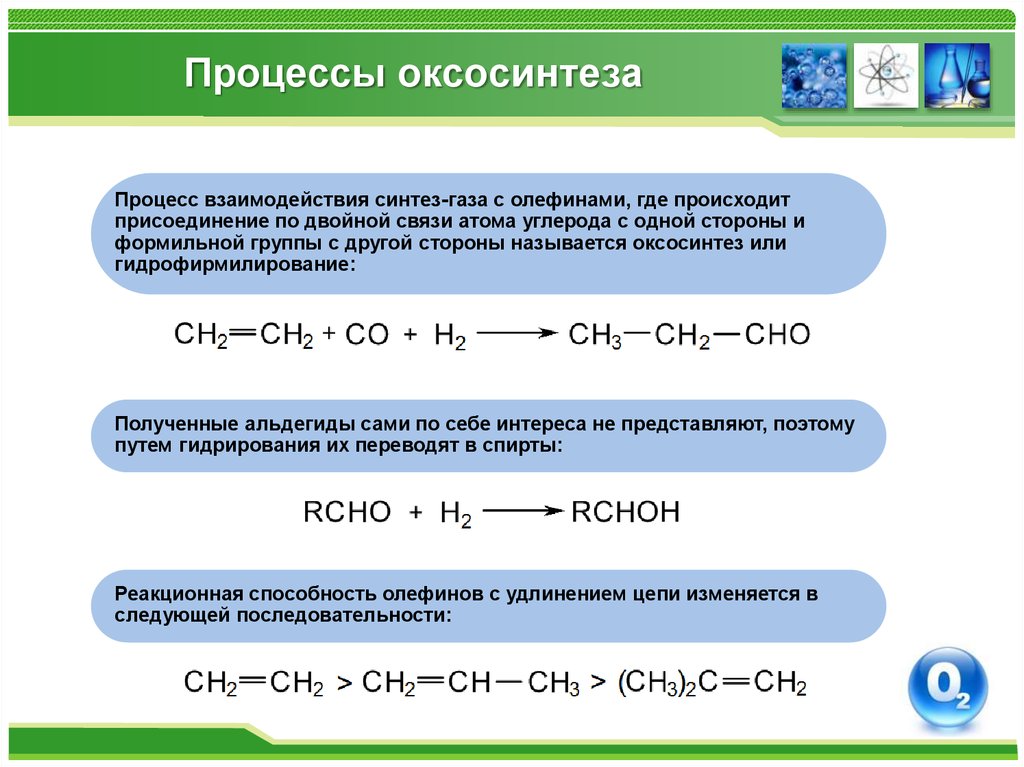
67. Процессы оксосинтеза
Процесс взаимодействия синтез-газа с олефинами, где происходитприсоединение по двойной связи атома углерода с одной стороны и
формильной группы с другой стороны называется оксосинтез или
гидрофирмилирование:
Полученные альдегиды сами по себе интереса не представляют, поэтому
путем гидрирования их переводят в спирты:
Реакционная способность олефинов с удлинением цепи изменяется в
следующей последовательности:
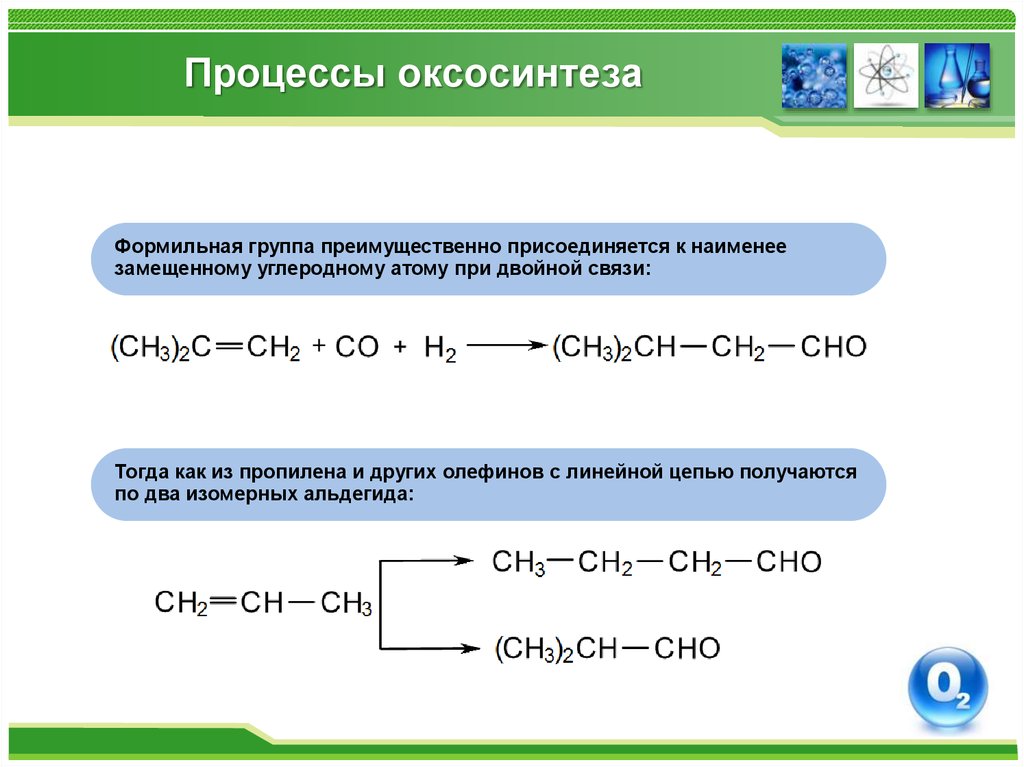
68. Процессы оксосинтеза
Формильная группа преимущественно присоединяется к наименеезамещенному углеродному атому при двойной связи:
Тогда как из пропилена и других олефинов с линейной цепью получаются
по два изомерных альдегида:
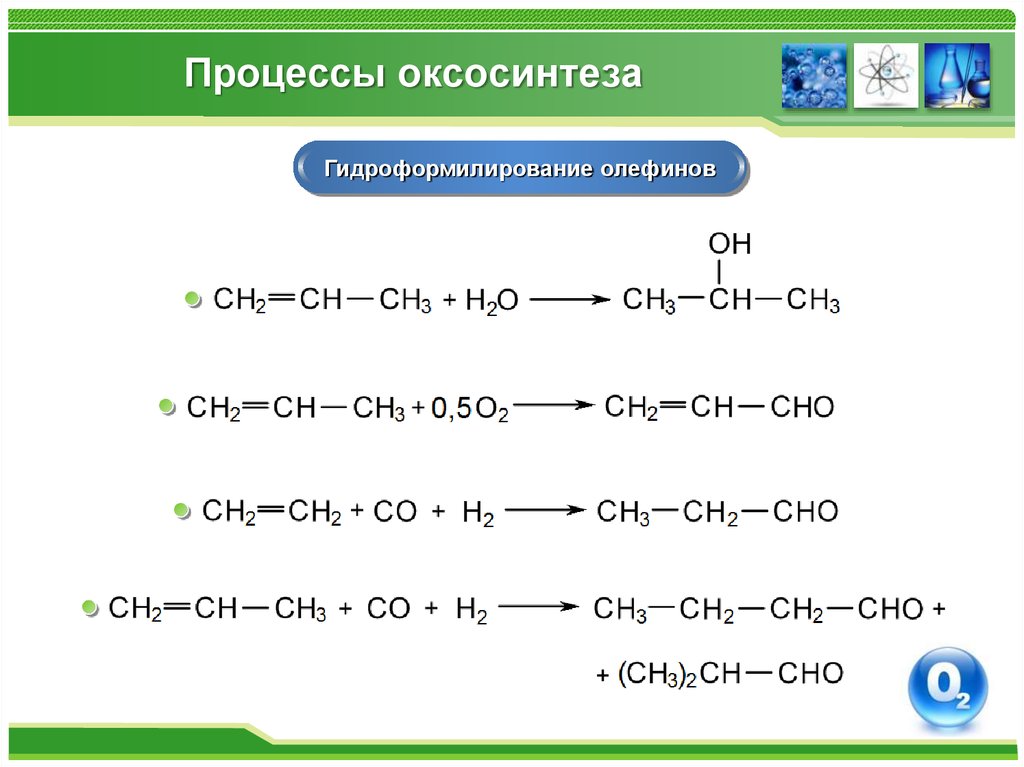
69. Процессы оксосинтеза
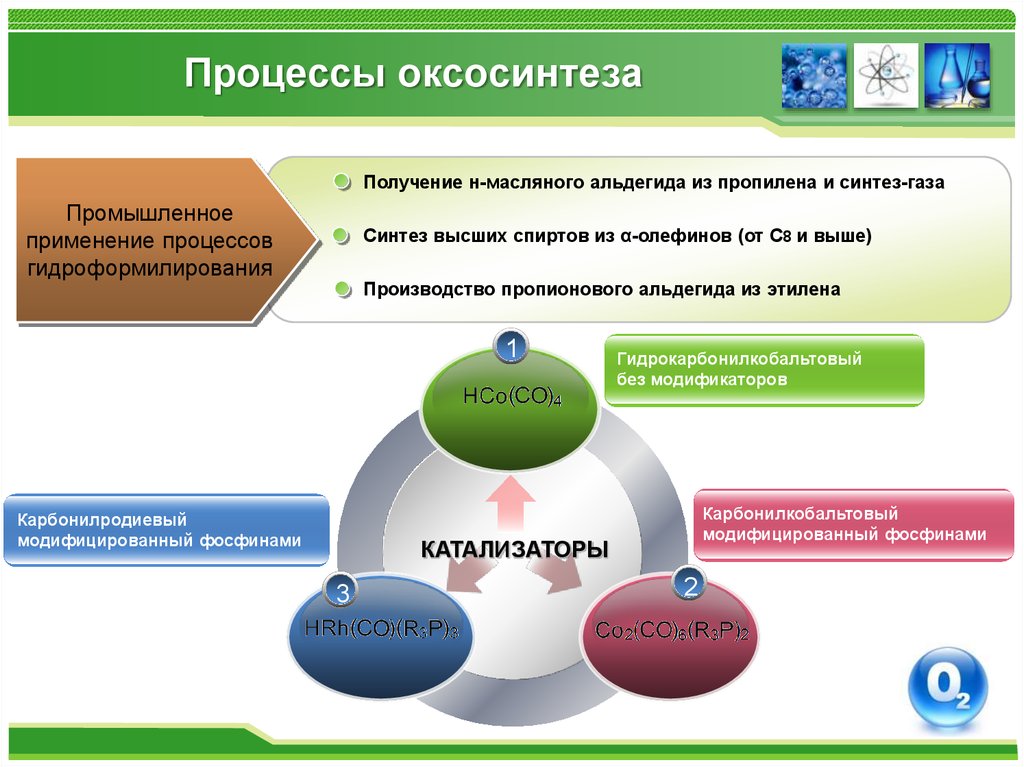
Гидроформилирование олефинов70. Процессы оксосинтеза
Получение н-масляного альдегида из пропилена и синтез-газаПромышленное
применение процессов
гидроформилирования
Синтез высших спиртов из α-олефинов (от С8 и выше)
Производство пропионового альдегида из этилена
1
Карбонилродиевый
модифицированный фосфинами
Гидрокарбонилкобальтовый
без модификаторов
Карбонилкобальтовый
модифицированный фосфинами
КАТАЛИЗАТОРЫ
3
2
71. Процессы оксосинтеза
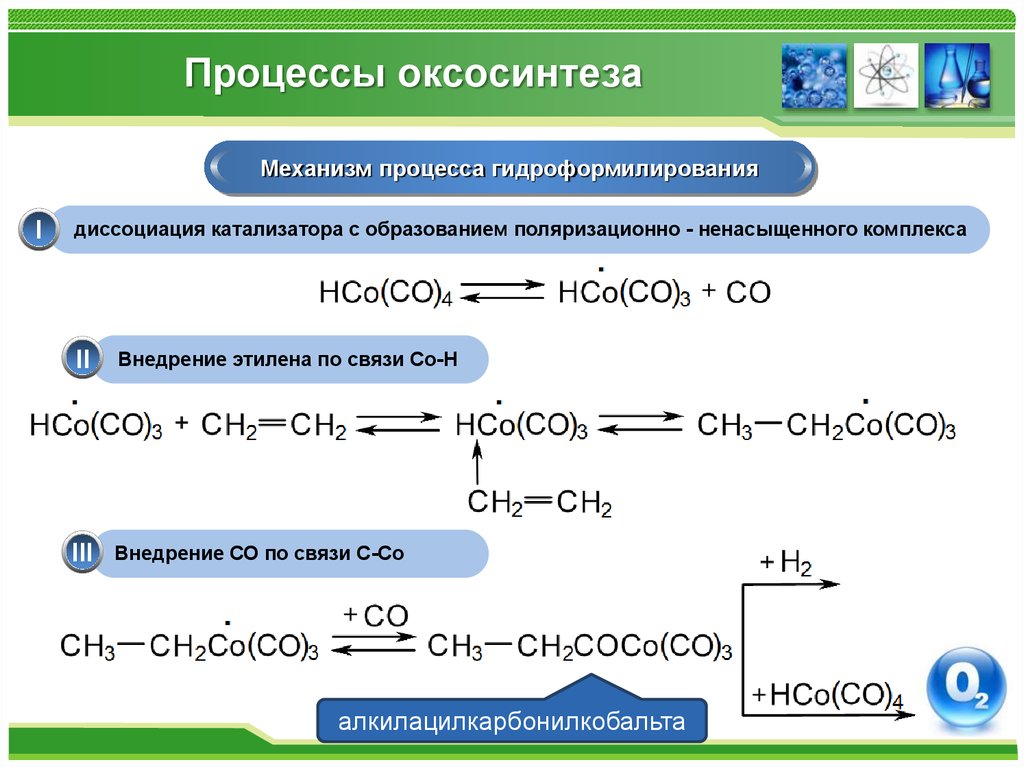
Механизм процесса гидроформилированияI
диссоциация катализатора с образованием поляризационно - ненасыщенного комплекса
II
Внедрение этилена по связи Co-H
III
Внедрение СО по связи С-Со
алкилацилкарбонилкобальта
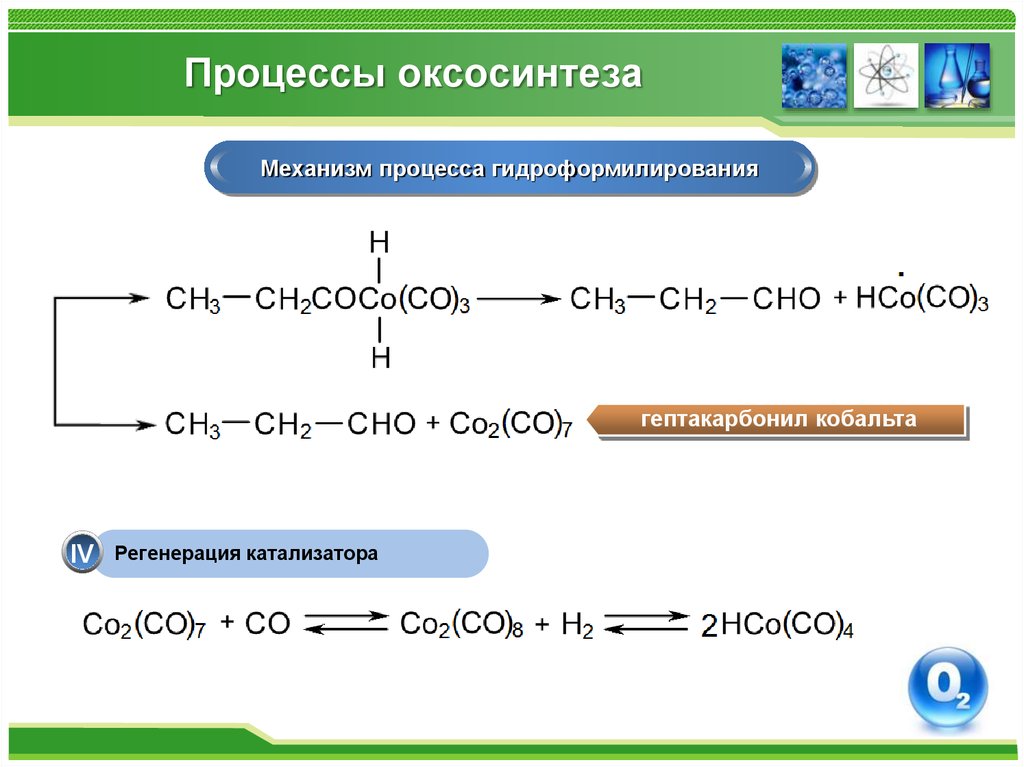
72. Процессы оксосинтеза
Механизм процесса гидроформилированиягептакарбонил кобальта
IV
Регенерация катализатора
73. Процессы оксосинтеза
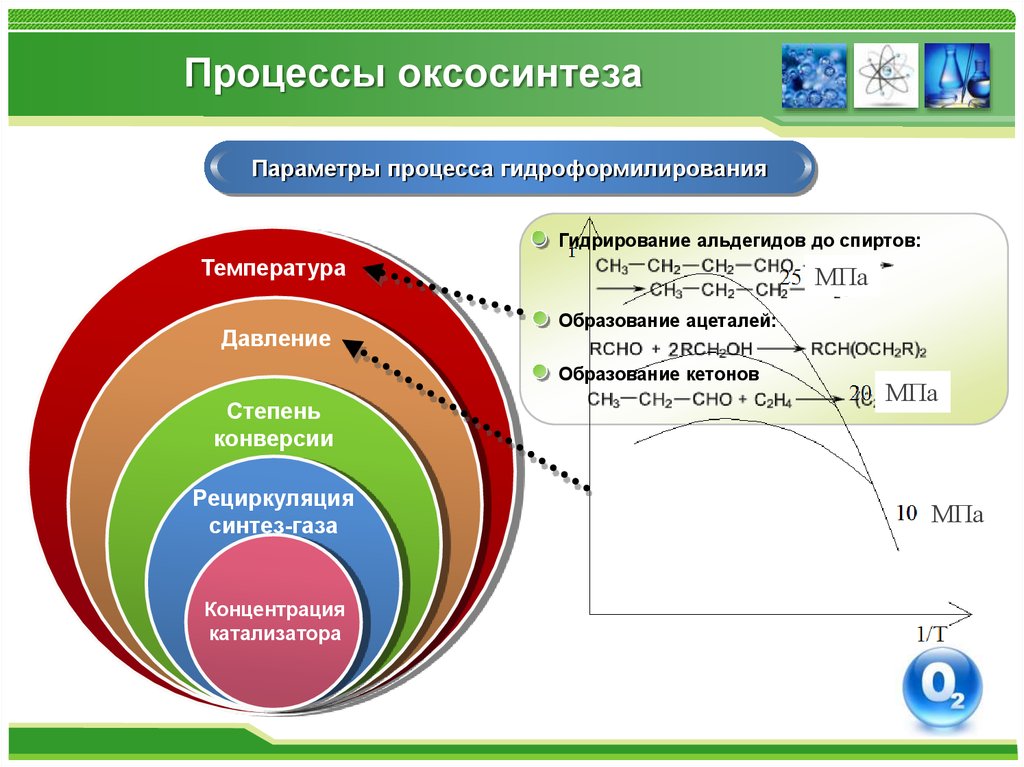
Параметры процесса гидроформилированияГидрирование альдегидов до спиртов:
Температура
Давление
МПа
Образование ацеталей:
Образование кетонов
Степень
конверсии
Рециркуляция
синтез-газа
Концентрация
катализатора
МПа
МПа
74. Процессы оксосинтеза
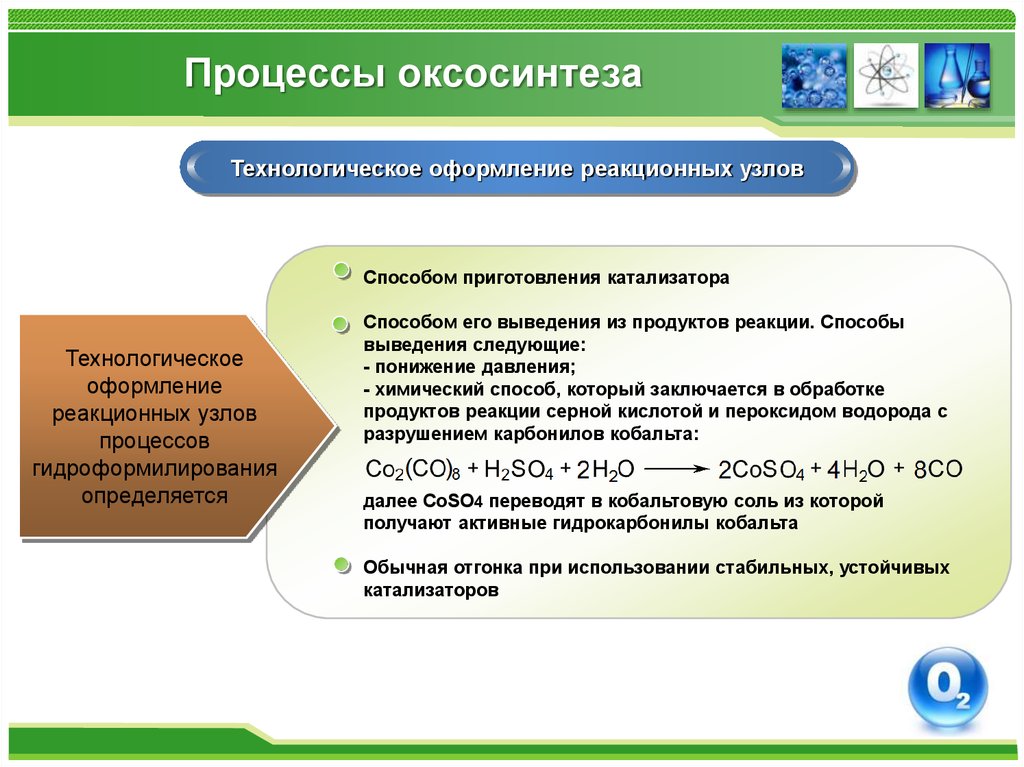
Технологическое оформление реакционных узловСпособом приготовления катализатора
Технологическое
оформление
реакционных узлов
процессов
гидроформилирования
определяется
Способом его выведения из продуктов реакции. Способы
выведения следующие:
- понижение давления;
- химический способ, который заключается в обработке
продуктов реакции серной кислотой и пероксидом водорода с
разрушением карбонилов кобальта:
далее СоSO4 переводят в кобальтовую соль из которой
получают активные гидрокарбонилы кобальта
Обычная отгонка при использовании стабильных, устойчивых
катализаторов
75. Процессы оксосинтеза
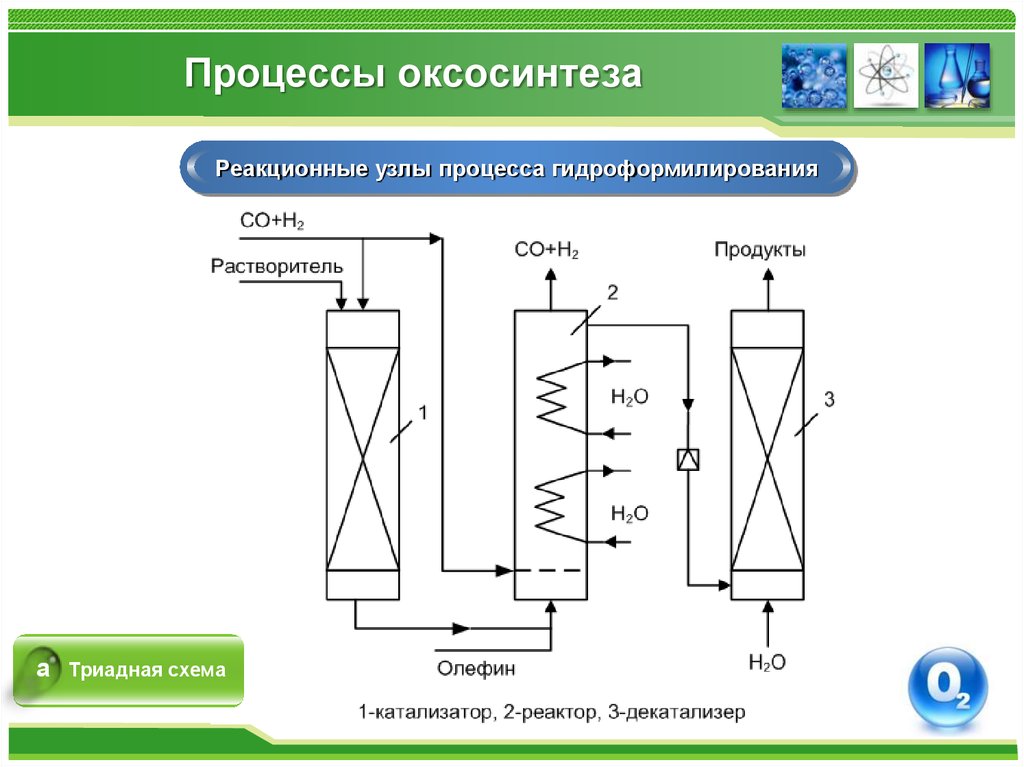
Реакционные узлы процесса гидроформилированияа
Триадная схема
76. Процессы оксосинтеза
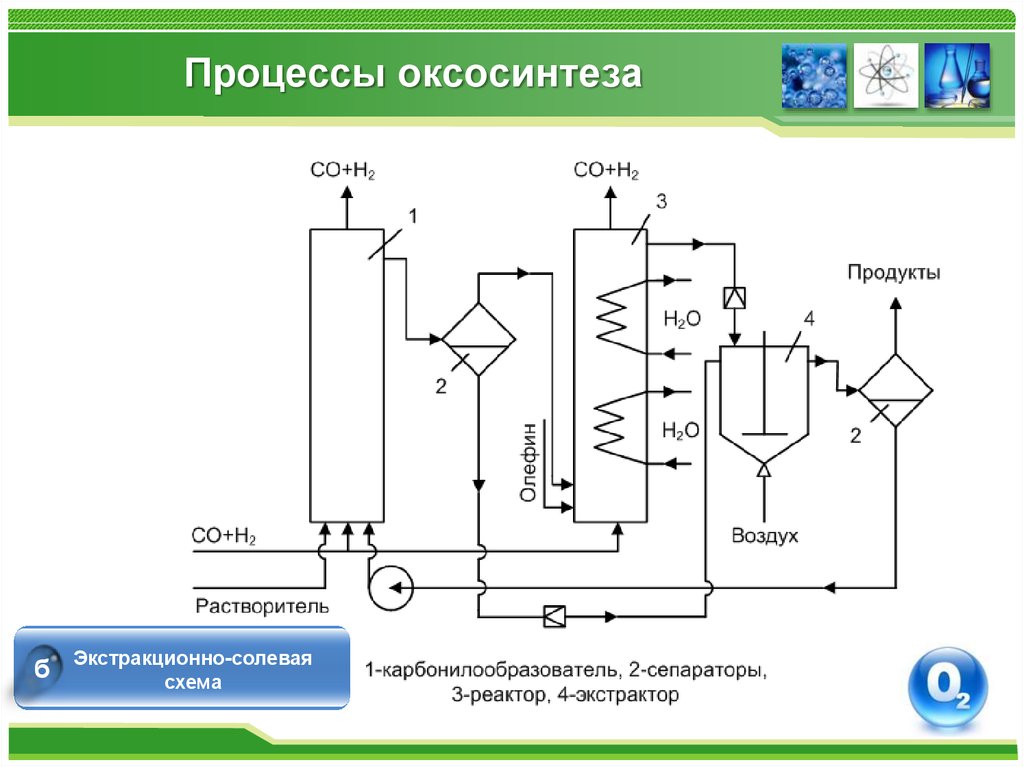
бЭкстракционно-солевая
схема
77. Процессы оксосинтеза
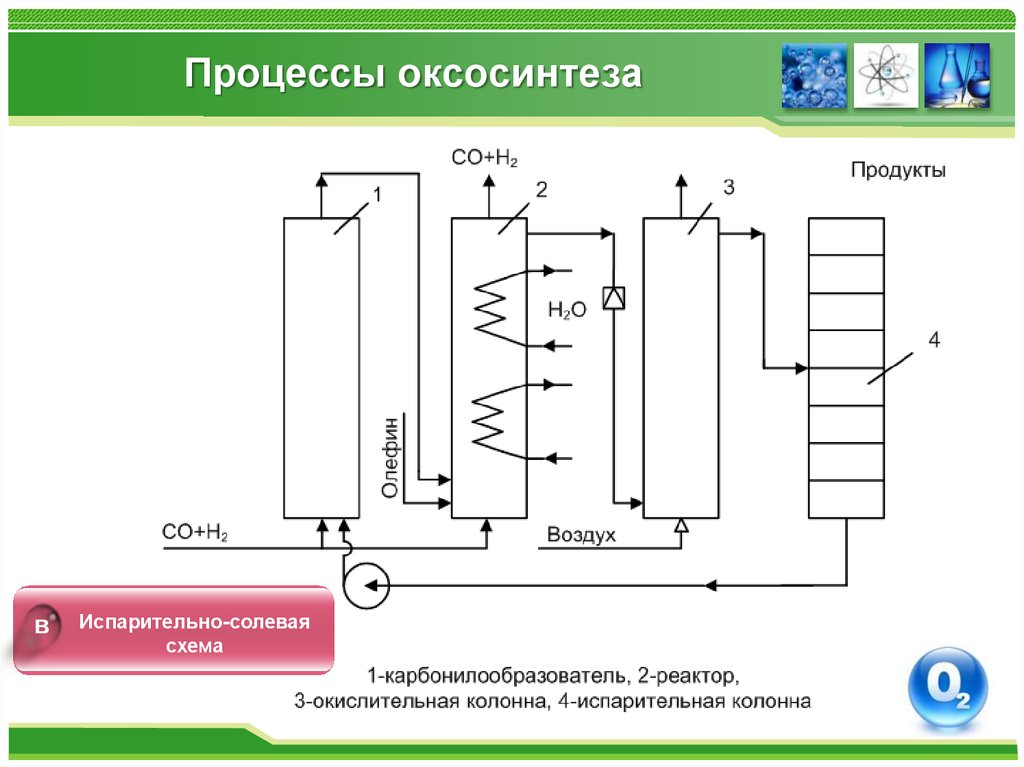
вИспарительно-солевая
схема
78. Процессы оксосинтеза
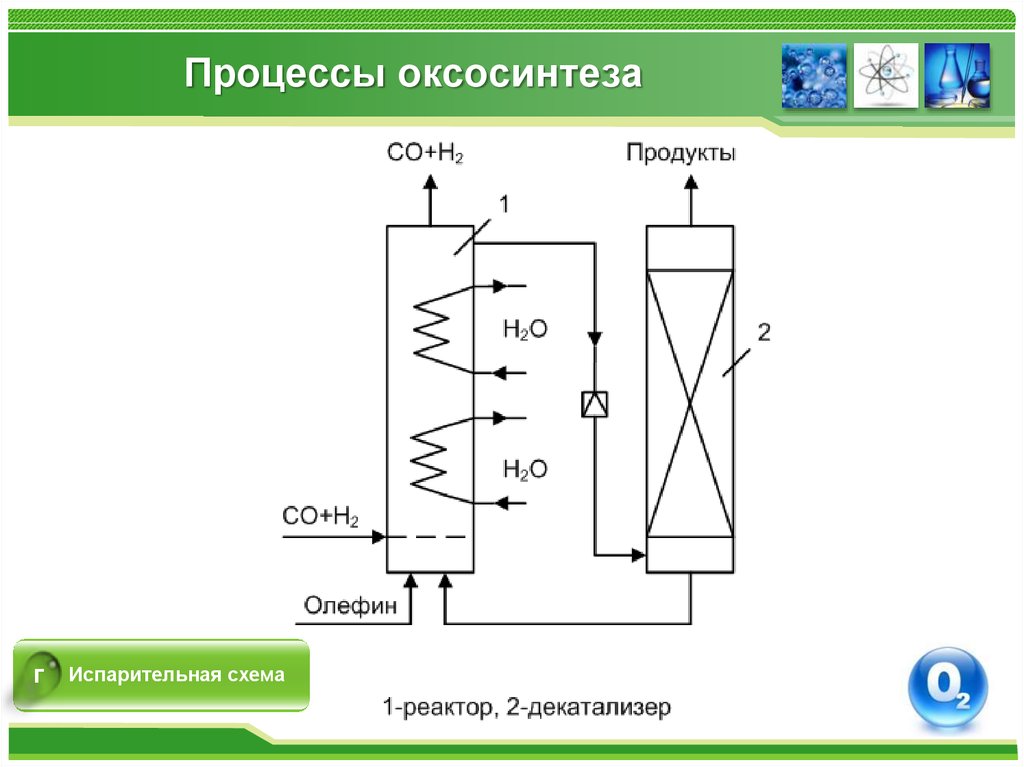
гИспарительная схема
79. Процессы конденсации по карбонильной группе
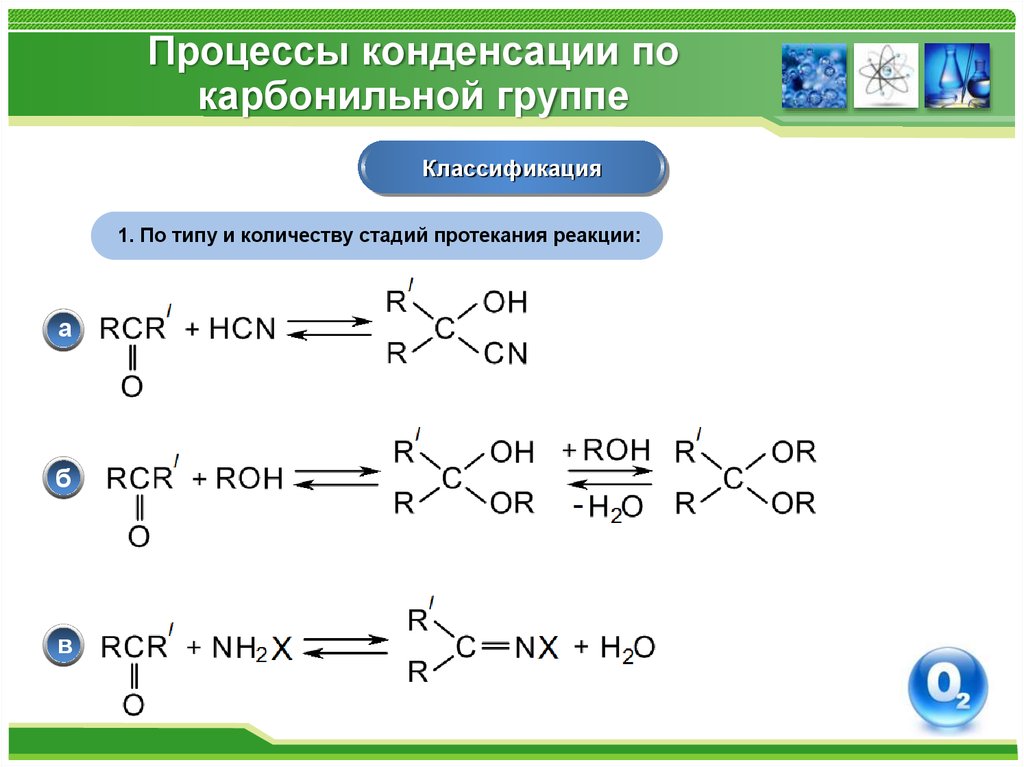
Классификация1. По типу и количеству стадий протекания реакции:
а
б
в
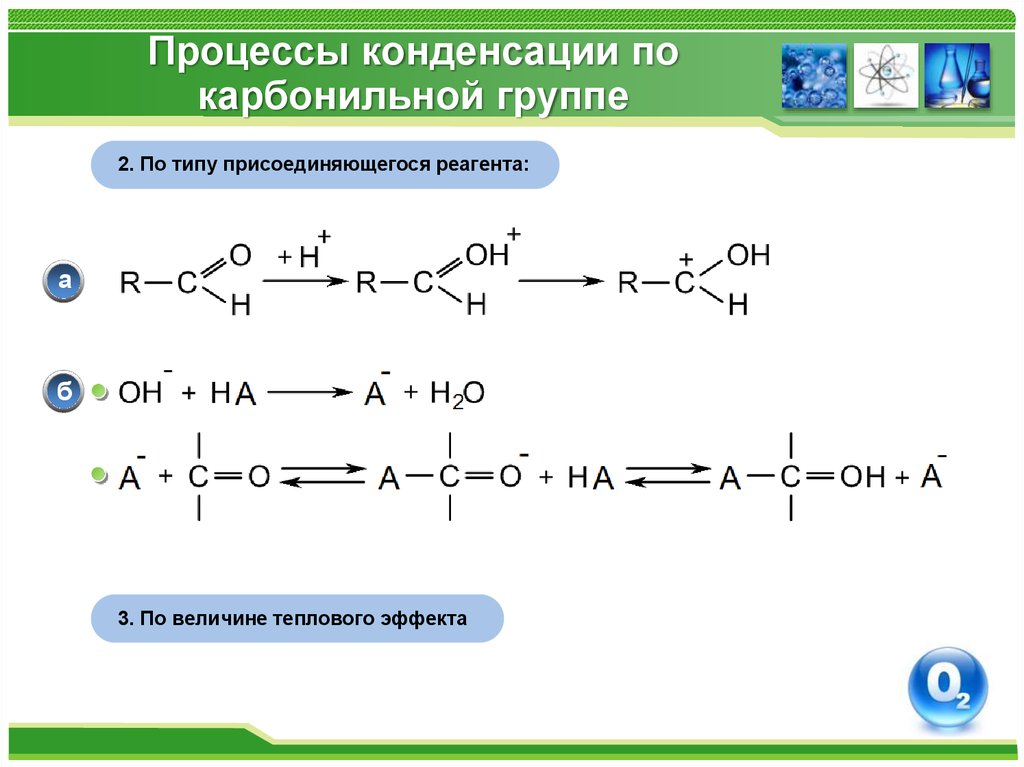
80. Процессы конденсации по карбонильной группе
2. По типу присоединяющегося реагента:а
б
3. По величине теплового эффекта
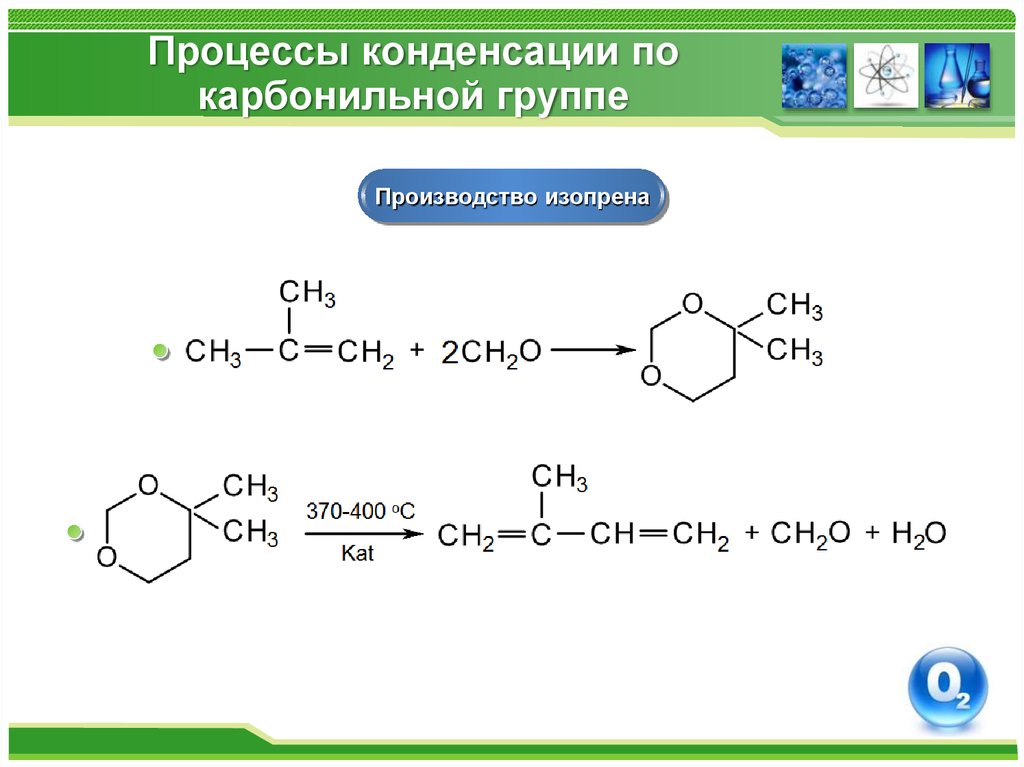
81. Процессы конденсации по карбонильной группе
Производство изопрена82. Процессы конденсации по карбонильной группе
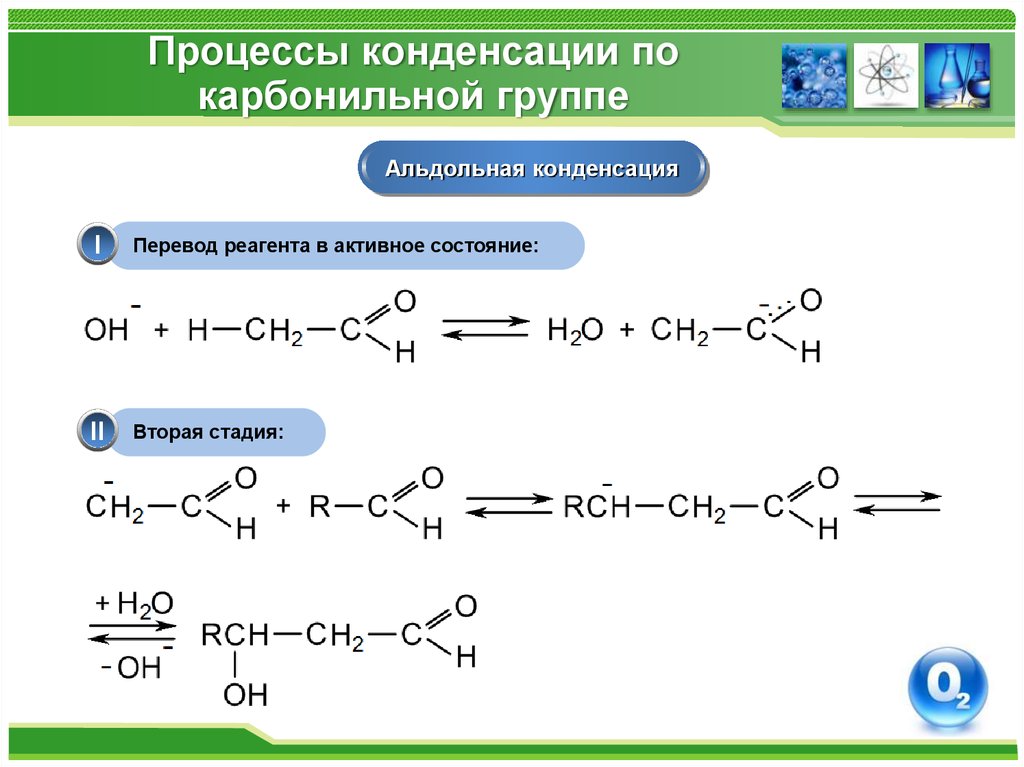
Альдольная конденсацияI
Перевод реагента в активное состояние:
II
Вторая стадия:
83. Процессы конденсации по карбонильной группе
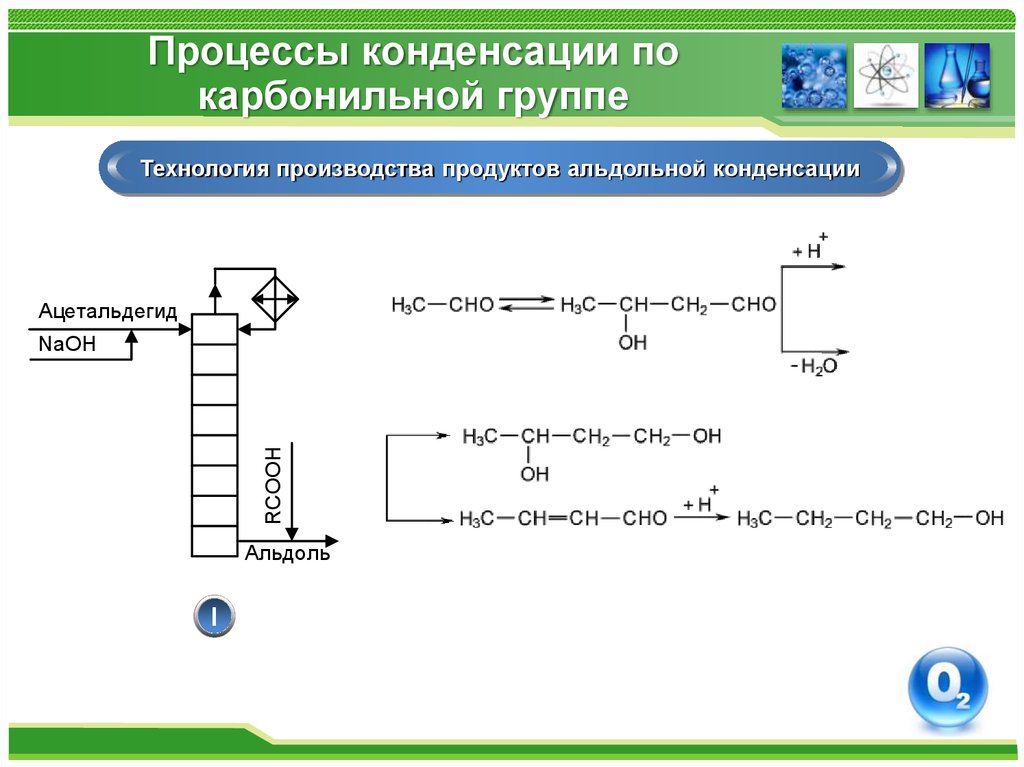
Технология производства продуктов альдольной конденсацииАцетальдегид
RCOOH
NaOH
Альдоль
I
84. Процессы конденсации по карбонильной группе
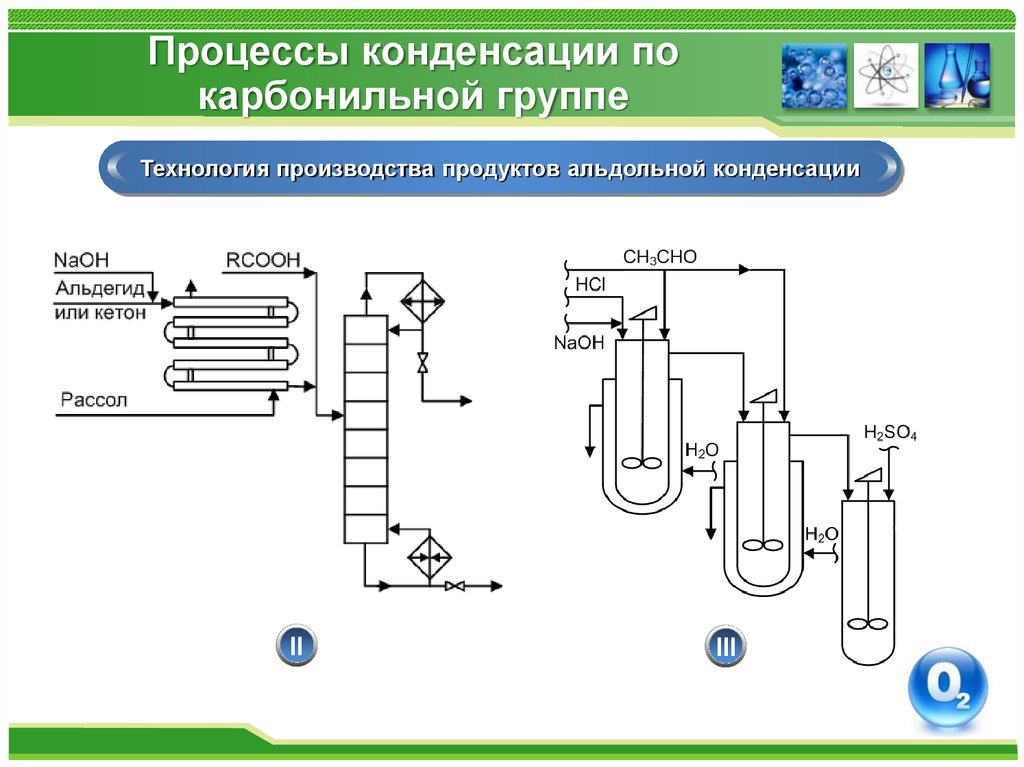
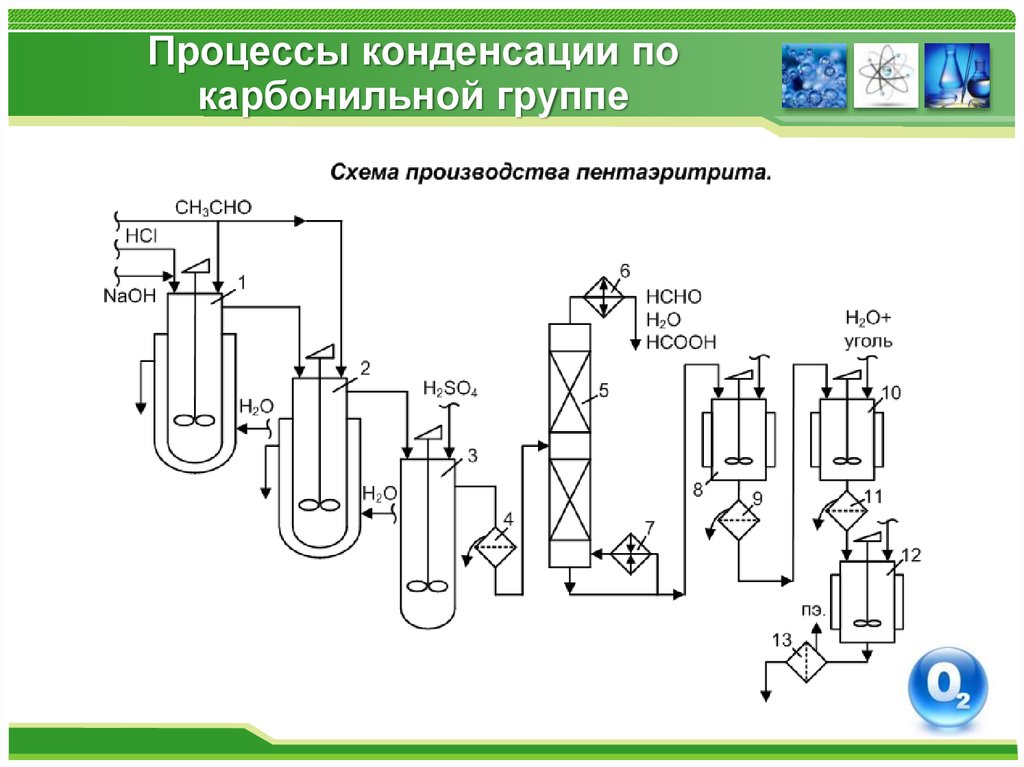
Технология производства продуктов альдольной конденсацииII
III



 Химия
Химия








