Похожие презентации:
Атом і атомне ядро
1.
Виконалаучениця 9-Б
Яна
Ортинська
2.
3.
Схема будови спектрографа4.
400700
а
400
550
б
400
700
в
500
700
г
Види оптичних спектрів: а – суцільний;
б – лінійчатий випромінювання;
в – лінійчатий поглинання; г - смугастий
5.
Закономірності в атомному спектріводню
1885 р. Я. Бальмер – частоти видимої
частини спектра
1
R( 2
2
1
де
m
може
бути
3,
4,
5,…
∞
),
2
m
R – стала величина
1906 р. Лайман – частоти в
ультрафіолетовій частині спектра
R ( 1 2 1 2), де m може бути 2, 3, 4,…∞
1
m
6.
1908 р. Пашен – частоти вінфрачервоній частині спектра
R ( 1 2 1 2),
3
m
де m може бути 4, 5, 6,…∞
Всі лінії спектра водню можна виразити
однією формулою:
R ( 1 2 1 2)
n
m
де n і m – цілі числа, причому m > n
7.
Прилад, за допомогою якого Резерфорд вивчаврозсіювання частинок
1 – мікроскоп, 2 – екран, 3 – свинцевий контейнер з
радіоактивним препаратом, 4 – мішень (дротинка),
5 – шланг до вакуумного насосу, 6 – корпус
8.
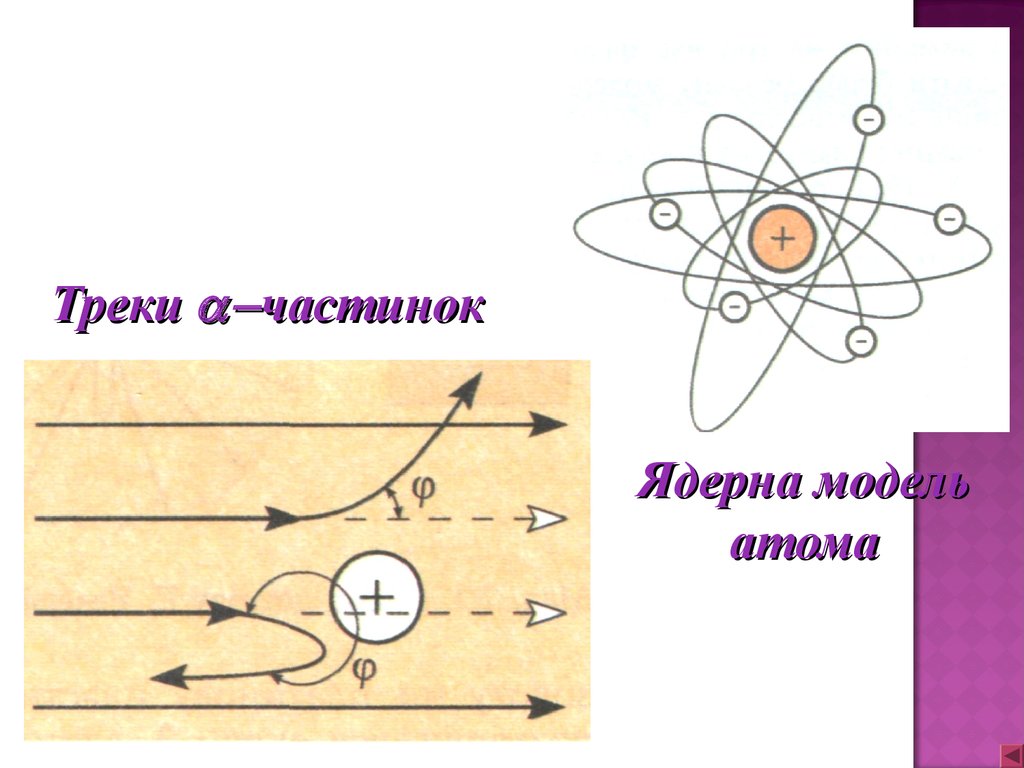
Треки частинокЯдерна модель
атома
9.
Енергетичні рівні атома10.
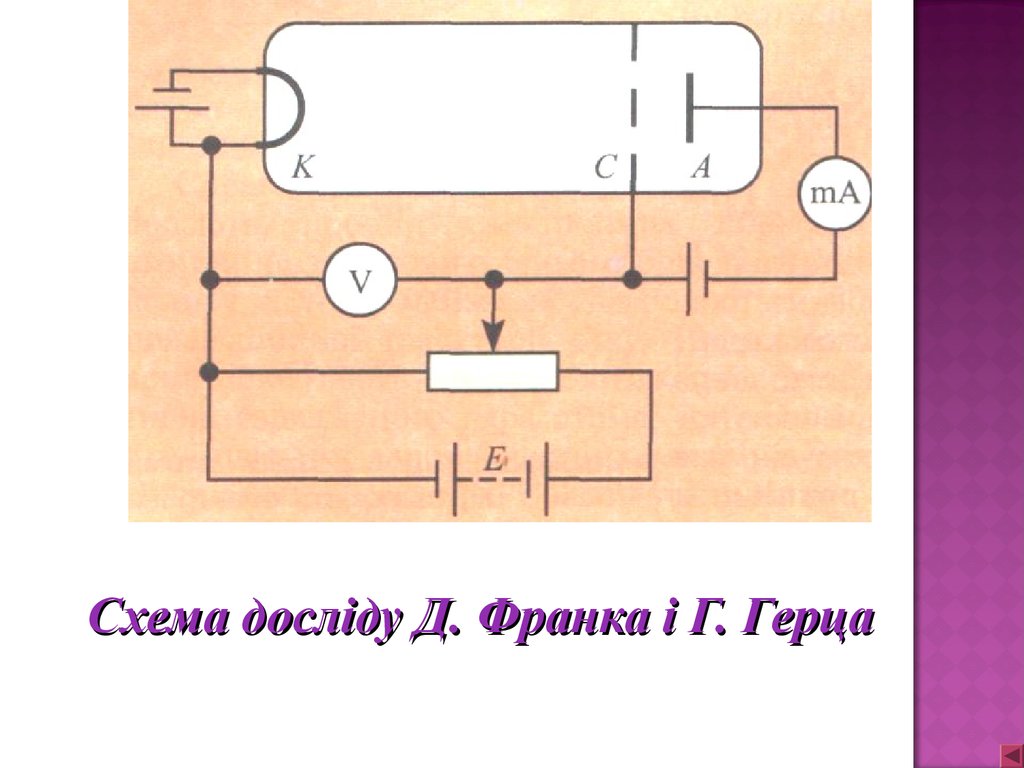
Схема досліду Д. Франка і Г. Герца11.
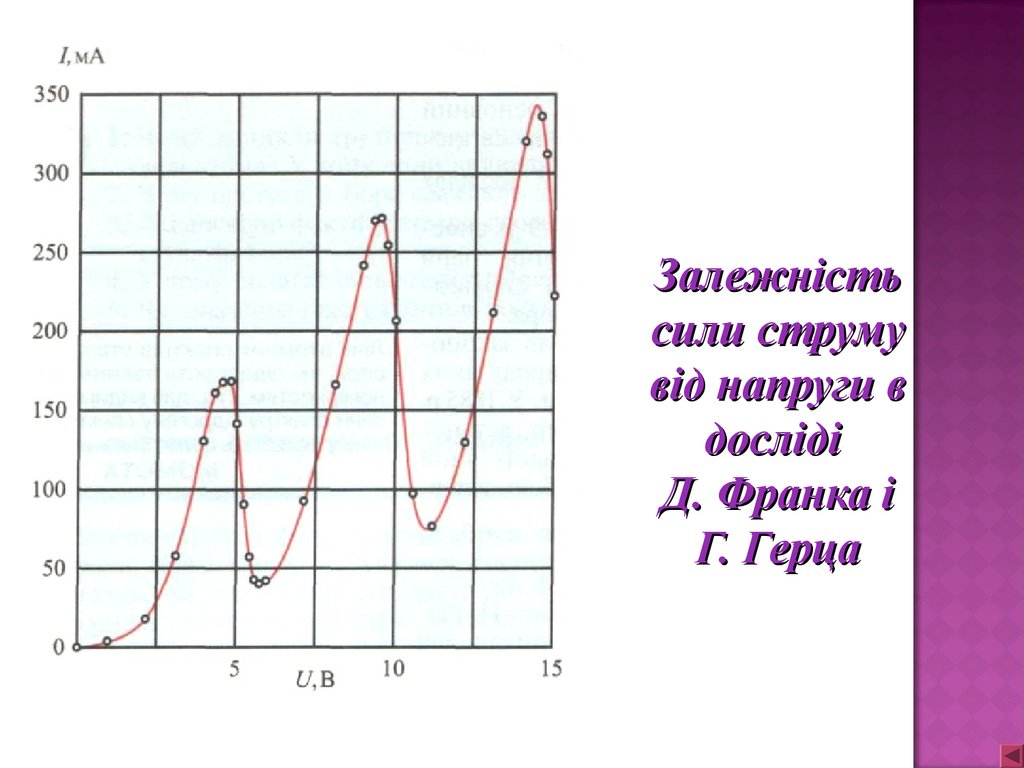
Залежністьсили струму
від напруги в
досліді
Д. Франка і
Г. Герца
12.
13.
1919 рік.14
7
1
1
Е. Резерфорд
N He O H
H
4
2
p
1
1
17
8
– протон
1
1
14.
1932 рік.9
4
1
0
Д. Чедвік
Be He C n
n
4
2
– нейтрон
12
6
1
0
15.
11
H
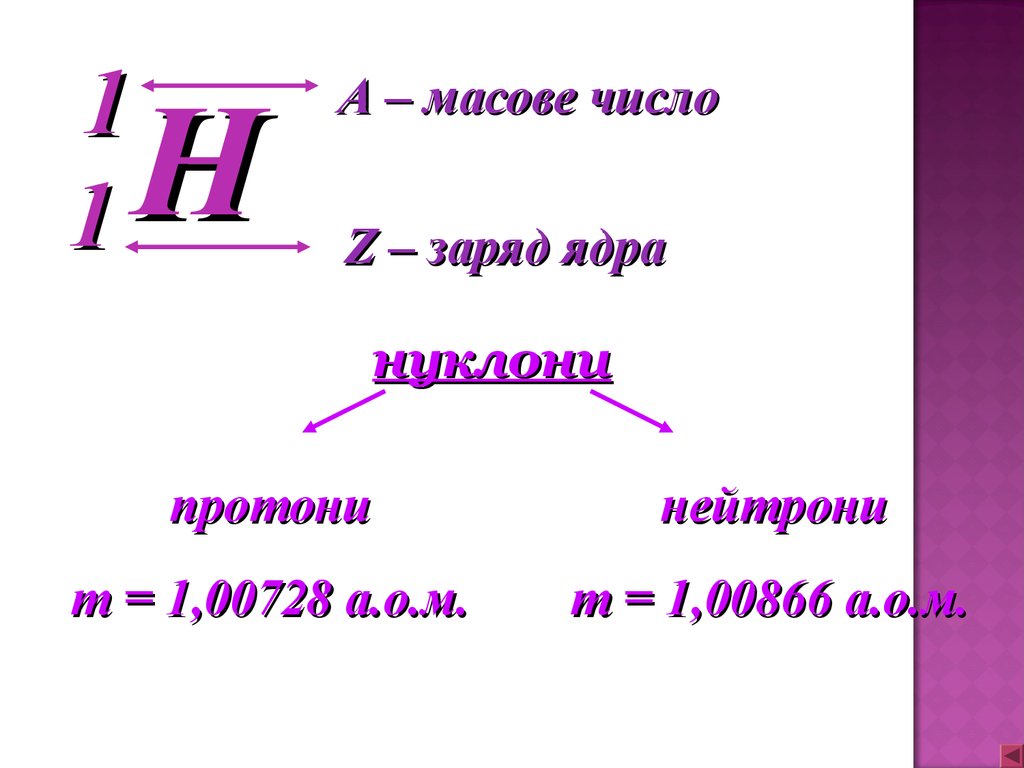
А – масове число
Z – заряд ядра
нуклони
протони
нейтрони
m = 1,00728 а.о.м.
m = 1,00866 а.о.м.
16.
кількість протонів у ядрі – Zкількість нейтронів – N = A – Z
ізотопи
1
1
2
1
Z=1
Z=1
Z=1
N= 0
N =1
N=2
H
H
3
1
H









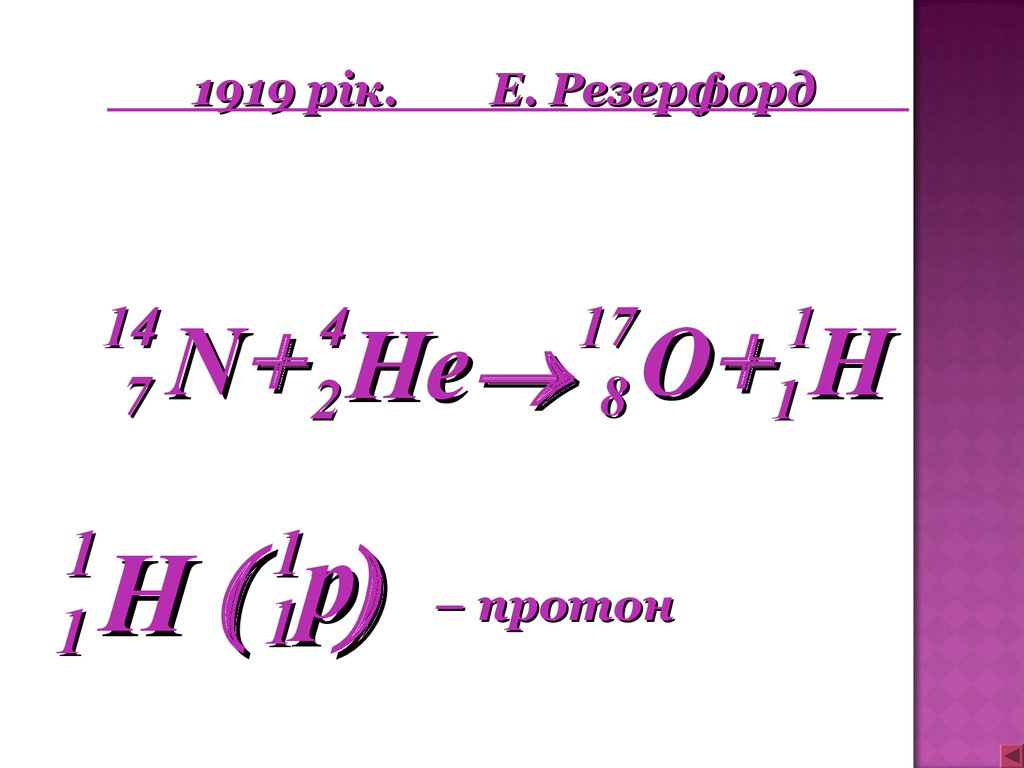



 Физика
Физика








