Похожие презентации:
Свойства и функции белков
1.
2.
Белкичрезвычайно
разнообразны
по
своим
свойствам, что определяется их пространственной
структурой.
Есть белки, растворимые (например, фибриноген) и нерастворимые
(например, фибрин) в воде. Глобулярные белки растворимы, а
фибриллярные белки- нерастворимы в воде.
Есть белки очень устойчивые (например, кератин) и неустойчивые
(например, фермент каталаза с легко изменяющейся структурой).
У белков встречается разнообразная форма молекул — от нитей
(миозин - белок мышечных волокон) до шариков (гемоглобин)
3.
Виды белков по функциямФерменты (альдолаза, каталаза, пероксидаза и т. д.)
Запасные белки (казеин)
Гормоны (паратгормон, инсулин, соматропин)
Транспортные белки (гемоглобин, гемоциан)
Токсины. Микробные- ботулический, столбнячный,
дифтерийный, холерный. Токсины змей, пауков скорпионов,
грибов, пчел
Антибиотики (грамицидин)
Защитные белки (антитела, интерфероны, гамма-глобулины)
Двигательные белки (актин, миозин)
Структурные белки (коллаген, склеротин, мукопротеины)
4.
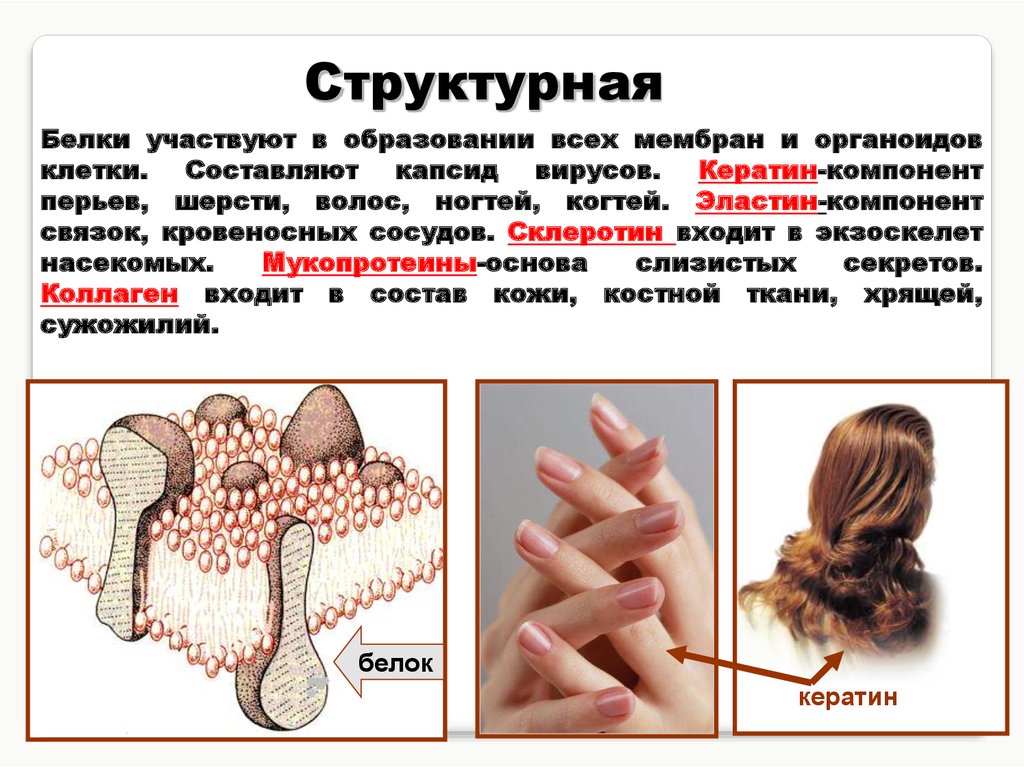
СтруктурнаяБелки участвуют в образовании всех мембран и органоидов
клетки. Составляют капсид вирусов. Кератин-компонент
перьев, шерсти, волос, ногтей, когтей. Эластин-компонент
связок, кровеносных сосудов. Склеротин входит в экзоскелет
насекомых.
Мукопротеины-основа
слизистых
секретов.
Коллаген входит в состав кожи, костной ткани, хрящей,
сужожилий.
белок
кератин
5. Структурная функция
Структурные белки цитоскелета, как своего рода арматура,придают форму клеткам и многим органоидам и участвуют в
изменении формы клеток.
Коллаген и эластин — основные компоненты межклеточного
вещества соединительной ткани (например, хряща), а из
другого структурного белка кератина состоят волосы, ногти,
перья птиц и некоторые раковины.
Структурная функция
6.
КаталитическаяВ каждой клетке имеются сотни ферментов.
Они помогают осуществлять биохимические
реакции, действуя как биокатализаторы.
7.
ТранспортнаяНапример, г е м о г л о б и н
крови переносит кислород.
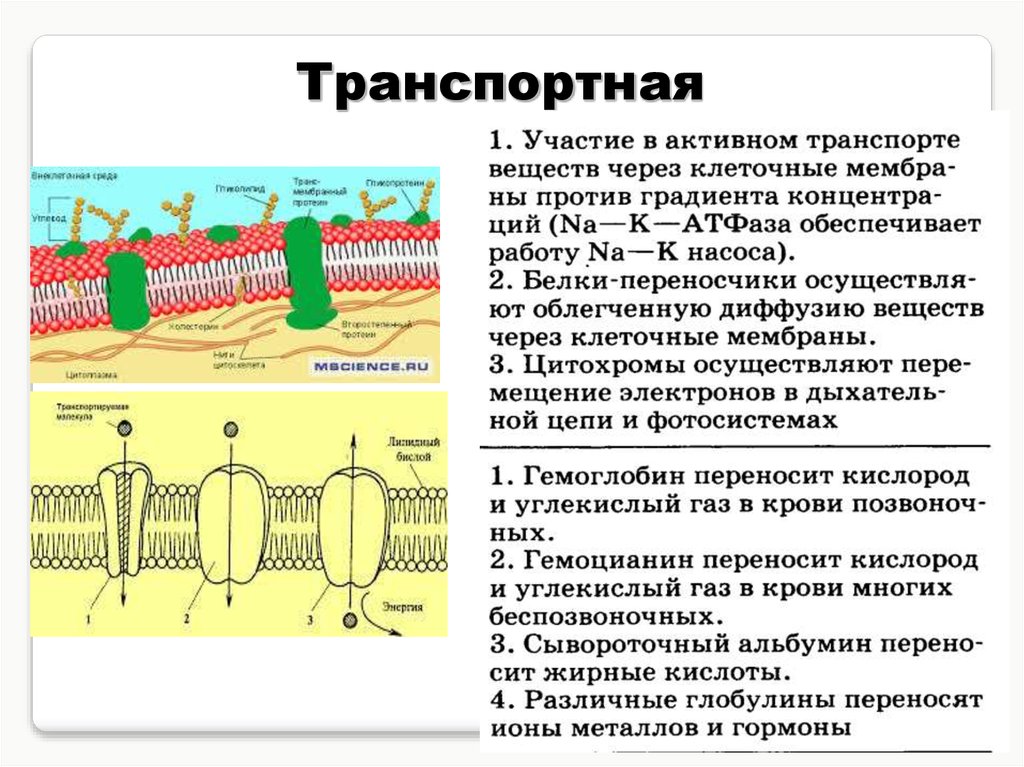
8. Транспортная функция
Транспортный белок гемоглобин переноситкислород из лёгких к остальным тканям и
углекислый газ от тканей к лёгким, а также
гомологичные ему белки, найденные во всех
царствах живых организмов.
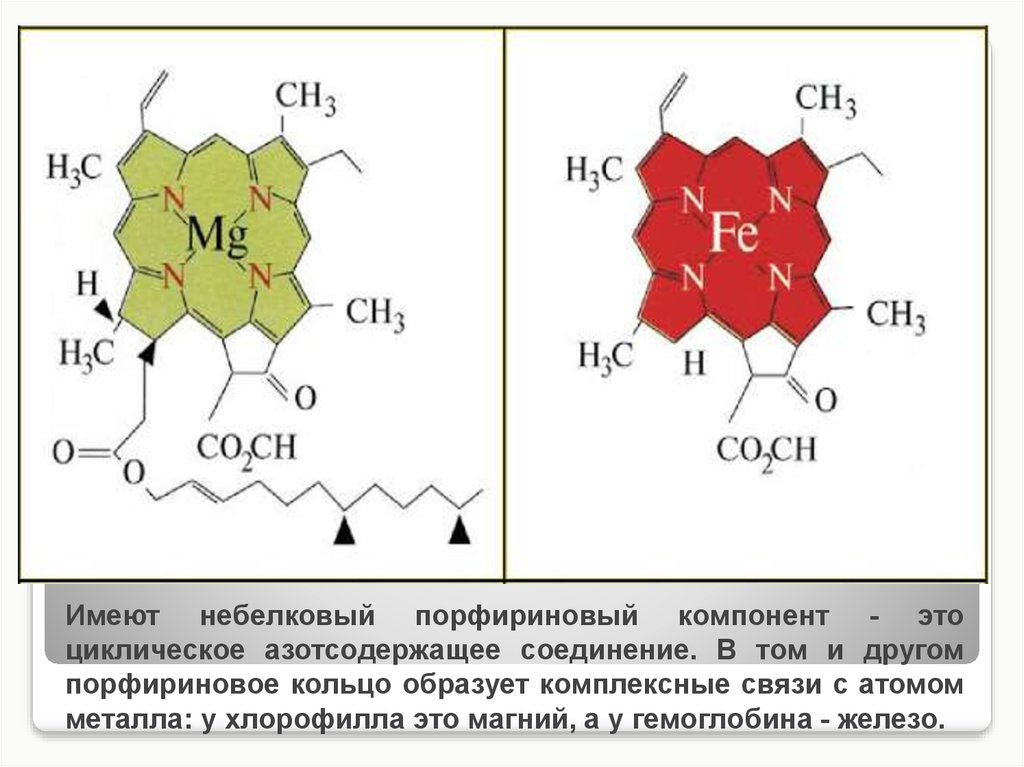
9. Имеют небелковый порфириновый компонент - это циклическое азотсодержащее соединение. В том и другом порфириновое кольцо
образует комплексные связи с атомомметалла: у хлорофилла это магний, а у гемоглобина - железо.
10.
РегуляторнаяБелки гормоны
физиологические
процессы.
регулируют различные
Например, инсулин регулирует
уровень углеводов в крови.
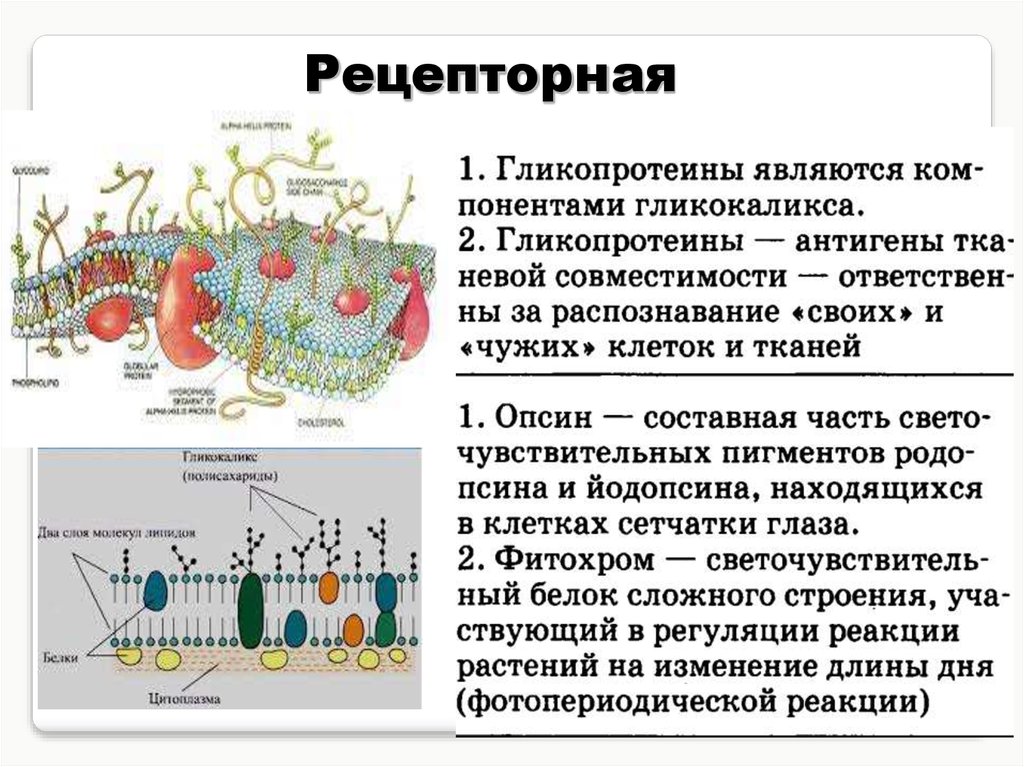
11.
РецепторнаяНапример, инсулин регулирует
уровень углеводов в крови.
12.
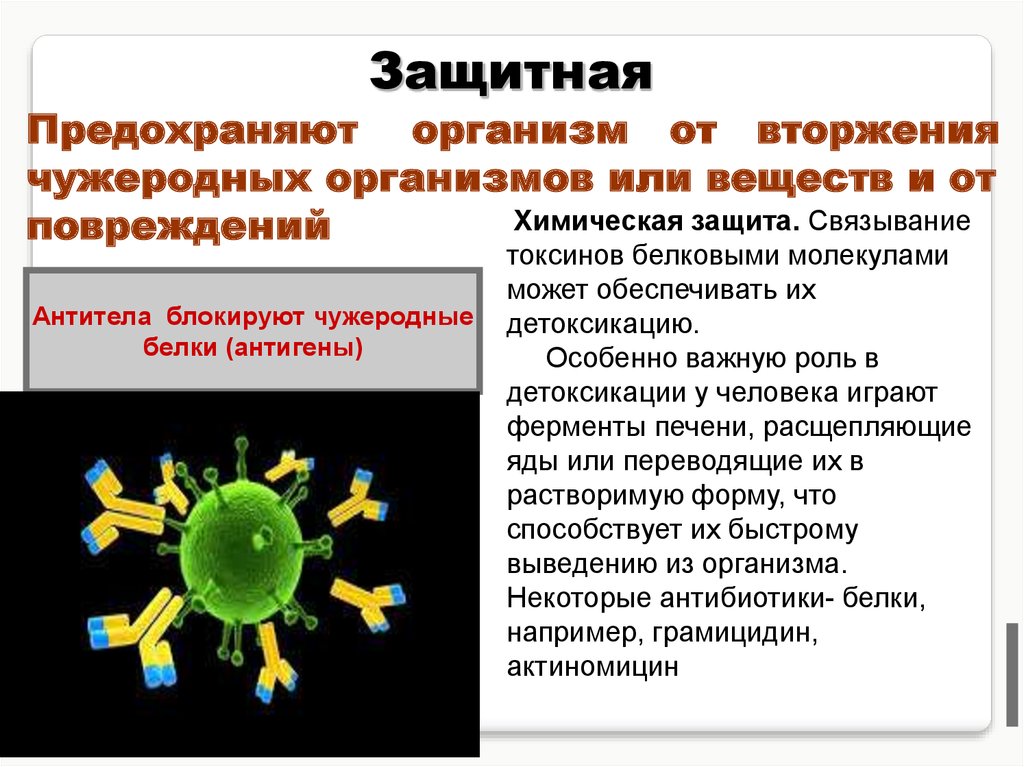
ЗащитнаяПредохраняют организм от вторжения
чужеродных организмов или веществ и от
Химическая защита. Связывание
повреждений
Антитела блокируют чужеродные
белки (антигены)
токсинов белковыми молекулами
может обеспечивать их
детоксикацию.
Особенно важную роль в
детоксикации у человека играют
ферменты печени, расщепляющие
яды или переводящие их в
растворимую форму, что
способствует их быстрому
выведению из организма.
Некоторые антибиотики- белки,
например, грамицидин,
актиномицин
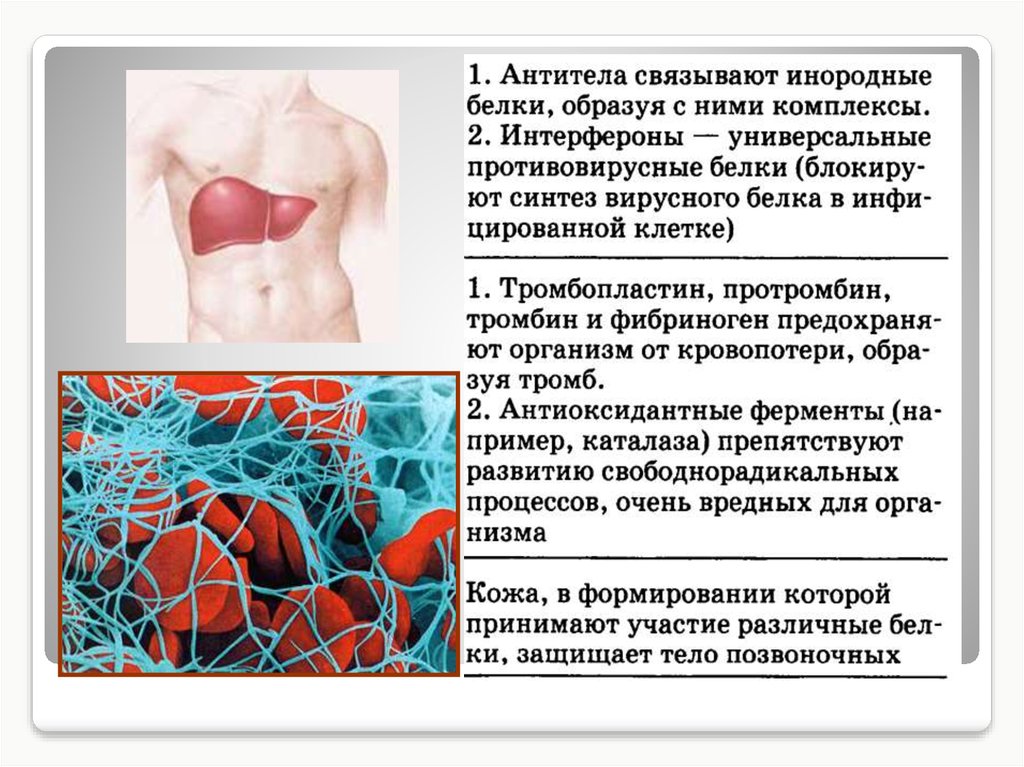
13.
14.
Сократительная.
Актин и миозин – белки мышц
15.
ЭнергетическаяПри недостатке углеводов или
жиров окисляются молекулы
белков.
При полном расщеплении белка до конечных
продуктов выделяется энергия:
1г белка - 17.6 кДж
Но в качестве источника энергии белки используются крайне
редко.
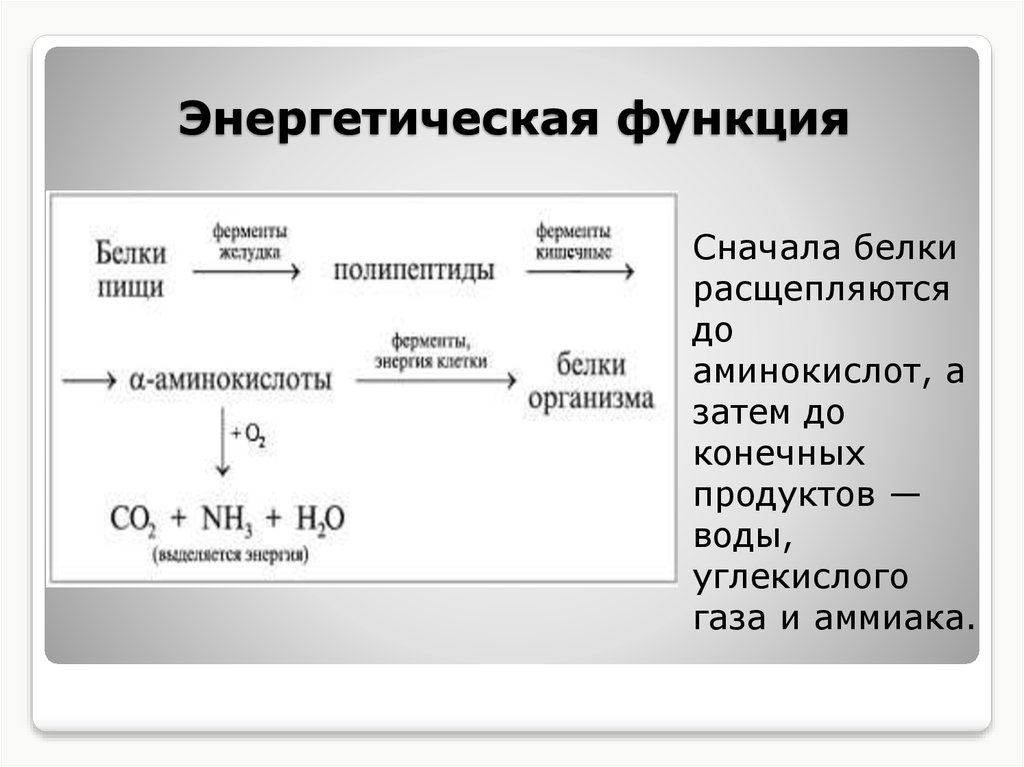
16. Энергетическая функция
Сначала белкирасщепляются
до
аминокислот, а
затем до
конечных
продуктов —
воды,
углекислого
газа и аммиака.
17. Пищевая функция
Запасающаяфункция
18.
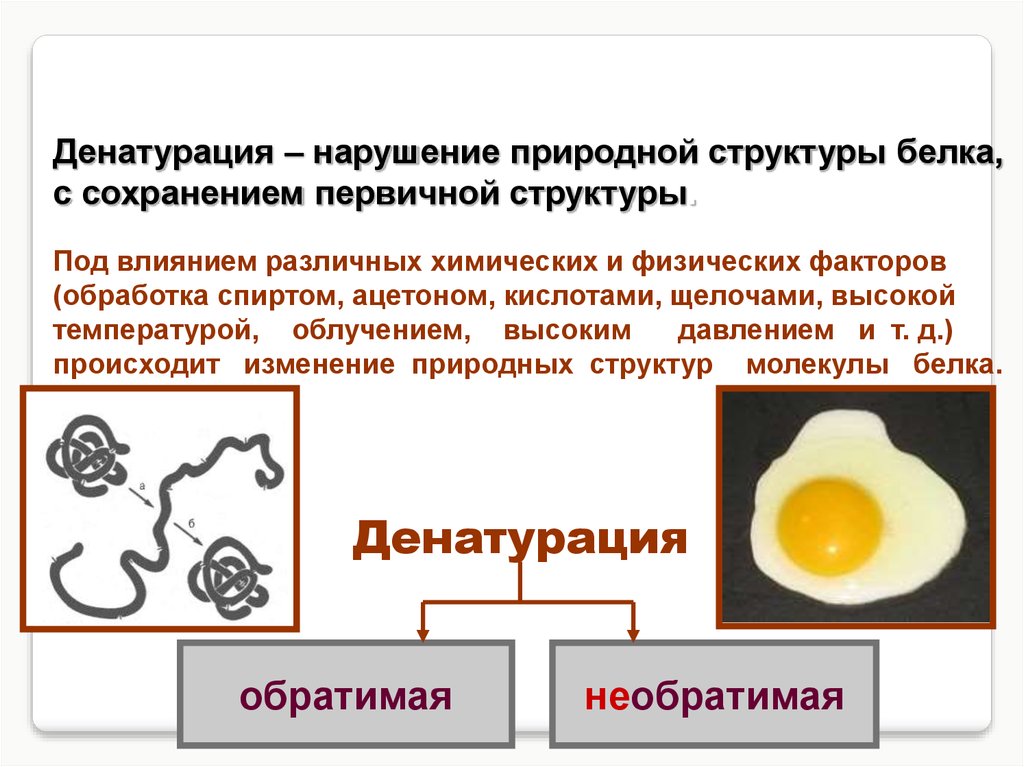
Денатурация – нарушение природной структуры белка,с сохранением первичной структуры.
Под влиянием различных химических и физических факторов
(обработка спиртом, ацетоном, кислотами, щелочами, высокой
температурой, облучением, высоким
давлением и т. д.)
происходит изменение природных структур молекулы белка.
Денатурация
обратимая
необратимая
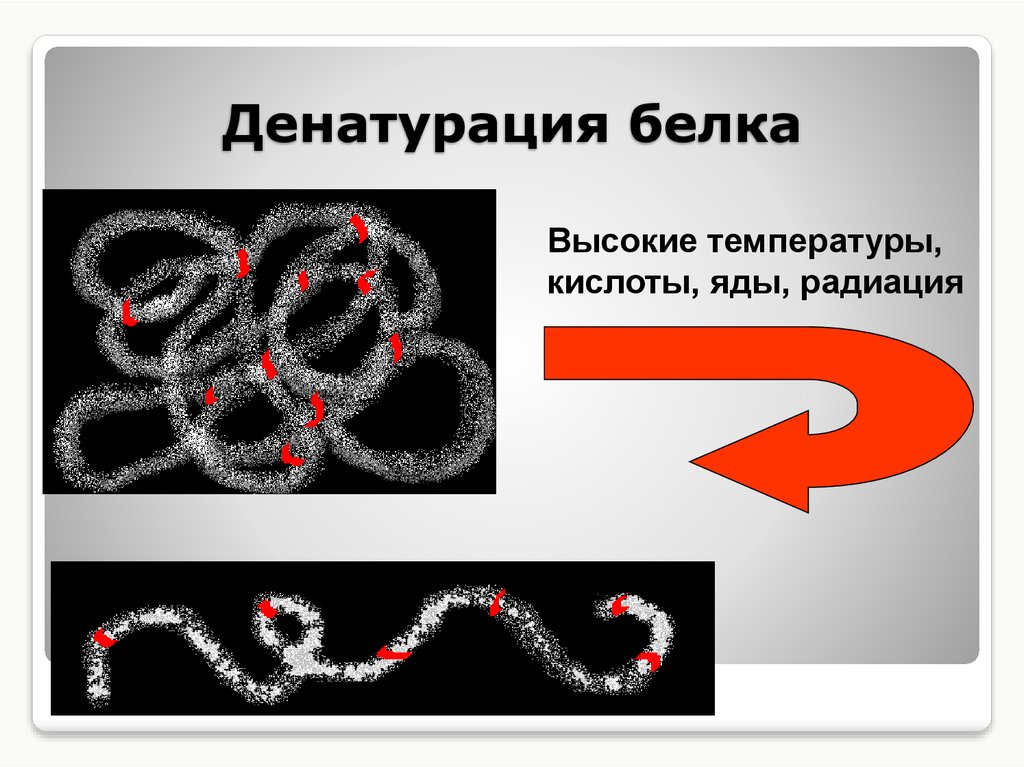
19. Денатурация белка
Высокие температуры,кислоты, яды, радиация
20. Ренатурация белка
При нормальныхусловиях белок
ренатурирует –
восстанавливает
свою структуру
21.
22. Биуретовая реакция на белки
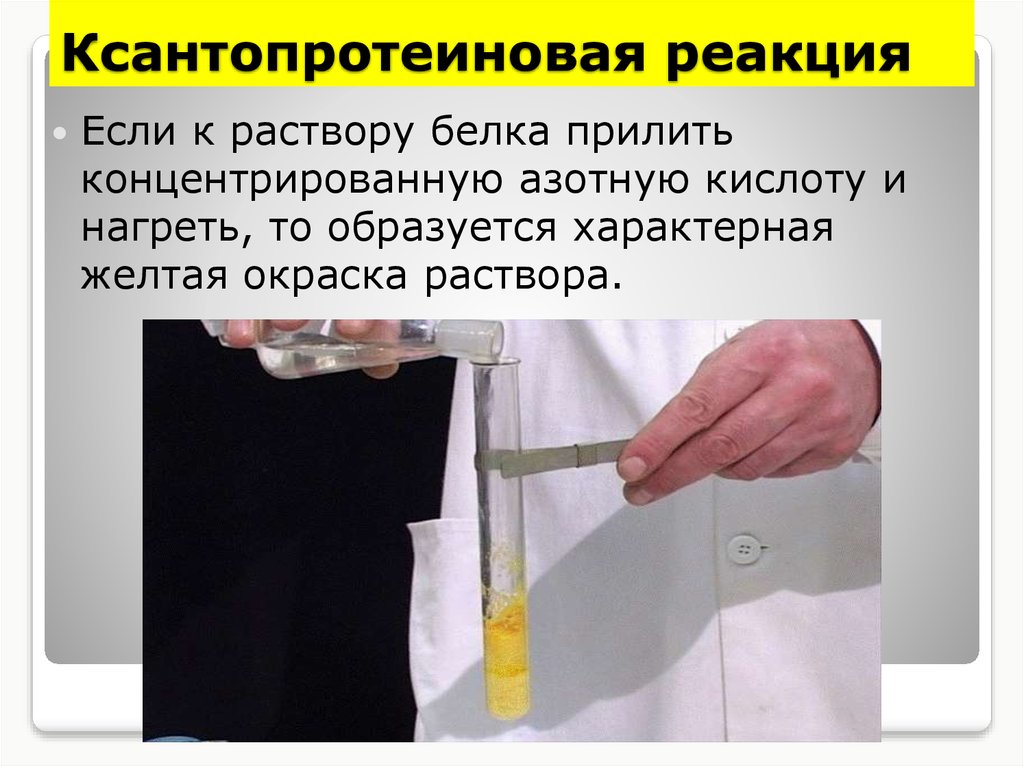
23. Ксантопротеиновая реакция
Если к раствору белка прилитьконцентрированную азотную кислоту и
нагреть, то образуется характерная
желтая окраска раствора.
24. Разрушение белка- денатурация. Действие серной кислоты на белок.
25. Денатурация белка сульфатом меди.
Денатурация белка сульфатоммеди
Денатурация белка сульфатом
меди.
26. Денатурация белка сульфатом меди.
27.
Вывод:Роль белков в жизни клетки огромна.
Современная биология показала, что
сходство и различие организмов
определяется
в конечном счете
набором белков.
Домашнее задание:
Учебник параграф 3,4
Справочник таб. 27,28 стр. 106-111

















 Биология
Биология