Похожие презентации:
Исследование термодинамических процессов водяного пара. Смеси идеальных газов. Влажный воздух. (Занятие 5)
1. Часть 1
Техническаятермодинамика
Занятие 5
Исследование термодинамических процессов водяного пара.
Смеси идеальных газов. Влажный воздух.
2.
Уравнение состояния реальных газовRT
v
RT
p
v v b v b
p м ол
a
2
v
Уравнение Ван-дер-Ваальса (1873):
a
RT
p 2
v b
v
a
p 2 v b RT
v
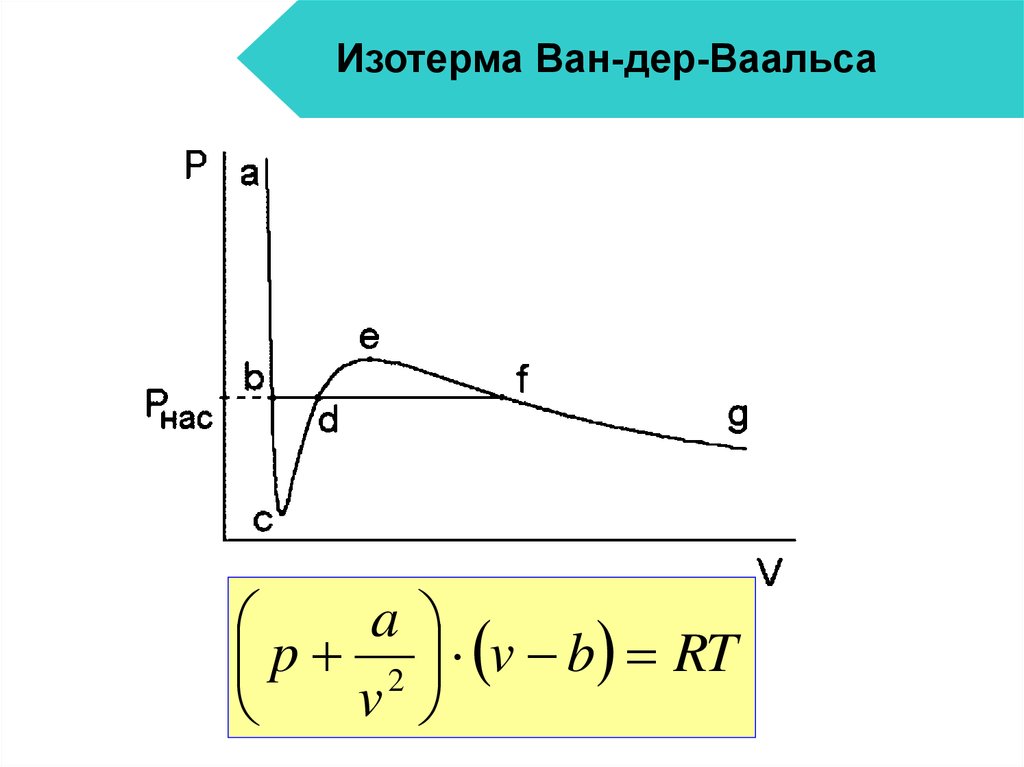
3. Изотерма Ван-дер-Ваальса
ap 2 v b RT
v
4. Изотерма Ван-дер-Ваальса
5.
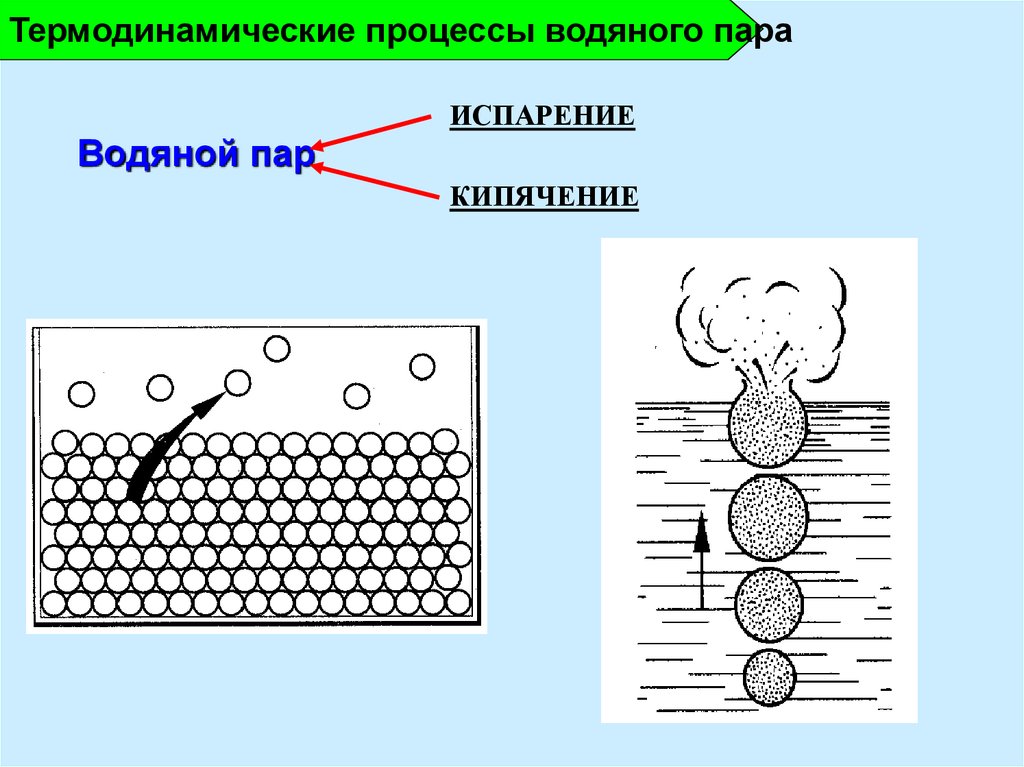
Термодинамические процессы водяного параИСПАРЕНИЕ
Водяной пар
КИПЯЧЕНИЕ
6.
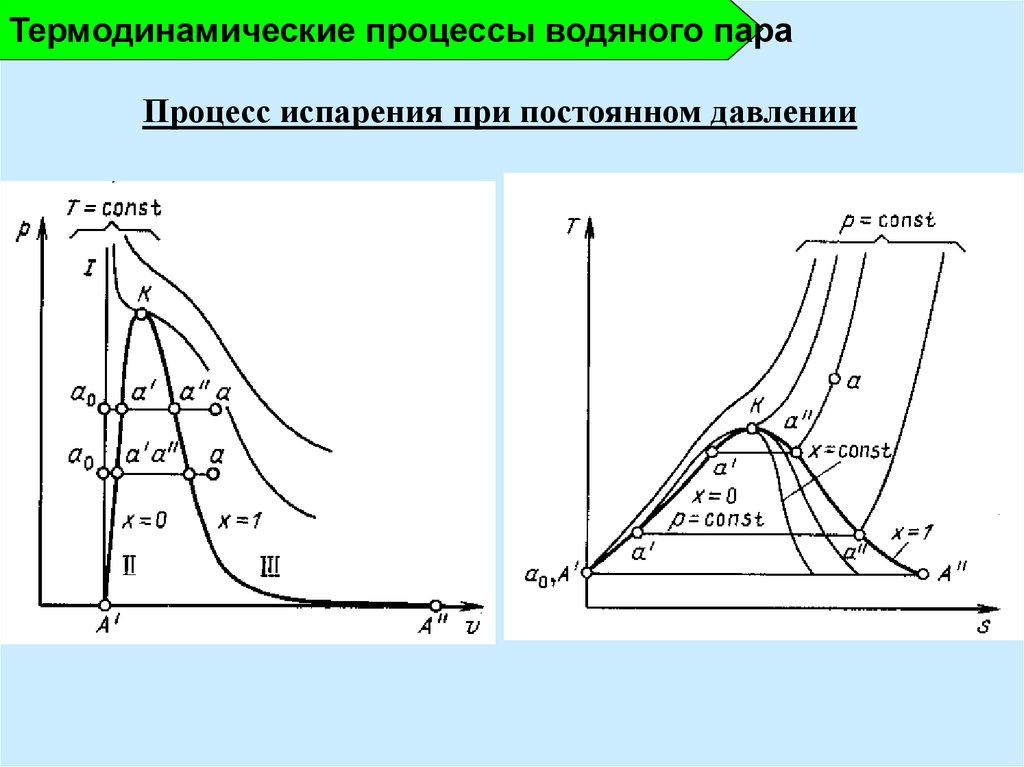
Термодинамические процессы водяного параПроцесс испарения при постоянном давлении
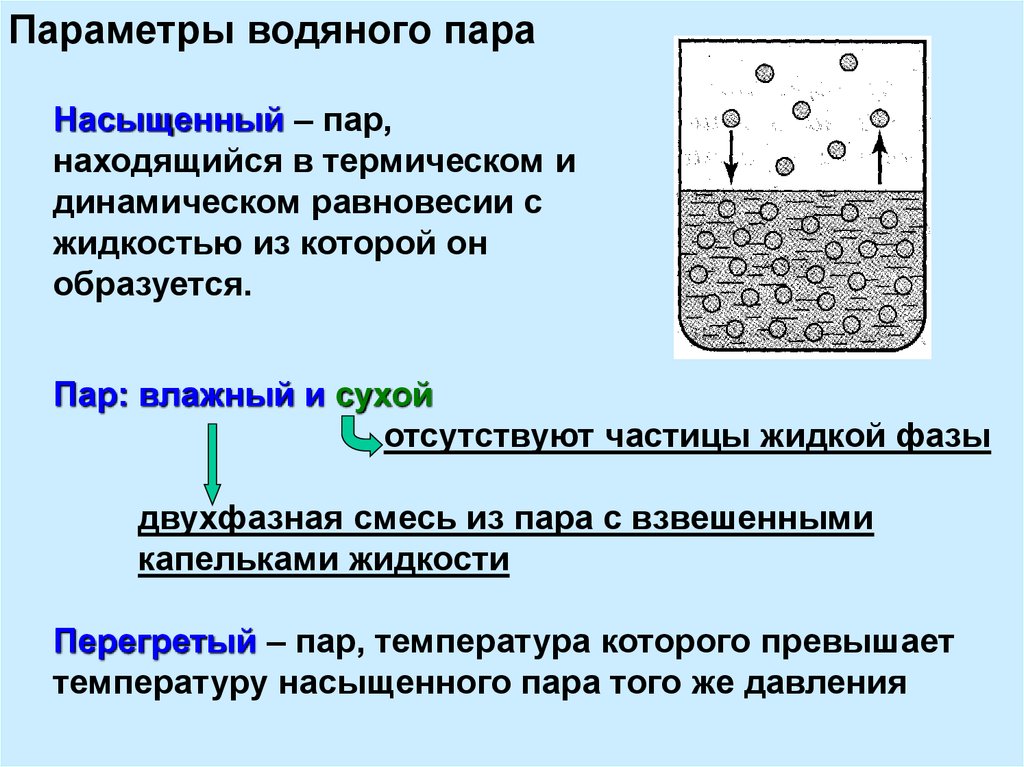
7. Параметры водяного пара
Насыщенный – пар,находящийся в термическом и
динамическом равновесии с
жидкостью из которой он
образуется.
Пар: влажный и сухой
отсутствуют частицы жидкой фазы
двухфазная смесь из пара с взвешенными
капельками жидкости
Перегретый – пар, температура которого превышает
температуру насыщенного пара того же давления
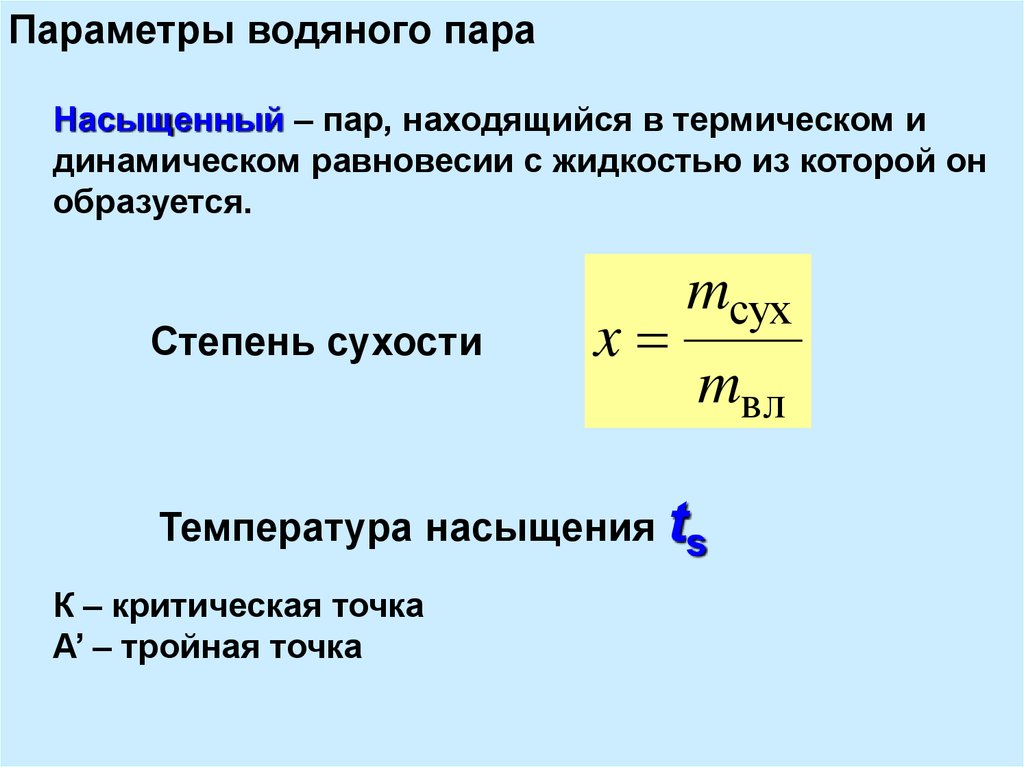
8. Параметры водяного пара
Насыщенный – пар, находящийся в термическом идинамическом равновесии с жидкостью из которой он
образуется.
Степень сухости
x
mсух
mвл
Температура насыщения ts
К – критическая точка
А’ – тройная точка
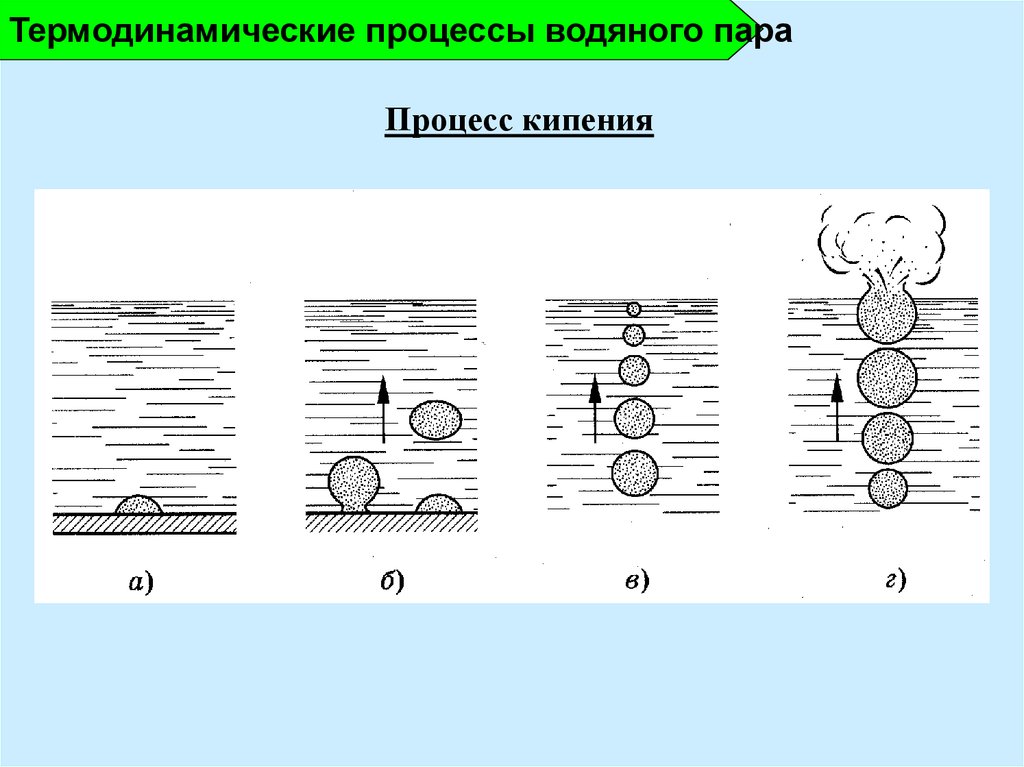
9.
Термодинамические процессы водяного параПроцесс кипения
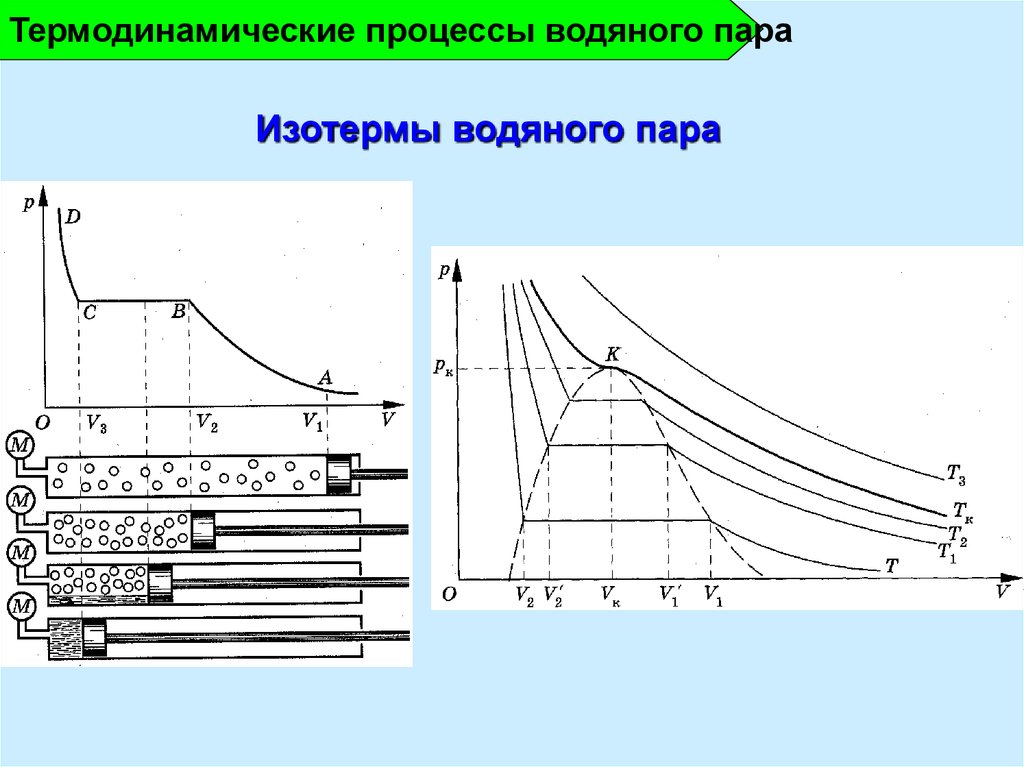
10.
Термодинамические процессы водяного параИзотермы водяного пара
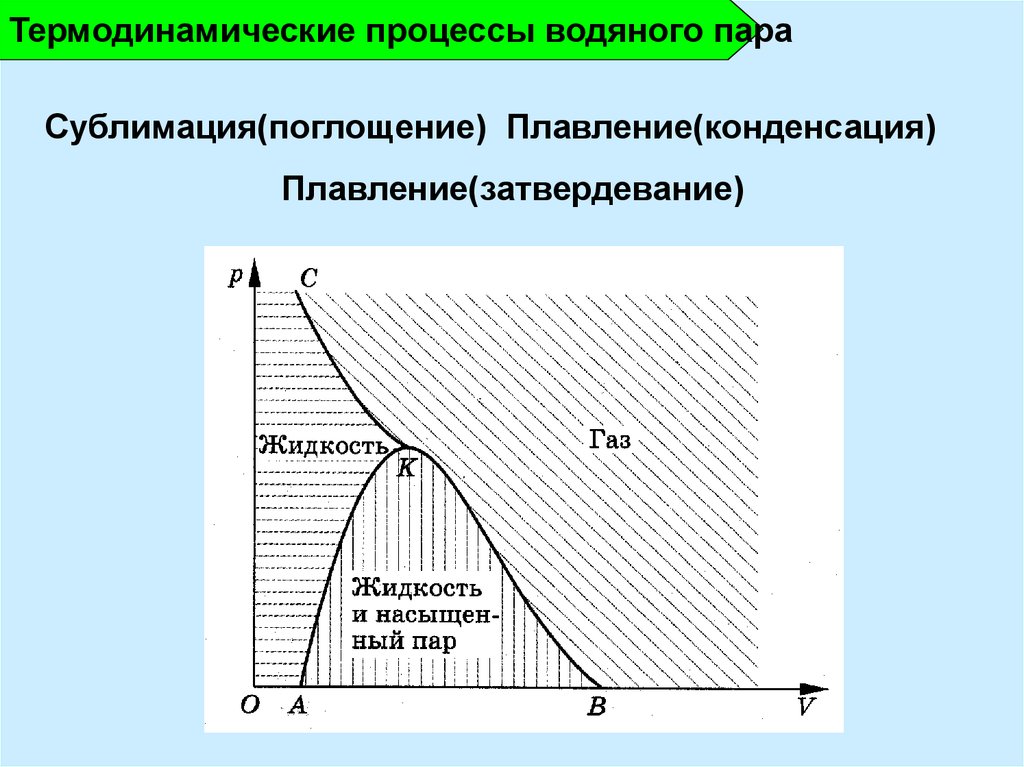
11.
Термодинамические процессы водяного параСублимация(поглощение) Плавление(конденсация)
Плавление(затвердевание)
12. Номограммы термодинамического состояния водяного пара
13. Смеси идеальных газов
Газовая смесь – механическая смесь отдельных компонентовразличных газов, химически не реагирующих между собой и
близких по свойствам к идеальным газам
Для газовых смесей справедливы следующие положения:
1. Каждый газ, входящий в смесь, имеет
температуру, равную температуре смеси.
2. Любой из газов, входящих в смесь,
распространяется по всему объему смеси, и
поэтому объем любого газа равен объему смеси.
14. Смеси идеальных газов
3. Каждый из газов, входящих в смесь,подчиняется своему уравнению состояния.
4. Смесь в целом является как бы новым газом
и подчиняется своему уравнению состояния.
5. Число молей смеси равно сумме молей
составляющих компонентов: см 1 2 n
15. Смеси идеальных газов
Закон Дальтона - давление смеси газов, химически невзаимодействующих друг с другом, равно сумме их
парциальных давлений
Парциальное давление – давление, которое имел бы газ, если
бы он один при той же температуре занимал весь объем смеси
n
p pi
i 1
16. Смеси идеальных газов
Для каждого компонента смеси уравнение состоянияследует записывать так:
piVсм mi Ri Tсм
Массовая доля
mn
gn
mсм
Объемная доля
Vn
rn
Vсм
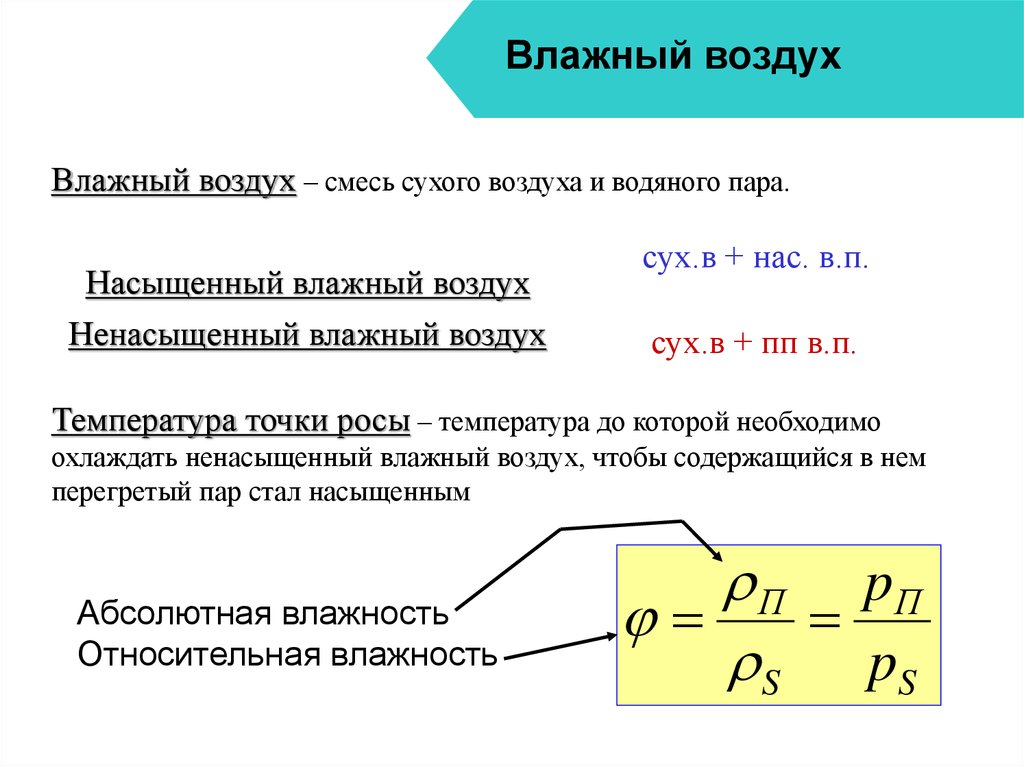
17. Влажный воздух
Влажный воздух – смесь сухого воздуха и водяного пара.Насыщенный влажный воздух
Ненасыщенный влажный воздух
сух.в + нас. в.п.
сух.в + пп в.п.
Температура точки росы – температура до которой необходимо
охлаждать ненасыщенный влажный воздух, чтобы содержащийся в нем
перегретый пар стал насыщенным
Абсолютная влажность
Относительная влажность
П pП
S pS
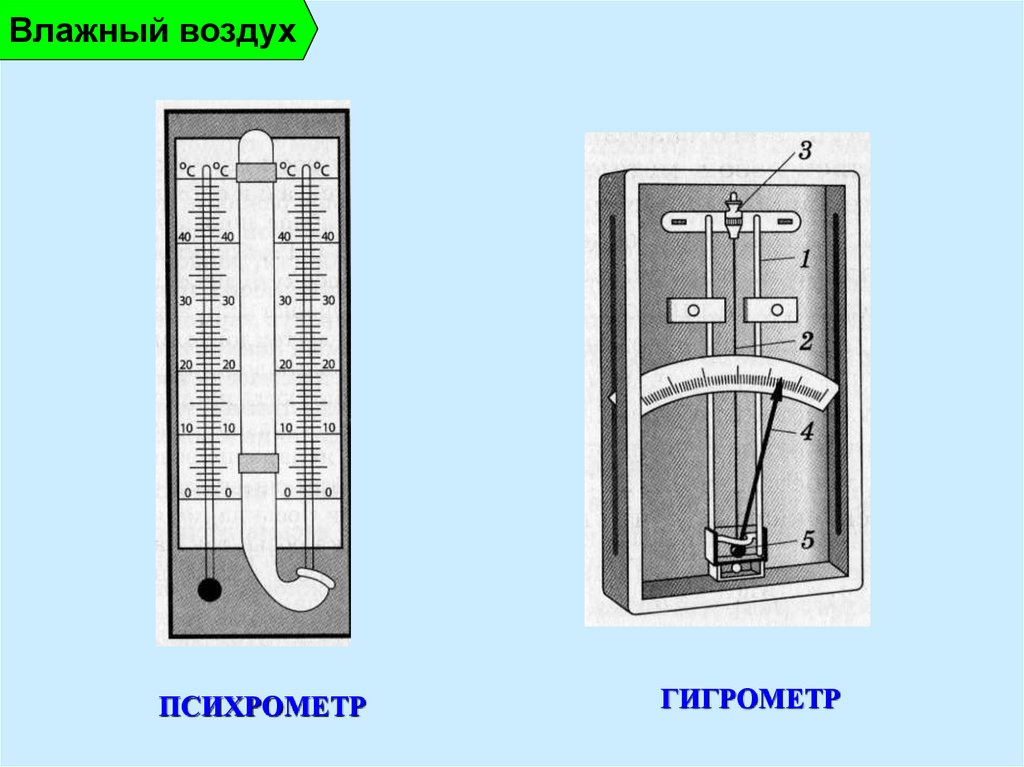
18.
Влажный воздухПСИХРОМЕТР
ГИГРОМЕТР
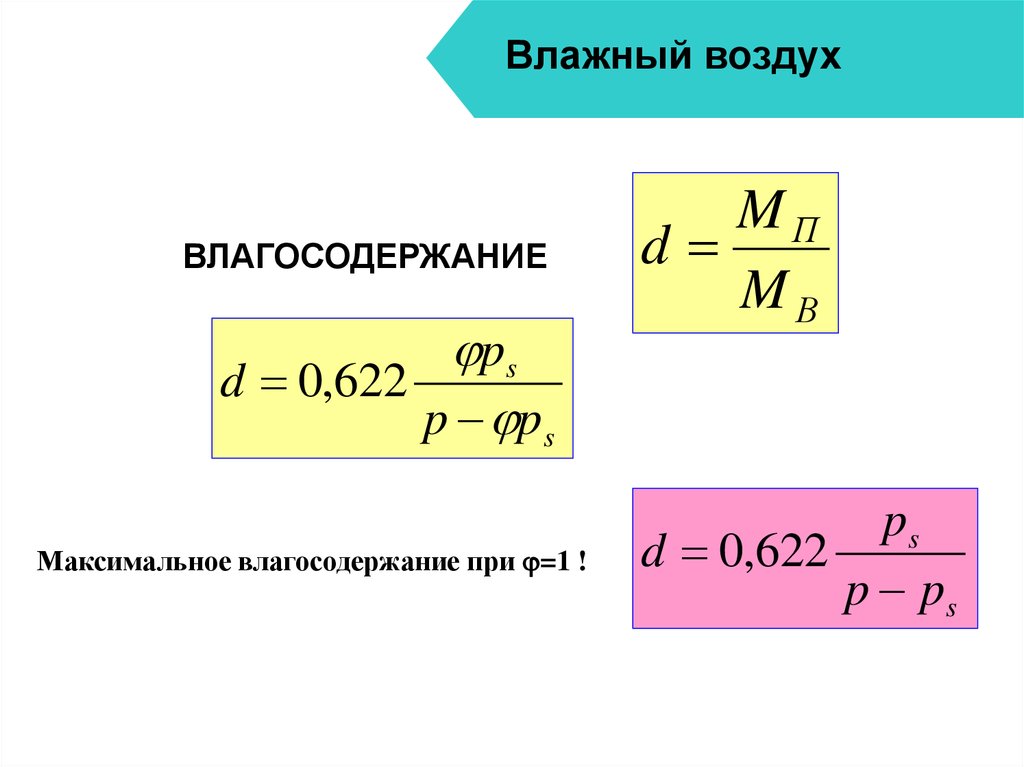
19. Влажный воздух
ВЛАГОСОДЕРЖАНИЕps
d 0,622
p ps
Максимальное влагосодержание при =1 !
MП
d
MВ
ps
d 0,622
p ps
20. Влажный воздух Теплоемкость и энтальпия
с p c pв dс pпПри теплоемкости сухого воздуха 1 кДж/(кг·К) и
водяного пара 2 кДж/(кг·К)
с p 1 2d
21. Влажный воздух Энтальпия
i iв diпПри теплоемкости сухого воздуха 1 кДж/(кг·К) и
водяного пара 2 кДж/(кг·К), а также с учетом
теплоты парообразования 2500 кДж/(кг·К)
i c pв t (2500 c pпt )d
или
i t (2500 2t )d
кДж/кг










 Физика
Физика








