Похожие презентации:
Атом и атомное ядро
1. Атом и атомное ядро
2. Атомная и ядерная физика – раздел физики, изучающий строение атома и атомного ядра и процессы, связанные с ними
3.
Атом – наименьшая частицахимического элемента, носитель
его свойств.
Элементарные частицы – это первичные,
неразложимые частицы, из которых, по
предположению, состоит вся материя.
В соответствии с этим определением к
элементарным частицам не могут быть
отнесены молекулы, атомы и атомные
ядра, которые поддаются делению на
составные части – атом делится на ядро и
орбитальные электроны,
ядро – на нуклоны.
4. Строение атома
1Строение атома
1) Опыт Резерфорда (1906 г)
5.
6.
2) Выводы Э. РезерфордаУченому понадобилось несколько лет,
чтобы понять столь неожиданное
рассеяние -частиц на большие углы.
В атомах большая часть «пустая»,
а отлетающие обратно –частицы
встречают на своем пути «сгусток»
положительно зараженной массы.
Этот сгусток был назван ядром атома.
7.
3) Строение атомаАтом
Ядро
состоит из нуклонов
(протонов и нейтронов)
Определяет массу
атома.
m(ядра) m(атома).
R(ядра) << R(атома)
Электронная
оболочка
состоит из
электронов
Определяет размер
атома.
R(эл.об.) = R(атома)
m(эл.об.) 0.
8. Состав атома
Атомы химических элементов состоят изтрех частиц:
протоны
1
1
р
или р+
нейтроны
0
1
n
или n0
электроны
1
0
e
или е–
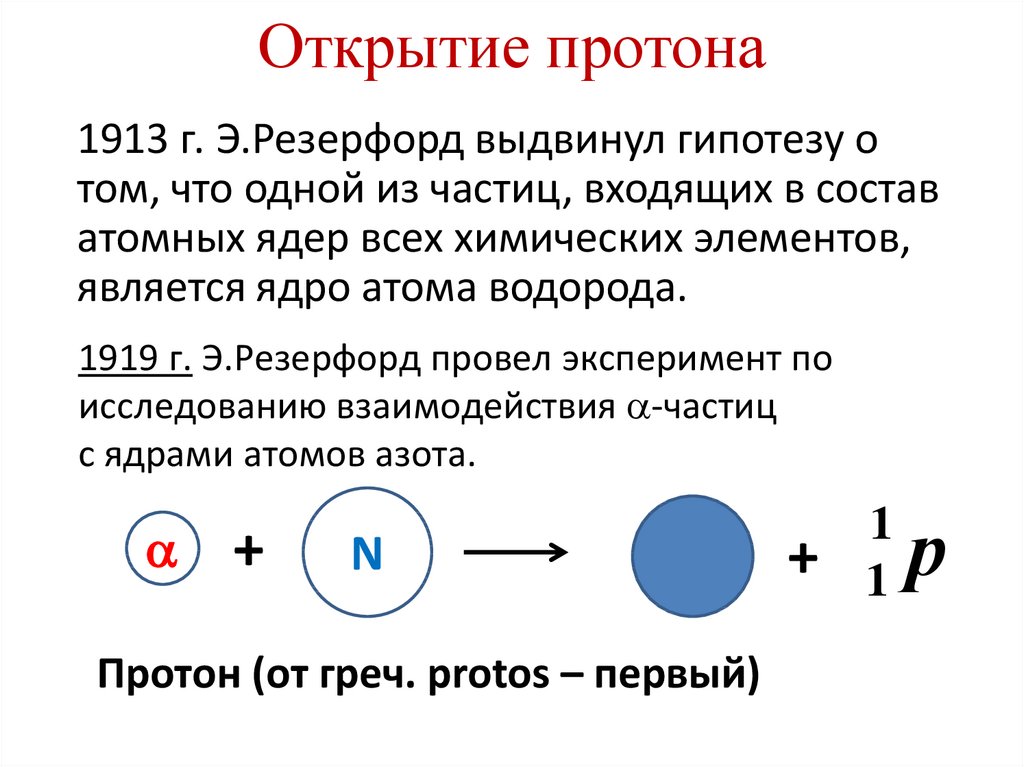
9. Открытие протона
1913 г. Э.Резерфорд выдвинул гипотезу отом, что одной из частиц, входящих в состав
атомных ядер всех химических элементов,
является ядро атома водорода.
1919 г. Э.Резерфорд провел эксперимент по
исследованию взаимодействия -частиц
с ядрами атомов азота.
+
N
Протон (от греч. protos – первый)
+
1
1
р
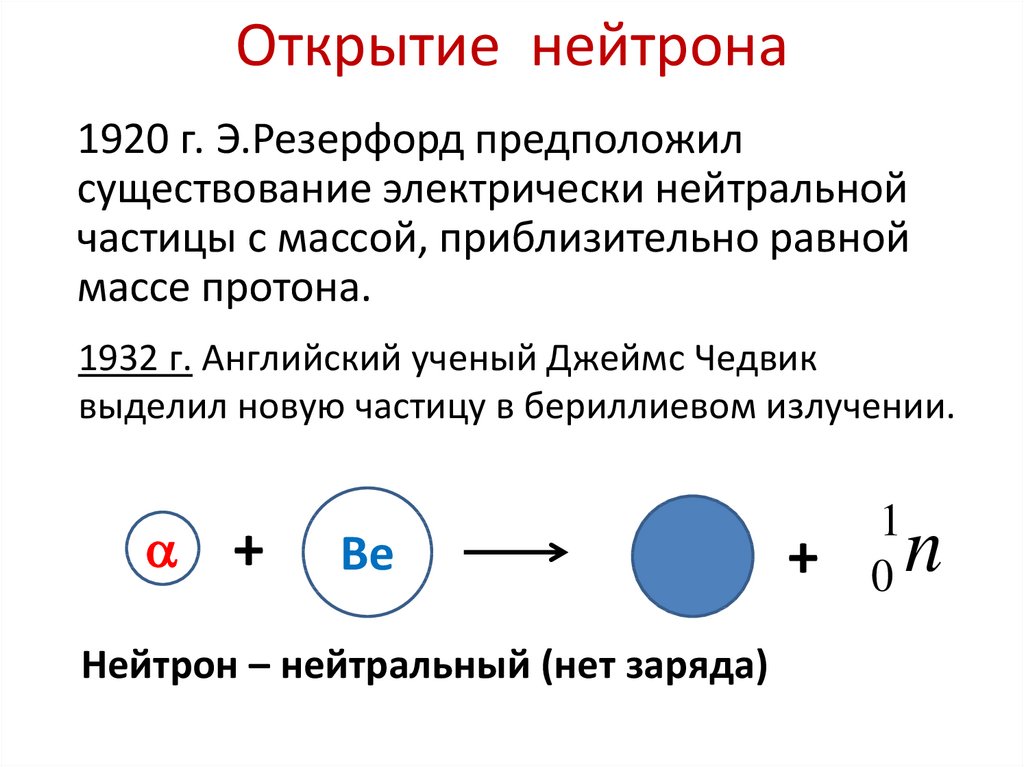
10. Открытие нейтрона
1920 г. Э.Резерфорд предположилсуществование электрически нейтральной
частицы с массой, приблизительно равной
массе протона.
1932 г. Английский ученый Джеймс Чедвик
выделил новую частицу в бериллиевом излучении.
+
Ве
Нейтрон – нейтральный (нет заряда)
+
1
0
n
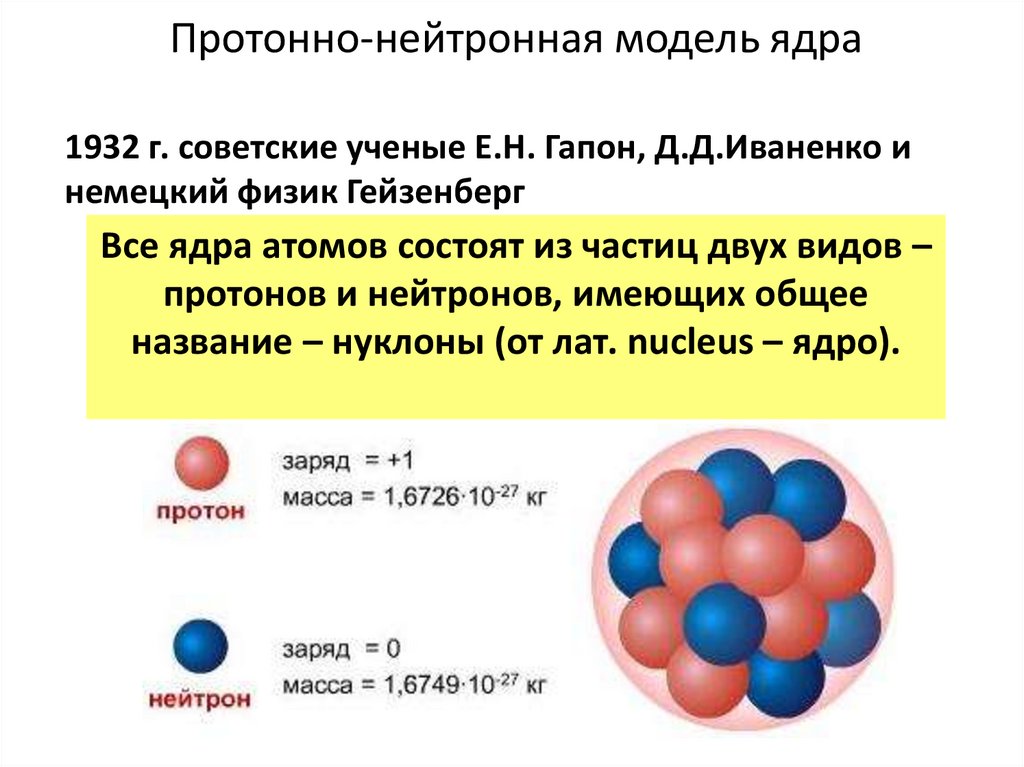
11. Протонно-нейтронная модель ядра
1932 г. советские ученые Е.Н. Гапон, Д.Д.Иваненко инемецкий физик Гейзенберг
Все ядра атомов состоят из частиц двух видов –
протонов и нейтронов, имеющих общее
название – нуклоны (от лат. nucleus – ядро).
12. 4) Количественная характеристика атомов
AZ
7
3
Х
Li
А – массовое число атома
Z – зарядовое число атома
Масса атомов: 7 а.е.м.
Заряд ядра: + 3
Состав ядра:
число протонов: 3
число нейтронов: 4
Число электронов: 3
} нуклоны
13.
Опишите характеристики исостав атомов
14
6
C
Масса атомов: 14 а.е.м.
Заряд ядра: + 6
Состав ядра:
число протонов: 6
нуклоны
число нейтронов: 8
Число электронов: 6
}
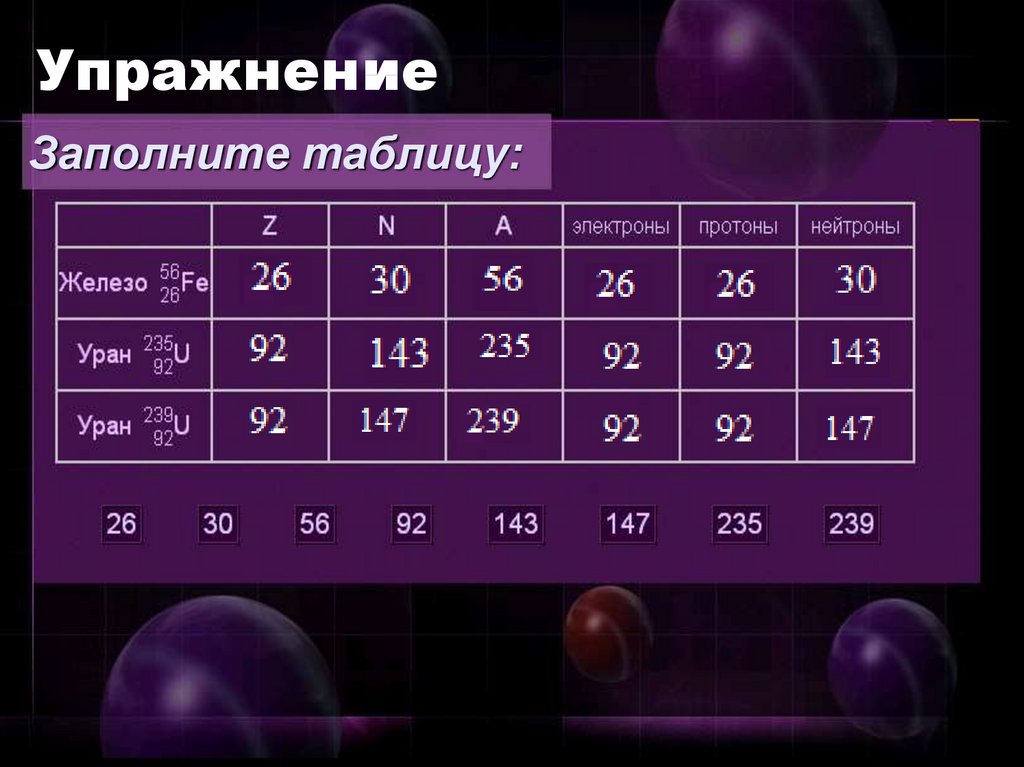
14.
Задание. С помощью периодической таблицыМенделеева определите состав ядер указанных
ниже элементов:
235
92


























 Физика
Физика








