Похожие презентации:
Первый закон термодинамики
1. I закон термодинамики
I ЗАКОН ТЕРМОДИНАМИКИ2. Закон сохранения энергии
ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИЭнергия в природе не возникает из
ничего и не исчезает: количество
энергии неизменно, она только
переходит из одной формы в другую.
3.
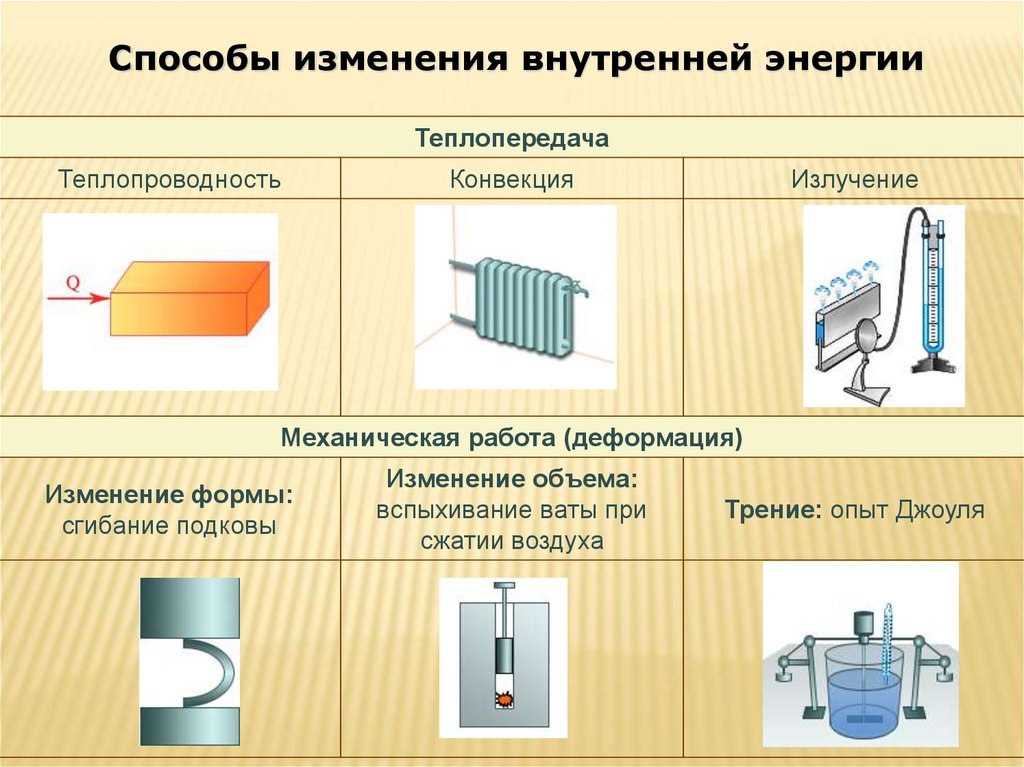
Способы изменения внутренней энергииТеплопередача
Теплопроводность
Конвекция
Излучение
Механическая работа (деформация)
Изменение формы:
сгибание подковы
Изменение объема:
вспыхивание ваты при
сжатии воздуха
Трение: опыт Джоуля
4. I закон термодинамики
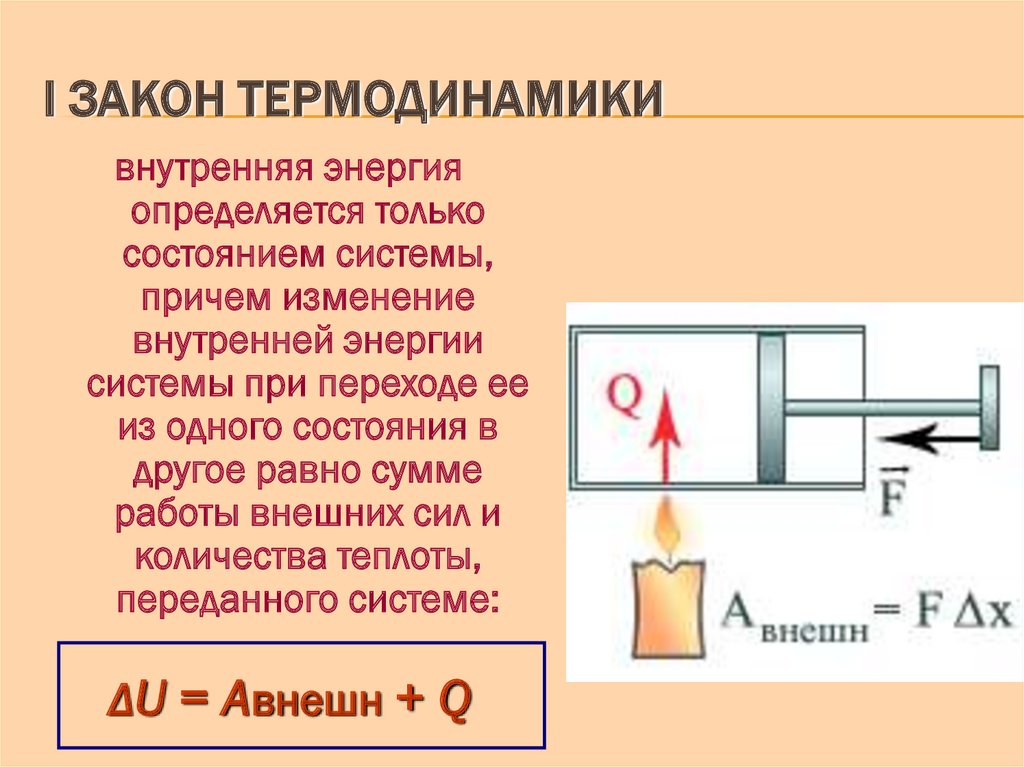
I ЗАКОН ТЕРМОДИНАМИКИвнутренняя энергия
определяется только
состоянием системы,
причем изменение
внутренней энергии
системы при переходе ее
из одного состояния в
другое равно сумме
работы внешних сил и
количества теплоты,
переданного системе:
ΔU = Aвнешн + Q
5. Если при нагревании газ расширяется и при этом совершает работу A, то первый закон термодинамики можно сформулировать
ЕСЛИ ПРИ НАГРЕВАНИИ ГАЗ РАСШИРЯЕТСЯ ИПРИ ЭТОМ СОВЕРШАЕТ РАБОТУ A, ТО ПЕРВЫЙ
ЗАКОН ТЕРМОДИНАМИКИ МОЖНО
СФОРМУЛИРОВАТЬ ПО-ДРУГОМУ:
Q = ΔU + AI
Количество теплоты, переданное газу, равно сумме
изменения его внутренней энергии и работы,
совершенной газом.
Так как работа газа и работа внешних сил вследствие 3го закона Ньютона равны по модулю и имеют
противоположный знак:
Aвнешн = –AI
6. I закон термодинамики и изопроцессы
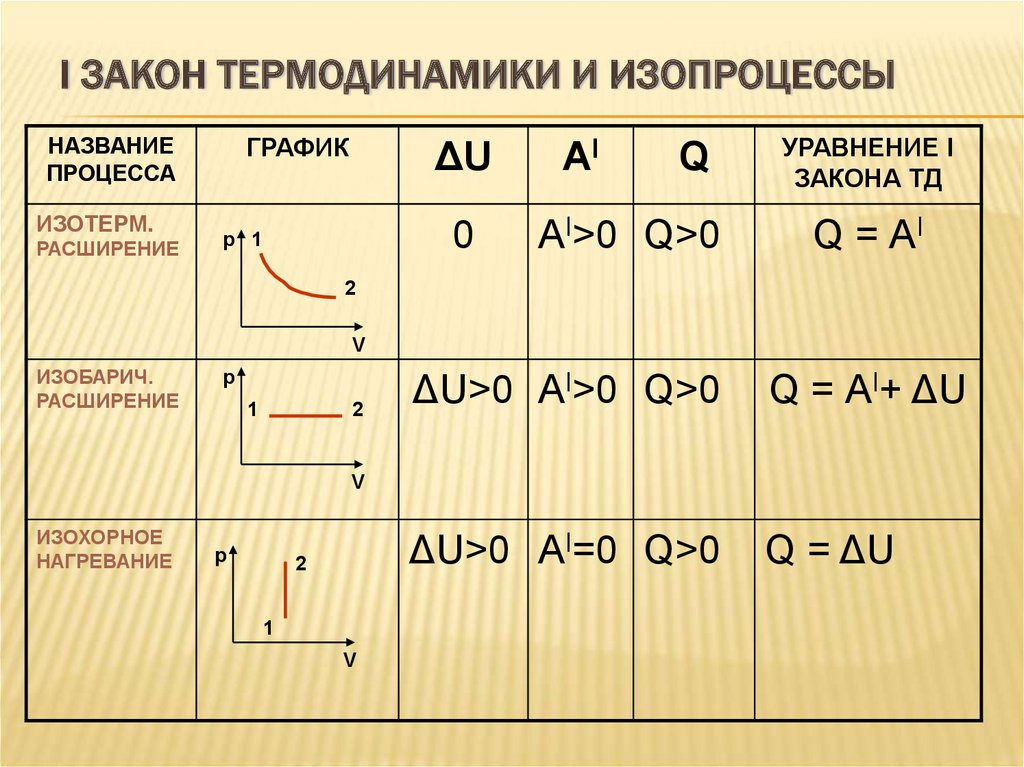
I ЗАКОН ТЕРМОДИНАМИКИ И ИЗОПРОЦЕССЫНАЗВАНИЕ
ПРОЦЕССА
ИЗОТЕРМ.
РАСШИРЕНИЕ
ГРАФИК
ΔU
0
р 1
AI
Q
АI>0 Q>0
УРАВНЕНИЕ I
ЗАКОНА ТД
Q = АI
2
V
ИЗОБАРИЧ.
РАСШИРЕНИЕ
р
1
2
ΔU>0 АI>0 Q>0
Q = АI+ ΔU
ΔU>0 АI=0 Q>0
Q = ΔU
V
ИЗОХОРНОЕ
НАГРЕВАНИЕ
р
2
1
V
7. I закон термодинамики и изопроцессы
I ЗАКОН ТЕРМОДИНАМИКИ И ИЗОПРОЦЕССЫНАЗВАНИЕ
ПРОЦЕССА
ИЗОТЕРМ.
СЖАТИЕ
ГРАФИК
ΔU
0
р 2
AI
Q
АI<0 Q<0
УРАВНЕНИЕ I
ЗАКОНА ТД
Q = АI
1
V
ИЗОБАРИЧ.
СЖАТИЕ
р
2
1
ΔU<0 АI<0 Q<0
Q = АI+ ΔU
ΔU<0 АI=0 Q<0
Q = ΔU
V
ИЗОХОРНОЕ
ОХЛАЖДЕНИЕ
р
1
2
V
8. Адиабатный процесс
АДИАБАТНЫЙ ПРОЦЕСС– это модель
термодинамического
процесса, происходящего в р
системе без теплообмена с
окружающей средой.
р0
Линия на термодинамической
диаграмме состояний системы, р1
изображающая равновесный
р2
(обратимый) адиабатический
процесс, называется адиабатой.
V
V1
V2
9. I закон термодинамики и изопроцессы
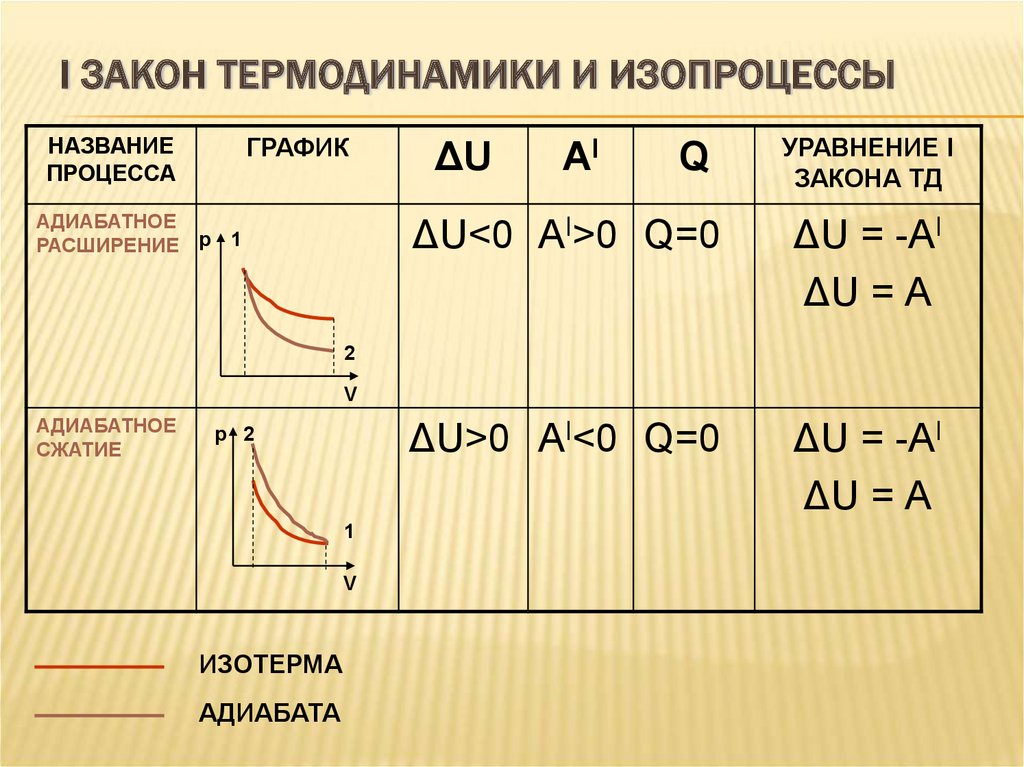
I ЗАКОН ТЕРМОДИНАМИКИ И ИЗОПРОЦЕССЫНАЗВАНИЕ
ПРОЦЕССА
ГРАФИК
АДИАБАТНОЕ
РАСШИРЕНИЕ р
1
ΔU
AI
Q
УРАВНЕНИЕ I
ЗАКОНА ТД
ΔU<0 АI>0 Q=0
ΔU = -АI
ΔU = А
ΔU>0 АI<0 Q=0
ΔU = -АI
ΔU = А
2
V
АДИАБАТНОЕ
СЖАТИЕ
р 2
1
V
ИЗОТЕРМА
АДИАБАТА
10. ЗАДАНИЯ
1.2.
Изучить материал;
Записать в тетрадь таблицы.






 Физика
Физика








