Похожие презентации:
Химические свойства оксидов
1.
(подсказки ученику)Задание № 1: составить уравнения
возможных реакций
(на примере темы «Химические свойства оксидов»)
Составитель:
Анна Валерьевна Дзенис
учитель химии
СП ЦО 109 в ФНКЦ ДГОИ
2.
Уважаемые восьмиклассники!Предлагаемая презентация поможет вам научиться
выполнять задания вида «Составить уравнения возможных
реакций» на примере темы «Химические свойства оксидов».
Презентация содержит:
- алгоритм выполнения задания (последовательность действий),
- обучающие примеры (в них с помощью анимации показана
последовательность действий),
- тренировочные примеры (их нужно выполнить в тетради
самостоятельно, а чтобы проверить себя, нажмите
соответствующую выноску),
- справочный материал (выноска-облачко), который может
понадобиться при выполнении упражнения.
УСПЕХОВ!
3.
1) В левой части схемы под формулой каждого исходноговещества подпишите, к какому классу оно относится.
2) Проверьте, могут ли реагировать вещества, принадлежащие к
этим классам.
3) Если взаимодействие возможно, определите, к каким классам
относятся продукты реакций.
4) В правой части схемы реакции (после "→ ") внизу подпишите
названия классов образующихся веществ.
5) Составьте формулы продуктов реакции в соответствии с
тем, к каким классам они относятся. (Не забудьте, составляя
формулы, поставить значения валентностей и определить
индексы!)
4.
Задание:составить уравнение возможной реакции
ВаO + HCl
→ ….
Если вы
забыли
свойства
оксидов
Решение:
II
ВаO
основный
оксид
+ 2 HCl →
=
кислота
I
ВаCl2 +
соль
H2O
вода
(Взаимодействие возможно,
так как основные оксиды реагируют с кислотами)
Следующий
пример
5.
Задание: составить уравнение возможной реакцииРешение:
II
III
3 SrO + 2 H3PO4 →
= Sr 3 (PO4) 2 + 3 H2O
основный
оксид
Если вы
забыли
свойства
оксидов
кислота
соль
Проверьте
себя
вода
Следующий
пример
6.
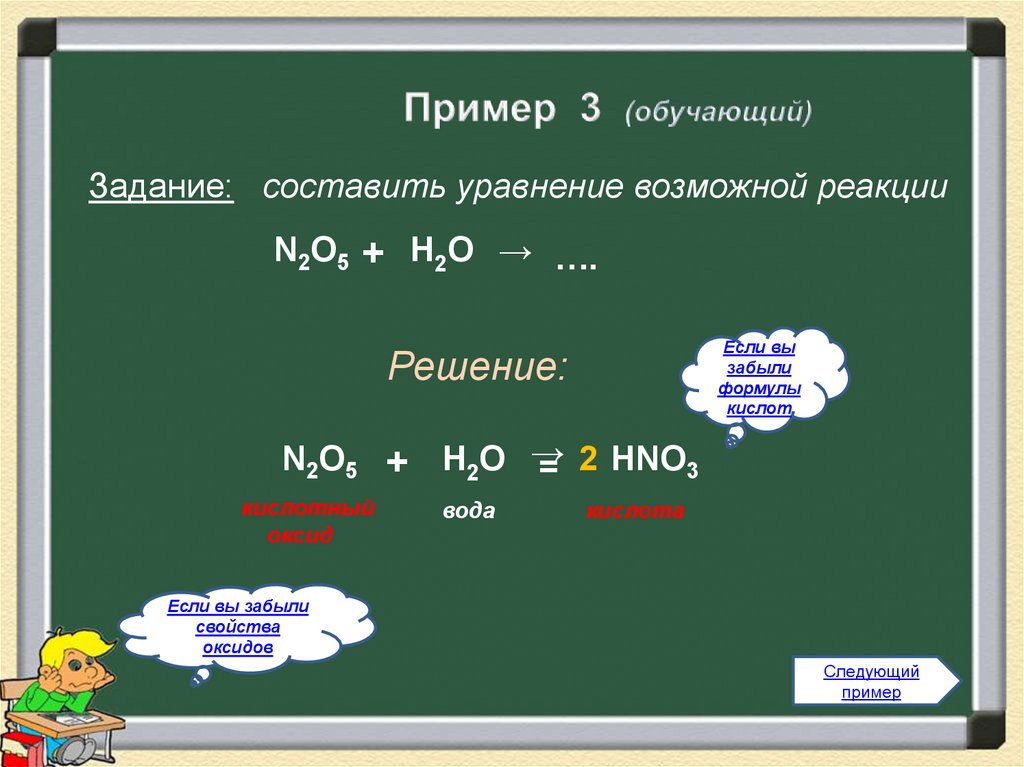
Задание: составить уравнение возможной реакцииN2O5 + Н2О → ….
Если вы
забыли
формулы
кислот
Решение:
N2O5 + Н2О →
= 2 НNO3
кислотный
оксид
вода
кислота
Если вы забыли
свойства
оксидов
Следующий
пример
7.
Задание: составить уравнение возможной реакцииРешение:
СuO
основный
оксид
Если вы
забыли
свойства
оксидов
+
Н2О →
≠
вода
Подсказки: 1) Каков характер данного оксида меди?
2) Обратите внимание, какие основные
оксиды взаимодействуют с водой.
3) Будет ли реагировать с водой данный
оксид? Почему?
Следующий
пример
8.
Задание: составить уравнение возможной реакцииРешение:
I
I
а) Rb2O + Н2О →
= 2 RbОН
основный
оксид
щелочь
вода
б) SiO2 + Н2О →
≠
кислотный
оксид
Если вы
забыли
свойства
оксидов
вода
Проверьте
себя
Подсказки:
1) Каков характер
оксида рубидия?
Может ли он
реагировать с
водой? Почему?
2) Каков характер
оксида кремния(IV)?
Будет ли
реагировать с
водой данный
оксид? Почему?
Следующий
пример
9.
Задание: составить уравнение возможной реакцииР2O5 +
NaOH → ….
Если вы забыли
формулу
кислотного
остатка
Решение:
I
III
Р2O5 + 6 NaOH →
= 2 Na 3РO4 + 3 Н2О
кислотный
оксид
Если вы забыли
свойства
оксидов
щелочь
соль
вода
Следующий
пример
10.
Задание: составить уравнение возможной реакцииЕсли вы
забыли
формулу
кислотного
остатка
Решение:
I
SO3
кислотный
оксид
Если вы
забыли
свойства
оксидов
II
+ 2 KOH →
= K2 SO4 + Н2О
щелочь
соль
Проверьте
себя
вода
Следующий
пример
11.
Задание: составить уравнение возможной реакцииРешение:
К2О + Na2O →
≠
основный
оксид
основный
оксид
Подсказка: 1) Каков характер данных оксидов?
2) Возможно ли взаимодействие между такими оксидами?
Если вы
забыли
свойства
оксидов
Проверьте
себя
Следующий
пример
12.
Задание: составить уравнение возможной реакцииSiO2 + CaO → ….
Если вы
забыли
формулу
кислотного
остатка
Решение:
II
SiO2
кислотный
оксид
Если вы
забыли
свойства
оксидов
+
II
CaO →
= Ca SiO3
основный
оксид
соль
Следующий
пример
13.
Задание: составить уравнение возможной реакцииРешение:
I
Rb2O
основный
оксид
Если вы
забыли
свойства
оксидов
Если вы
забыли
формулу
кислотного
остатка
II
+ CO2 →
= Rb 2CO3
кислотный
оксид
соль
Проверьте
себя
Следующий
пример
14.
Задание: составить уравнения возможных реакцийа) СO2
+ Ва(ОН)2 →
б) Н2О
+ CaO →
Если вы
забыли
формулу
кислотного
остатка
в) SiO2 + Н2О →
г) НNO3 + MgО →
д) Li2O + CO2 →
Если вы
забыли
свойства
оксидов
е) SrO
+
CaО →
ж) Н2О + HgO →
з) SO3
+ Н2О →
Проверьте
себя
15.
Проверьте себяII
+ Ва(ОН)2 = ВаСO3 + Н2О
кислотный
оксид
щелочь
соль
II
+ CaO = Са(ОН)2
вода
основный
оксид
в) SiO2 + Н2О ≠
(исключение)
вода
II
кислотный
оксид
щелочь
I
б) Н2О
вода
I
а) СO2
II
г) 2 НNO3 + MgО = Mg(NO3)2 + Н2О
кислота
основный
оксид
соль
вода
продолжение
16.
Проверьте себя(продолжение)
д) Li2O
основный
оксид
е) SrO
основный
оксид
I
II
+ CO2 = Li2CO3
кислотный
оксид
+
соль
CaО ≠
основный
оксид
ж) Н2О + HgO ≠
вода
з) SO3
кислотный
оксид
основный
оксид
+ Н2О = Н2SO4
вода
кислота

















 Химия
Химия








