Похожие презентации:
Щелочные металлы
1.
2.
ЦЕЛИ УРОКА :• Обучающие: расширить знания учащихся о химических
свойствах металлов на примере щелочных, рассмотреть
особенности взаимодействия щелочных металлов с
неметаллами и водой, опираясь на знания зависимости
свойств от особенности строения.
• Развивающие: способствовать дальнейшему развитию
логического мышления учащихся- формировать умение
сравнивать, обобщать. Продолжить развитие навыков
самообразования: умение работать с книгой, инструкцией
текстом.
• Воспитывающие: воспитание устойчивого интереса к
предмету, коммуникативную культуру, самостоятельность,
ответственное отношение к порученному делу.
3.
Назовите закономерности в строенииатомов щелочных металлов:
- Сходство внешнего электронного слоя.
- Последовательное изменение атомных
радиусов.
- Увеличение числа электронных слоев в
атоме.
- Радиусы атомов увеличиваются от Li к
Cs, следовательно увеличиваются и
восстановительные свойства металлов
от Li к Cs.
4.
Проверь себя(работа с таблицей Д.И. Менделеева)
• Сравните атомы элементов, поставив знаки <, > или =
вместо *:
а)
б)
в)
г)
д)
заряд ядра: Li * Rb, Na * Al, Ca * К;
число электронных слоев: Li * Rb, Na * Al, Ca * К;
число электронов на внешнем уровне: Li * Rb, Na * Al, Ca * К;
радиус атома: Li * Rb, Na * Al, Ca * K;
восстановительные свойства: Li * Rb, Na * Al, Ca * K.
5.
6.
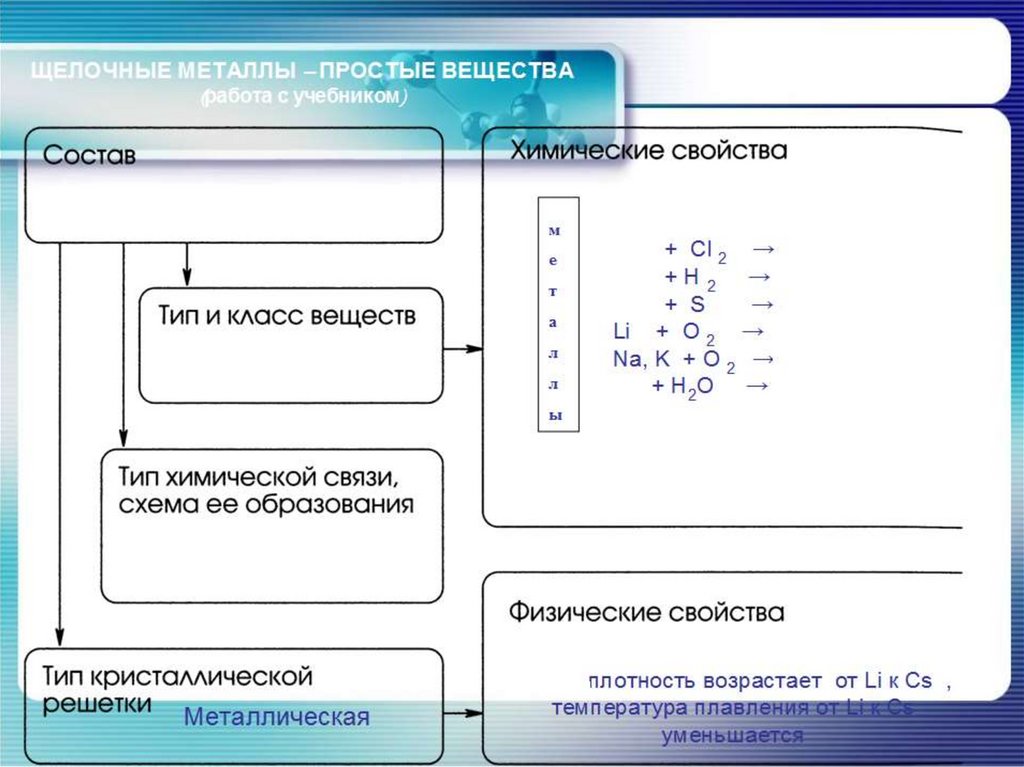
ЩЕЛОЧНЫЕ МЕТАЛЛЫ – ПРОСТЫЕ ВЕЩЕСТВА(работа с учебником)
м
е
т
а
Простые
Металлы
л
л
+ Cl 2 → хлориды
+ H 2 → гидриды
+ S
→ сульфиды
Li + O 2 → оксид
Na, K + O 2 →пероксид
+ H2O →щелочь + Н 2
ы
Металлическая
МЕ0– 1 е → МЕ+1
Металлическая
Серебристо-белые, мягкие, металлический
блеск, плотность возрастает от Li к Cs ,
температура плавления от Li к Cs
уменьшается
7.
Проверь себя(самостоятельная работа)
Дополните схемы взаимодействия щелочных металлов с неметаллами
общими формулами и названиями продуктов реакции.
а) М+ Н 2
б) М+ S
_____________
____________
______________________________
в) М+ С12 ________________
г) М+ N2
_____________________
____________________________
8.
Проверь себяСоставьте уравнения реакций с кислородом:
а) лития ________________ ; б) натрия _______________
Расставьте степени окисления элементов, покажите стрелкой
переход электронов. Назовите продукты реакций.
1.
2. Дайте
характеристику реакции лития с кислородом:
Допишите уравнения реакций. Как изменяется скорость реакций,
в указанной стрелкой последовательности?
1) расположенных
по числу и составу
исходных веществ и продуктов реакции
_____________
а) изменению
Li + H O→ ……………………….
2) по
степеней окисления……………………………………………
атомов - _______________
б)
Na + H O→……………………….
……………………………………………
в) К + Н О→………………………..
……………………………………………
3) по
направлению - _______________________
, от чего
это зависит
………………………..
Объясните
………………………..
4)Объясните,
по тепловому
эффекту
-____________________
Назовите продукты реакций.
.
Опишите,
реакций Опишите, как доказать их образование.
образование.
5)………………………............................................
по агрегатному состоянию веществ- ________________
2
2
2







 Химия
Химия








