Похожие презентации:
Производство серной кислоты
1. Презентация на тему «Производство серной кислоты»
Выполнила:Ученица 11
французского класса
Александрова
Валентина
2.
Серная кислота H2SO4 :сильная двухосновная кислота,
отвечающая высшей степени окисления
серы (+6).
тяжёлая
маслянистая жидкость без цвета и запах
а
в технике серной кислотой называют её
смеси как с водой, так и с серным
ангидридом SO3.
3.
бесцветная маслянистая жидкостьКислота серная
техническая.
4.
Структурная формула серной кислотыСырьём для получения серной
кислоты служат
сера
сульфиды металлов
сероводород
отходящие газы теплоэлектростанций
сульфаты железа
кальция
5.
Основные стадии получения сернойкислоты:
Обжиг сырья с получением SO2
Окисление SO2 в SO3
Абсорбция SO3
В промышленности применяют два
метода окисления SO2 в производстве
серной кислоты:
контактный — с использованием
твердыхкатализаторов(контактов)
нитрозный — с оксидами азота.
6.
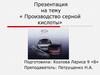
Схемы производства серной кислоты7.
реакции по производству сернойкислоты из минерала пирита на
катализаторе — оксиде ванадия (V).
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
2SO2 + O2 (V2O5) → 2SO3
Нитрозный метод получения серной
кислоты
SO2 + NO2 → SO3 + NO↑.
2NO+O2 → 2NO2
8.
При реакции SO3 с водой выделяется огромноеколичество теплоты и серная кислота начинает
закипать с образованием "туманов"
SO3 + H2O = H2SO4 + Q Поэтому
SO3смешивается с H2SO4, образуя раствор
SO3 в 91% H2SO4 - олеум
Получение серной кислоты из железного
купороса - термическое разложение сульфата
железа (II) с последующим охлаждением смеси
2FeSO4·7H2O→Fe2O3+SO2+H2O+O2
SO2+H2O+O2 ⇆ H2SO4
9.
Естественные источникисерной кислоты
10.
Производство серной
кислоты
на
Бийском
олеумном
заводе
установки очистки серной кислоты
цеха по производства серной
кислоты концерна Стирол









 Химия
Химия