Похожие презентации:
Характеристика азота и фосфора. Свойства азота
1.
«Характеристика азота и фосфора.Свойства азота.»
2.
НАХОЖДЕНИЕ АЗОТА В ПРИРОДЕ:в свободном состоянии в атмосфере
3.
НАХОЖДЕНИЕ АЗОТА В ПРИРОДЕ:в виде соединений
неорганических
В небольших количествах
в почве: в виде солей аммония
и нитратов.
органических
Азот растений и животных
(Нуклеиновые кислоты,
белковые вещества)
4.
ПРИЗНАКИСРАВНЕНИЯ
ПОЛОЖЕНИЕ В
ПСХЭ
СТРОЕНИЕ
АТОМА
АЗОТ
2 период V группа
Главная подгруппа
Порядковый номер 7;
относительная атомная масса
14
N+7) )
2 5
Число электронов
в атоме 7,
протонов в ядре 7, число
нейтронов в ядре 7
Электронная схема: 1s22s22p3
ФОСФОР
3 периодV группа
главная подгруппа
Порядковый номер 15;
относительная атомная масса
31
Р +15 )2)8)5
Число электронов в атоме 15,
протонов в ядре 15, число
нейтронов в ядре 16
Электронная схема:
1s22s22p6 3s22p3
СТЕПЕНИ
ОКИСЛЕНИЯ
+1,+2,+3,+4,
+5,-3
+3, +5, -3
5.
Определите степени окисления азота всоединениях:
HNО3, NН3, NO, KNО2, NО2,
N2О,НNO2
с.о.
-3
0
+1
+2
+3
+4
+5
соединение
NH3
N2
N2O
NO
N 2 O3
NO2
N 2 O5
6.
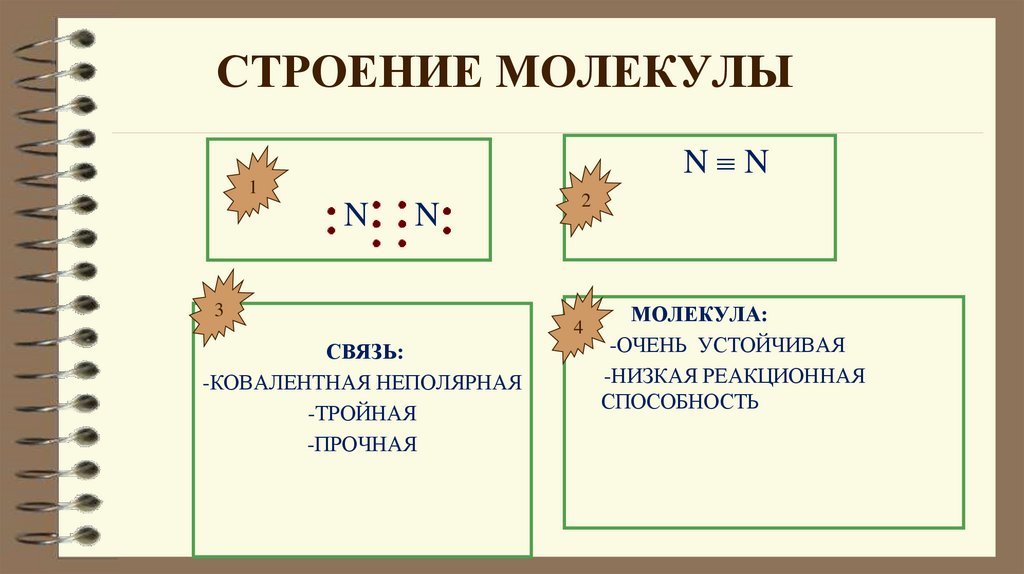
СТРОЕНИЕ МОЛЕКУЛЫN N
1
N
N
3
СВЯЗЬ:
-КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ
-ТРОЙНАЯ
-ПРОЧНАЯ
2
4
МОЛЕКУЛА:
-ОЧЕНЬ УСТОЙЧИВАЯ
-НИЗКАЯ РЕАКЦИОННАЯ
СПОСОБНОСТЬ
7.
Получение.1. В промышленности азот получают
дистилляцией воздуха,
2. в лаборатории – термическим разложением
соединений (чаще всего NH4NO2):
NH4NO2 → N2 + 2H2O
3. Фосфор получают путем прокаливания
фосфата кальция с углем и песком в
электропечах при 15000С:
2Ca3(PO4)2 + 10C + 6SiO2 → 6CaSiO3 + 10CO + P4
8.
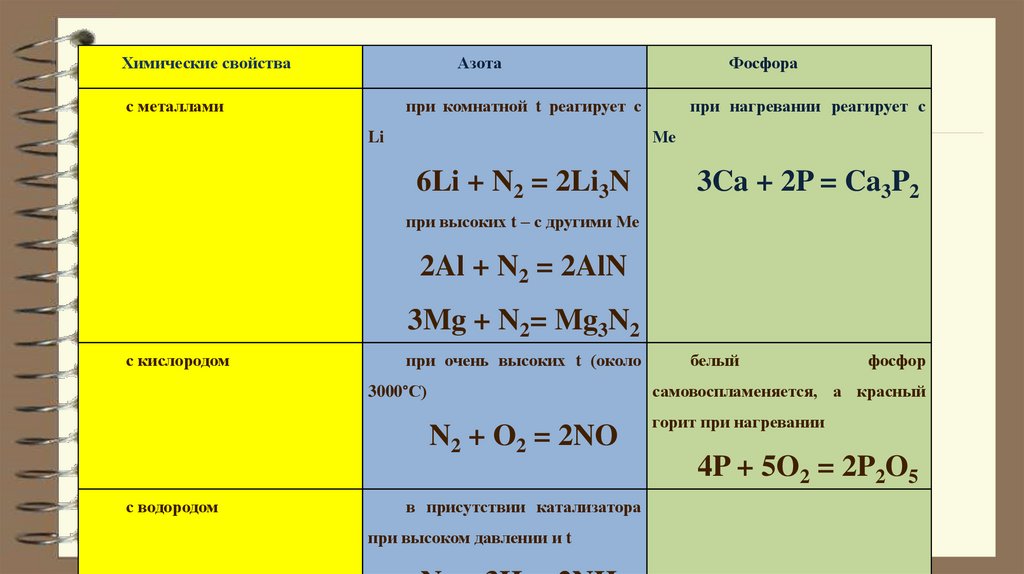
Химические свойстваАзота
с металлами
Фосфора
при комнатной t реагирует с
при нагревании реагирует с
Ме
Li
6Li + N2 = 2Li3N
3Ca + 2P = Ca3P2
при высоких t – с другими Ме
2Al + N2 = 2AlN
3Mg + N2= Mg3N2
с кислородом
при очень высоких t (около
фосфор
самовоспламеняется, а красный
3000°С)
N2 + O2 = 2NO
с водородом
белый
в присутствии катализатора
при высоком давлении и t
горит при нагревании
4P + 5O2 = 2P2O5
9.
ПрименениеПолучение аммиака
Создание инертной атмосферы
Создание низких температур
Насыщение поверхности стали
для повышения прочности
10.
выводы1. Газ без цвета , вкуса и запаха
2. Молекула двухатомна
3. Содержание в воздухе 78 %
4. В лаборатории получают разложением KMnO4 и H2O2
5. В промышленности – из жидкого воздуха
6. Химически малоактивен
7. Взаимодействует почти со всеми простыми веществами
8. С ним связаны процессы дыхания и фотосинтеза
9. Является составной частью белков
10. Участвует в круговороте веществ в природе








 Химия
Химия