Похожие презентации:
Химические свойства и применение кислорода
1.
ХИМИЧЕСКИЕ СВОЙСТВАИ ПРИМЕНЕНИЕ
КИСЛОРОДА
2.
Химические свойства – способностьвеществ превращаться в другие под
воздействием определенных условий:
при изменении температуры, давления
и т. д.
3.
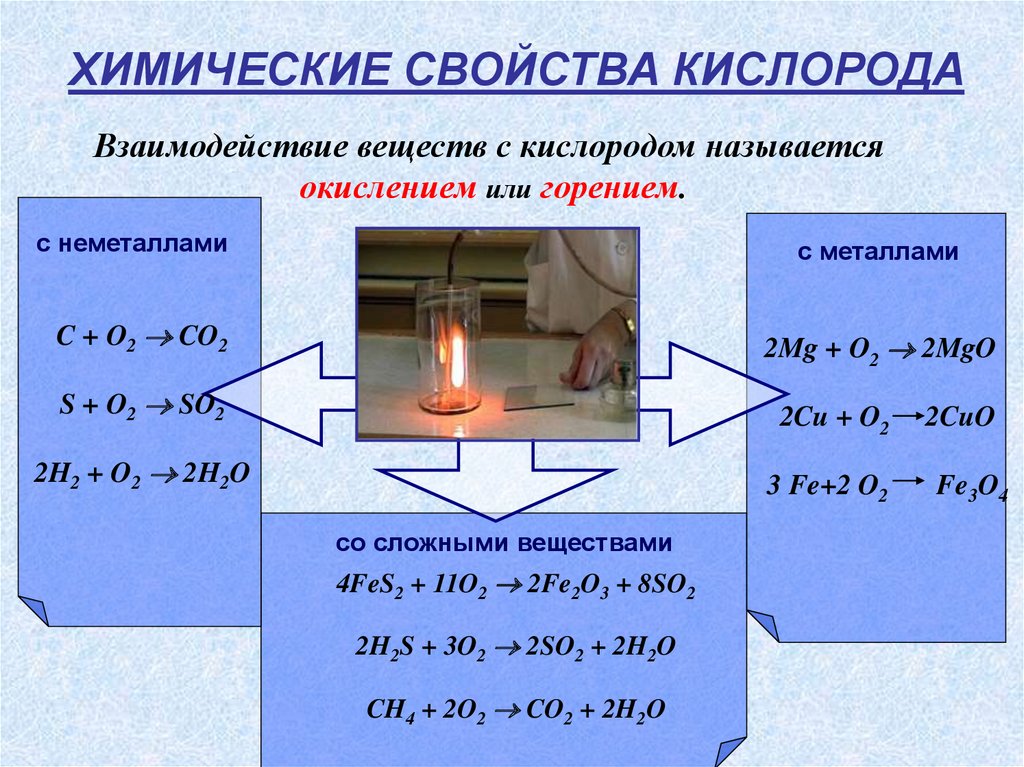
ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОРОДАВзаимодействие веществ с кислородом называется
окислением или горением.
с неметаллами
с металлами
C + O2 CO2
2Mg + O2 2MgO
S + O2 SO2
2Cu + O2
2H2 + O2 2H2O
3 Fe+2 O2
со сложными веществами
4FeS2 + 11O2 2Fe2O3 + 8SO2
2H2S + 3O2 2SO2 + 2H2O
CH4 + 2O2 CO2 + 2H2O
2CuO
Fe3O4
4.
Кислород – сильный окислитель.С кислородом реагируют все элементы, кроме
Au, Pt, He, Ne и Ar.
В результате взаимодействия веществ с
кислородом образуется оксиды.
Оксиды – сложные вещества, которые
состоят из двух элементов, одним из которых
является кислород.
5.
ВЗАИМОДЕЙСТВИЕ ПРОСТЫХ И СЛОЖНЫХВЕЩЕСТВ С КИСЛОРОДОМ НАЗЫВАЕТСЯ
ОКИСЛЕНИЕМ.
ГОРЕНИЕ —ХИМИЧЕСКАЯ РЕАКЦИЯ,ПРИ
КОТОРОЙ ПРОИСХОДИТ ОКИСЛЕНИЕ
ВЕЩЕСТВ С ВЫДЕЛЕНИЕМ ТЕПЛА И СВЕТА.
6. ЗАДАНИЕ № 1
Вставь вместо «?» необходимую формулу с коэффициентом.А)
4P
+
?
=
2P2O5
Б)
?
+
3O2
=
2Al2O3
В)
4K
+
2O2
=
Г)
2PH3
+
4O2
=
?
+
3H2O
Д)
2C2H2
+
5 O2
=
2CO2
+
?
?
7. ЗАДАНИЕ № 2
10оксидов
ЗАДАНИЕ № 2
Напишите формулы всех оксидов,
которые можно составить из записей в приведенных карточках. Назовите
оксиды
Ва
О5
Al2
О
С
Н2
О
О
N2
Р2
Fe
К2
О
О5
С
О
О3
Fe2
О2
О3
8. Задание № 3
Из перечисленных формул веществвыпишите оксиды, и назовите их:
HCl, SO3, KOH, CO2, HBr, ZnO, NaOH,
H2SO4, MgO, Al2O3, ZnS, K2O.
9.
НАХОЖДЕНИЕ КИСЛОРОДА В ПРИРОДЕОн всюду и везде:
В камне, в воздухе, в воде.
Он и в утренней росе,
И в небес голубизне.
Литосфера - 47% по m (в составе оксидов, солей)
Гидросфера - 85,8% (в основном в составе воды)
Атмосфера - 23% по m, 21% по V
Растения - 40%
Животные - 20%
Тело человека - 65%
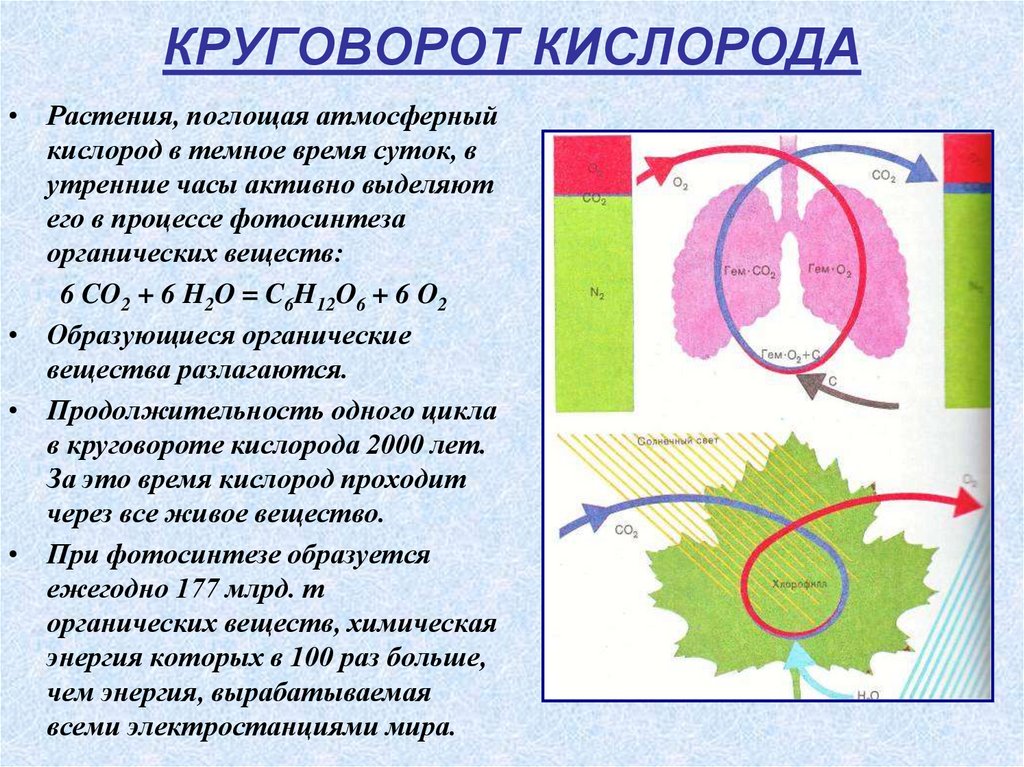
10. КРУГОВОРОТ КИСЛОРОДА
• Растения, поглощая атмосферныйкислород в темное время суток, в
утренние часы активно выделяют
его в процессе фотосинтеза
органических веществ:
6 CO2 + 6 H2O = C6H12O6 + 6 O2
• Образующиеся органические
вещества разлагаются.
• Продолжительность одного цикла
в круговороте кислорода 2000 лет.
За это время кислород проходит
через все живое вещество.
• При фотосинтезе образуется
ежегодно 177 млрд. т
органических веществ, химическая
энергия которых в 100 раз больше,
чем энергия, вырабатываемая
всеми электростанциями мира.
11.
ПРИМЕНЕНИЕ КИСЛОРОДА• Находит широкое применение в
медицине и промышленности.
• При высотных полётах лётчиков
снабжают специальными приборами
с кислородом.
• При многих лёгочных и сердечных
заболеваниях, а также при операциях
дают вдыхать кислород из
кислородных подушек.
• Кислородом в баллонах снабжают
подводные лодки.
• Горение рыхлого горючего материала,
пропитанного жидким кислородом,
сопровождается взрывом, что даёт
возможность применять кислород
при взрывных работах.
• Жидкий кислород применяют в
реактивных двигателях, в автогенной
сварке и резке металлов, даже под
водой.
11










 Химия
Химия








