Похожие презентации:
Строение твердых тел
1. Строение твердых тел
• Презентация разработана преподавателем КСи ПТ Каракашевой И.В.
Санкт – Петербург
2016
2. Цели урока
Образовательные:
познакомить учащихся со строением твердых тел, видами кристаллических
решеток и их дефектов;
обеспечить усвоение понятий, связанных с отличиями в строении вещества;
актуализировать знания о строении вещества;
расширить общий кругозор учащихся
Развивающие:
создать условия для развития коммуникативных навыков;
создать условия для развития аналитических способностей учащихся, умения
анализировать, сопоставлять, сравнивать , обобщать, делать выводы;
создать условия для развития памяти, внимания, воображения
Воспитательные:
способствовать развитию умения отстаивать свою точку зрения;
способствовать развитию культуры взаимоотношений при работе в
коллективе
2
3.
Твердые тела• Сохраняют объём и форму
• Плохо сжимаются
• Плохо растягиваются
• Имеют дальний порядок в расположении
частиц
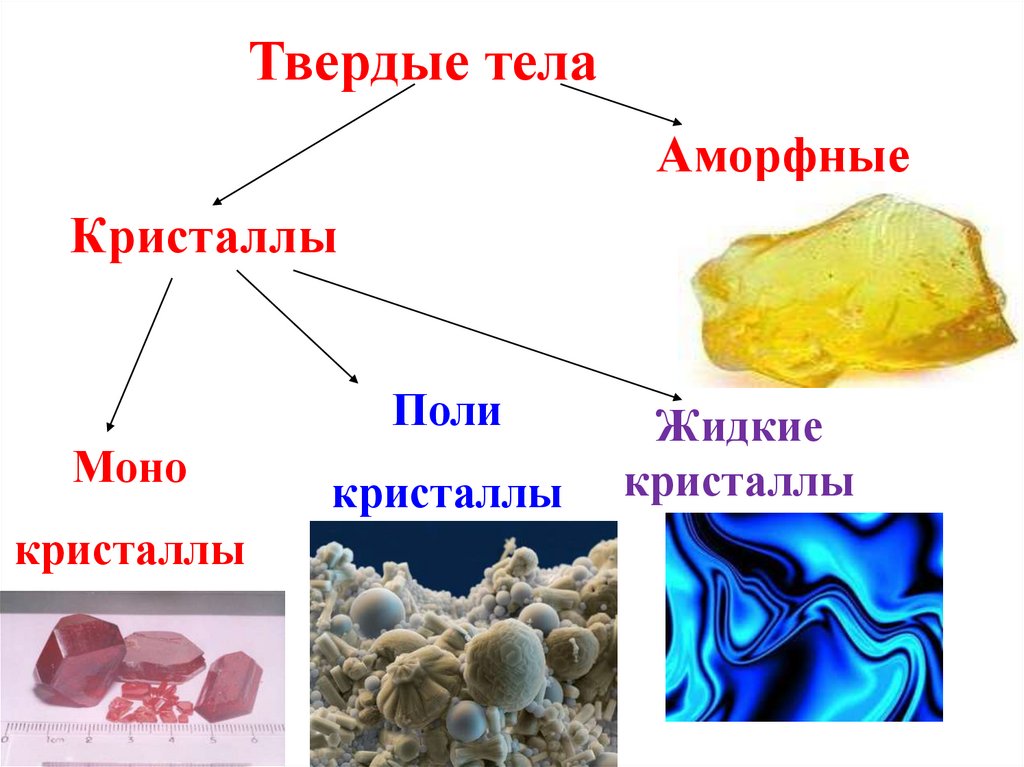
4.
Твердые телаАморфные
Кристаллы
Поли
Моно
кристаллы
кристаллы
Жидкие
кристаллы
5. Монокристаллы (кристаллиты)
• Твердые тела, иногда обладающие правильнойгеометрической формой.
• Главный признак: периодически повторяющаяся
внутренняя структура во всем объеме (каменная
соль, кварц, алмаз, турмалин и т.д.)
• Основное свойство: анизотропия, т.е. различие
свойств кристалла по разным направлениям
• Кристаллической решеткой называется
пространственная сетка, узлы которой(точки,
соответствующие наиболее устойчивому положению
равновесия частиц) совпадают с центрами атомов
или молекул
6. Монокристаллы (кристаллиты)
Типичная (повторяющаяся вдольлюбой прямой) часть
кристаллической решетки
называется элементарной
ячейкой.
• В кристаллитах элементарные ячейки одинаковы
как у окружающих данный атом ближайших его
соседей (ближний порядок), так и у атомов,
находящихся от него на значительных расстояниях
вплоть до границ зерен (дальний порядок).
7. Монокристаллы (кристаллиты)
• В кристаллитах соблюдаются ближний и дальнийпорядки.
• Вследствие диффузии отдельные атомы могут
покидать свои места в узлах кристаллической
решетки, однако при этом упорядоченность
кристаллического строения в целом не нарушается
Расположение атомов в кристаллическом (а) и аморфном (б) веществе
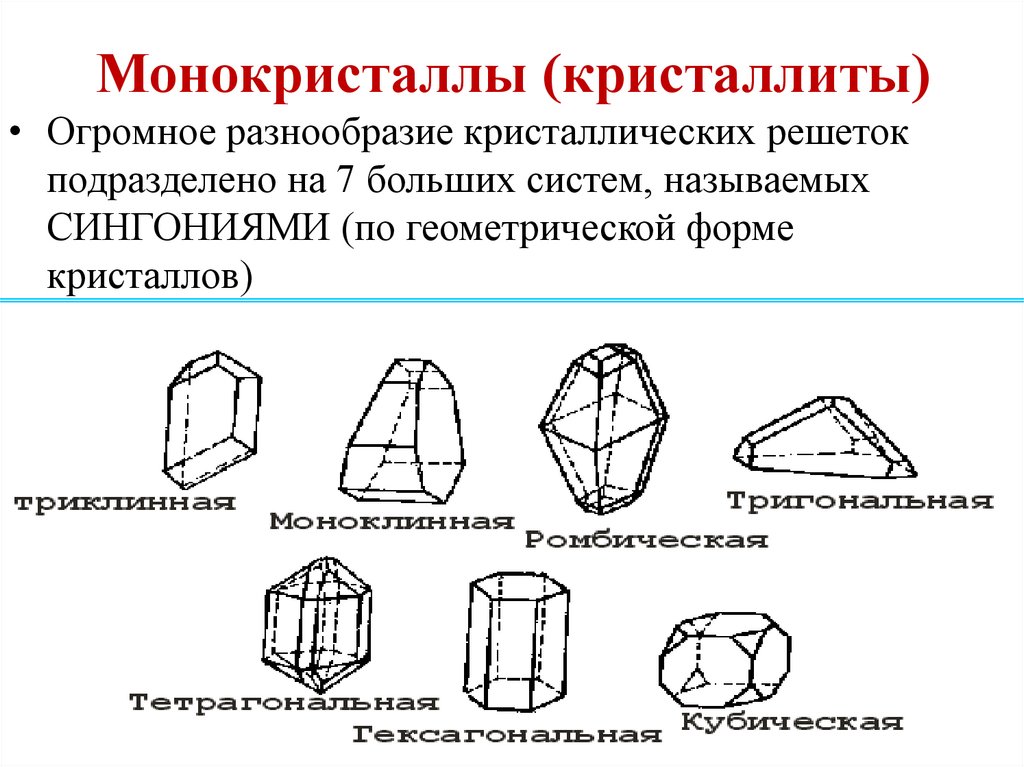
8. Монокристаллы (кристаллиты)
• Огромное разнообразие кристаллических решетокподразделено на 7 больших систем, называемых
СИНГОНИЯМИ (по геометрической форме
кристаллов)
9. Поликристаллы
• Твердые тела, состоящие из отдельных, беспорядочнорасположенных, сросшихся между собой зеренкристаллитов.
• В соседних зернах кристаллические решетки
повернуты.относительно друг друга на некоторый
угол.
• Поликристаллы изотропны, т.е. имеют одинаковые
свойства по всем направлениям.
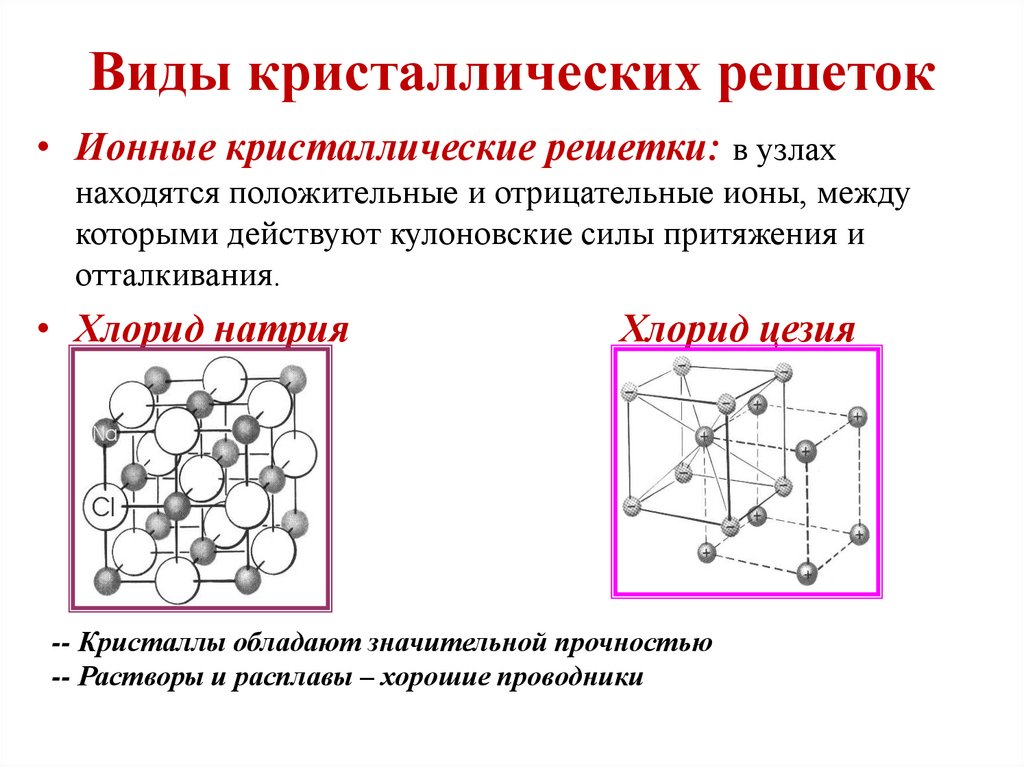
10. Виды кристаллических решеток
• Ионные кристаллические решетки: в узлахнаходятся положительные и отрицательные ионы, между
которыми действуют кулоновские силы притяжения и
отталкивания.
• Хлорид натрия
Хлорид цезия
-- Кристаллы обладают значительной прочностью
-- Растворы и расплавы – хорошие проводники
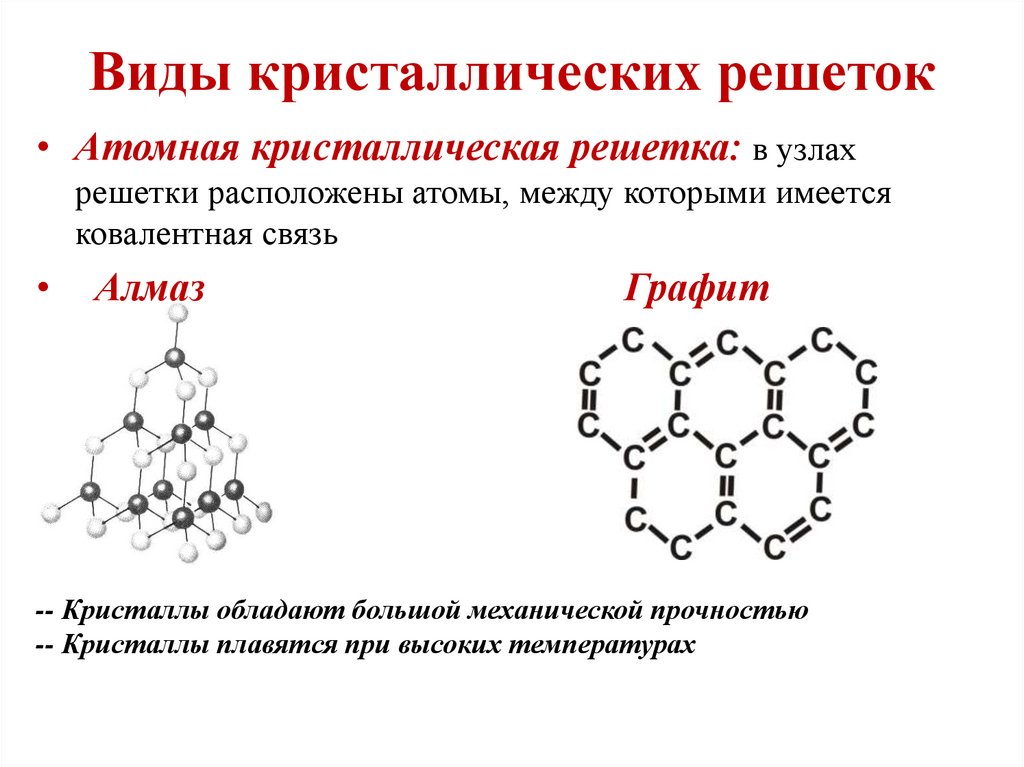
11. Виды кристаллических решеток
• Атомная кристаллическая решетка: в узлахрешетки расположены атомы, между которыми имеется
ковалентная связь
Алмаз
Графит
-- Кристаллы обладают большой механической прочностью
-- Кристаллы плавятся при высоких температурах
12.
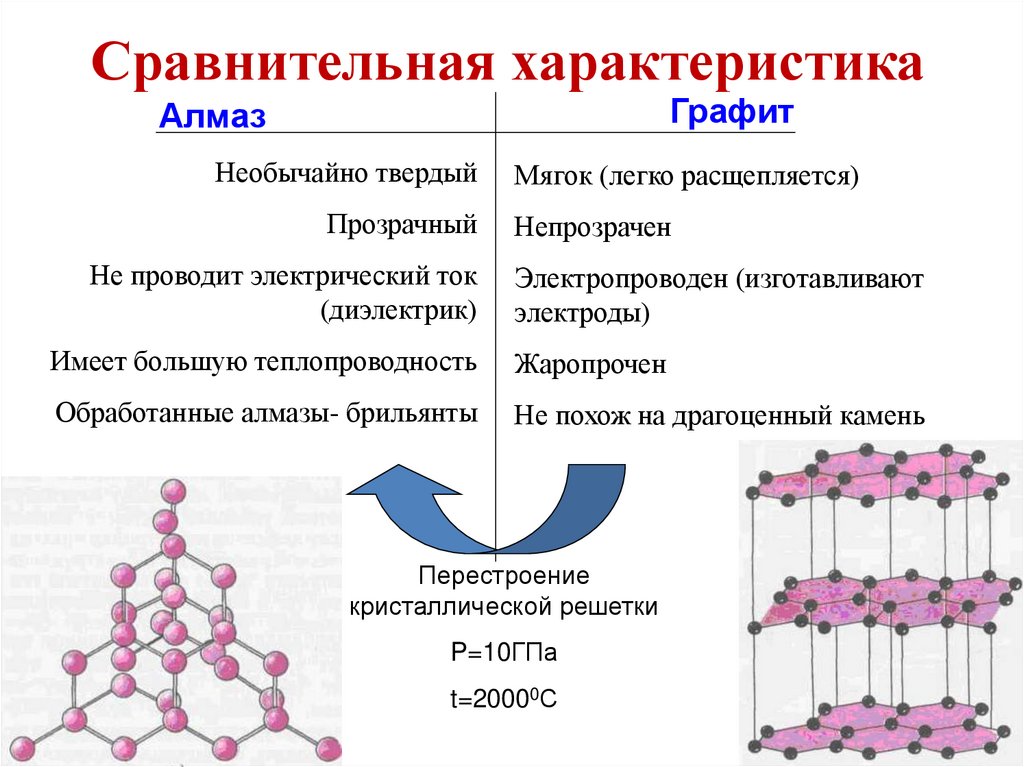
Сравнительная характеристикаГрафит
Алмаз
Необычайно твердый
Прозрачный
Не проводит электрический ток
(диэлектрик)
Мягок (легко расщепляется)
Непрозрачен
Электропроводен (изготавливают
электроды)
Имеет большую теплопроводность
Жаропрочен
Обработанные алмазы- брильянты
Не похож на драгоценный камень
Перестроение
кристаллической решетки
P=10ГПа
t=20000С
13. Виды кристаллических решеток
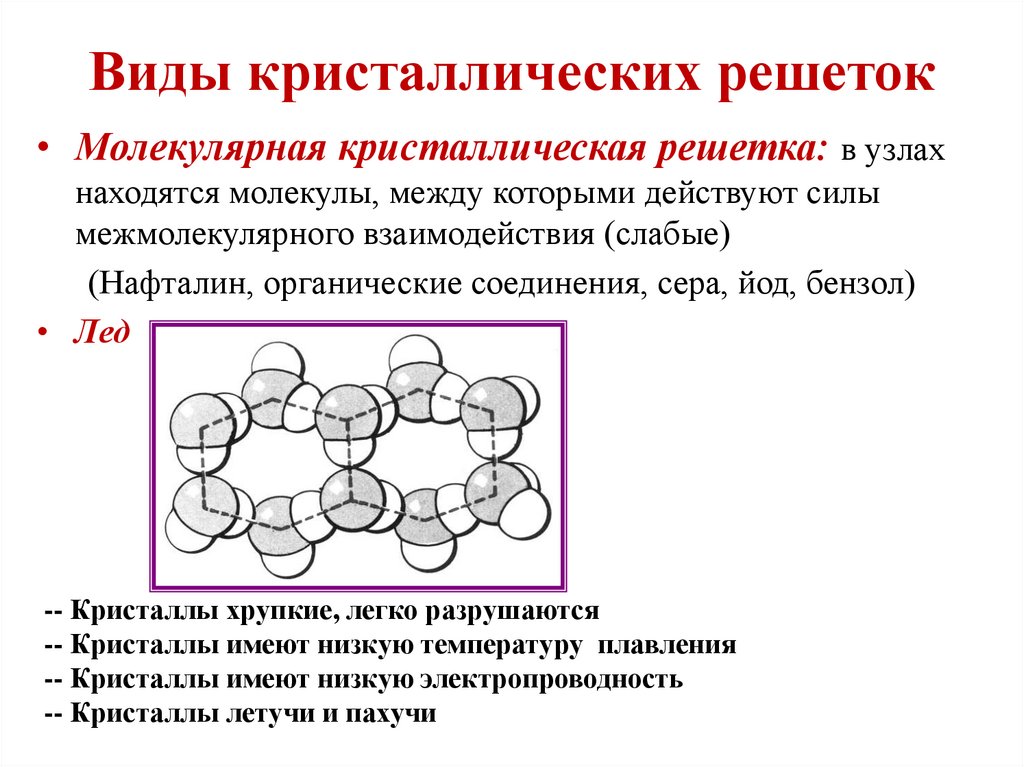
• Молекулярная кристаллическая решетка: в узлахнаходятся молекулы, между которыми действуют силы
межмолекулярного взаимодействия (слабые)
(Нафталин, органические соединения, сера, йод, бензол)
• Лед
-- Кристаллы хрупкие, легко разрушаются
-- Кристаллы имеют низкую температуру плавления
-- Кристаллы имеют низкую электропроводность
-- Кристаллы летучи и пахучи
14. Виды кристаллических решеток
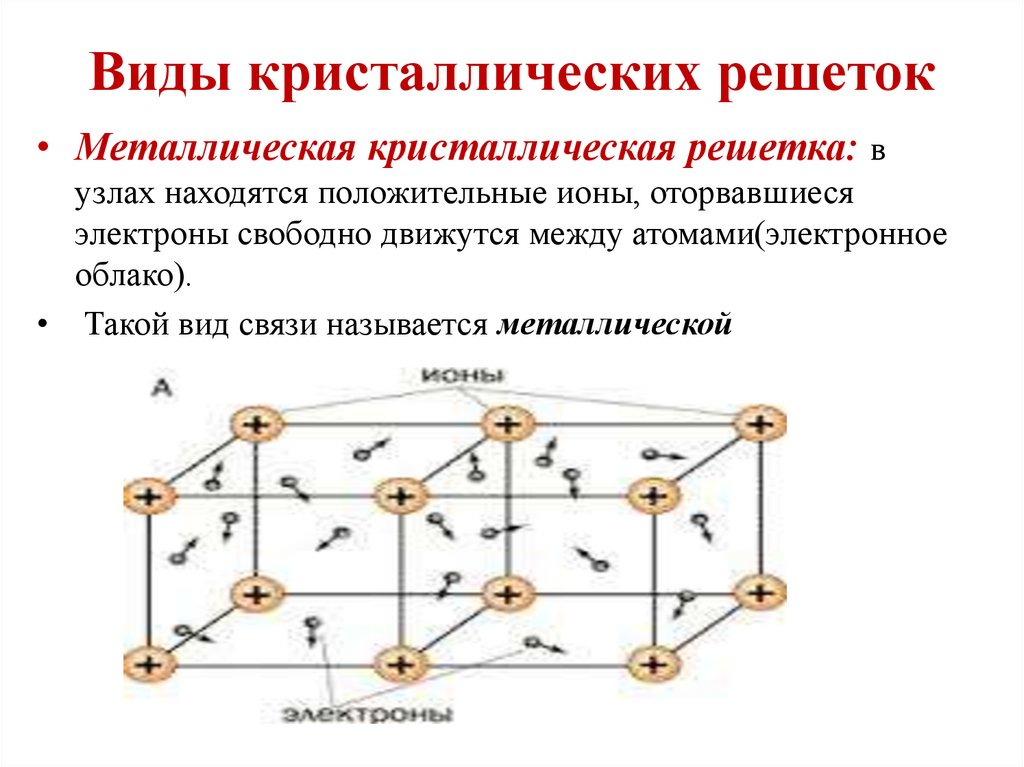
• Металлическая кристаллическая решетка: вузлах находятся положительные ионы, оторвавшиеся
электроны свободно движутся между атомами(электронное
облако).
• Такой вид связи называется металлической
15. Виды кристаллических решеток
• Металлическая кристаллическая решетка:• Обладают все металлы
-- Кристаллы обладают большой прочностью
-- Кристаллы обладают высокой теплопроводностью
-- Кристаллы обладают высокой электропроводностью
16. Виды кристаллических решеток
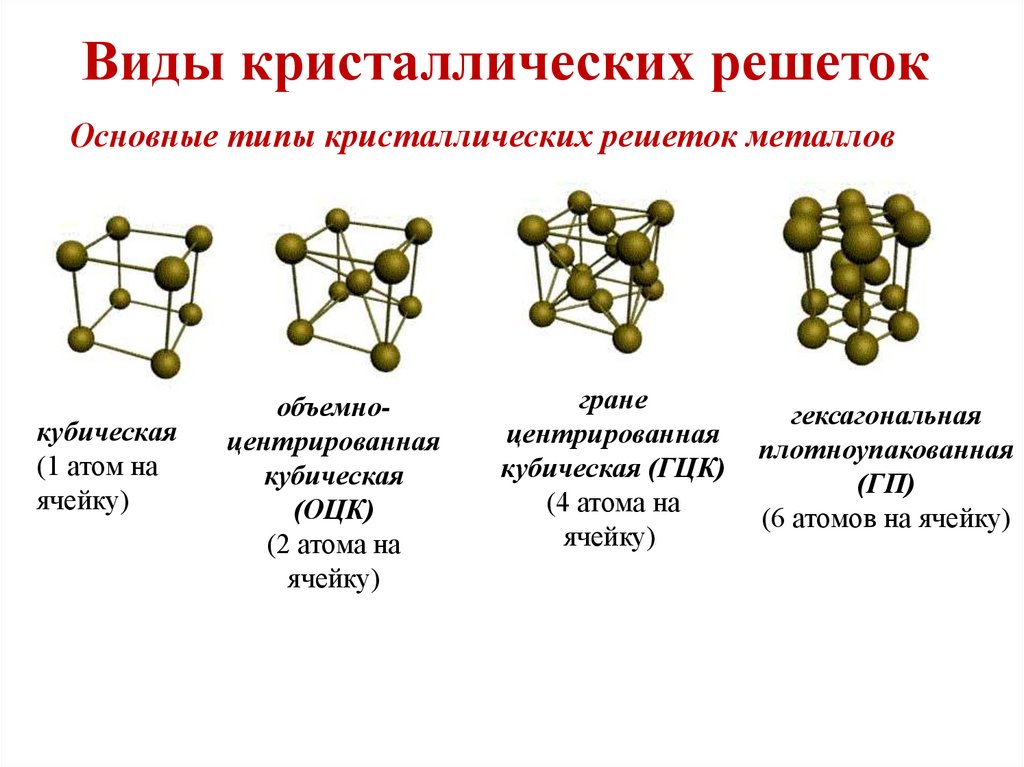
Основные типы кристаллических решеток металловкубическая
(1 атом на
ячейку)
объемноцентрированная
кубическая
(ОЦК)
(2 атома на
ячейку)
гране
центрированная
кубическая (ГЦК)
(4 атома на
ячейку)
гексагональная
плотноупакованная
(ГП)
(6 атомов на ячейку)
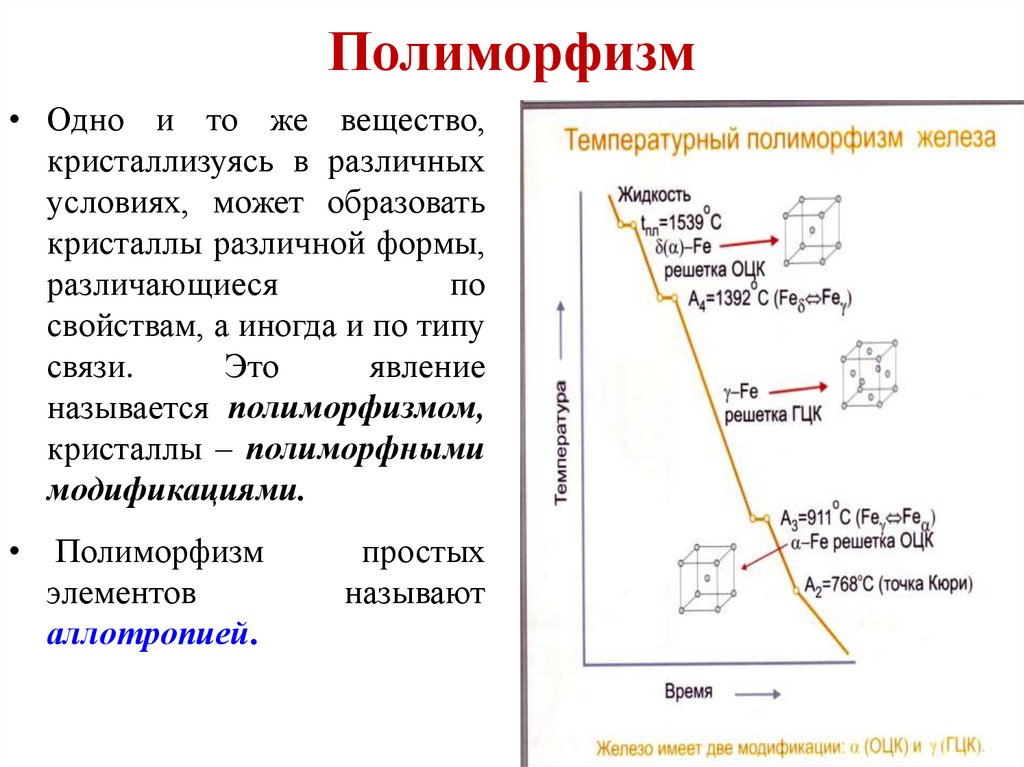
17. Полиморфизм
• Одно и то же вещество,кристаллизуясь в различных
условиях, может образовать
кристаллы различной формы,
различающиеся
по
свойствам, а иногда и по типу
связи.
Это
явление
называется полиморфизмом,
кристаллы – полиморфными
модификациями.
Полиморфизм
элементов
аллотропией.
простых
называют
18. Дефекты кристаллической решетки
• Идеальный кристалл может существовать только притемпературе абсолютного нуля.
• При любых других температурах все реальные
кристаллы несовершенны, т.е. в них наблюдаются
нарушения идеального расположения атомов,
называемые дефектами.
Основные виды дефектов
• Точечные
• Линейные
• Поверхностные
• Объемные
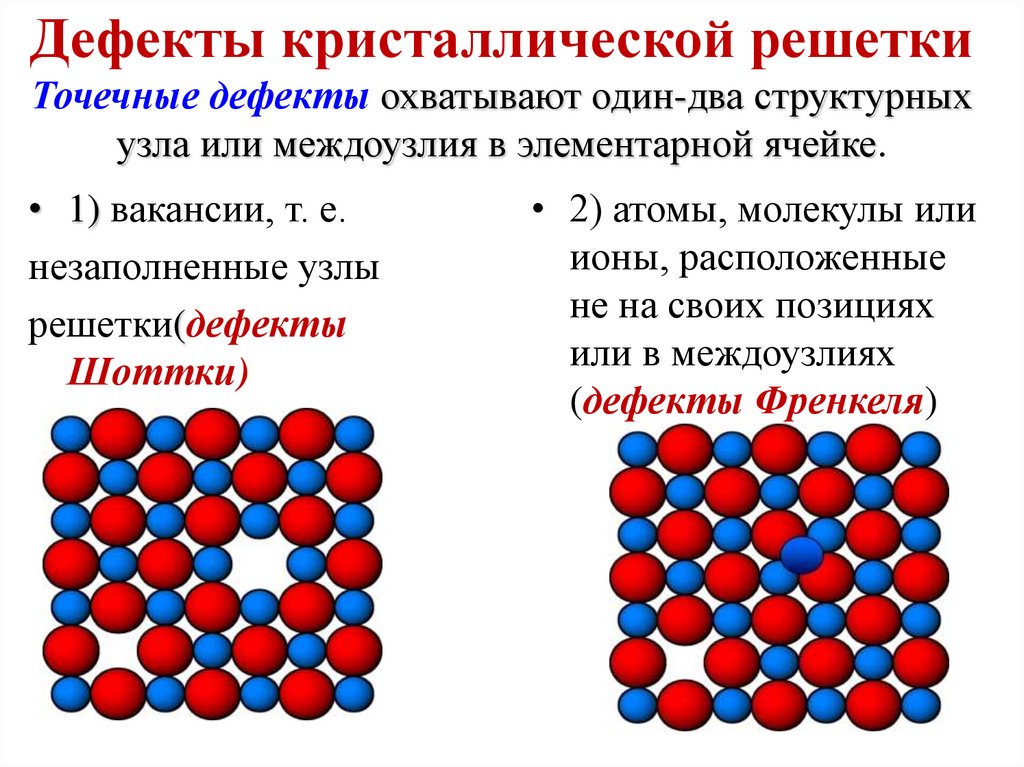
19. Дефекты кристаллической решетки Точечные дефекты охватывают один-два структурных узла или междоузлия в элементарной ячейке.
Дефекты кристаллической решеткиТочечные дефекты охватывают один-два структурных
узла или междоузлия в элементарной ячейке.
• 1) вакансии, т. е.
незаполненные узлы
решетки(дефекты
Шоттки)
• 2) атомы, молекулы или
ионы, расположенные
не на своих позициях
или в междоузлиях
(дефекты Френкеля)
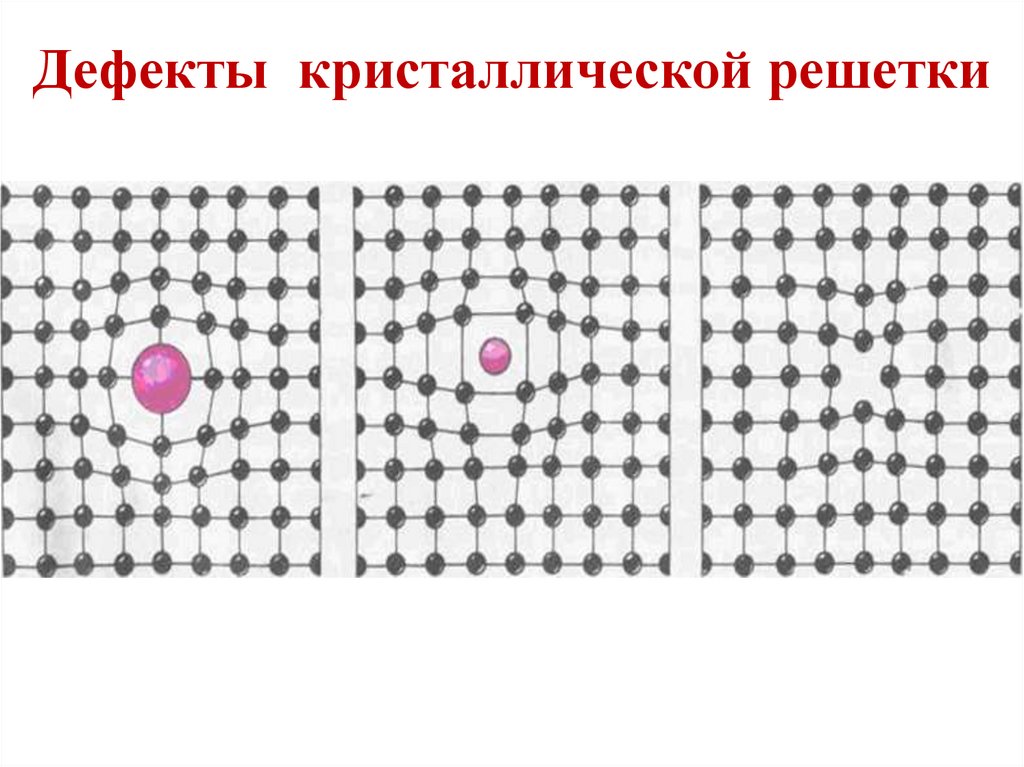
20. Дефекты кристаллической решетки
21. Дефекты кристаллической решетки
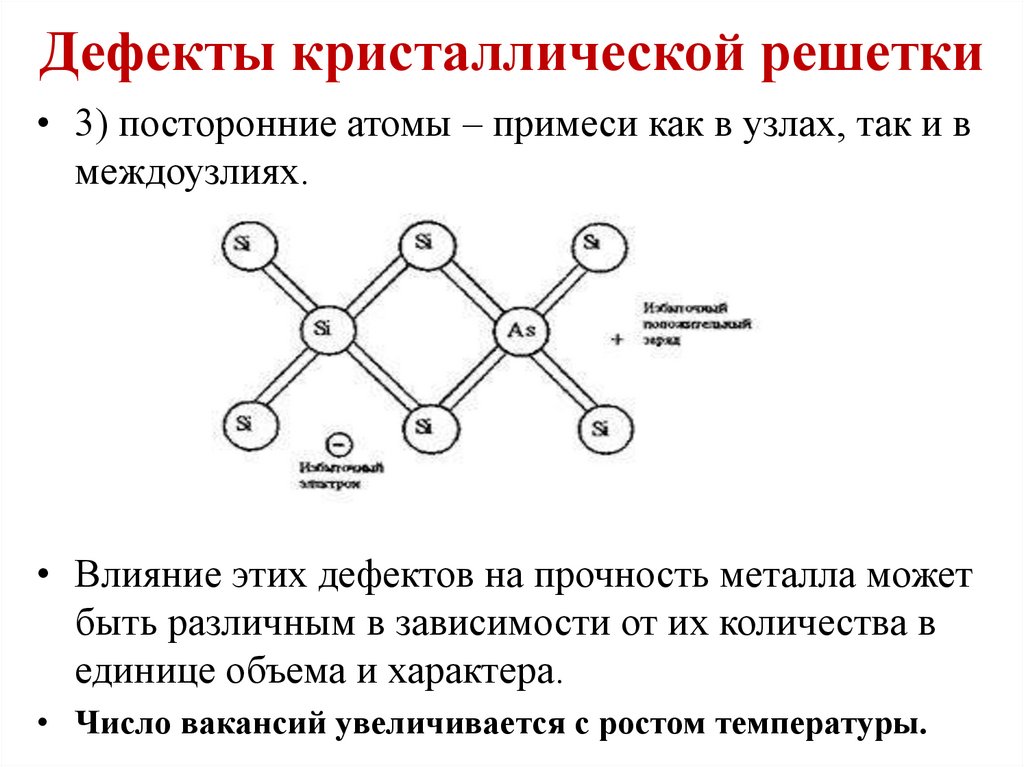
• 3) посторонние атомы – примеси как в узлах, так и вмеждоузлиях.
• Влияние этих дефектов на прочность металла может
быть различным в зависимости от их количества в
единице объема и характера.
• Число вакансий увеличивается с ростом температуры.
22.
Дефекты кристаллической решетки23. Междоузлие
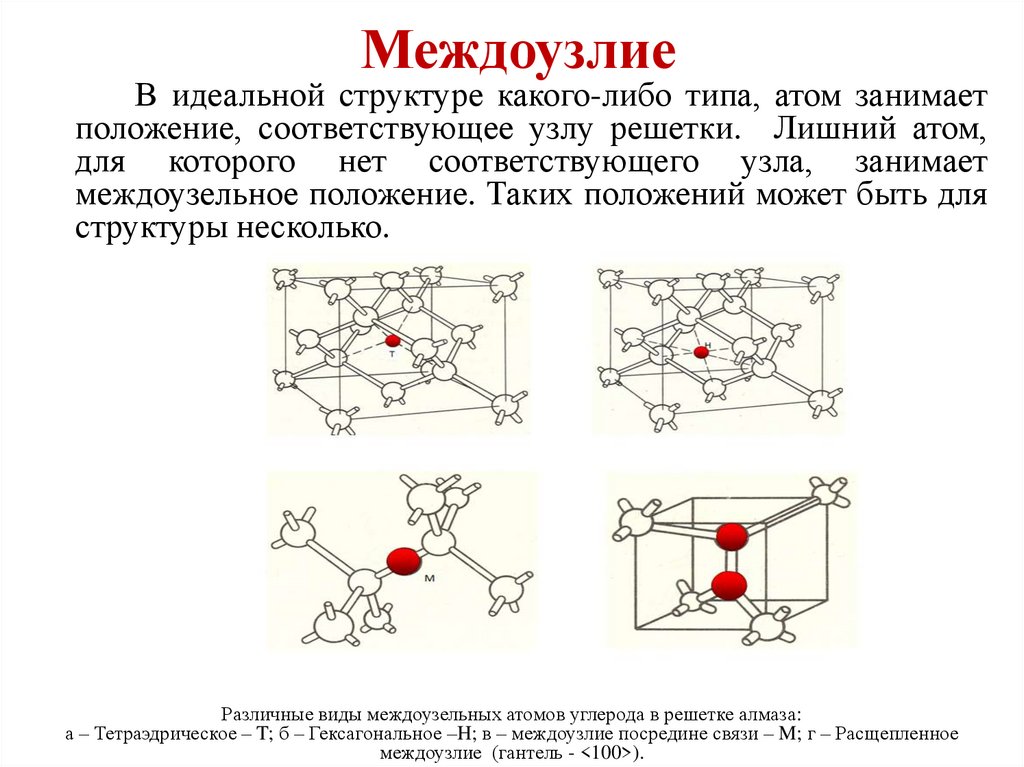
В идеальной структуре какого-либо типа, атом занимаетположение, соответствующее узлу решетки. Лишний атом,
для которого нет соответствующего узла, занимает
междоузельное положение. Таких положений может быть для
структуры несколько.
Различные виды междоузельных атомов углерода в решетке алмаза:
а – Тетраэдрическое – T; б – Гексагональное –H; в – междоузлие посредине связи – M; г – Расщепленное
междоузлие (гантель - <100>).
24. Собственное междоузлие в алмазе
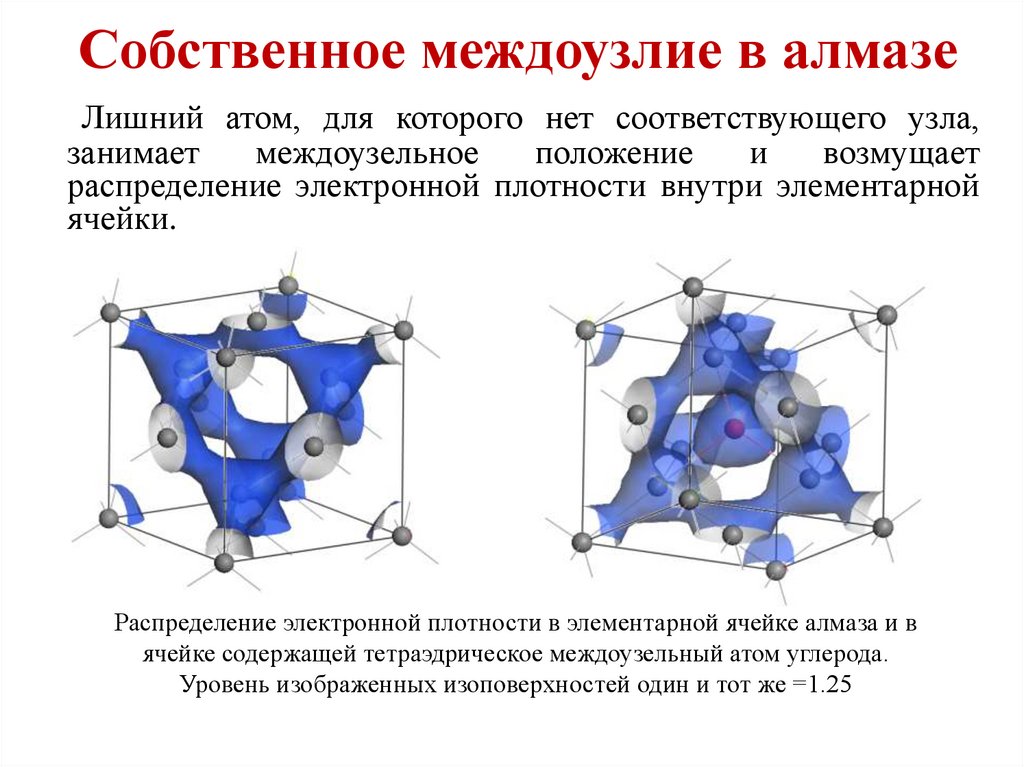
Лишний атом, для которого нет соответствующего узла,занимает
междоузельное
положение
и
возмущает
распределение электронной плотности внутри элементарной
ячейки.
Распределение электронной плотности в элементарной ячейке алмаза и в
ячейке содержащей тетраэдрическое междоузельный атом углерода.
Уровень изображенных изоповерхностей один и тот же =1.25
25. Модель образования вакансии в простых веществах
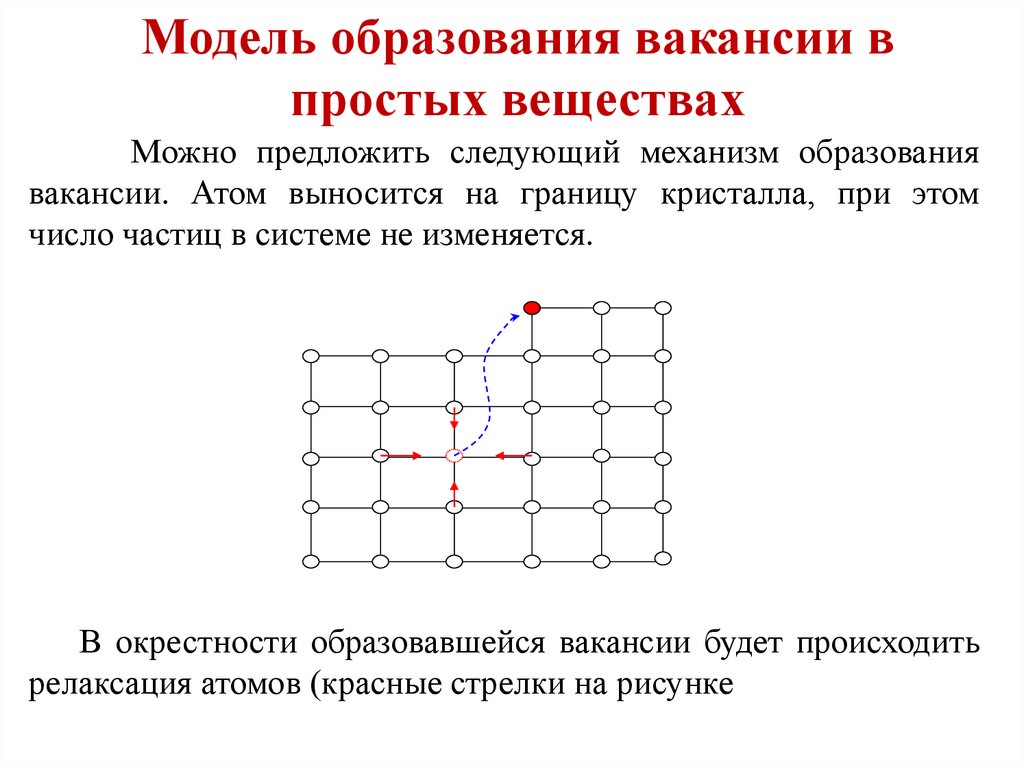
Можно предложить следующий механизм образованиявакансии. Атом выносится на границу кристалла, при этом
число частиц в системе не изменяется.
В окрестности образовавшейся вакансии будет происходить
релаксация атомов (красные стрелки на рисунке
26. Одиночная вакансия в алмазе
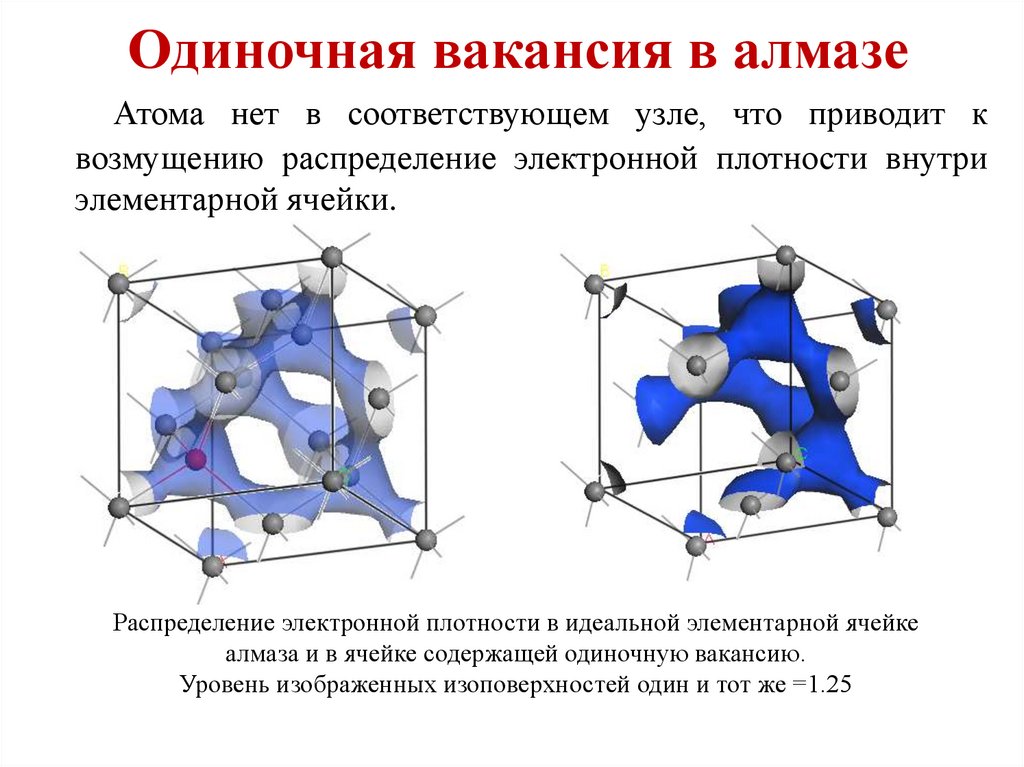
Атома нет в соответствующем узле, что приводит квозмущению распределение электронной плотности внутри
элементарной ячейки.
Распределение электронной плотности в идеальной элементарной ячейке
алмаза и в ячейке содержащей одиночную вакансию.
Уровень изображенных изоповерхностей один и тот же =1.25
27. Дефекты кристаллической решетки
• Линейные дефекты имеют длину, значительнопревышающую их поперечные размеры.
• К ним относятся дислокации, т. е. дефекты,
образующиеся в решетке в результате смещений
кристаллографических плоскостей.
• Дислокации обладают высокой подвижностью, поэтому
существенно уменьшают прочность металла
• Максимальная плотность дислокаций, может составить
1013 см-2. При дальнейшем росте плотности дислокаций
происходит разрушение металла.
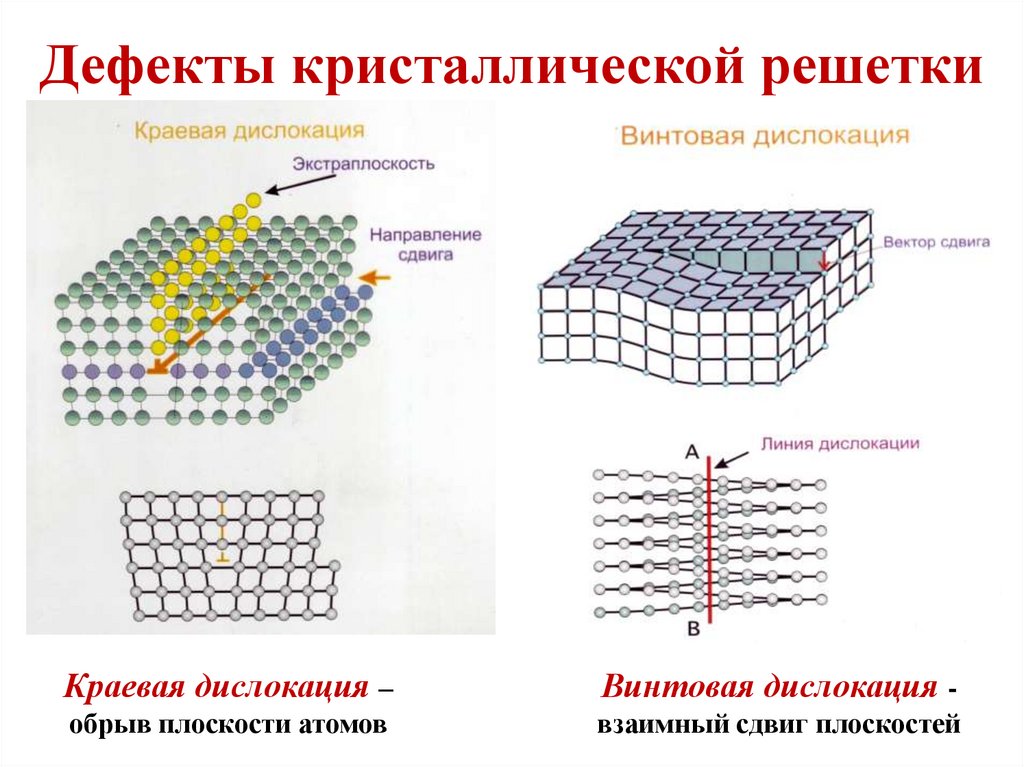
28. Дефекты кристаллической решетки
Краевая дислокация –Винтовая дислокация -
обрыв плоскости атомов
взаимный сдвиг плоскостей
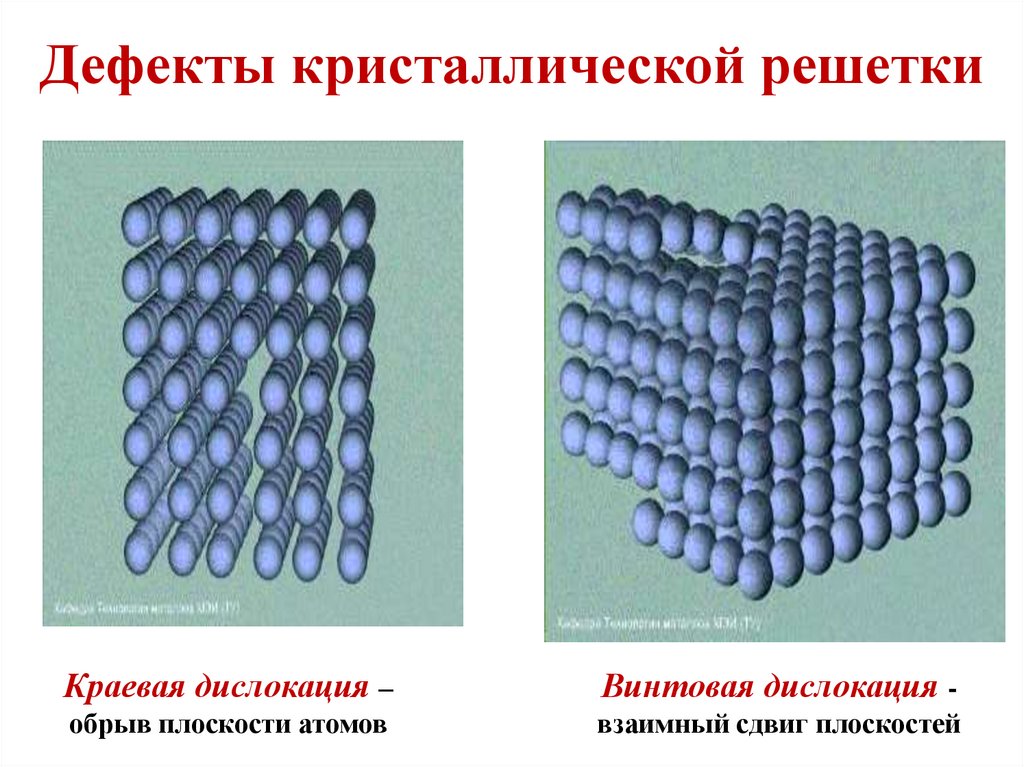
29. Дефекты кристаллической решетки
Краевая дислокация –Винтовая дислокация -
обрыв плоскости атомов
взаимный сдвиг плоскостей
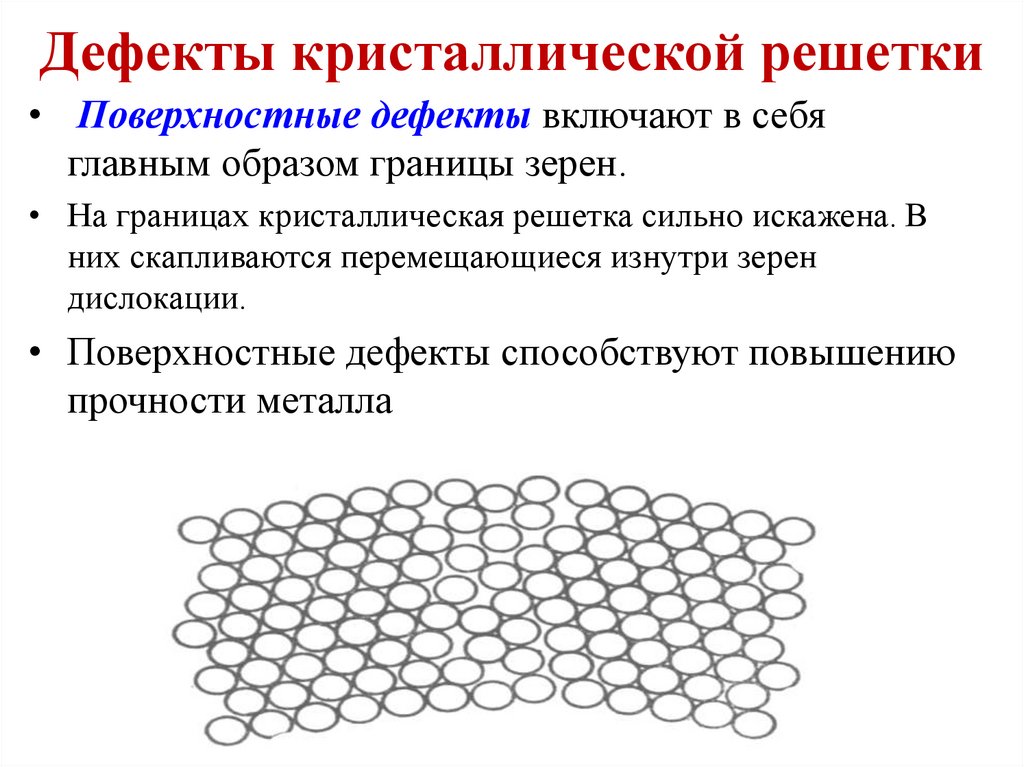
30. Дефекты кристаллической решетки
• Поверхностные дефекты включают в себяглавным образом границы зерен.
• На границах кристаллическая решетка сильно искажена. В
них скапливаются перемещающиеся изнутри зерен
дислокации.
• Поверхностные дефекты способствуют повышению
прочности металла
31. Дефекты кристаллической решетки
• Объемные дефекты кристаллической решеткивключают трещины и поры.
• Уменьшают плотность металла, снижает его
прочность.
• Трещины являются сильными концентраторами
напряжений, в десятки и более раз повышающими
напряжения создаваемые в металле рабочими
нагрузками. Последнее обстоятельство наиболее
существенно влияет на прочность металла.
32. Жидкие кристаллы
• Жи́дкие криста́ллы — это фазовое состояние, в котороепереходят некоторые вещества при определенных условиях
(температура, давление, концентрация в растворе).
• Жидкие кристаллы обладают одновременно свойствами как
жидкостей (текучесть), так и кристаллов (анизотропия).
• По структуре ЖК представляют собой вязкие жидкости,
состоящие из молекул вытянутой или дискообразной формы,
определённым образом упорядоченных во всем объёме этой
жидкости.
• Характерное свойство ЖК - способность изменять ориентацию
молекул под воздействием электрических полей.
• Жидкие кристаллы открыл в 1888 году австрийский ботаник Ф.
Рейнитцер
33. Жидкие кристаллы
• По своим общим свойствам ЖК можно разделить на две большиегруппы:
• термотропные ЖК, образующиеся в результате нагревания
твердого вещества и существующие в определенном интервале
температур и давлений.
• лиотропные ЖК, которые представляют собой двух- или более
компонентные системы, образующиеся в смесях стержневидных
молекул данного вещества и воды (или других полярных
растворителей). Эти стержневидные молекулы имеют на одном
конце полярную группу, а большая часть стержня представляет
собой гибкую гидрофобную углеводородную цепь. Такие
вещества называются амфифилами (например, фосфолипиды)
• Амфифильные молекулы, как правило, плохо растворяются в
воде ( одним из вариантов амфифилов со сложной структурой
может служить система мыло-вода)
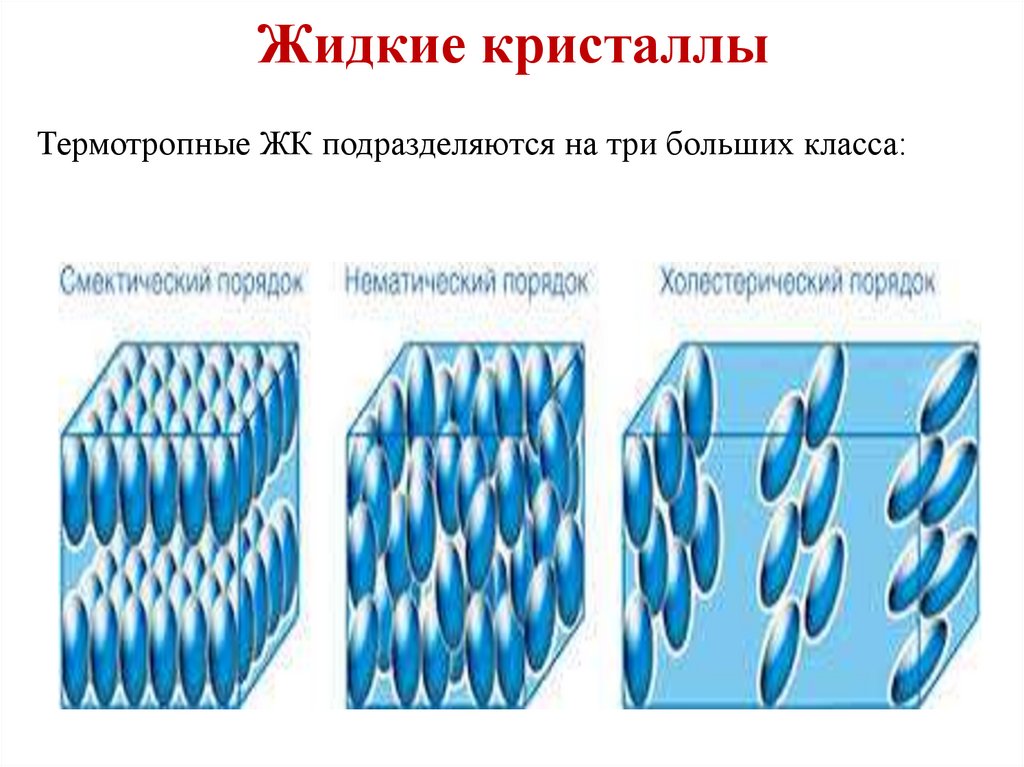
34. Жидкие кристаллы
Термотропные ЖК подразделяются на три больших класса:35. Нематические жидкие кристаллы
• В этих кристаллах отсутствует дальнийпорядок в расположении центров тяжести
молекул,
• У них нет слоистой структуры,
• Их молекулы скользят непрерывно в
направлении своих длинных осей, вращаясь
вокруг них, но при этом сохраняют
ориентационный порядок: длинные оси
направлены вдоль одного преимущественного
направления.
• Они ведут себя подобно обычным жидкостям.
• Нематические фазы встречаются только в
таких веществах, у молекул которых нет
различия между правой и левой формами.
36. Смектические жидкие кристаллы
• Кристаллы имеют слоистуюструктуру
• Толщина смектического слоя
определяется длиной молекул
• Вязкость смектиков
значительно выше, чем у
нематиков, и плотность по
нормали к поверхности слоя
может сильно меняться
37. Холестерические жидкие кристаллы
Образуются, в основном, соединениями холестерина и других
стероидов.
• Это нематические ЖК, но их длинные оси повернуты друг
относительно друга так, что они образуют спирали, очень
чувствительные к изменению
• Холестерики ярко окрашены
• Малейшее изменение температуры (до тысячных долей
градуса) приводит к изменению шага спирали и,
соответственно, к изменению окраски ЖК.
38.
Аморфные телаАморфными называются вещества, атомы которых
расположены в пространстве хаотично.
К ним относят клей, смолу, канифоль, стекло,
янтарь и др.
39.
Аморфные тела• Не имеют кристаллической решетки
• Не имеют температуры плавления
• Изотропны
• Обладают текучестью
• Имеют только ближний порядок
• Способны переходить в кристаллическое и жидкое
состояние
40. Домашнее задание
• Ф.10 §72• ответить на вопросы к параграфу




















 Химия
Химия








