Похожие презентации:
Теория электрической диссоциации
1.
2.
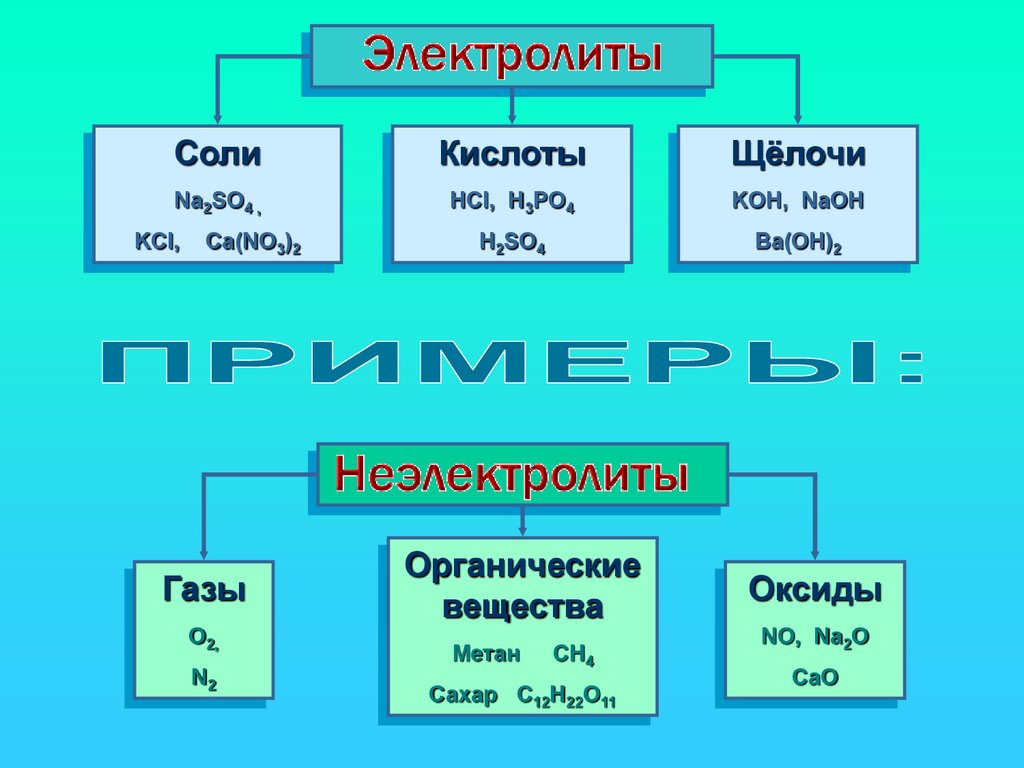
Все вещества по отношению к электрическому току можно разделить на :их растворы
или расплавы
их растворы
или расплавы
ПРОВОДЯТ
НЕ ПРОВОДЯТ
электрический ток
электрический ток
Вид химической связи
Ионная или
ковалентная
сильно полярная
Ковалентная
неполярная
или мало полярная
3.
CолиКислоты
Щёлочи
Na2SO4 ,
HCl, H3PO4
KOH, NaOH
H2SO4
Ba(OH)2
KCl,
Ca(NO3)2
Газы
O2,
N2
Органические
вещества
Метан
CH4
Сахар C12H22O11
Оксиды
NO, Na2O
CaO
4.
Классы неорганических веществ сточки зрения ТЭД
5.
ОдноосновныеДвухосновные
HClO4, HNO3,
HCl,
HBr
H2SO4, H2CO3,
H2S,
H2SiO3
Трёхосновные
Четырёхосновные
H3PO4,
H3BO3
H4P2O7,
H4SiO4
С точки зрения ТЭД, кислотами называются
электролиты, которые в водном растворе диссоциируют
на ионы водорода и ионы кислотных остатков.
6.
+HCl = H + Cl
+
HNO3 = H +
-
NO3
+
2-
+
3-
H2 SO4 = 2H + SO4
H3 PO4 = 3H + PO4
Кислоты – это электролиты, которые
диссоциируют на катионы водорода и
анионы кислотного остатка
7.
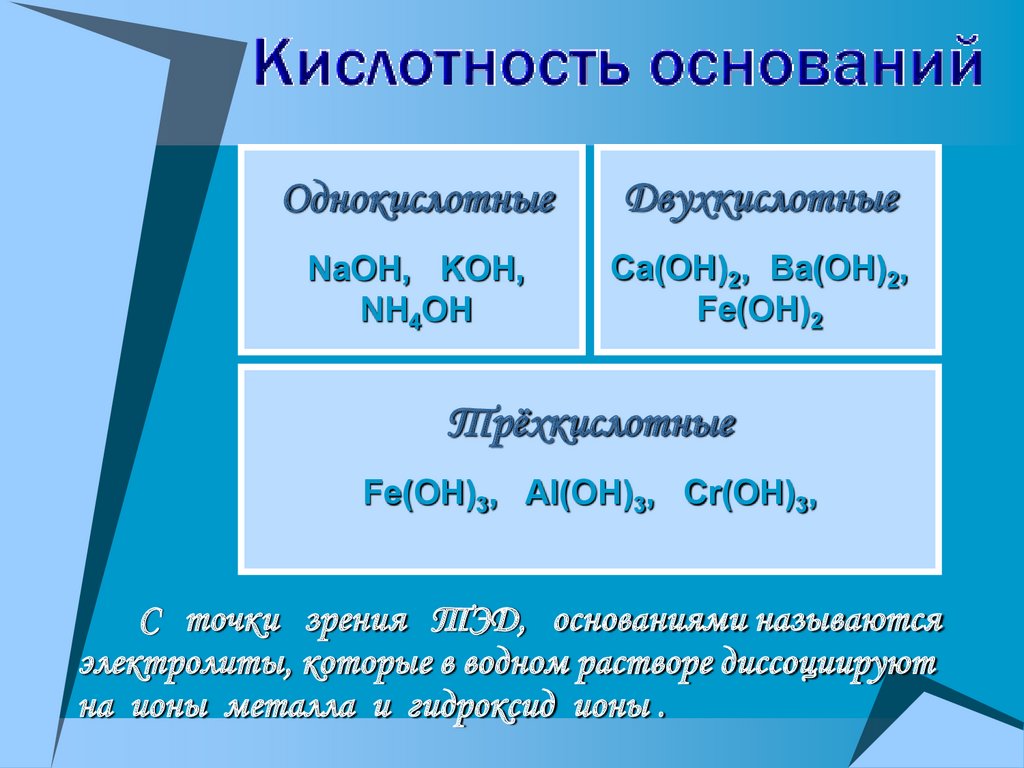
ОднокислотныеДвухкислотные
NaOH, KOH,
NH4OH
Ca(OH)2, Ba(OH)2,
Fe(OH)2
Трёхкислотные
Fe(OH)3, Al(OH)3, Cr(OH)3,
С точки зрения ТЭД, основаниями называются
электролиты, которые в водном растворе диссоциируют
на ионы металла и гидроксид ионы .
8.
NaOH = Na+ + OHBa(OH)2 = Ba2+ + 2OHKOH = K+ + OH-Основания – это электролиты,
которые диссоциируют на катионы
металла и анионы гидроксогрупп
9.
NaCl = Na+ + ClKNO3 = K+ + NO3Al2(SO4)3 = 2Al3+ + 3SO42Соли – это электролиты, которыедиссоциируют на катионы металла или
аммония NH4+ и анионы кислотных
остатков
10.
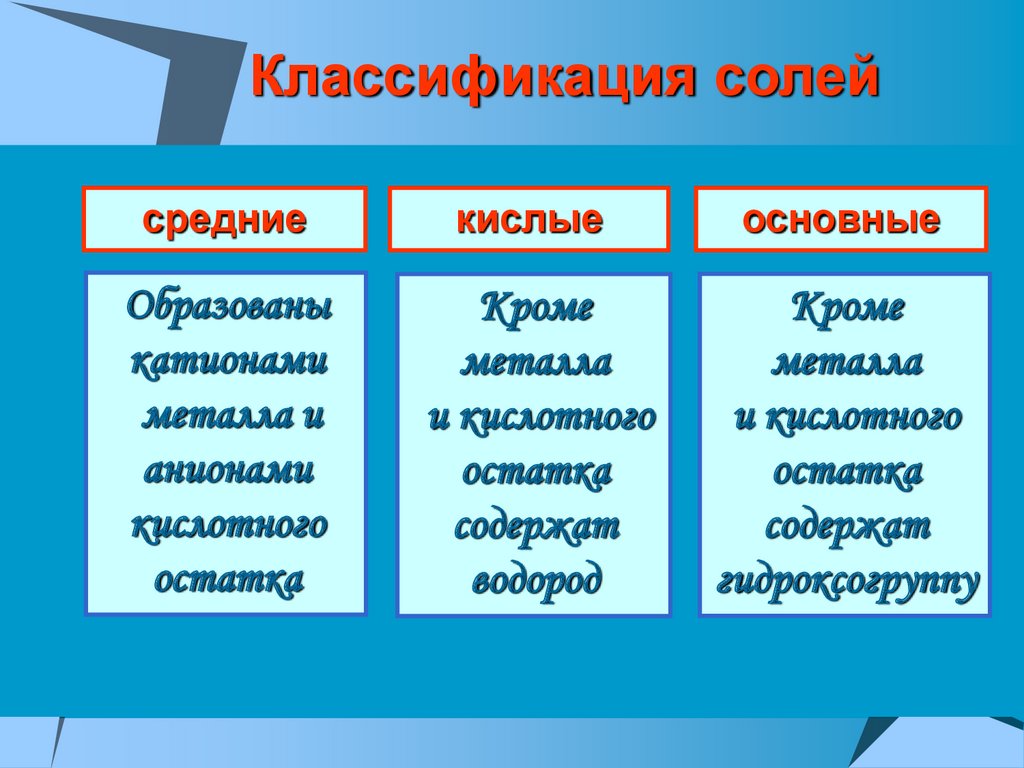
Классификация солейсредние
кислые
основные
Образованы
катионами
металла и
анионами
кислотного
остатка
Кроме
металла
и кислотного
остатка
содержат
водород
Кроме
металла
и кислотного
остатка
содержат
гидроксогруппу
11.
Na2SO4 = 2Na+ + SO42AlCl3 = Al3+ + 3ClFe2(SO4)3 = 2Fe3+ + 3SO42-С точки зрения ТЭД, средними солями
называются электролиты, которые в водном
растворе диссоциируют на ионы металла и
ионы кислотного остатка
12.
+NaHSO4 Na +
-
+
HSO4 H +
+
HSO4
2SO4
NaHSO4 Na + H
++
SO4
2-
С точки зрения ТЭД, кислыми солями
называются электролиты, которые в водном
растворе диссоциируют на ионы металла , ионы
кислотного остатка и образуют ионы водорода
13.
Ba(OH)Cl =-
BaOH
BaOH+
Ba2+
+ Cl
-
-
+ OH
С точки зрения ТЭД, основными
солями называются электролиты, которые в
водном растворе диссоциируют на ионы
металла , ионы кислотного остатка и
образуют гидроксид ионы
14.
15.
Условия протекания реакцииионного обмена
Реакции в растворах электролитов
протекают когда:
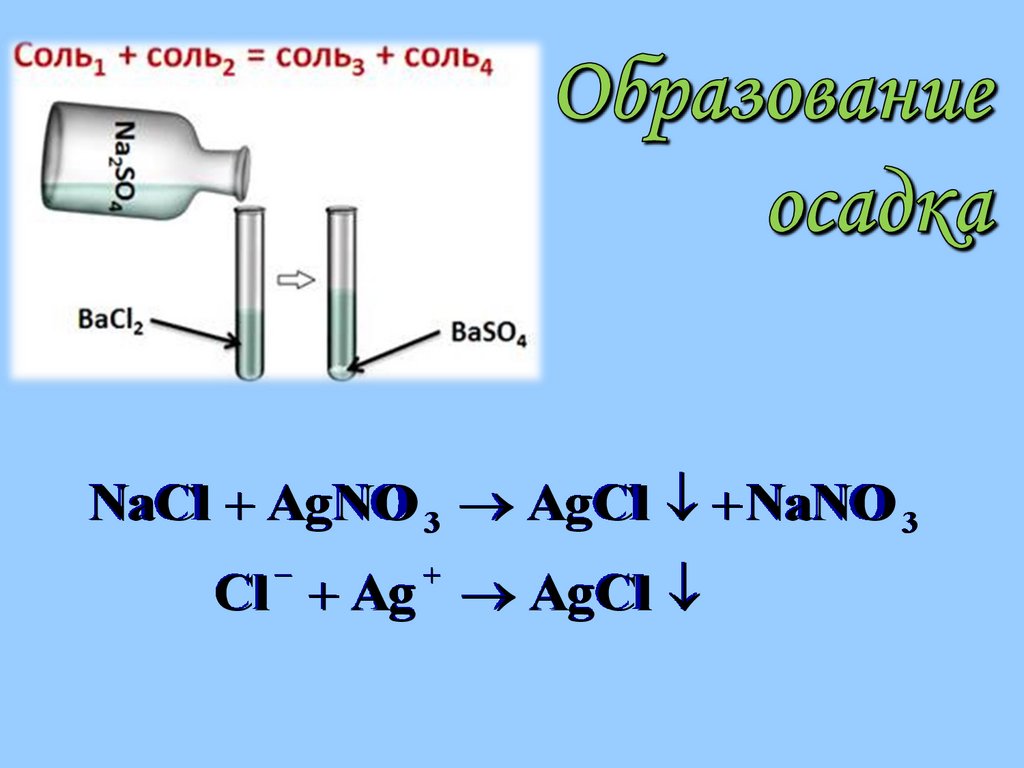
Образуется или растворяется осадок;
Выделяется газ;
Образуется малодиссоциирующее
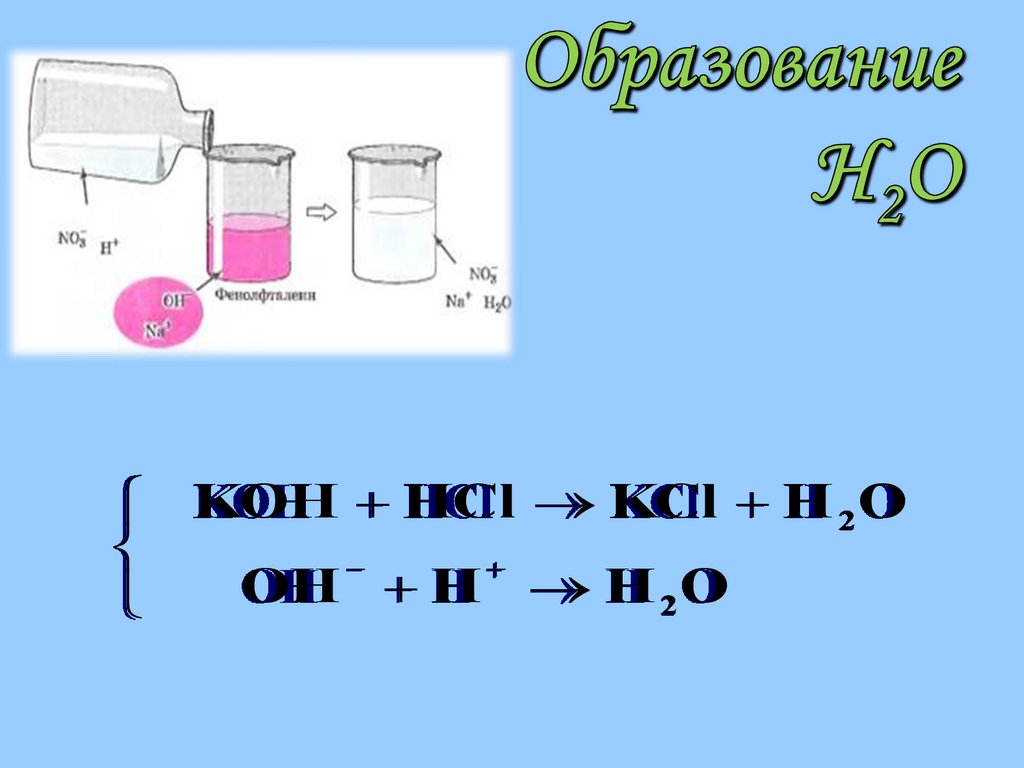
вещество (например Н2О)
16.
17.
18.
NaCl AgNO 3 AgCl NaNO 3Cl Ag AgCl
19.
20.
K 2S 2HCl 2KCl H 2S2
S 2H H 2S
21.
22.
KOH HCl KCl H 2OOH H H 2O

















 Химия
Химия








