Похожие презентации:
Подготовка воды к количественному химическому анализу. Количественное определение азота, аммиака, нитритов, нитратов
1.
ФГБОУ ВО «Северо-Западный государственныймедицинский университет имени И.И. Мечникова»
Минздрава России
Подготовка воды к
количественному химическому
анализу. Количественное
определение азота, аммиака,
нитритов, нитратов
2.
Причины обуславливающие наличиеаммиака и аммонийных солей в воде
• Поступление хозяйственно-бытовых сточных вод,
свидетельствует о свежем загрязнении органическими
веществами животного происхождения
• Присутствует в артезианских водах и являются
продуктами восстановления нитратов
• Отмечается повышенное содержание аммиака в
болотистых и торфяных водах, вследствие распада
растительных остатков
• Может быть и в чистой воде
3.
Процессы самоочищение воды – процессы удалениевзвешенных веществ и биохимическое расщепление и
окисление растворенных в воде органических веществ.
Процессы самоочищения воды осуществляется за счет:
- Разбавления чистыми водами. Зависит от дебита
водоисточника и количества вносимых загрязнений
- Осаждения частиц на дно. На скорость осаждение частиц
влияет: скорость течения воды водоисточника, характер
русла, качественная характеристика вносимых загрязнений
- Минерализации органических веществ. На процесс
минерализации влияют: климатические условия,
количество и качество вносимых загрязнений, количество и
характер животных и растительных форм
4.
Минерализация• Процесс превращения органических веществ в минеральные
• Протекает в две фазы: аммонификации белка, нитрификация белка
Характеристика процессов минерализации
Фазы минерализации
Характеристика
Фаза аммонификации белка
- процесс постепенного превращения белковой
молекулы через стадии альбумоз, пептонов,
полипептидов, аминокислот до конечного
продукта распада – аммиака (NH3).
- наиболее активно протекает в аэробных
условиях, но может проходить и в анаэробных
Фаза нитрификации
- NH3 под действием ферментов
нитрифицирующих бактерий группы Nitrosomas
окисляется до NO2- NO2- под действием ферментов бактерий
Nitrobacter окисляются до NO3-
5.
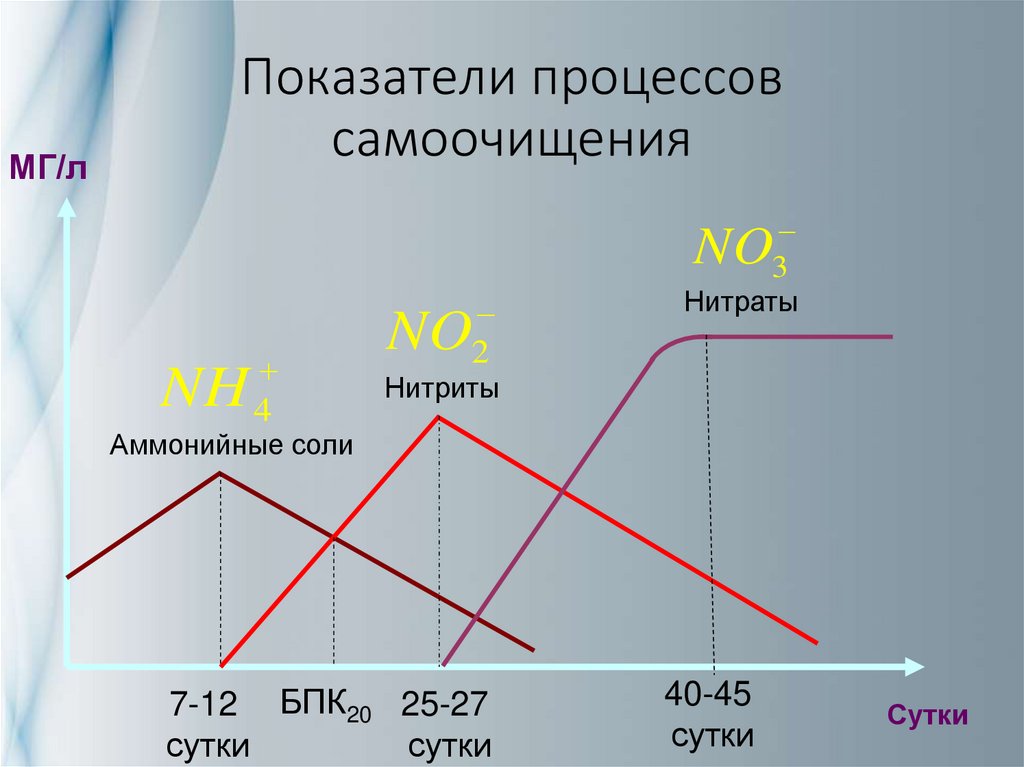
МГ/лПоказатели процессов
самоочищения
3
NO
NH
4
2
NO
Нитраты
Нитриты
Аммонийные соли
7-12 БПК20 25-27
сутки
сутки
40-45
сутки
Сутки
6.
Показатели характеризующиепроцессы самоочищения
Аммиак
- показатель свежего загрязнения воды
органическими веществами животного
происхождения, срок давности загрязнения 7-12
суток(0,1-0,2 мг/л)
- ПДК в воде = 2 мг/л, 3 класс опасности (СанПиН
2.1.4.1074-01)
7.
Показатели характеризующие процессысамоочищения (продолжение)
Нитриты
• Представляют собой продукты окисления
аммиака под влиянием микроорганизмов в
процессе нитрификации
• Наличие нитритов свидетельствуют о
возможном загрязнении воды органическими
азотсодержащими веществами, указывают на
определенную давность загрязнения (25-27
суток) (0,001-0,002 мг/л)
8.
Показатели характеризующие процессысамоочищения (продолжение)
Нитраты
• Конечные продукты минерализации
органических
• Наличие нитритов свидетельствуют о
возможном загрязнении воды органическими
азотсодержащими веществами, указывают на
определенную давность загрязнения (25-27
суток) (45 мг/л)
9.
Определение аммиака(ГОСТ 33045-2014)
Сущность метода: Настоящий метод основан на способности
аммиака и ионов аммония взаимодействовать с реактивом
Несслера с образованием окрашенного в желто-коричневый
цвет соединения с последующим фотометрическим
определением и расчетом массовой концентрации
определяемых компонентов в пробе исследуемой воды.
Подготовка пробы для исследования:
- влияние на анализ остаточного активного хлора устраняют
добавлением эквивалентного количества
серноватистокислого натрия;
- жесткости - добавлением раствора виннокислого калиянатрия и большого количества железа;
- цветности и мутности - осветлением гидроокисью алюминия,
сульфатом алюминия,
- сульфатом цинка или сульфатом меди с последующей
фильтрацией осветленных растворов.
10.
Определение аммиака(ГОСТ 33045-2014)
Проведение исследования: К 100 мл исследуемой,
осветленной или подготовленной пробы
прибавляют 2 мл сегнетовой соли, перемешивают,
затем прибавляют 2 мл реактива Несслера и снова
перемешивают. Через 10 мин приступают к
измерению оптической плотности раствора на
фотоэлектроколориметре.
11.
Определение нитритов(ГОСТ 33045-2014)
Сущность метода заключается во взаимодействии нитритов в
исследуемой пробе воды с сульфаниловой кислотой в
присутствии а-нафтиламина с образованием краснофиолетового окрашенного соединения с последующим
фотометрическим определением и расчетом массовой
концентрации нитритов в пробе исследуемой воды.
Подготовка пробы для исследования:
- влияние на анализ остаточного активного хлора устраняют
добавлением эквивалентного количества
серноватистокислого натрия;
- жесткости - добавлением раствора виннокислого калиянатрия и большого количества железа;
- цветности и мутности - осветлением гидроокисью алюминия,
сульфатом алюминия,
- сульфатом цинка или сульфатом меди с последующей
фильтрацией осветленных растворов.
12.
Определение нитритов(ГОСТ 33045-2014)
Проведение исследования: К 100 мл
исследуемой или осветленной пробы прибавляют
5 мл реактива Грисса, перемешивают. Через 40
мин выдерживания пробы при комнатной
температуре или через 10 мин (при помещении
пробы в водяную баню при температуре от 50°С
до 60°С с последующим охлаждением) проводят
измерение оптической плотности раствора на
фотоэлектроколориметре
13.
Определение нитратов(ГОСТ 33045-2014)
Сущность метода заключается во взаимодействии нитратов с
фенолдисульфоновой кислотой с образованием нитропроизводных
фенола, которые со щелочами образуют окрашенные в желтый цвет
соединения, и последующим фотометрическим определением и
расчетом массовой концентрации азота нитратов в пробе
исследуемой воды.
Проведение исследования: Определению мешают хлориды в концентрации
более 10 мг/дм3. Их влияние устраняют в процессе подготовки пробы
исследуемой воды к анализу добавлением раствора сернокислого серебра.
После этого 10 мл свободного от хлоридов фильтрата выпаривают в
фарфоровой чашке на водяной бане досуха (не прокаливая), а затем, охладив
чашку, добавляют 20 капель (2 мл) раствора фенолдисульфоновой
(сульфофеноловой) кислоты, тщательно растирают его стеклянной палочкой
до полного смешивания с сухим остатком. Через 5 мин добавляют 20 мл
дистиллированной воды и 5 - 6 мл раствора аммиака до получения
максимальной интенсивности окраски. Окрашенный раствор количественно
переносят в мерную колбу вместимостью 50 мл и доводят до метки
дистиллированной водой. Окрашенный раствор колориметрируют на
электроколориметре.












 Химия
Химия Экология
Экология








