Похожие презентации:
Неорганические вещества
1.
Неорганические вещества.Юсуповой Екатерины Максимовной
«МАОУ Ангарский лицей №2 им.
М.К.Янгеля» 10фх класс
2.
Неорганическиевещества.
-простые вещества и соединения, не являющиеся органическими, то
есть, не содержащие углерода, а также некоторые
углеродсодержащие соединения (карбиды, цианиды, карбонаты, оксиды
углерода, CO и СO2 и некоторые другие вещества.
Делятся на:
Простые вещества
Сложные вещества
3.
Простые вещества.– это вещества, состоящие из атомов одного элемента.
П од р а здел я ютс я н а д в е б ол ь ш и е г ру п п ы :
Металлы
Металлы - это группа простых тел, обладающих
известными характерными свойствами, которые в
типических представителях резко отличают металлы от
других химических элементов.
К металлам относятся: железо, медь, цинк, кальций,
алюминий, золото, серебро, натрий, олово и т.д.
Неметаллы
Неметаллами - группа простых тел, обладающих
известными характерными свойствами, которые
резко отличают неметаллы от других химических
элементов.
К неметаллам относятся: водород, кислород,
фосфор, сера, углерод, неон и т.д.
4.
Сложные вещества.- это вещества, состоящие из атомов двух и более элементов.
Подразделяются на четыре
большие группы:
• оксиды
• основания
• кислоты
• соли
5.
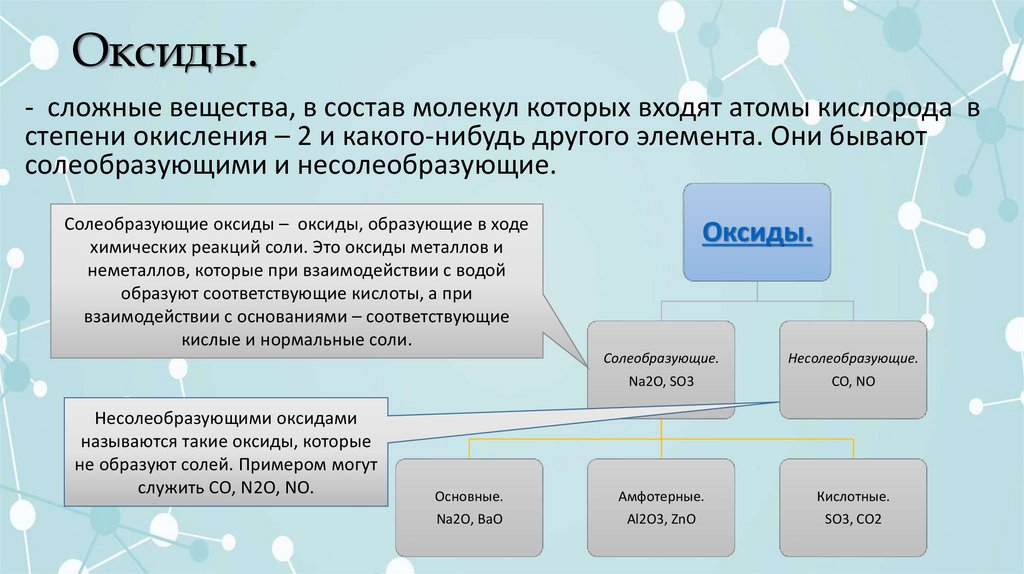
Оксиды.- сложные вещества, в состав молекул которых входят атомы кислорода в
степени окисления – 2 и какого-нибудь другого элемента. Они бывают
солеобразующими и несолеобразующие.
Солеобразующие оксиды – оксиды, образующие в ходе
химических реакций соли. Это оксиды металлов и
неметаллов, которые при взаимодействии с водой
образуют соответствующие кислоты, а при
взаимодействии с основаниями – соответствующие
кислые и нормальные соли.
Несолеобразующими оксидами
называются такие оксиды, которые
не образуют солей. Примером могут
служить СО, N2O, NO.
Оксиды.
Солеобразующие.
Несолеобразующие.
Na2O, SO3
CO, NO
Основные.
Амфотерные.
Кислотные.
Na2O, BaO
Al2O3, ZnO
SO3, CO2
6.
Основания.
- это вещества, молекулы которых состоят из молекул металла и гидроксгруппы - ОН. Основания образуются при взаимодействии ряда металлов
(натрий, калий) или некоторых оксидов (оксид кальция CaO) с водой.
• Растворимые в воде основания называются щелочами.
Растворы щелочей «мыльные», скользкие на ощупь и
довольно едкие. К щелочам относят гидроксиды
щелочных и щелочноземельных металлов
• Нерастворимые основания – это амфотерные гидроксиды,
которые при взаимодействии с кислотами выступают как
основания, а со щёлочью ведут себя, как кислоты.
7.
Кислоты.- это группа соединений с известной, довольно определенной химической
функцией. Эта функция выражена в таких типичных представителях
этой группы, как серная кислота H2SO4, азотная кислота HNO3,
соляная кислота НСl и прочие.
Классификация кислот по содержанию кислорода:
• бескислородные (HCl, H2S, HBr)
• кислородсодержащие (HNO3, H2SO4, H3PO4).
8.
Соли.- это химическое соединение, образовавшееся в результате
взаимодействия кислоты и основания.
• Средние соли
- все атомы водорода в кислоте замещены металлом.
• Кислые соли
- могут образовывать только двух- или многоосновные кислоты.
• Двойные соли - атомы водорода двух- или многоосновной кислоты замещены не
одним металлом, а двумя различными.
• Соли основные - можно рассматривать как продукты неполного или частичного
замещения гидроксильных групп оснований кислотными
остатками.






 Химия
Химия








