Похожие презентации:
Кислоты, их классификация и свойства
1.
Кислоты, ихклассификация и
свойства.
Лабораторная работа Составитель:
учитель химии МКОУ Симоновской
ООШ им.А.Ф Щербатова. Крылусова Л.С
2.
Кислоты, их классификация исвойства.
3.
Кислоты, их классификация исвойства.
Цели урока: Сформировать понятие о
кислотах как о классе электролитов,
рассмотреть их классификацию и обшие
свойства кислот в свете ионных
представлений.
4.
Химические свойства кислот.Задачи: Осуществить реакции между серной
кислотой и основанием, оксидом металла,
металлом, солью, соблюдая правила
безопасности Выяснить при каких условиях
идут эти реакции.
5.
Химические свойства кислотЦель: осуществление эксперимента,
подтверждающего химические свойства
кислот
6.
Приборы и реактивы:Растворы: H2SO4; NaOH; Na2CO3; Ba(NO3)2 ;
NaCI; CuO; Zn
3. индикатор: метилоранжевый (м/о);
4. 6 пробирок
5. спиртовка; держатель; спички
7.
Повторить правила ТБ8.
Ход работыдействия наблюдения уравнения реакций
выводы
9.
действия наблюдения уравненияреакций выводы
Действия
NaOH Р-р, б/ц
H2SO4 +м/о р-р красный
р-р оранжевый
10.
ВыводКислоты взаимодействуют с оксидами
металлов без условий
11.
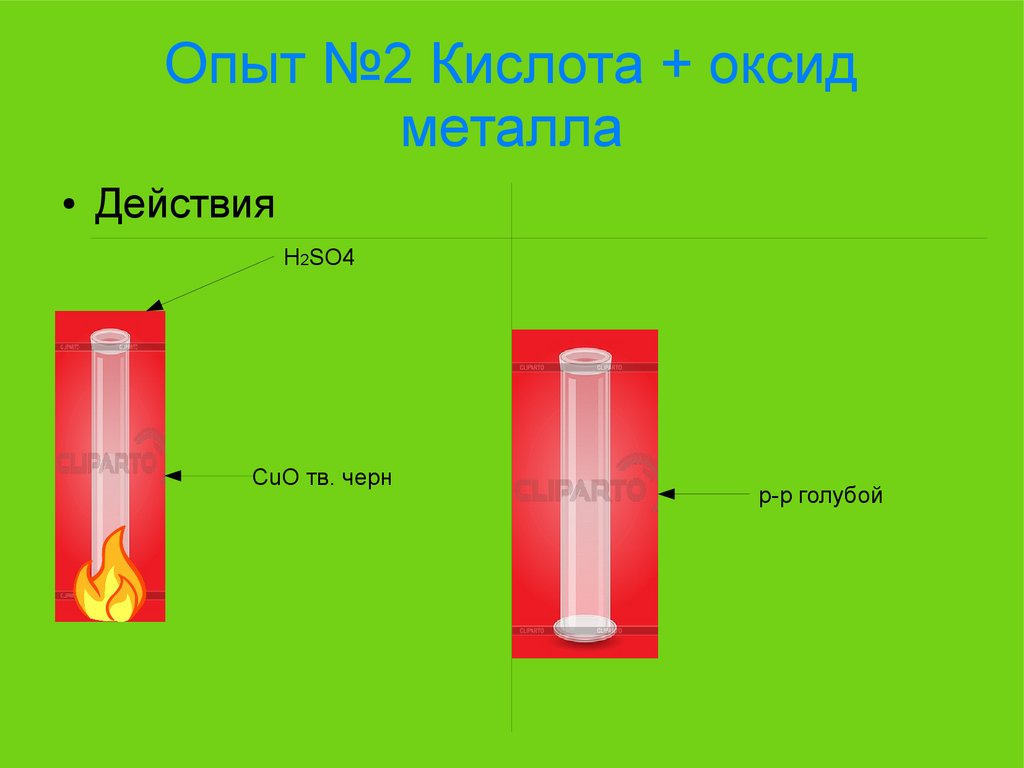
Опыт №2 Кислота + оксидметалла
Действия
H2SO4
CuO тв. черн
р-р голубой
12.
ВыводКислоты взаимодействуют с оксидами
металлов без условий
13.
Опыт №3 Кислота + металлДействия Наблюдения:
H2SO4
Газ б/ц, б/з
Zn тв.
14.
ВыводКислоты реагируют с металлами если:
Металл стоит до Н2 (см. э/х ряд) Соль
растворима НЕ РАССМАТРИВАТЬ HNO3;
H2SiO3; H2SO4 (конц)
15.
Опыт №4 Кислота + сольH2SO4
Газ б/ц, б/з
Na2CO3 р-р б/ц
H2SO4 H2SO4
NaCl р-р, б/ц
H2SO4
Бел.
Ba(NO3)2 р-р, б/ц
16.
ВыводКислота реагирует с солью
если:
Выпадает осадок;
Выделяется газ
17.
ЗаданиеЗаписать уравнения
реакций в
молекулярном и ионном
виде
18.
ЛитератураО.С.Габриелян ,. Химия. 8
класс :
учеб. для ОУ - М.: Дрофа,
2007.


















 Химия
Химия








