Похожие презентации:
ОГЭ химия 2021 задание 13
1.
Основнойгосударственный экзамен
Химия 2021
Задание 13
2.
Задание 13. Электролиты и неэлектролиты. Катионыи анионы. Электролитическая диссоциация кислот,
щелочей и солей (средних).
Примерное время выполнения задания – 2 минуты
Уровень сложности задания – базовый
Максимальный балл за выполнение задания - 1
Задание № 13 направлено на проверку знания сильных и слабых
электролитов, а также умения составлять уравнения
электролитической диссоциации неорганических веществ,
объяснять сущность процесса электролитической диссоциации
и реакции ионного обмена.
Задание содержит перечень из пяти веществ. Необходимо
выбрать два из них, которые соответствуют данному условию.
В ответе нужно записать номера выбранных вариантов.
3.
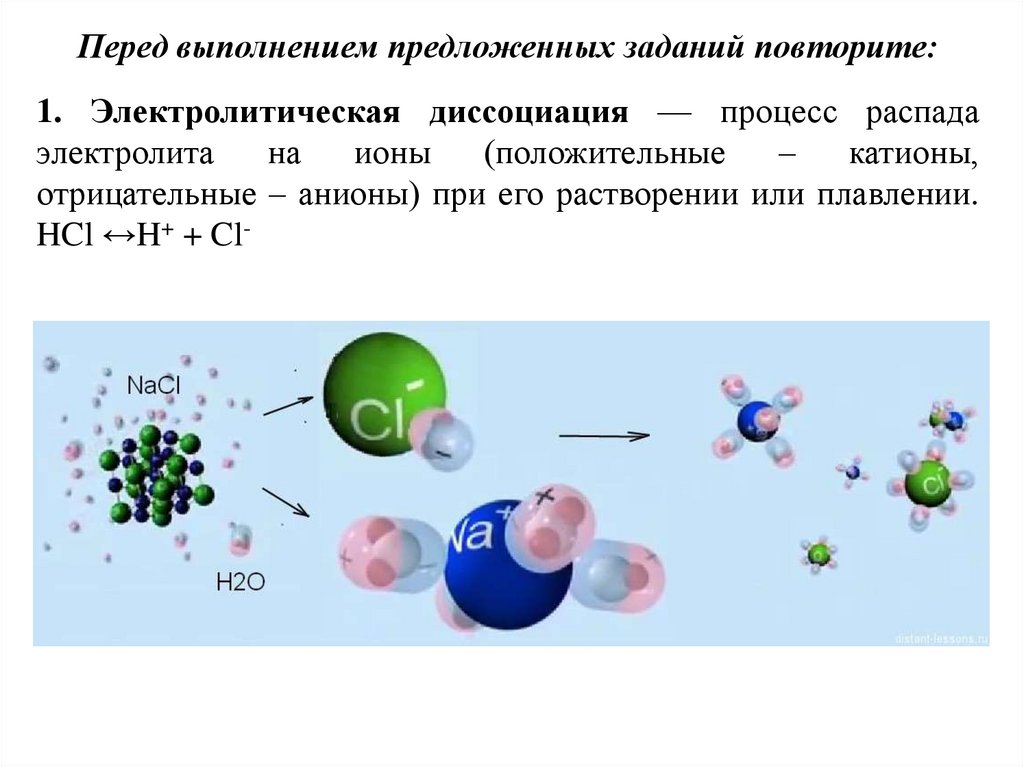
Перед выполнением предложенных заданий повторите:1. Электролитическая диссоциация — процесс распада
электролита
на
ионы
(положительные
–
катионы,
отрицательные – анионы) при его растворении или плавлении.
HCl ↔H+ + Cl-
4.
2. Сильные электролиты - это вещества, которые при растворении вводе практически полностью распадаются на ионы. Как правило, к
сильным электролитам относятся вещества с ионными или сильно
полярными связями: все хорошо растворимые соли, сильные кислоты
(HCl, HBr, HI, HClO4, H2SO4, HNO3) и сильные основания
(LiOH, NaOH, KOH, RbOH, CsOH, Ba(OH)2, Sr(OH)2, Ca(OH)2).
5.
3. Слабые электролиты-вещества, частично диссоциирующие наионы. Растворы слабых электролитов наряду с ионами содержат
недиссоциированные молекулы. Слабые электролиты не могут дать
большой концентрации ионов в растворе.
6.
4. Неэлектролиты — вещества, в молекулах которых имеютсятолько ковалентные неполярные или малополярные связи. К ним
относятся все простые вещества, оксиды неметаллов, многие
органические соединения.







 Химия
Химия








