Похожие презентации:
Окислительно-восстановительные процессы
1.
Окислительновосстановительные процессы2.
Индивидуальная работаЗадание 1: Запишите определения на выданных листочках
1) ОВР – это....
2) Степень окисления – это...
3) Окислитель – это...
4) Восстановление – это....
5) Восстановитель – это....
6) Окисление – это.....
3.
Задание 2: Работа у доскиА) Подчернуть схемы, показывающие процесс
окисления:
a) S0→S-2
c) S0→S+4
b) S+4→ S+6
d) S+6→S0
Б) Подчернуть схемы, показывающие процесс
восстановления:
a) N0→N-3
c) N+3→N+5
b) N+2→ N+4
d) N+5→N0
4.
С) Расставьте коэффициенты в схемах ОР методом электронногобаланса. Укажите окислитель и восстановитель.
a) Na + S → Na2S
……………………………
……………………………
b) WO3 + Ca → CaO + W
……………………………
……………………………
c) Al + Cl2 → AlCl3
……………………………
………………………
d) Al + HCl → AlCl3 + H2
…………………………….
…………………………….
5.
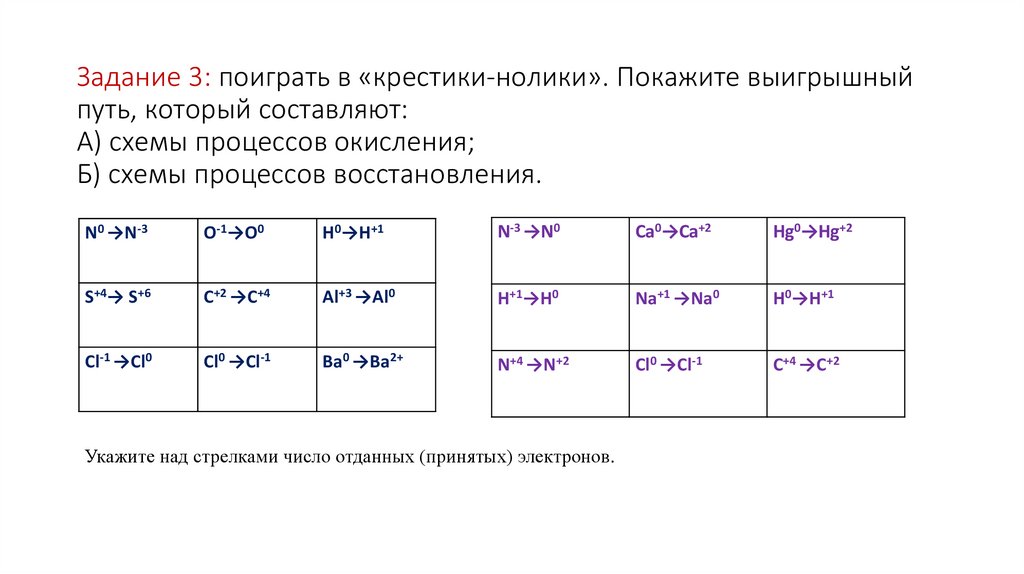
Задание 3: поиграть в «крестики-нолики». Покажите выигрышныйпуть, который составляют:
А) схемы процессов окисления;
Б) схемы процессов восстановления.
N0 →N-3
O-1→O0
H0→H+1
N-3 →N0
Ca0→Ca+2
Hg0→Hg+2
S+4→ S+6
C+2 →C+4
Al+3 →Al0
H+1→H0
Na+1 →Na0
H0→H+1
Cl-1 →Cl0
Cl0 →Cl-1
Ba0 →Ba2+
N+4 →N+2
Cl0 →Cl-1
C+4 →C+2
Укажите над стрелками число отданных (принятых) электронов.




 Химия
Химия








