Похожие презентации:
Металлы. Особенности строения атомов металлов и их положения в ПСХЭ. Физические свойства
1. МЕТАЛЛЫ Особенности строения атомов металлов и их положения в ПСХЭ. Физические свойства
2. Металлы и небесные тела
Золото – СолнцеСеребро – Луна
Ртуть – Меркурий
Медь – Венера
Железо – Марс
Олово – Юпитер
Свинец - Сатурн
3. Роль металлов в истории развития человечества
История древних цивилизацийнеразрывно связана с
использованием металлов для
изготовления орудий труда,
предметов обихода,
украшений.
Украшение из меди
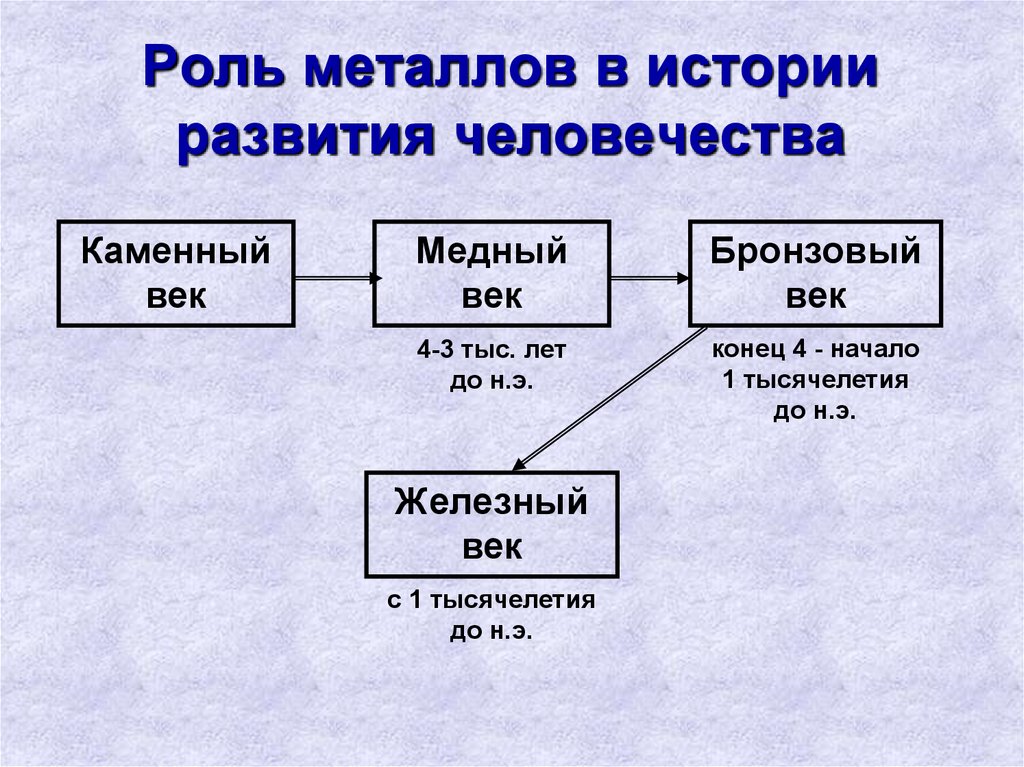
4. Роль металлов в истории развития человечества
Каменныйвек
Медный
век
Бронзовый
век
4-3 тыс. лет
до н.э.
конец 4 - начало
1 тысячелетия
до н.э.
Железный
век
с 1 тысячелетия
до н.э.
5. Почему после каменного века наступил медный?
?Почему после каменного века
наступил медный?
Тит Лукреций Кар
«О природе вещей»
«… Все-таки в употребление
вошла раньше медь, чем
железо, так как была она
мягче, причем изобильней
гораздо…»
Самородок меди
6. Бронзовый век
При выплавкеметаллов человек
использовал не
чистую медную руду,
а содержащую
одновременно медь и
олово.
В результате была
получена бронза –
сплав меди и олова.
7. Железный век
Смена бронзовоговека на железный
связана с развитием
техники и технологии
выплавки металлов.
Только когда человек
смог увеличить
температуру в печи до
15400С наступил
железный век.
8. Положение металлов в ПСХЭ
9. Положение металлов в ПСХЭ
Группы металловЩелочные
металлы.
Свое название
получили от
названия
соответствующих
им гидроксидов –
щелочей.
Щелочноземельные
металлы.
Название указывает
на то, что оксиды этих
металлов (раньше
называли «землями»)
при растворении в
воде образуют
щелочи.
10. Строение атомов металлов
Особенности строения атомовметаллов:
1.
2.
На внешнем энергетическом
уровне 1 – 3 электрона.
Относительно большой радиус
атомов.
Металлы могут проявлять только
восстановительные свойства.
11. Строение кристаллов металлов
?Какой вид химической связи
характерен для металлов?
Металлическая химическая
связь (мет.х.св.)
?
Какой вид кристаллической решетки
в металлах?
Металлическая кристаллическая
решетка (мет.кр.реш.)
12. Металлическая химическая связь
Химическая связь между атомамиметалла, осуществляемая посредством
общих свободно перемещающихся
электронов называют металлической
связью. Эта связь характерна для
типичных металлов, для их сплавов и их
интерметаллических соединений,
образованных атомами разных
металлов.
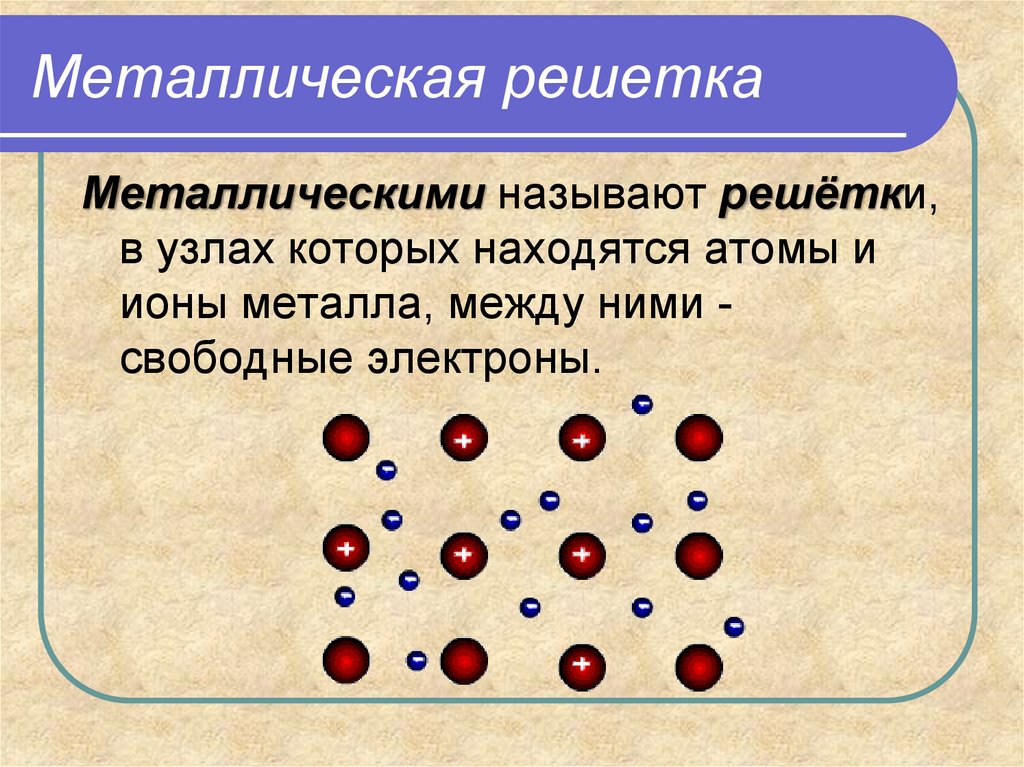
13. Металлическая решетка
Металлическими называют решётки,в узлах которых находятся атомы и
ионы металла, между ними свободные электроны.
14. Физические свойства металлов
1.2.
3.
4.
5.
6.
Твердое агрегатное
состояние.
Серый цвет.
Металлический
блеск.
Электропроводность.
Теплопроводность.
Пластичность,
ковкость.
искл. – Hg
искл. – Cu (красн.),
Au (желт.),
Cs (золотистый)
Ag Cu Au Al … Hg Pb Mn
понижение
Au Ag Cu Sn Pb Zn… Bi Mn
понижение












 Химия
Химия








