Похожие презентации:
Положение атомов - металлов в ПСХЭ Д.И.Менделеева. 9 класс
1. Положение атомов - металлов в ПСХЭ Д.И.Менделеева
Простые вещества –Металлы.
2. В 2006 году в США в штате было стихийное бедствие – ураган «Катрина». В результате сильнейшего в мире урагана все конструкции
домов разрушились, после потопаначали основательно разрушаться под
воздействием солевого раствора океана.
P.S.
Как вы знаете, конструкции жилых помещений
созданы из металлической арматуры.
3. Внимание вопрос:
Какие воздействия оказаны наконструкции домов?
Физические
Химические
4.
Из каких же металлов сооружатьконструкции домов , чтобы уберечь от
катастрофы?
5.
6. Металлическая кристаллическая решетка
++
+
+
+
7. Физические свойства металлов
ТвердостьПлотность
Плавкость
Электропроводность
Теплопроводность
Металлический блеск
Пластичность
8. «Давайте построим дом!»
Чтобы было …Прочным (свойства:
твердость, плотность,
тугоплавкость,
не пластичность )
Безопасным
(свойства: малая
электропроводность и теплопроводность)
Красивым
(свойства: металлический блеск)
9.
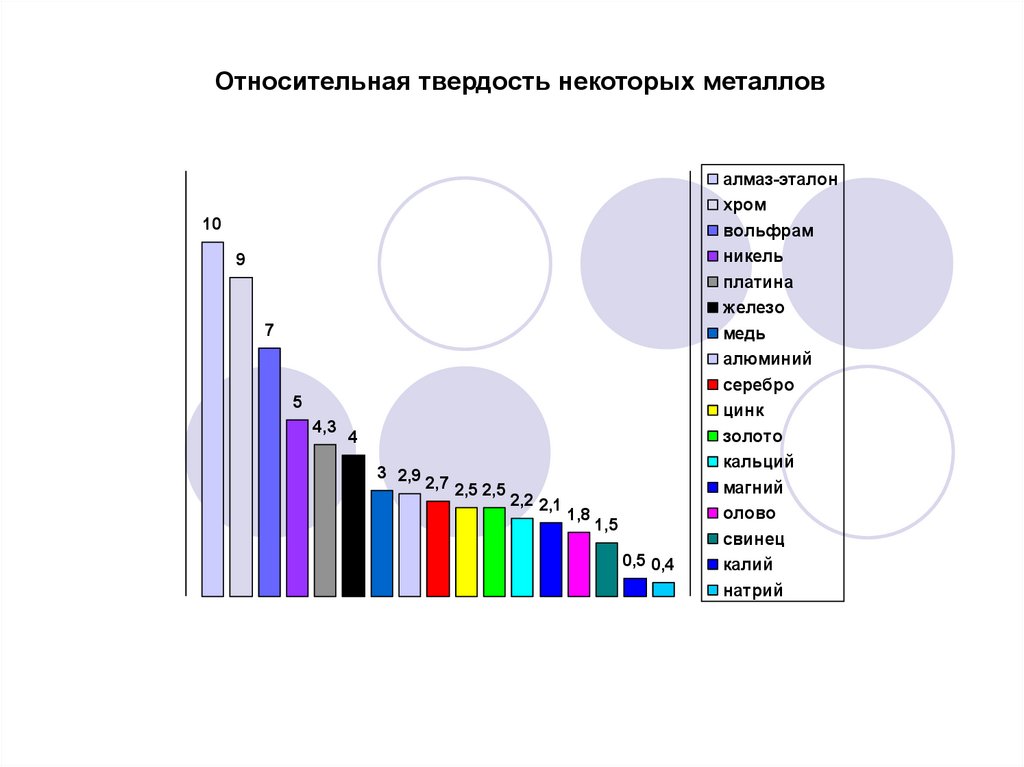
Относительная твердость некоторых металловалмаз-эталон
хром
вольфрам
10
никель
9
платина
железо
7
медь
алюминий
серебро
5
цинк
4,3
золото
кальций
4
3 2,9
2,7 2,5 2,5
2,2 2,1
магний
1,8
олово
свинец
1,5
0,5 0,4
калий
натрий
10.
Плотность некоторых металлов21,45
19,3
13,6
11,34
10,5
8,9 8,9
7,87
7,3 7,14
2,7
Тяжелые металлы
1,74
1,54 0,97
0,86
Легкие металлы
Платина
Золото
ртуть
свинец
серебро
медь
никель
железо
олово
цинк
алюминий
магний
кальций
натрий
калий
11. Температура плавления некоторых металлов
3370ртуть
калий
натрий
олово
свинец
цинк
1755
1539
1452
1083
1063
851 961
651 660
419
232 328
63,5 98
-39
магний
алюминий
кальций
серебро
золото
медь
никель
железо
платина
вольфрам
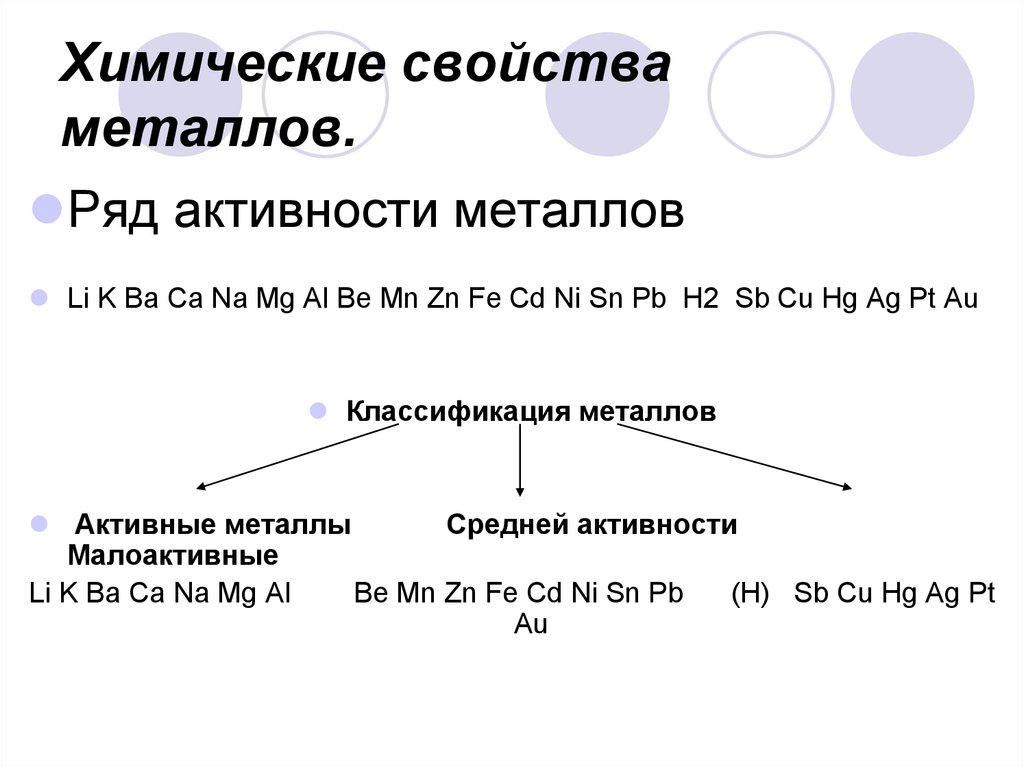
12. Химические свойства металлов.
Ряд активности металловLi K Ba Ca Na Mg Al Be Mn Zn Fe Cd Ni Sn Pb H2 Sb Cu Hg Ag Pt Au
Классификация металлов
Активные металлы
Средней активности
Малоактивные
Li K Ba Ca Na Mg Al
Be Mn Zn Fe Cd Ni Sn Pb
(Н) Sb Cu Hg Ag Pt
Au
13. Общие свойства металлов
МеталлНеметалл
Основной
оксид
Кислотный
оксид
Основание
Кислота
Соль
14. Химические свойства с:
С неметалламиС кислородом
С водой
С кислотами
С солями
15. Докончите уравнения реакций:
I. Взаимодействие с кислородом:1.K+ O2=
2. Fe + O2=
3. Cu + O2=
II. Взаимодействие с водой:
4. Na + H2O=
5. Zn + H2O=
6. Hg + H2O=
III. Взаимодействие с растворами кислот:
7. Na + H2SO4 =
8. Zn + H2 SO4 =
9. Hg + HCl =
IV. Взаимодействие с растворами солей:
10. Сa + CuSO4=
11. Zn + AgNO3=
12. Cu + FeCl3=
V. Взаимодействие с неметаллами:
13. Ва + Cl2=
14. Hg + S =
15. Li + N2 =
16. Лабораторная работа «Свойства металлов с кислотами и с солями»
Опыт№ 1.1. В пробирку положите кусочек цинка и
добавьте 2 мл HCl, учитывая, что
пробирка вмещает 10 мл.
Рассмотрите химические свойства
натрия и цинка с соляной кислотой.
Напишите уравнения реакций.
Сделайте соответствующие выводы.
17. Лабораторная работа «Свойства металлов с кислотами и с солями»
Опыт№2.1. Железный гвоздь опустите в раствор
NaCl. Что вы наблюдаете?
2. Эту же гвоздь опустите в раствор
CuSO4. Что вы наблюдаете?
Напишите соответствующие
уравнения реакций.
18. Рефлексия
Какие металлы нужно брать длясооружения зданий, чтобы они не
подвергались химическим
воздействиям?
19.
Домашнее задание:Изучить §7 «Сплавы»
Упражнения 1,2.

















 Химия
Химия








