Похожие презентации:
Теория электролитической диссоциации
1.
Теорияэлектролитической
диссоциации
1877 г.
Сванте Аррениус
2.
Электролитическая диссоциация —это процесс распада электролита на ионы.
3.
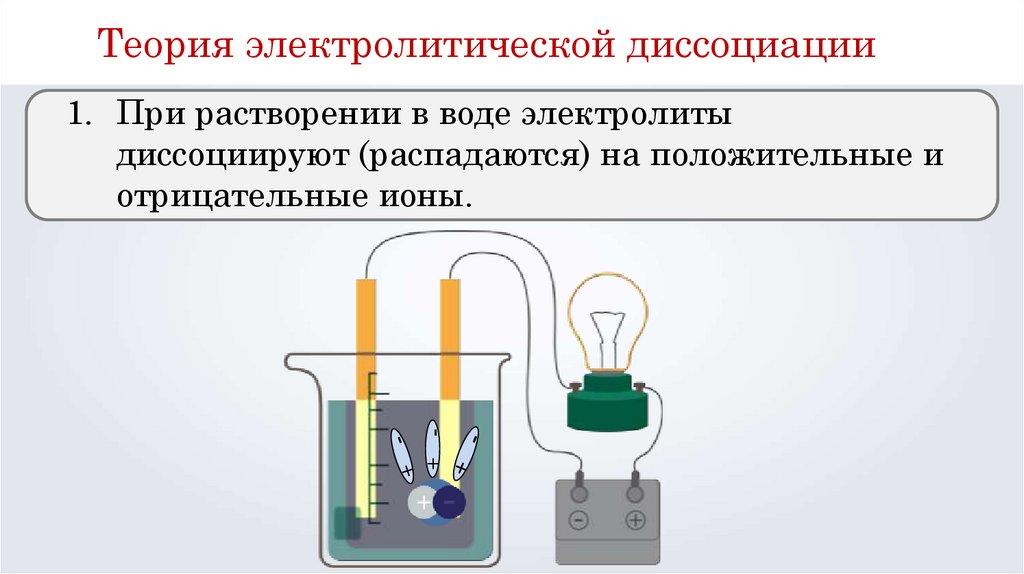
Теория электролитической диссоциации+
-
1. При растворении в воде электролиты
диссоциируют (распадаются) на положительные и
отрицательные ионы.
4.
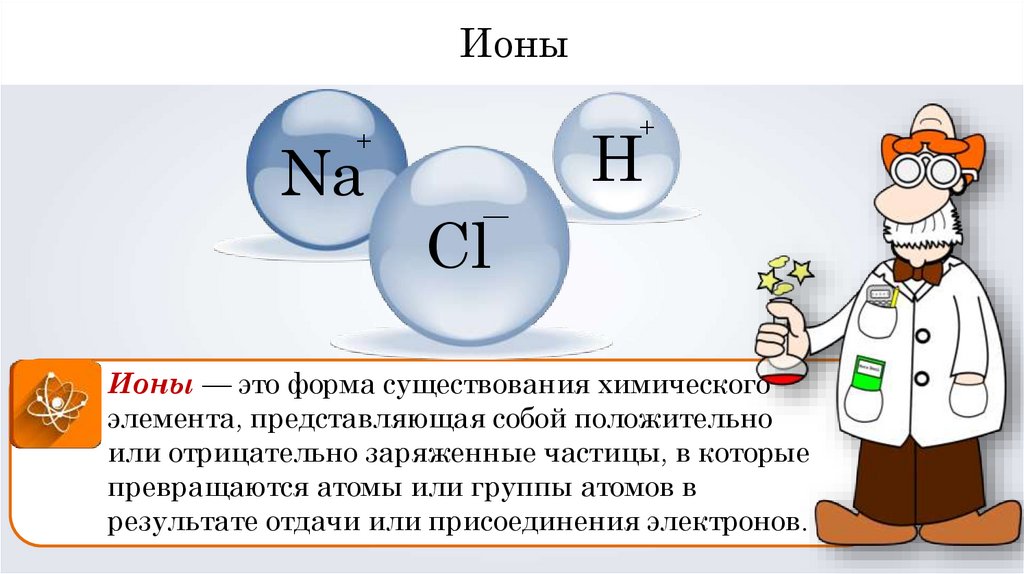
Ионы+
H
+
Na
—
Cl
Ионы — это форма существования химического
элемента, представляющая собой положительно
или отрицательно заряженные частицы, в которые
превращаются атомы или группы атомов в
результате отдачи или присоединения электронов.
5.
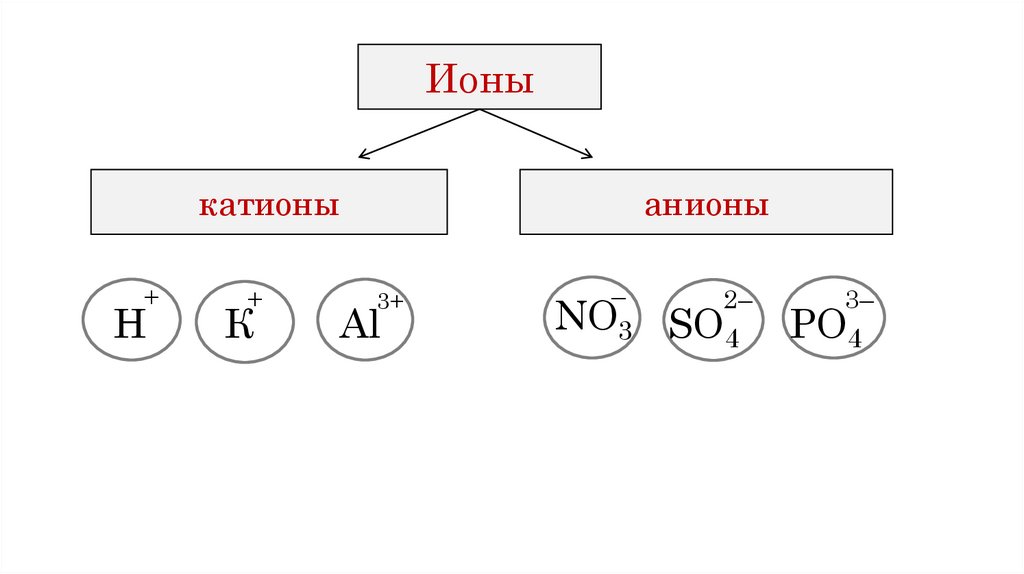
Ионыкатионы
+
Н
+
К
анионы
3+
Al
–
NO3
2–
SO4
3–
PO4
6.
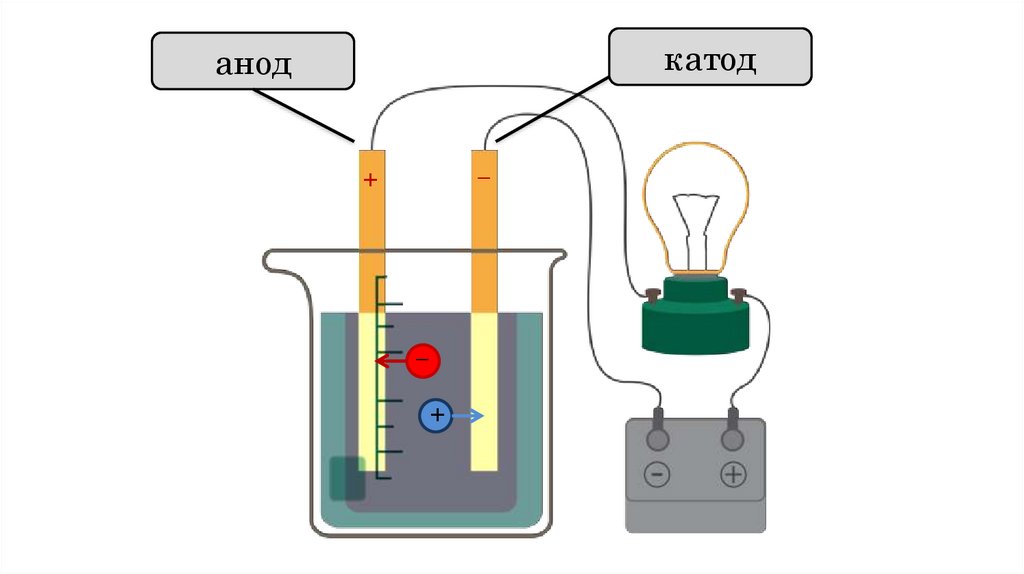
Теория электролитической диссоциации3. Под действием электрического тока, положительно
заряженные ионы движутся к отрицательно
заряженному полюсу источника тока — катоду,
поэтому их называют катионами, а отрицательно
заряженные ионы движутся к положительному
полюсу источника тока — аноду, поэтому их
называют анионами.
7.
катоданод
–
+
–
+
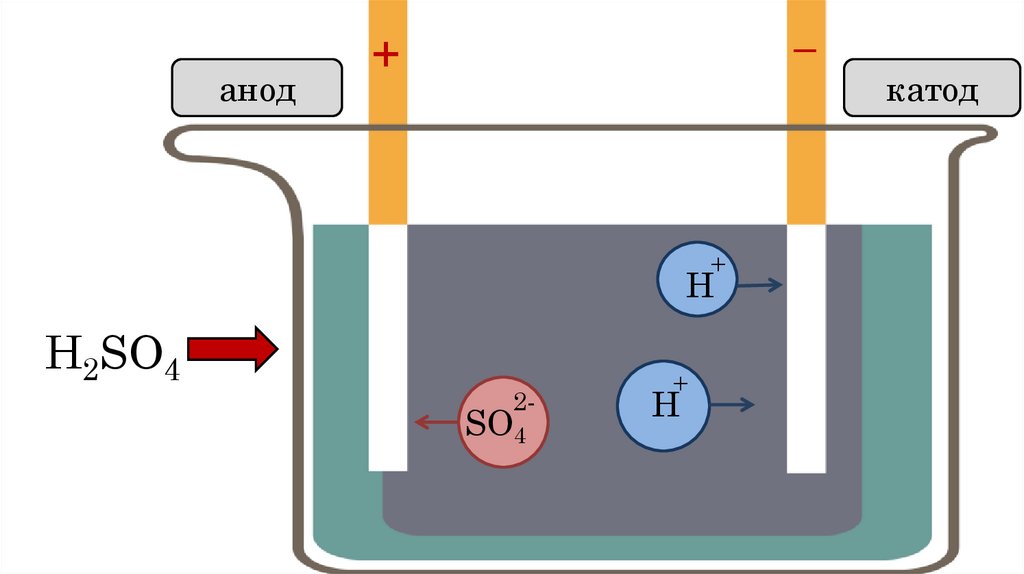
8.
анод–
+
+
Н
H2SO4
2-
SO4
+
Н
катод
9.
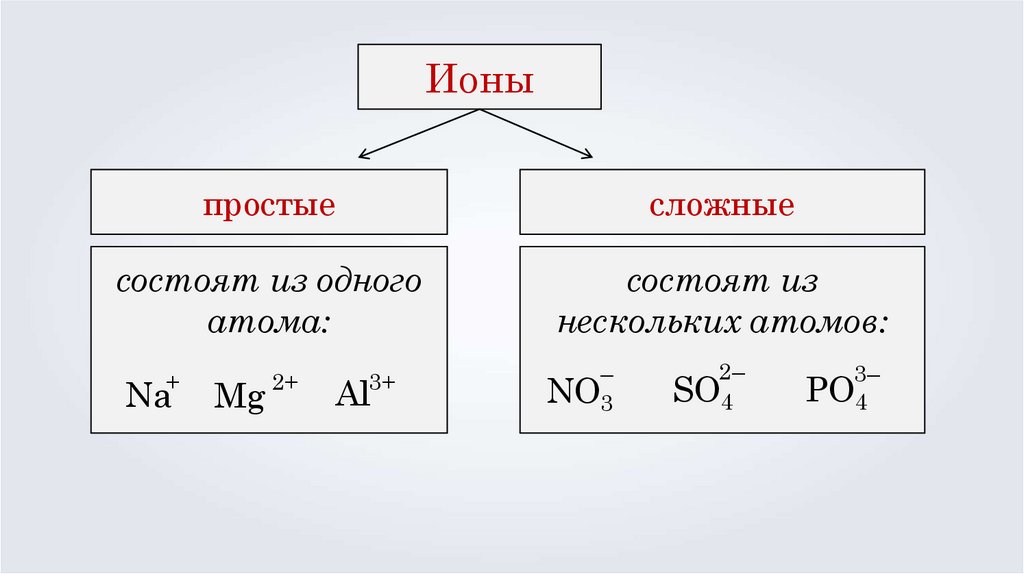
Ионыпростые
сложные
состоят из одного
атома:
состоят из
нескольких атомов:
+
Na
Мg
2+
3+
Al
–
NO3
2–
SO4
3–
PO4
10.
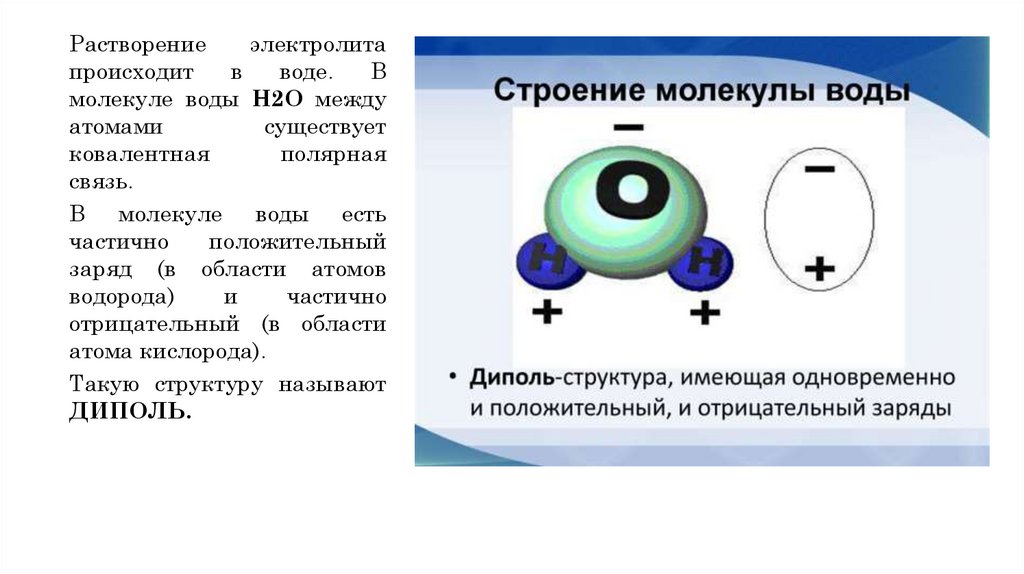
Растворениеэлектролита
происходит
в
воде.
В
молекуле воды H2O между
атомами
существует
ковалентная
полярная
связь.
В молекуле воды есть
частично
положительный
заряд (в области атомов
водорода)
и
частично
отрицательный (в области
атома кислорода).
Такую структуру называют
ДИПОЛЬ.
11.
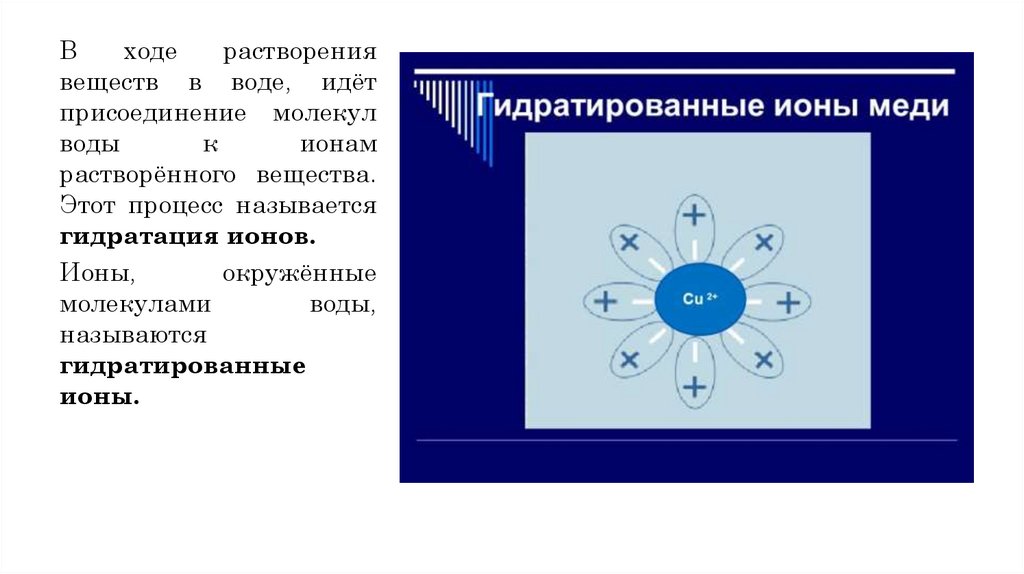
Входе
растворения
веществ в воде, идёт
присоединение молекул
воды
к
ионам
растворённого вещества.
Этот процесс называется
гидратация ионов.
Ионы,
окружённые
молекулами
воды,
называются
гидратированные
ионы.
12.
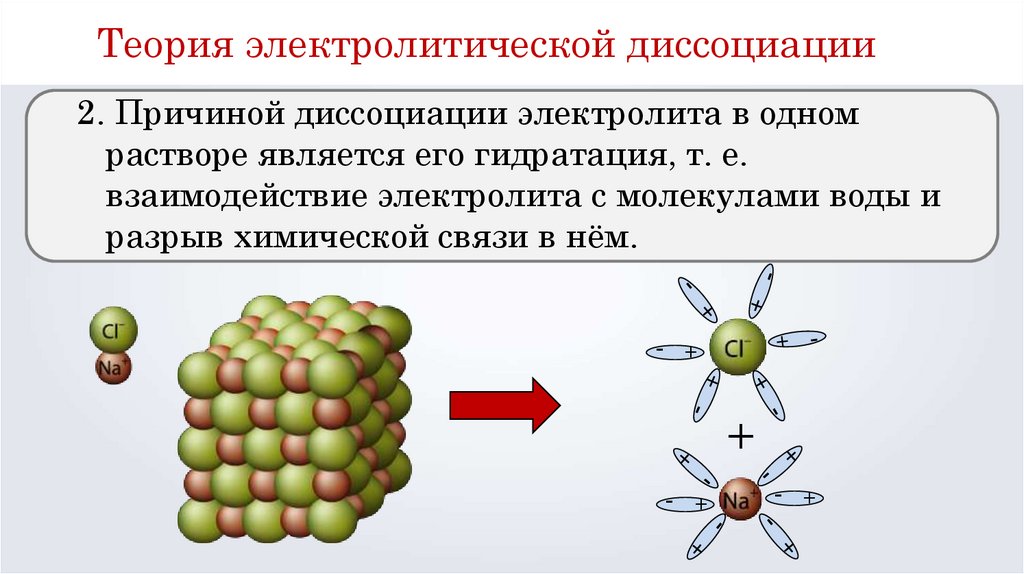
Теория электролитической диссоциации2. Причиной диссоциации электролита в одном
растворе является его гидратация, т. е.
взаимодействие электролита с молекулами воды и
разрыв химической связи в нём.
+
-
+
+
-
+
-
13.
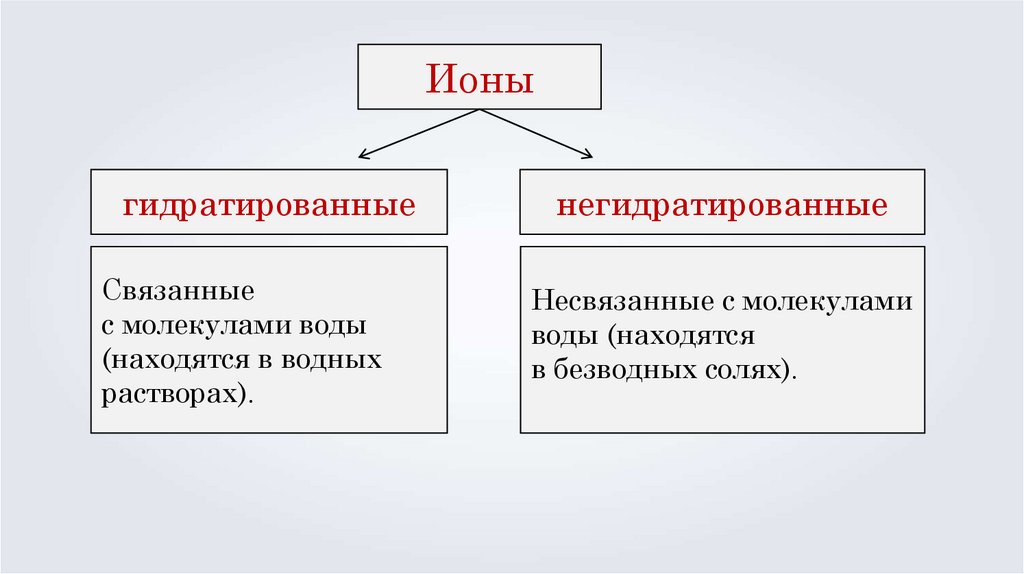
Ионыгидратированные
Связанные
с молекулами воды
(находятся в водных
растворах).
негидратированные
Несвязанные с молекулами
воды (находятся
в безводных солях).
14.
ИоныГидратированные
могут иметь
окраску
2+
Сu
Негидратированные
бесцветные
2+
Сu




 Химия
Химия








