Похожие презентации:
Химическая термодинамика
1.
В данной презентациииспользовался материал:
www.kgasu.ru/images/
2.
– область химии, изучающая энергетикухимических процессов, возможности и условия
самопроизвольного
протекания
химических
реакций,
а
также
условия
установления
химического равновесия.
Паровая машина (18 в.) – теплота и работа.
В основе ТД лежат три закона или начала.
3. Термодинамическая система (ТС)
• Объект изучения химическойтермодинамики термодинамическая
система (ТС). ТС – это тело или группа
тел, выделенных для рассмотрения,
отделенных от окружающей среды (ОС),
реальной или воображаемой границей.
4.
• ТС бывают:• 1. Изолированные – отсутствуют, какие-либо
формы обмена с окружающей средой.
• 2. Открытыми – система обменивается с
окружающей средой энергией и веществом.
• 3.Закрытые - система обменивается с
окружающей средой только энергией, обмен
веществом невозможен.
5.
В ходе различных превращений системапереходит из одного энергетического состояния
в другое. То или иное состояние системы опр-ся
или хар-ся термодинамическими параметрами.
Основными параметрами системы являются:
.
В зависимости от постоянства параметров
процессы делятся на:
изохорные (V = const),
изобарные (p = const)
изотермические (T = const).
6.
Др. параметры, зависящие от основных, наз-сясистемы.
В химии наиболее часто используются :
• внутренняя энергия U и её изменение U
при V = const;
• энтальпия (теплосодержание) H и её изменение H при p = const;
• энтропия S и её изменение S;
• энергия Гиббса G и её изменение G при
p = const и T = const.
Для ф-ций состояния хар-но, что их изм-ние в
хим. р-ции опр-ся
и
или
протекания процесса.
7.
• Также для описания состояния тсиспользуют две функции процесса- это
работа (А) и теплота (Q). Их изменение
зависит от пути перехода из начального
состояния в конечное.
8. Внутренняя Энергия
Внутренняя энергия системы (U) – этополная энергия системы, включающая
энергию всех видов движения
молекул, атомов, ядер, электронов и других
структурных единиц, а также
энергию взаимодействия и др., кроме
кинетической и потенциальной энергии всей
системы как целого по отношению к другим
системам.
9.
Запас внутр. энергии системы зависит отпараметров состояния системы, природы в-ва и
прямо пропорционален массе вещества.
систему в
энергии.
, т.к. нельзя привести
состояние, полностью лишенное
Можно судить лишь об изменении внутренней
энергии системы
при её переходе из
начального состояния
в конечное :
,
10.
При переходе неизолированной системы изодного состояния в другое изменение её
внутренней энергии осуществляется путём
обмена с окружающей средой.
с
окружающей средой являются совершение
и выделение или поглощение
.
Это основа
,
к-рый
устанавливает
соотношение
между
теплотой (Q), работой (А) и изменением
внутренней энергии системы ( U).
11.
Раздел химии и хим. ТД, занятый расчётамитепловых эффектов, наз-ся термохимией.
:
аА + bB = cC + dD; Hp
ех:
Н2 + 1/2О2 = Н2О(ж); ΔΗ˚298 = -285,8 кДж,
Или так, но редко:
Н2 + 1/2О2 – 285,8 кДж = Н2О(ж)
или
Н2 + 1/2О2= Н2О(ж) + 285,8 кДж
12.
В основе термохимических расчётов реакцийлежит
(1836 – 1841):
Тепловой эффект реакции ( Нр)
не зависит от пути её протекания, а
определяется только природой и
физическим состоянием исходных веществ
и конечных продуктов.
Этот закон имеет
.
13.
.:
Нр = Н0обр.прод. – Н0обр.исх.
В общем случае тепловой эффект ΔΗр реакции типа:
aA + bB = cC + dD; ΔΗр
рассчитывается по уравнению
ΔΗр = cΔΗºC + dΔΗºD – aΔΗºΑ – bΔΗºB.
.
14.
Поскольку абсолютные значения энергии (т.д.ф-ций) измерить принципиально невозможно, то
для проведения термохим. расчётов вводят
специальные понятия
энтальпия (теплота) образования вещества
энтальпия (теплота) сгорания вещества.
–
это тепловой эффект реакции образования
одного моль данного сложного вещества из
соответствующих простых веществ,
устойчивых при данных условиях.
15.
• Для того, чтобы можно былотеоретически рассчитать и сравнивать
тепловые эффекты в основу
термохимических расчетов положены
энтальпии (теплоты) образования
отнесенные к стандартным условиям.
16.
1.стандартное давление – 0,1 МПа или 1 атм
стандартная температура – 25°C или 298 К.
2.
– это
наиболее устойчивое состояние в-ва в стандартных условиях (ех, у воды стандартное состояние
жидкое).
– это теплота образования 1 моль данного
в-ва в стандартном состоянии и стандартных
условиях
Н0298 обр или Н0298 f или Н0298.
Теплота обр-ния в-ва связана с его количеством
и выражается в Дж/моль или кДж/моль.
17. Пример
• Рассчитать какое количество теплотывыделится при сгорании 8 г метана.
18.
ЭНТРОПИЯПо з-ну сохранения энергии система может
самопроизвольно совершать работу только за
счёт собственной энергии, т.е. U 0.
У хим. р-ций это выражается в виде
эффекта Н 0. Этот фактор
является
из движущих сил хим. р-ции и
называется энергетическим (энтальпийным).
движущей силой является структурный
(энтропийный) фактор. Для поиска
процессов в природе был
сформулирован второй з-н ТД.
19.
Л.Больцман (1877): Т.д. вероятность Wсостояния системы – это число микросостояний,
реализующих данное макросостояние:
где S – энтропия; k – константа Больцмана.
R
8 , 31
23 Дж
k
1 , 38 10
23
N
К
6 , 02 10
Чем больше микросостояний у данного макросостояния, тем оно
. Т.о.:
Энтропия есть мера молекулярного
беспорядка, представляющая логарифмическое выражение т.д. вероятности
состояния системы.
20.
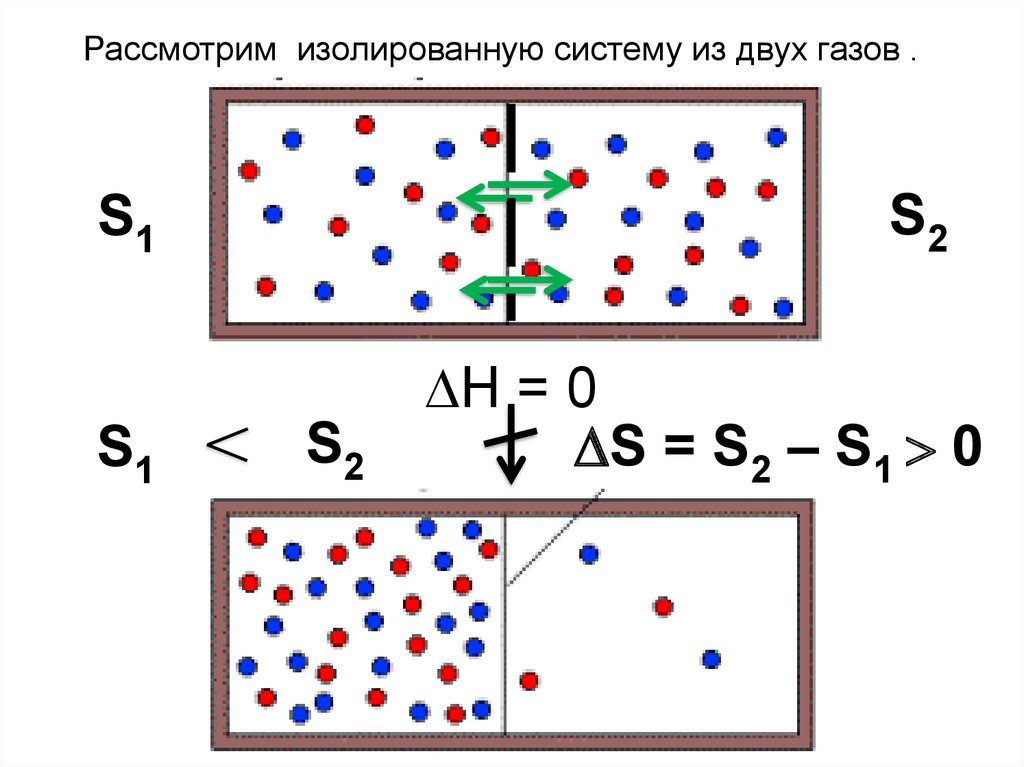
Рассмотрим изолированную систему из двух газов .S2
S1
S1
S2
Н = 0
S = S2 – S1 0
21. 2-ой закон термодинамики
• В изолированной системесамопроизвольно протекают такие
процессы, которые ведут к росту
энтропии.
22.
Энтропия, SС
т-ры энтропия
в-ва ум-ся (ум-ся скорость
Газ
движения частиц, число микросостояний и Т.Д. вероятность
W системы).
ΔSконд
Планк
предположил,
что
при
Ж
т-ре абс. нуля Т=0К энтропия
Кр.
совершенного
(идеального)
ΔSкр
кристалла любого вещества
должна быть равна нулю.
0 Температура, К
Это предположение стало
Рис.4. Зависимость
энтропии вещества от
температуры
23.
S хим. реакции также не зависит от путипроцесса, а определяется лишь энтропией
начального и конечного состояний:
S = ν2 S0прод. – ν1 S0исх.
ν - число молей соответствующих веществ.
Для химической реакции типа:
ΔSр рассчитывается как:
ΔSр=cSºC+dSºD– aSºΑ– bSºB
24.
С учетом одновременного действия двухпротивоположных факторов движущей силой для
р-ций, протекающих при P,T=const, принята
( ) – ф-ция состояния,
называемая также изобарно-изотермич. потенциалом или свободной энергией.
В качестве критерия для определения
направления самопроизвольного протекания хим.
процессов (при р,Т=const) используется
G или G = G2 – G1.
В зав-сти от знака G возможны три случая.
25.
реакция термодинамически возможнаПри постоянной т-ре и давлении хим. р-ции
протекают самопроизвольно только в
направлении ум-ния энергии Гиббса в
системе ( G 0).
реакция ТД невозможна
ТД возможны как прямая, так и обр. р-ция
Это ТД условие установления химического
равновесия в реакционной системе.
26.
Энергия Гиббса связана с энтальпией, энтропиейи температурой:
.
Её изм-ние G:
.
При этом возможны четыре основных случая:
I. Если
,а
, то G < 0. Такие р-ции
ТД возможны при любой температуре.
II. Если
,а
, то всегда G > 0. Такие
реакции ТД невозможны при любых т-рах.
III. Если
и
, то реакция возможна
только при высоких т-рах, когда Н < T S .
IV. Если
и
, то реакция возможна при
низких температурах, когда Н > T S .
27.
Стандартная энергия Гиббса обр-ния в-ва( G0обр. 298) – изм-ние энергии Гиббса в р-ции обрния 1 моль соед-ния из соотв-щих простых в-в,
когда все участвующие в-ва нах-ся в станд. сост.,
а р-ция проходит при станд. усл-ях. (кДж/моль)
Стандартная энергия Гиббса
условно равна
.
обр-ния
Энергия Гиббса – ф-ция сост-я системы.
G реакции зависит только от природы, физ. или
агр. состояния реагентов и продуктов р-ции, их
кол-ва и не зависит от пути:
G = G0298 прод. G0298 реаг
28.
Стандартные термодинамические потенциалы образованиянекоторых химических веществ
Вещест- Состояво
ние
ВаО
к (крист)
ВаСО3
к
СН4
г (газ)
С6Н6 ж (жидк)
С
Графит
С
Алмаз
Н0298,
кДж
моль
-558,6
-1218,0
-74,9
82,9
0
1,8
S0298,
Дж
моль К
70,6
112,6
186,2
269,2
5,4
2,4
G0298,
кДж
моль
-528,4
-1138,8
-50,8
129,7
0
2,55



























 Химия
Химия