Похожие презентации:
Адсорбция из растворов на разных поверхностях раздела фаз
1.
АДСОРБЦИЯ ИЗ РАСТВОРОВНА РАЗНЫХ ПОВЕРХНОСТЯХ РАЗДЕЛА ФАЗ
2.
Адсорбция – самопроизвольноеконцентрирование вещества на поверхности раздела фаз
Удельная адсорбция (Г) –
избыточное количество вещества
на единичной площади поверхности раздела фаз
Γ
N N ' N"
s
[моль/м2]
N – общее число молей растворенного вещества
N', N" – число молей растворенного вещества в каждой фазе
s – площадь поверхности раздела фаз
3.
ТЕРМОДИНАМИКА АДСОРБЦИИРастворитель (1)
z
Растворенное вещество (2)
z
"
c1’’
+
0
-
"
c2’’
ГРП
c
+
ФПР 0
-
c
c1 ’
c2 ’
'
'
Г = Г1 + Г2
Эквимолекулярная поверхность
Г1 = 0
0
Г2
c z c' dz c z c' ' dz
2
2
2
0
2
4.
Определение величины адсорбции Г2c2 ” = 0
'
Г 2 с (s)
c
2
2 δ
c (S)
c2 '
2
Γ2 c
(S)
2
δ
Гексиловый спирт – вода:
= 0,7 нм
с2(S) =5,8.10-2 моль/л
6·10-6 моль/м2
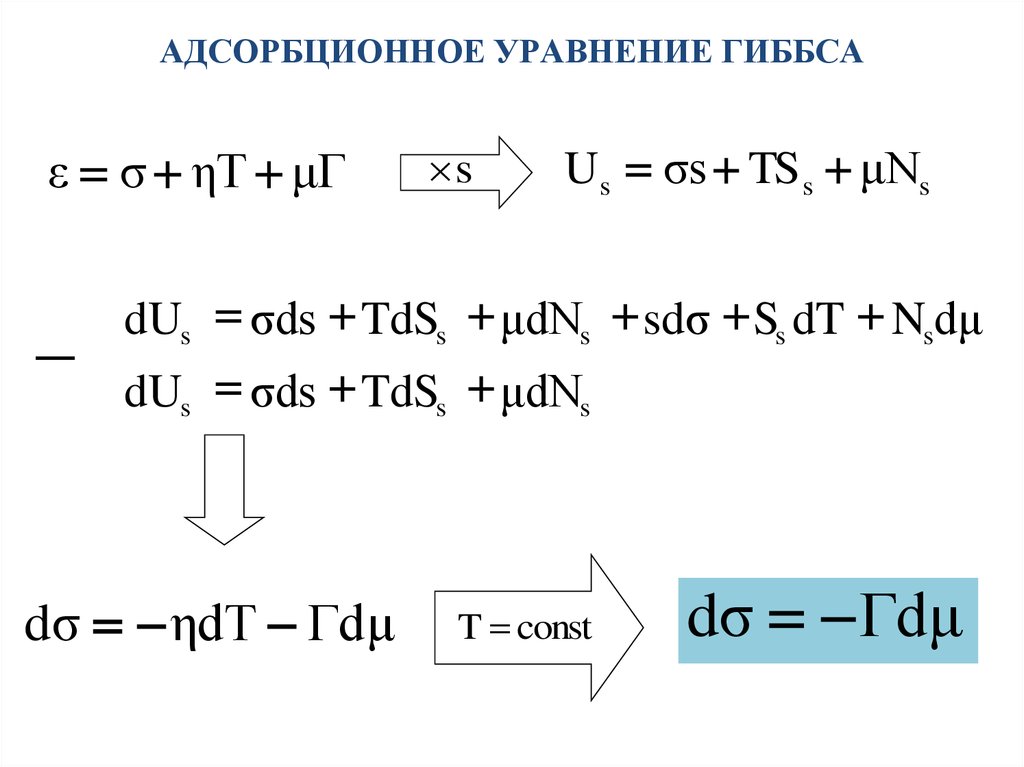
5. АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА
ε σ ηT μГs
Us σs TS s μNs
dUs σds TdSs μdNs sdσ Ss dT Nsdμ
dUs σds TdSs μdNs
dσ ηdT Гdμ
T const
dσ Гdμ
6. АДСОРБЦИОННОЕ УРАВНЕНИЕ ГИББСА
μ μ 0 RTln αcd αc
dμ RT
αc
при α = 1
c dσ
Γ
RT dc
7.
σσ
σ
σ0
σ0
σ0
d
>0
dc
c
Г<0
d
=0
dc
Г= 0
Отрицательная адсорбция
С(s) << C
Поверхностно-инактивные
вещества (ПИнВ)
Для воды:
Неорганические электролиты
(NaCl, KNO3, NaOH, H2SO4)
c
d
<0
dc
c
Г>0
Положительная адсорбция
С(s) >> C
Сахар
Поверхностно-активные
вещества (ПАВ)
Для воды:
Спирты, амины,
жирные кислоты, белки, липиды
8.
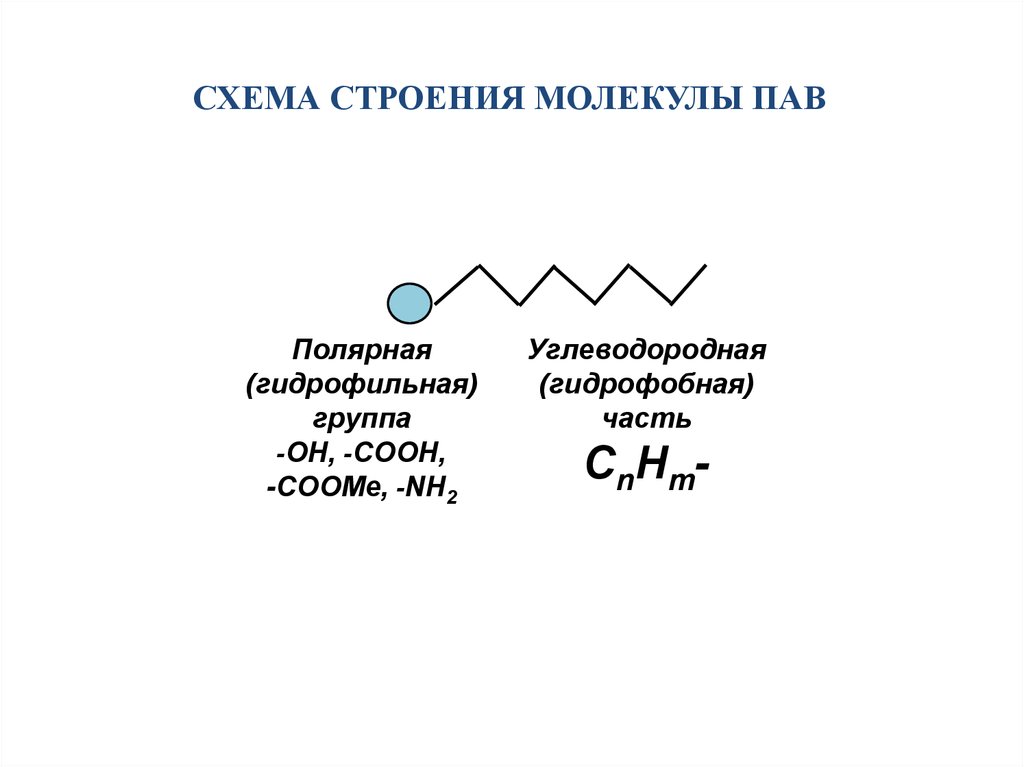
СХЕМА СТРОЕНИЯ МОЛЕКУЛЫ ПАВПолярная
(гидрофильная)
группа
-OH, -COOH,
-COOMe, -NH2
Углеводородная
(гидрофобная)
часть
СnHm-
9.
ЭНТРОПИЙНАЯ ПРИРОДА ПРОЦЕССА АДСОРБЦИИΔG = ΔH - TΔS < 0
ВОЗДУХ
H 2O
H2O + ПАВ
H 2O
10.
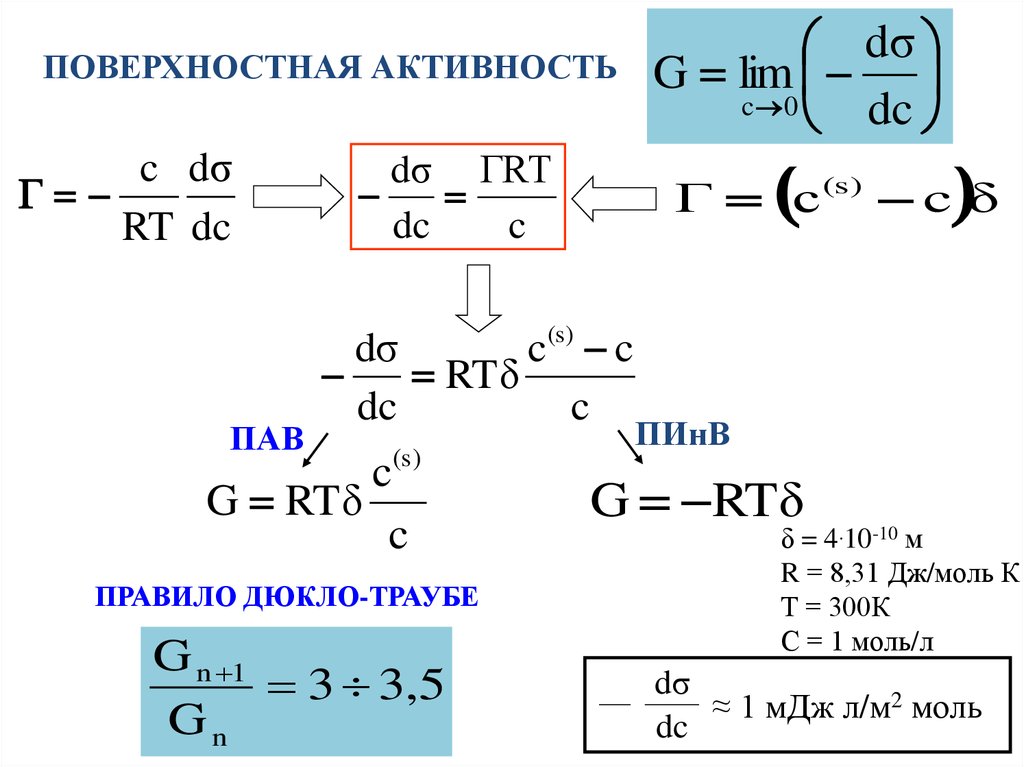
ПОВЕРХНОСТНАЯ АКТИВНОСТЬc dσ
RT dc
ПАВ
dσ ГRT
dc
c
ПРАВИЛО ДЮКЛО-ТРАУБЕ
G n 1
3 3,5
Gn
Г с(s) c δ
dσ
c(s) c
RTδ
dc
c
c(s)
G RTδ
c
dσ
G lim
c 0
dc
ПИнВ
G RTδ
δ = 4.10-10 м
R = 8,31 Дж/моль К
Т = 300К
С = 1 моль/л
dσ
≈ 1 мДж л/м2 моль
dc
11. УРАВНЕНИЕ ШИШКОВСКОГО
ИЗОТЕРМА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯσ
ПИнВ
σ0
(~72мДж/м2)
σПАВ
0
tgα = -dσ/dc= G
ПАВ
c
УРАВНЕНИЕ ШИШКОВСКОГО
σ(c) σ 0 bln Ac 1
12.
АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГОПри условии c < 1/A (Область Генри)
0 bAc
dσ
G Ab
dc
σ
σ0
n ПРАВИЛО ДЮКЛО-ТРАУБЕ
n+1 G n 1
n+2
Gn
3 3,5
с
c dσ c
Ab
Γ
G
c
RT dc RT
RT
13.
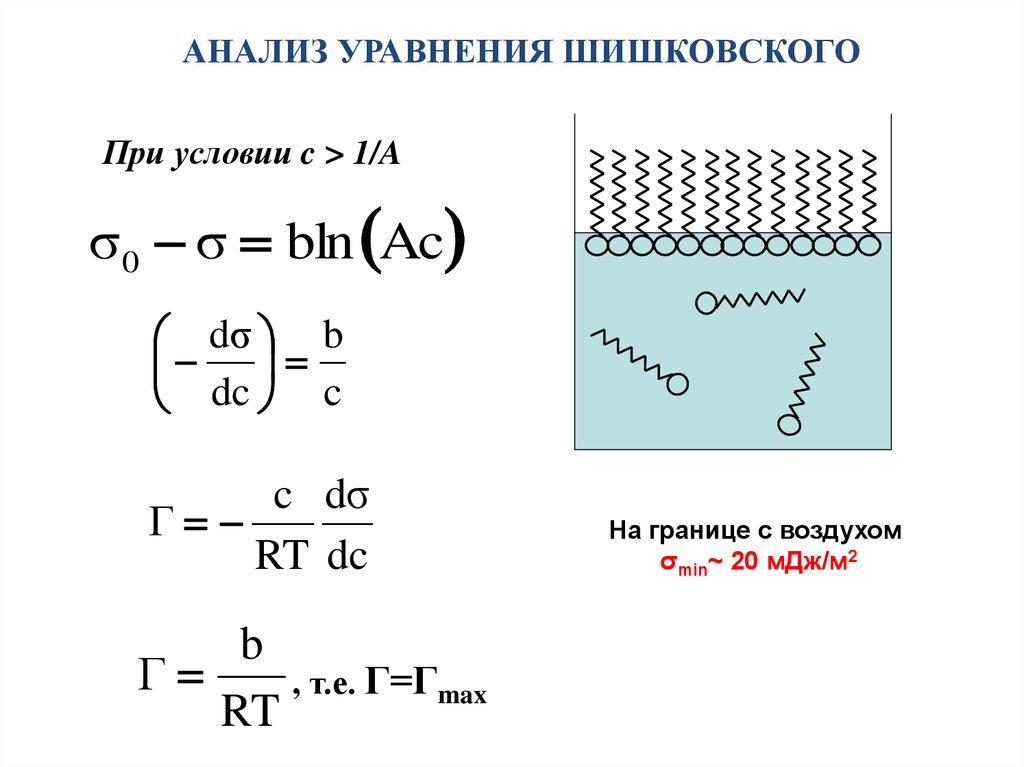
АНАЛИЗ УРАВНЕНИЯ ШИШКОВСКОГОПри условии c > 1/A
σ 0 σ bln Ac
dσ b
dc c
c dσ
Γ
RT dc
b
Г
, т.е. Г=Гmax
RT
На границе с воздухом
σmin~ 20 мДж/м2
14.
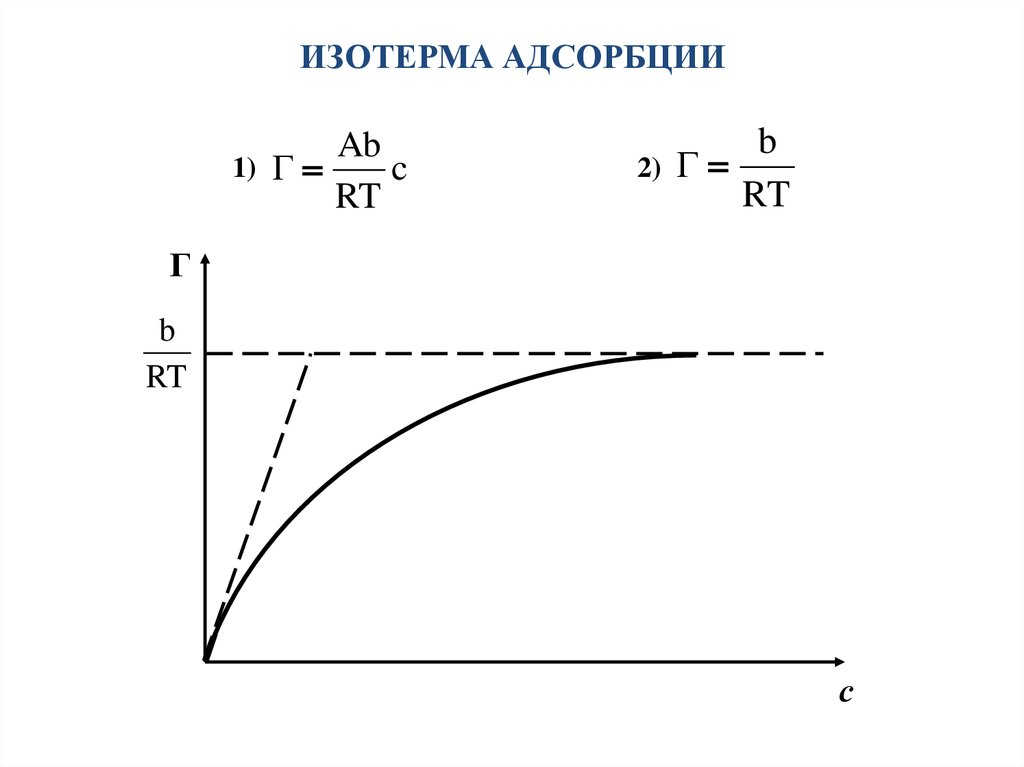
ИЗОТЕРМА АДСОРБЦИИ1)
Ab
Г
c
RT
2)
b
Г
RT
Г
b
RT
с
15.
ТЕОРИЯ МОНОМОЛЕКУЛЯРНОЙ АДСОРБЦИИУРАВНЕНИЕ ЛЕНГМЮРА
Γ Γ max
К равн c
1) C << 1/Кравн (область Генри)
Г = Гmax Кравн c
Г = Гmax/2
К равн c 1
3) C >> 1/ Кравн, Кравн c+1≈ Кравн c Г = Гmax
2) C = 1/ Кравн
Г
Г max
Адсорбционная активность
Гmax/2
k адс
K равн.
A
k дес
с
(Коэффициенты уравнения Шишковского: b = RTГmax; А = Кравн. )
1/A
16.
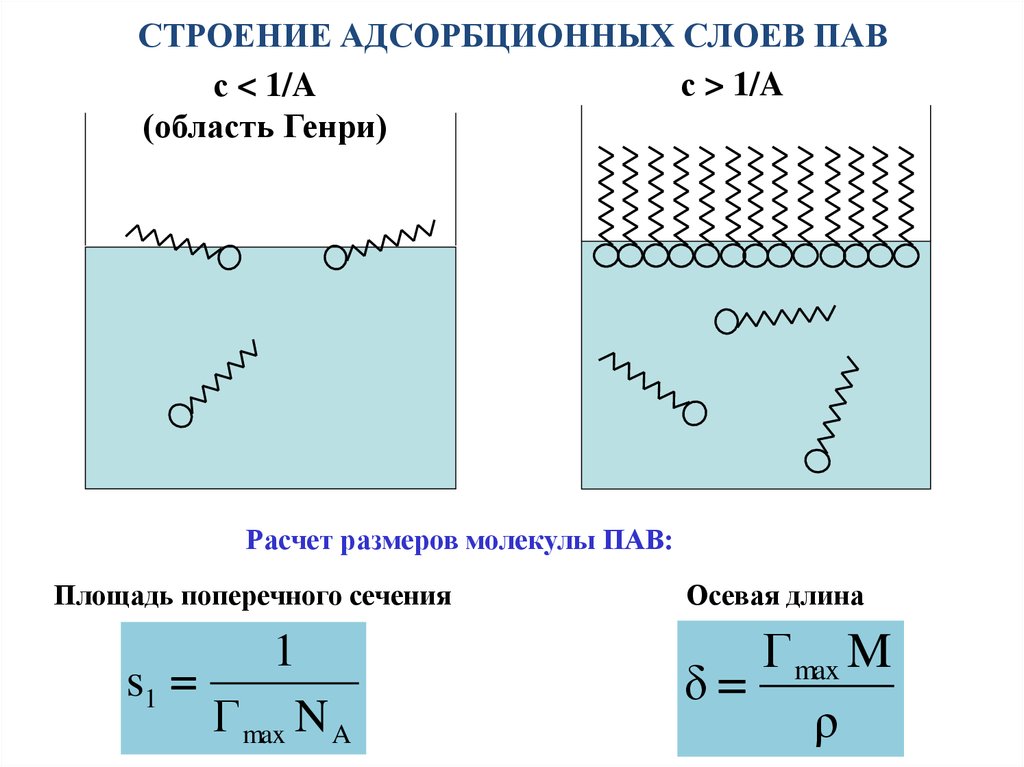
СТРОЕНИЕ АДСОРБЦИОННЫХ СЛОЕВ ПАВс > 1/A
с < 1/A
(область Генри)
Расчет размеров молекулы ПАВ:
Площадь поперечного сечения
1
s1
Г max N A
Осевая длина
Г max M
δ
ρ
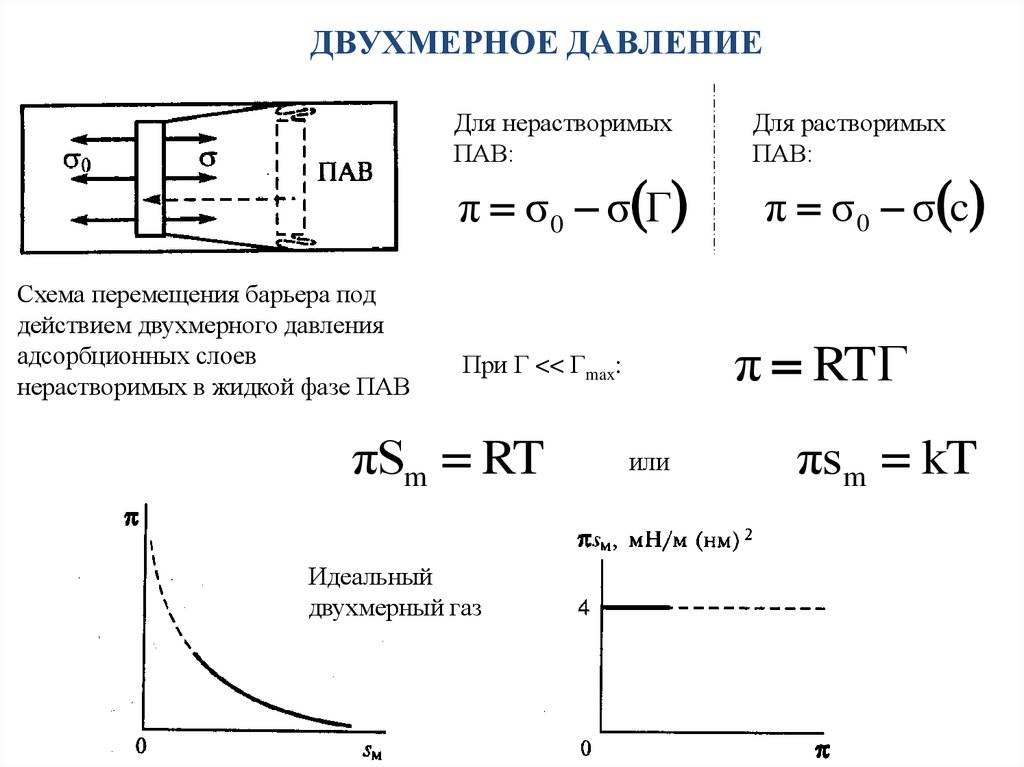
17. ДВУХМЕРНОЕ ДАВЛЕНИЕ
Для нерастворимыхПАВ:
π σ 0 σ Γ
Схема перемещения барьера под
действием двухмерного давления
адсорбционных слоев
нерастворимых в жидкой фазе ПАВ
Идеальный
двухмерный газ
π σ 0 σ c
π RTΓ
При Г << Гmax:
πSm RT
Для растворимых
ПАВ:
или
πs m kT
18. ВАННА ЛЕНГМЮРА
Учет площади молекул дает:Схема прибора Ленгмюра для
измерения адсорбционных слоев
нерастворимых ПАВ
sm s1 kT
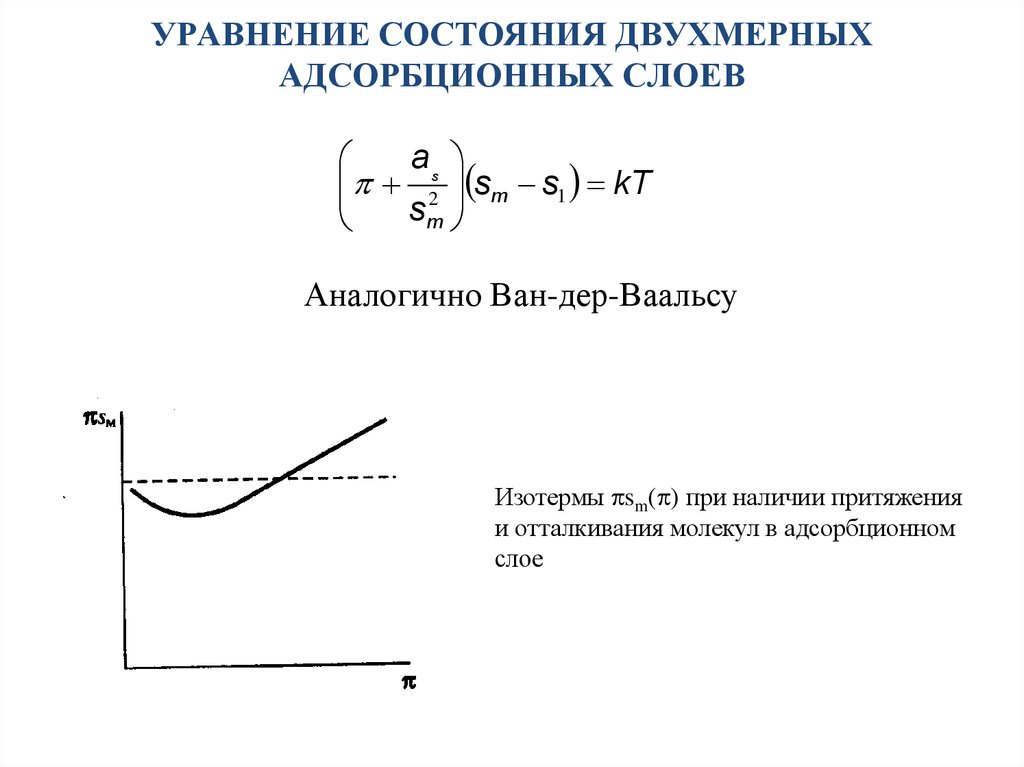
19. УРАВНЕНИЕ СОСТОЯНИЯ ДВУХМЕРНЫХ АДСОРБЦИОННЫХ СЛОЕВ
as2 sm s1 kT
sm
Аналогично Ван-дер-Ваальсу
Изотермы sm( ) при наличии притяжения
и отталкивания молекул в адсорбционном
слое
20. ТИПЫ ПОВЕРХНОСТНЫХ ПЛЕНОК
π ~ 20-50 мН/мπ, мН/м
S
Твердые S-пленки s1 0,206 нм2
Жидкие L2- пленки s1 0,22 нм2
L2
Жидкорастянутые L1-пленки s1 0,5-0,22 нм2
L1
0,2
0,25
π ~ 0,01 мН/м
L1-G
0,50
s1, нм2/молекула
G
10,0
Газообразные G-пленки
21. СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2-[[[(2,2-dipentadecyl-1,3-dioxolan-4-yl)methoxy]hydroxyphosphinyl]oxy]-N,N,N-trimethyl-, inner salt
СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА:Ethanaminium, 2-[[[(2,2-dipentadecyl-1,3-dioxolan-4yl)methoxy]hydroxyphosphinyl]oxy]-N,N,N-trimethyl-, inner salt
22. ФАЗОВЫЙ ПЕРЕХОД В МОНОСЛОЕ СМЕСИ ЛИПИДОВ DPPC:DPPG 7:1
ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯМОНОСЛОЕВ:
1- ЖИРНОЙ КИСЛОТЫ С
ОДНИМ УГЛЕВОДОРОДНЫМ РАДИКАЛОМ
2 - ФОСФОЛИПИДА С
ДВУМЯ УГЛЕВОДОРОДНЫМИ РАДИКАЛАМИ
ФАЗОВЫЙ ПЕРЕХОД В
МОНОСЛОЕ СМЕСИ
ЛИПИДОВ DPPC:DPPG 7:1
π, мН/м
1
2
S
S
L2
L2-L1
L2
L1
G
s1 ,
Å2
G
Флуоресцентная микроскопия
23.
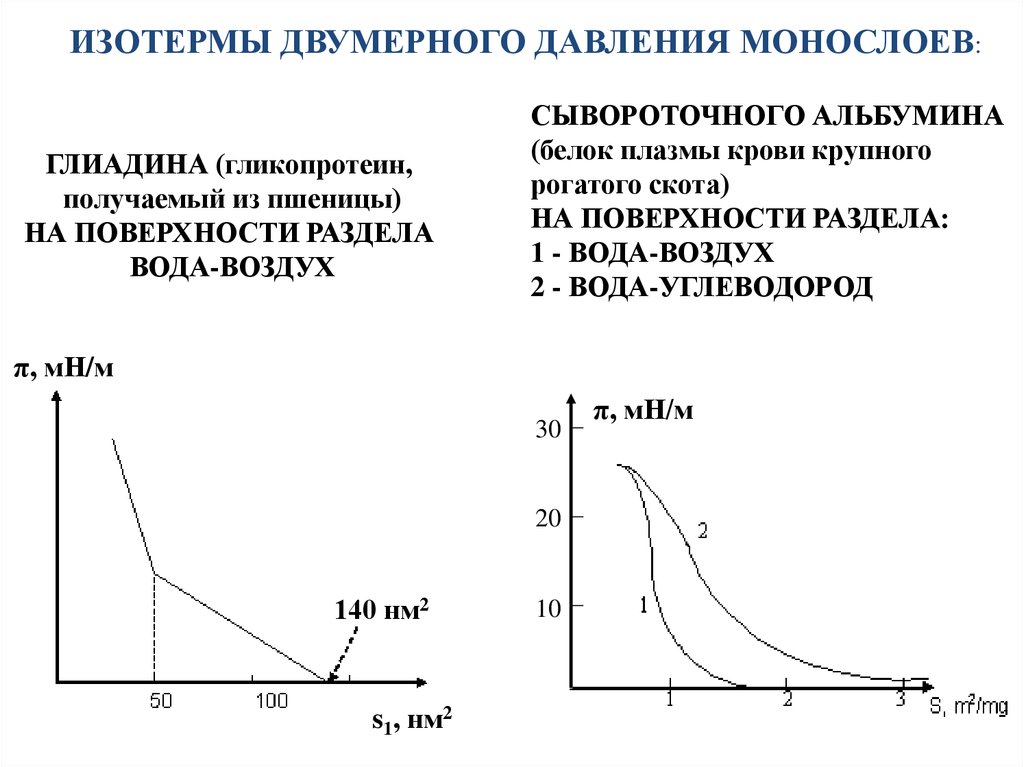
ИЗОТЕРМЫ ДВУМЕРНОГО ДАВЛЕНИЯ МОНОСЛОЕВ:ГЛИАДИНА (гликопротеин,
получаемый из пшеницы)
НА ПОВЕРХНОСТИ РАЗДЕЛА
ВОДА-ВОЗДУХ
СЫВОРОТОЧНОГО АЛЬБУМИНА
(белок плазмы крови крупного
рогатого скота)
НА ПОВЕРХНОСТИ РАЗДЕЛА:
1 - ВОДА-ВОЗДУХ
2 - ВОДА-УГЛЕВОДОРОД
π, мН/м
30
20
140 нм2
s1, нм2
10
π, мН/м
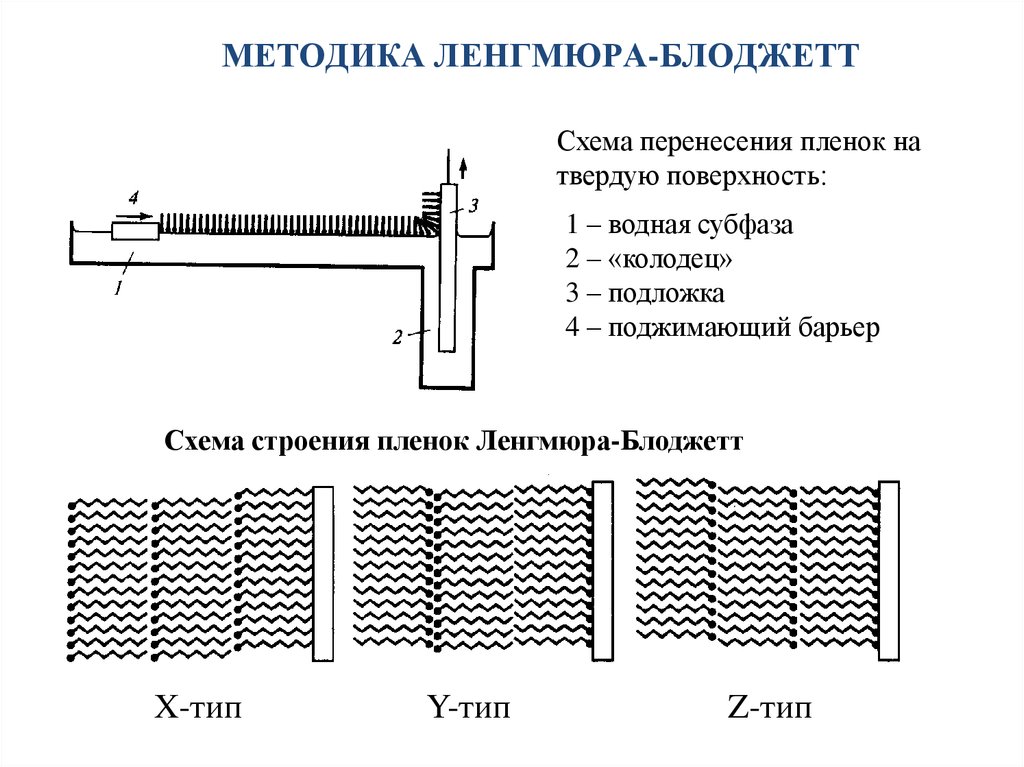
24. МЕТОДИКА ЛЕНГМЮРА-БЛОДЖЕТТ
Схема перенесения пленок натвердую поверхность:
1 – водная субфаза
2 – «колодец»
3 – подложка
4 – поджимающий барьер
Схема строения пленок Ленгмюра-Блоджетт
X-тип
Y-тип
Z-тип
25.
АДСОРБЦИЯНА ГРАНИЦЕ ДВУХ КОНДЕНСИРОВАННЫХ ФАЗ
Правило уравнивания полярностей Ребиндера:
Для границы 2-х конденсированных фаз поверхностно-активным
является вещество, имеющее промежуточную полярность по
сравнению с конденсированными фазами. Его молекулы
размещаются на границе 2-х конденсированных фаз таким образом,
чтобы снизить разность полярностей, существующую между
контактирующими фазами.
ОСОБЕННОСТИ АДСОРБЦИИ
НА ГРАНИЦЕ ДВУХ НЕСМЕШИВАЮЩИХСЯ ЖИДКОСТЕЙ
1. Область Генри:
Масло
2. На границе с неполярной жидкостью σmin~ 1
мДж/м2, но может быть и 0,01- 0,1 мДж/м2
3. Выход из воды – энтропийная природа
адсорбции; выход из масла – энтальпийная.
Вода
4. Правило Дюкло-Траубе работает при выходе из
воды, не работает при выходе из масла
26.
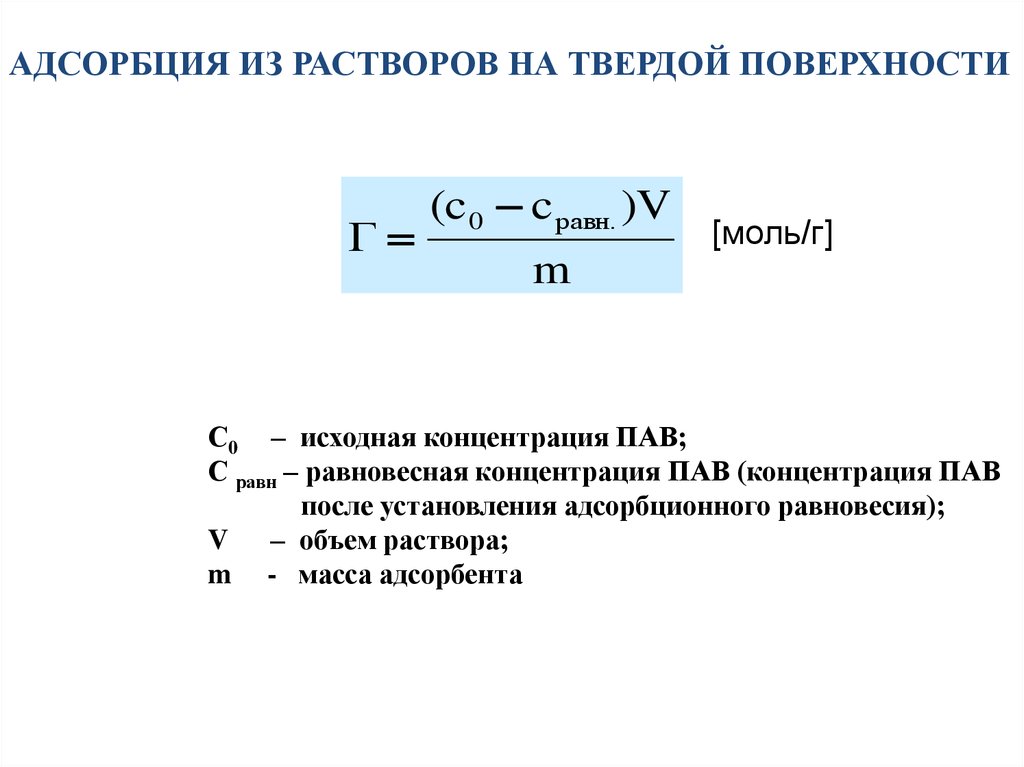
АДСОРБЦИЯ ИЗ РАСТВОРОВ НА ТВЕРДОЙ ПОВЕРХНОСТИΓ
(c 0 c равн. )V
[моль/г]
m
С0 – исходная концентрация ПАВ;
С равн – равновесная концентрация ПАВ (концентрация ПАВ
после установления адсорбционного равновесия);
V – объем раствора;
m - масса адсорбента
27.
АДСОРБЦИЯ НА ПОВЕРХНОСТИ ТВЕРДОГО ТЕЛАФизическая адсорбция
Б
А
Al2O3
C
Масло
Вода
Вода
Химическая адсорбция
В
Вода
Al2O3
УПРАВЛЕНИЕ СМАЧИВАНИЕМ С ПОМОЩЬЮ ПАВ












![СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2-[[[(2,2-dipentadecyl-1,3-dioxolan-4-yl)methoxy]hydroxyphosphinyl]oxy]-N,N,N-trimethyl-, inner salt СТРУКТУРНАЯ ФОРМУЛА ФОСФОХОЛИНА: Ethanaminium, 2-[[[(2,2-dipentadecyl-1,3-dioxolan-4-yl)methoxy]hydroxyphosphinyl]oxy]-N,N,N-trimethyl-, inner salt](https://cf.ppt-online.org/files/slide/q/QMiyGFvPVLpACxkREur75TNOgUJh8YdX2ecKq6/slide-20.jpg)



 Физика
Физика








