Похожие презентации:
Поверхностные явления. Лекция 15
1. Лекция 15
Поверхностныеявления.
Адсорбция
2.
Тончайшиймономолекулярный слой,
расположенный на границе
раздела двух фаз,
накапливает огромный
запас свободной
поверхностной энергии
(Gs).
3.
Поверхностное натяжение,адсорбция, адгезия и другие
процессы, протекающие на
границе раздела двух фаз,
называются поверхностными
явлениями.
4.
Они осуществляютсясамопроизвольно за
счет свободной
поверхностной
энергии.
5.
Поверхностные явленияиграют важную роль в
•дыхании,
•пищеварении,
•экскреции.
6.
Они протекают in vivo наразвитых поверхностях
раздела:
• поверхность кожи – 1,5 м2
• эритроцитов – 3000 м2
• альвеол – 1000 м
2
7. План
15.1 Поверхностная энергияи поверхностное натяжение
15.2 Адсорбция и ее виды
15.3 Адсорбция на границе
жидкость-газ
8.
15.1Энергетическоесостояние молекул
вещества в межфазном
поверхностном слое и в
глубине фазы
различно.
9.
Рассмотримсостояние молекул в
однокомпонентной
двухфазной системе:
вода – водяной пар.
10.
На молекулу воды,находящуюся в глубине фазы,
действуют силы
межмолекулярного
взаимодействия (f1), причем
их равнодействующая равна
нулю вследствие симметрии
силового поля.
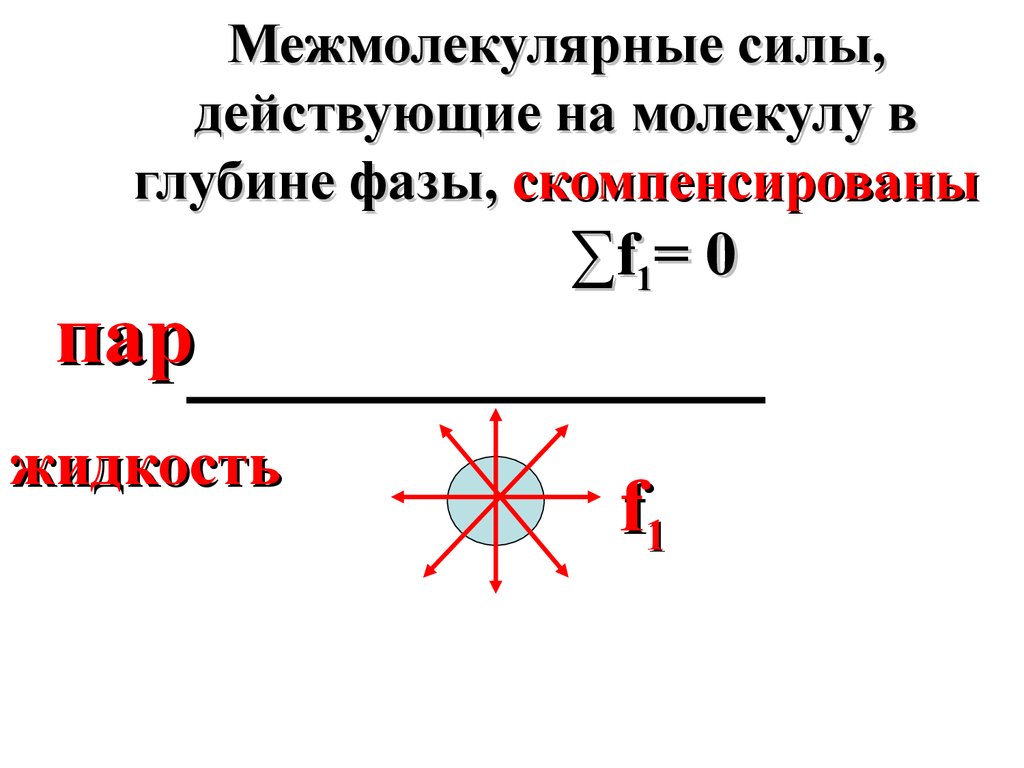
11.
Межмолекулярные силы,действующие на молекулу в
глубине фазы, скомпенсированы
пар
жидкость
∑f1= 0
f1
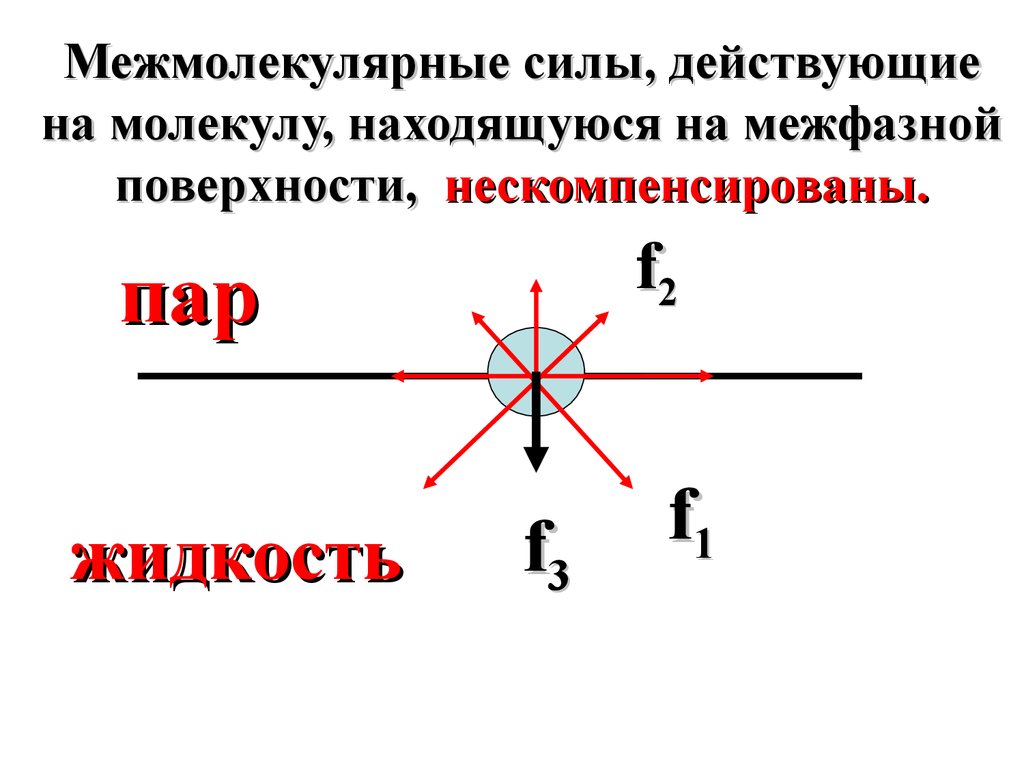
12.
Молекула на границе разделафаз в большей степени
испытывает действие
межмолекулярных сил со
стороны жидкой фазы (f1), чем
со стороны газообразной (f2).
Результирующий вектор силы
(f3) направлен внутрь жидкости.
13.
Межмолекулярные силы, действующиена молекулу, находящуюся на межфазной
поверхности, нескомпенсированы.
f2
пар
жидкость
f3
f1
14.
Сила f3 создает внутреннее(межмолекулярное) давление
жидкости, которое для воды
2
составляет 14 000 атм/см .
Межмолекулярное давлениеэто причина того, что
жидкости практически
несжимаемы.
15.
Вследствиенескомпенсированности сил
межмолекулярного
взаимодействия,
поверхностный слой имеет
избыточную свободную
энергию (по сравнению с
объемом жидкости):
G s = σ× S
16.
где S – площадь2
поверхности раздела фаз, м
σ – коэффициент
пропорциональности,
называемый
поверхностным
натяжением.
17.
Gsσ=
Дж
,
S
Н
=
м
м
Поверхностное натяжение
– это поверхностная энергия
единицы площади
поверхности раздела фаз.
2
18.
Поверхностноенатяжение – важная
характеристика
жидкостей; оно зависит
а) от
температуры,
б) от полярности
19.
С увеличениемтемпературы
поверхностное натяжение
жидкостей уменьшается,
т.к. разрывается часть
связей межмолекулярного
взаимодействия.
20.
Чем выше полярностьжидкости, тем больше ее
поверхностное
натяжение, т.к. с
увеличением полярности
возрастают силы
межмолекулярного
взаимодействия.
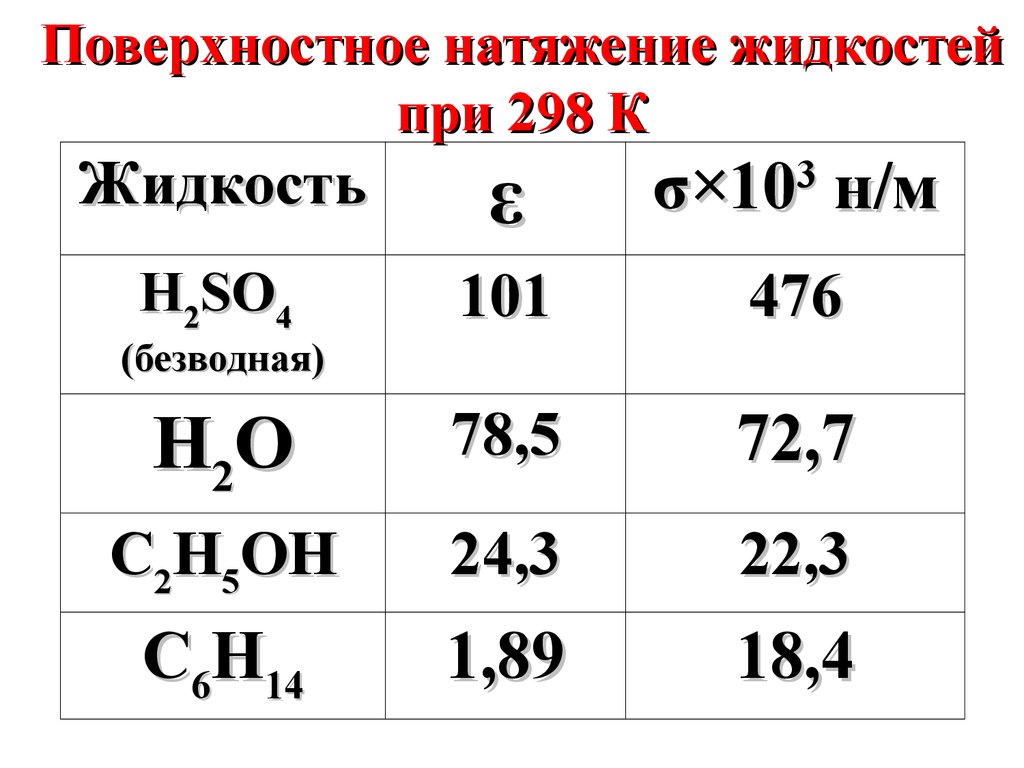
21.
Поверхностное натяжение жидкостейпри 298 К
Жидкость
ε
σ×103 н/м
H2SO4
101
476
H2O
78,5
72,7
C2H5OH
24,3
22,3
C6H14
1,89
18,4
(безводная)
22.
Поверхностноенатяжение – важная
характеристика
биологических
жидкостей.
В норме σ крови равно
-3
45,4×10 н/м.
23.
Измерениеповерхностного
натяжения крови важный
диагностический
тест.
24.
Изменения σ сыворотки кровисвидетельствует о наличии
онкологических заболеваний,
анафилактическом шоке и
других заболеваниях. Кроме
того, поверхностное натяжение
уменьшается с возрастом.
25.
Наиболее принятымметодом определения
поверхностного
натяжения является
сталогмометрический
метод.
26.
Согласно второмузакону
термодинамики Gs →
min. Это стремление
реализуется:
а) за счет уменьшения площади
поверхности (стремление жидкости
принять форму шара, слияние
капель);
27.
б) за счет адсорбции,т.к. при адсорбции
уменьшается
поверхностное
натяжение
жидкостей.
28.
15.2. Адсорбциейназывается концентрирование
какого-либо вещества в
поверхностном слое в
результате самопроизвольного
перехода его из объема фазы.
29.
Молекулы газаАктивированный уголь
30.
При адсорбцииразличают два
понятия:
• Адсорбент,
• Адсорбат.
31.
Адсорбент – вещество, наповерхности которого
идет адсорбция.
Адсорбат – вещество,
которое концентрируется
на поверхности
адсорбента.
32.
Адсорбция (Г) выражается в2
2
г/м или моль/м и
рассчитывается по формулам:
m
Г=
S
ν
Г=
S
m – масса адсорбата, г
ν – количество адсорбата, моль
S – площадь поверхности
33.
В зависимости отприроды сил,
действующих между
адсорбентом и
адсорбатом, различают
физическую и
химическую адсорбцию.
34.
Физическая адсорбцияобусловлена
межмолекулярным
взаимодействием (силы
Ван-дер-Ваальса). Энергия
этих взаимодействий
невелика и составляет
4-40 кДж/моль.
35.
Для физической адсорбциихарактерны:
• обратимость: одновременно с
адсорбцией протекает десорбция,
• неспецифичность: она
подчиняется правилу «подобное
растворяется в подобном»,
• экзотермичность (ΔадсН < О)
36.
В соответствии с принципомЛе Шателье, протеканию
физической адсорбции
способствует:
• понижение температуры,
• увеличение концентрации
адсорбата,
• повышение давления в системе
(при адсорбции газа или пара).
37.
Химическая адсорбция(хемосорбция)
осуществляется при
взаимодействии
адсорбента с адсорбатом с
образованием химической
(ковалентной) связи.
38.
Энергия связи прихемосорбции составляет
40-400 кДж/моль, что
делает ее практически
необратимой,
специфичной и
локализованной.
39.
Повышениетемпературы усиливает
хемосорбцию,
что приводит к
большому связыванию
адсорбата.
40.
По характеру межфазнойповерхности
различают адсорбцию, протекающую
на границе раздела:
А) жидкость/газ,
Б) жидкость/жидкость,
В) твердое тело/жидкость,
Г) твердое тело/газ
41.
15.3 При растворении в водекакого-либо вещества может
наблюдаться:
А) понижение ее
поверхностного натяжения.
Такие вещества называются
поверхностно-активными
(ПАВ);
42.
Б) повышение ееповерхностного натяжения.
Такие вещества
называются
поверхностно-инактивными
(ПИВ); к ним относятся
неорганические кислоты,
основания и соли;
43.
В) поверхностное натяжениежидкости не изменяется.
Такие вещества называются
поверхностнонеактивными (ПНВ).
К ним относятся глюкоза,
сахароза и другие сахара.
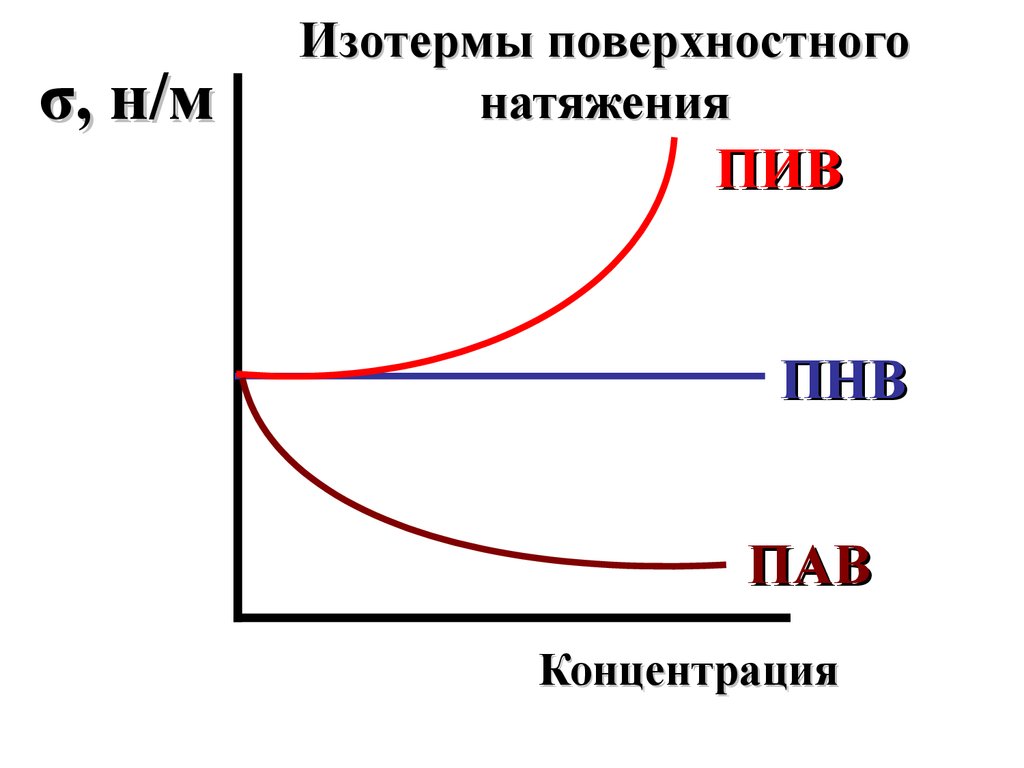
44.
σ, н/мИзотермы поверхностного
натяжения
ПИВ
ПНВ
ПАВ
Концентрация
45.
Поверхностноактивными (ПАВ)называются вещества,
уменьшающие
поверхностное
натяжение жидкостей.
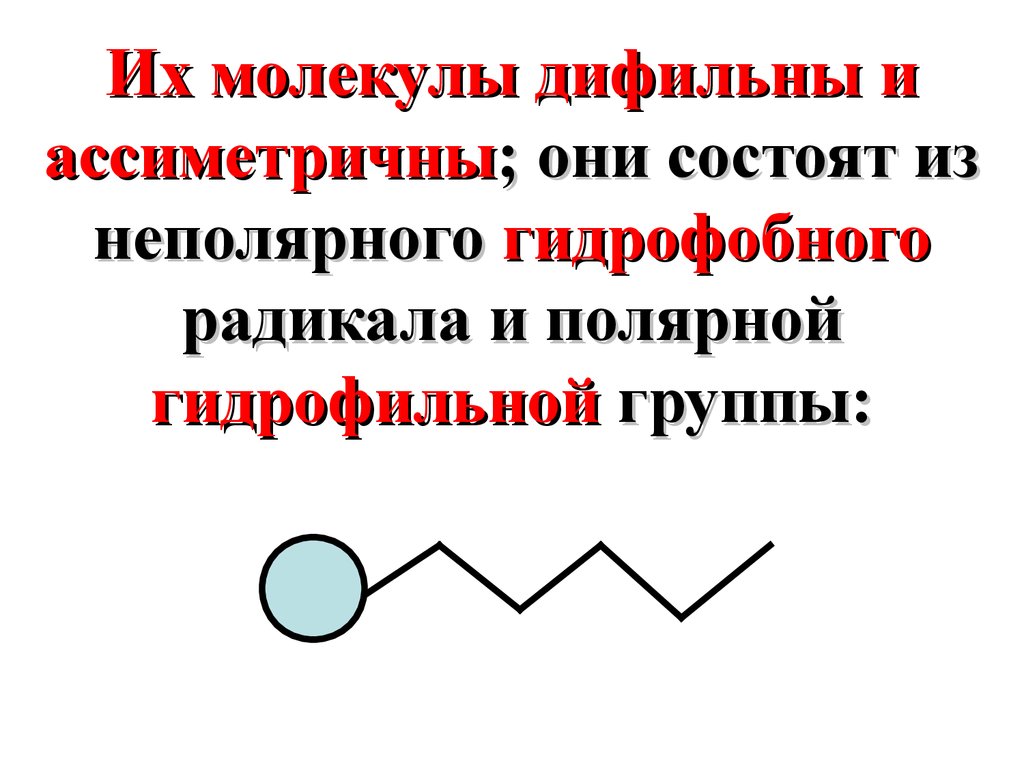
46.
Их молекулы дифильны иассиметричны; они состоят из
неполярного гидрофобного
радикала и полярной
гидрофильной группы:
47.
Классификация ПАВПАВ
Электролиты
(ионогенные)
Неэлектролиты
(неионогенные)
48.
Ионогенные ПАВделятся на:
1)Катионоактивные:
Соли и гидроксиды
алкиламмония
49.
Например,цетилтриметил аммоний
бромид, используемый
как антисептик
CH3- (CH2)15N (CH3)3 Br
50.
2) Аниононоактивные:• Соли карбоновых кислот
• R-COOMe,
• Соли сульфокислот
• R-SO3Me
51.
К неионогенным ПАВ относятся:•Карбоновые кислоты R-COOH,
• Сульфокислоты
R - SO3H,
• Спирты
R - OH,
• Тиолы
R - SH,
• Амины
R – NH2
52.
Поверхностно-активнымиявляются многие
биоактивные соединения:
• Жиры,
• Фосфолипиды
• Желчные кислоты
53.
В соответствии с правилом«Подобное стремится к
подобному», гидрофобные
радикалы направлены в
неполярную фазу (воздух), а
гидрофильные группы – в
полярную (вода). В результате
ПАВы концентрируются на
границе раздела двух фаз.
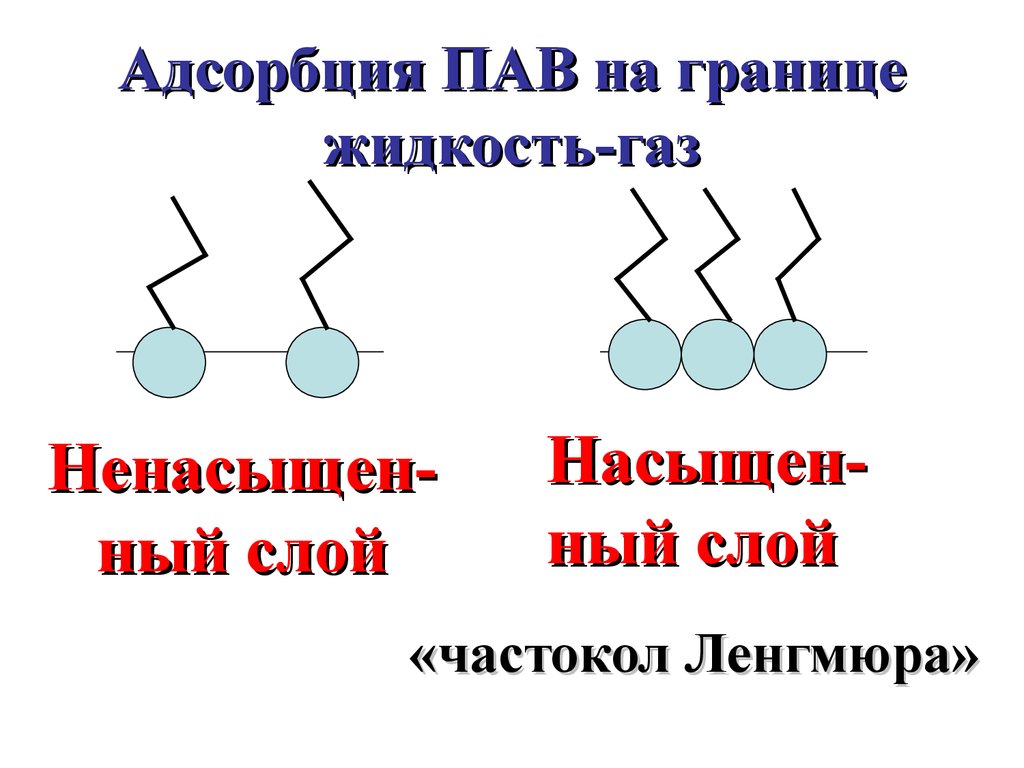
54.
Адсорбция ПАВ на границежидкость-газ
Ненасыщенный слой
Насыщенный слой
«частокол Ленгмюра»
55.
Поскольку молекулыПАВ менее полярны,
чем молекулы воды,
силы поверхностного
натяжения в
поверхностном слое
уменьшаются.
56.
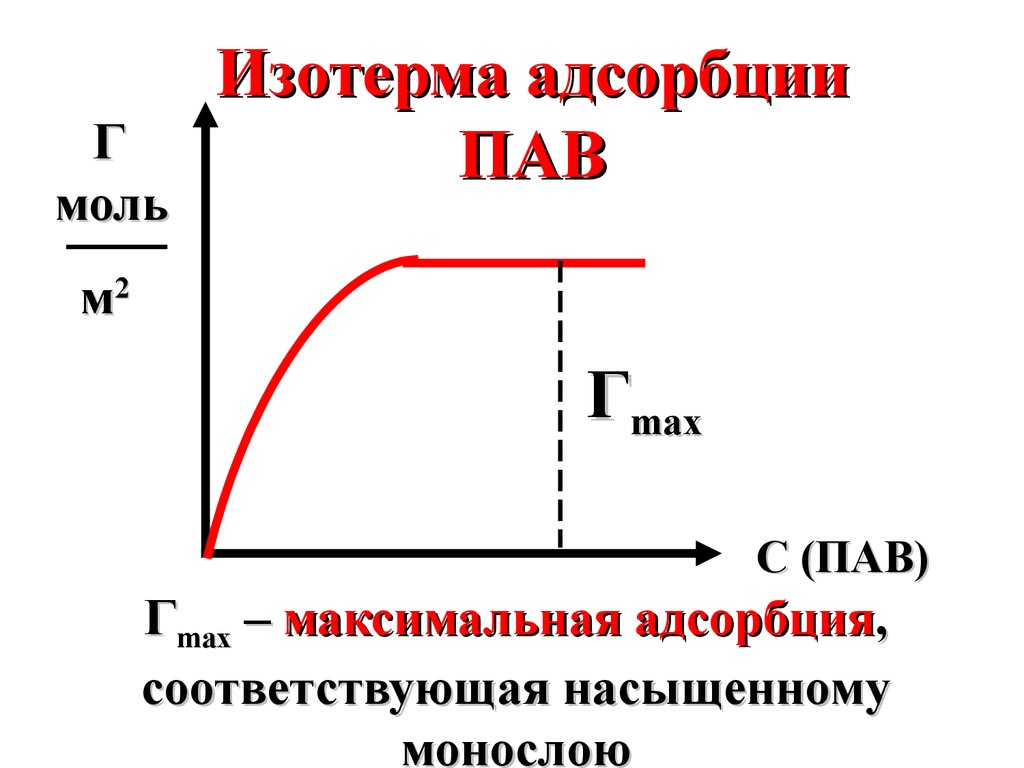
Гмоль
Изотерма адсорбции
ПАВ
м2
Гmax
С (ПАВ)
Гmax – максимальная адсорбция,
соответствующая насыщенному
монослою
57.
Зная Гmax можно рассчитатьа) длину молекулы ПАВ (ℓ)
ℓ=
Г max M
ρ
ρ – плотность ПАВ,
М- молярная масса ПАВ
58.
б)площадь,
занимаемую
молекулой ПАВ на границе
раздела фаз (s):
s=
1
Г max NA
где NA – число Авогадро
59.
Важнейшей характеристикойПАВ является их
поверхностная активность (g):
g=
Δσ
ΔC
где Δσ – уменьшение
поверхностного натяжения жидкости
при увеличении концентрации ПАВ
на ΔС
60.
Правило Дюкло-Траубе(1888): с увеличением длины
гидрофобного радикала на
группу -CH2- поверхностная
активность ПАВ возрастает
в 3-3,5 раза при одинаковой
молярной концентрации.
61.
Правило выполняетсядля членов одного
гомологического ряда:
спиртов, аминов,
карбоновых кислот и
т.д.
62.
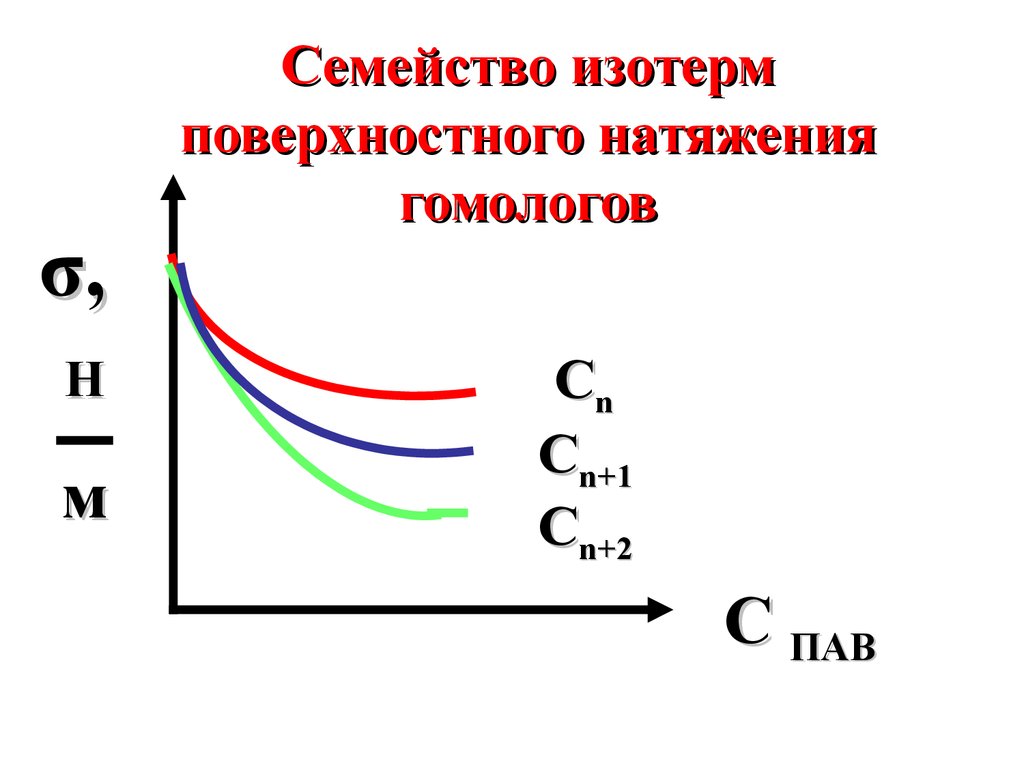
σ,Н
м
Семейство изотерм
поверхностного натяжения
гомологов
Сn
Сn+1
Сn+2
C ПАВ
63.
Семейство изотерм адсорбциигомологов
Г
моль
м2
Сn+2
Сn+1
Сn
С ПАВ
64.
Зависимость адсорбции ПАВ от ихконцентрации в растворе
описывается уравнением Гиббса
(1878):
Г=
dσ C ПАВ
×
RT
dс
65.
Влияние концентрации ПАВ наповерхностное натяжение растворов
описывается уравнением
Шишковского (1909):
σ = σо – а ln (1 + b ×cПАВ)
где a и b – параметры уравнения
(табл.),
σ – поверхностное натяжение
раствора, σо -поверхностное
натяжение растворителя
66.
Для расчета адсорбцииПАВ используется
объединенное уравнение
Гиббса-Шишковского:
Г=
a
RT
b c
×
1 + b c
67.
Применение ПАВ1)Как моющие средства:
молекулы ПАВ адсорбируются
на поверхности жирного
пятна, образуя гидрофильную
систему, хорошо растворимую
в воде.
68.
Жир69.
2) Как антисептики вхирургии:
антимикробная активность
ионогенных ПАВ значительно
выше (до 300 раз) активности
традиционно используемого
фенола.
70.
Обеззараживающее действиеПАВ объясняют их влиянием
на проницаемость клеточных
мембран микроорганизмов, а
также ингибирующим
действием на
ферментативные системы
бактерий.
71.
3) Для производствалипосом
Липосома (греч. «липос» жир, «сома» - тело) – это
надмолекулярная структура,
состоящая из бислоя
фосфолипидов и находящегося
между ними раствора.
72.
73.
Липосомы применяются длянаправленной доставки
лекарственного препарата к
пораженным органам и тканям.
74.
Липосомы могут переноситьширокий круг
фармакологически активных
веществ: противоопухолевые и
противомикробные препараты,
гормоны, ферменты, вакцины, а
также дополнительные
источники энергии для клетки и
генетический материал.
75.
При этомпрепарат не
отравляет
здоровые ткани
человека.
76.
Как носители лекарств,наиболее широкое применение
липосомы получили в
онкологии и пульмонологии
(лечение туберкулеза), т.е. в тех
областях медицины, в которых
используются наиболее
токсичные лекарственные
вещества.
77.
Благодаримза
внимание!!!












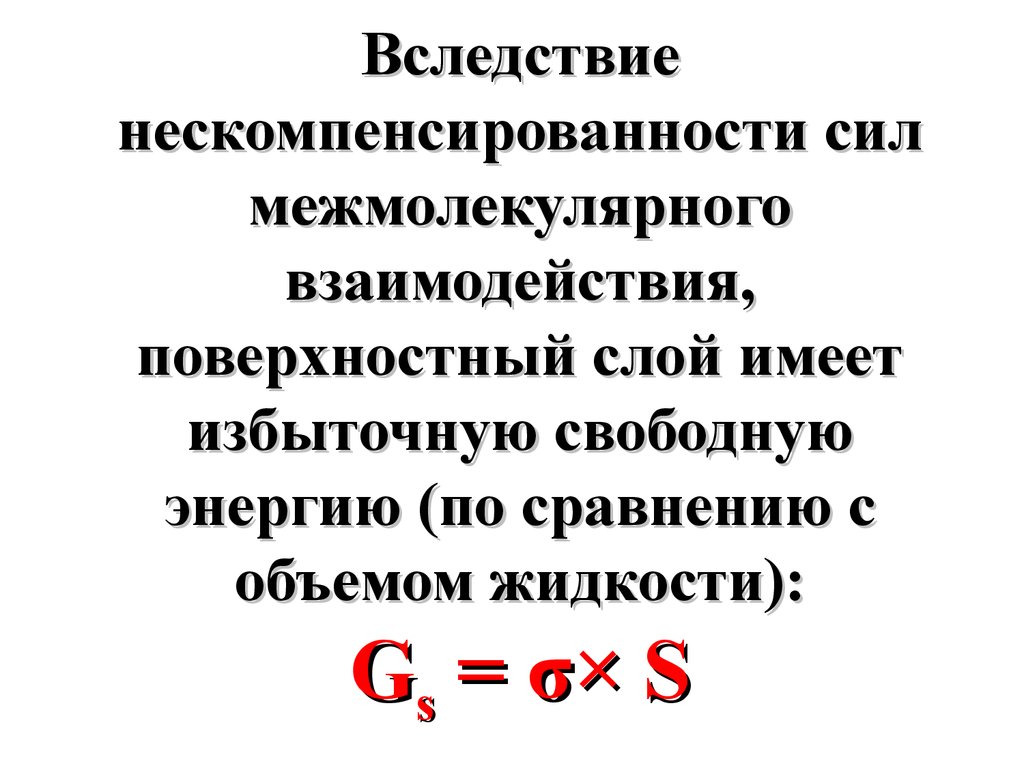










































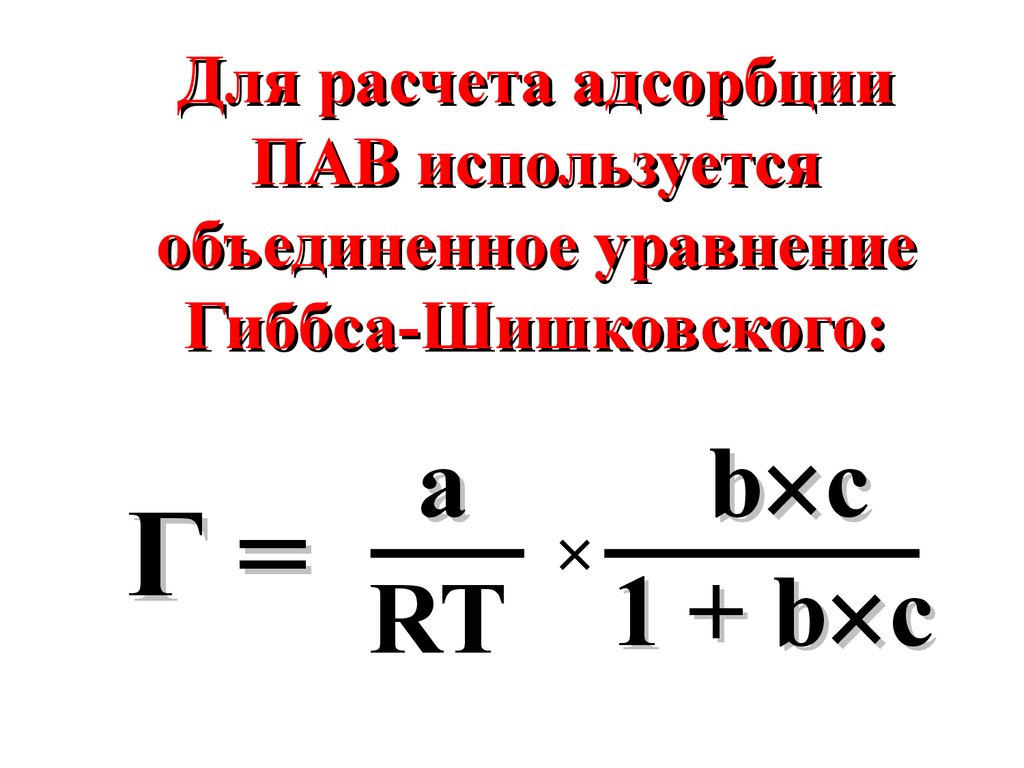











 Физика
Физика Химия
Химия








