Похожие презентации:
Ацетилен
1.
Ацетилен2.
В 1836 году получилацетилен, действуя
на карбид кальция
водой.
Э. Дэви
Ацетилен, или
этин
НС ≡ СН
С2Н2
В 1860 году дал
название
ацетилену.
П. Э. Бертло
180°
3.
Физические свойства ацетиленаАцетилен при обычных условиях представляет собой
бесцветный газ.
Смесь ацетилена с воздухом взрывается от искры.
Ацетилен плохо растворяется в воде.
Ацетилен хорошо растворяется в ацетоне: в одном объёме
ацетона при обычных условиях растворяется 25 объёмов
ацетилена.
4.
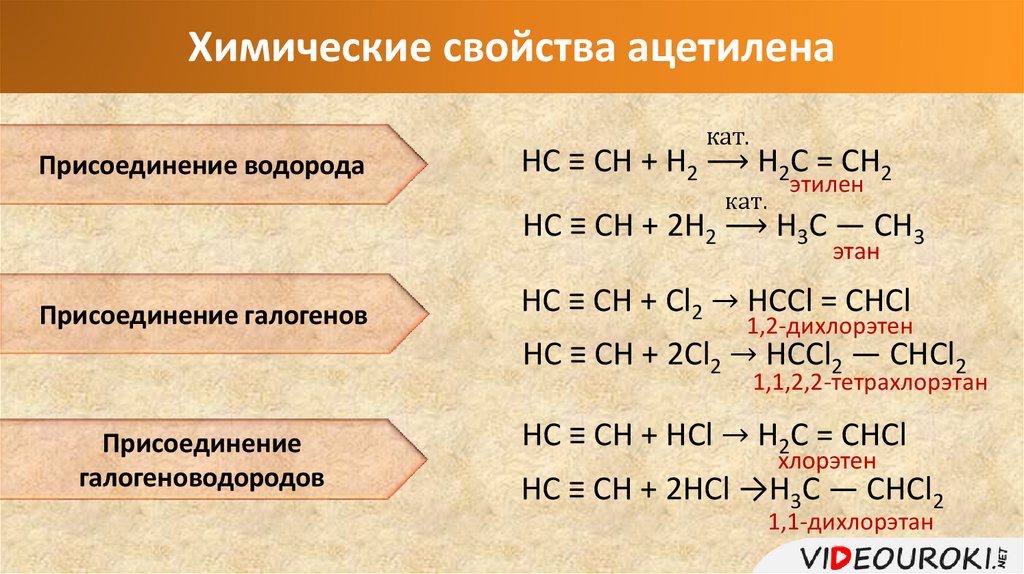
Химические свойства ацетиленаПрисоединение водорода
НС ≡ СН + Н2
кат.
НС ≡ СН + 2Н2
Присоединение галогенов
Н2С = СН2
кат.
этилен
Н3С ― СН3
этан
НС ≡ СН + Cl2 → НСCl = СНCl
1,2-дихлорэтен
НС ≡ СН + 2Cl2 → НСCl2 ― СНCl2
1,1,2,2-тетрахлорэтан
Присоединение
галогеноводородов
НС ≡ СН + НCl → Н2C = СНCl
хлорэтен
НС ≡ СН + 2НCl →Н3С ― СНCl2
1,1-дихлорэтан
5.
Реакция горения2С2Н2 + 5О2 → 4СО2↑ + 2Н2О
6.
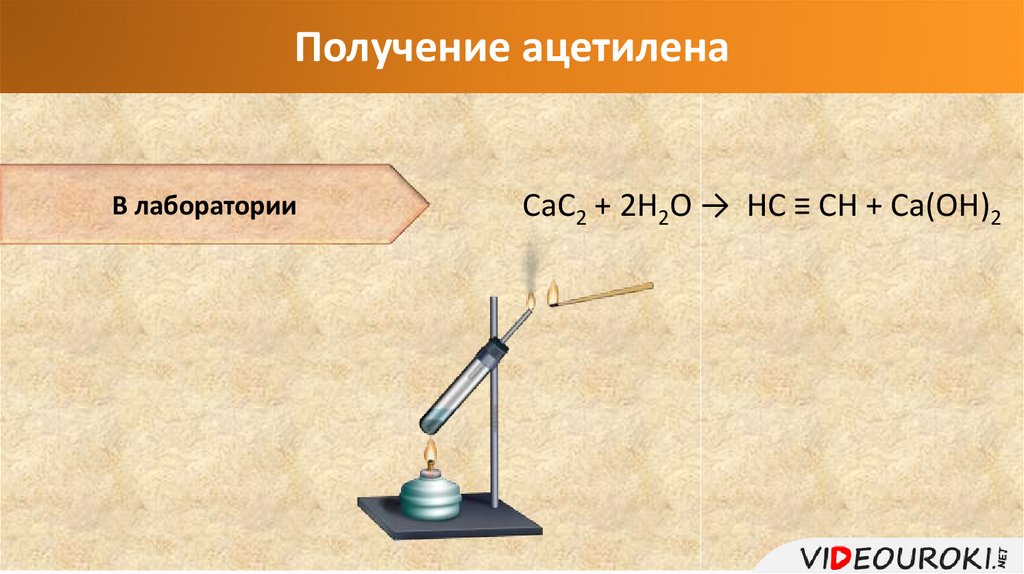
Получение ацетиленаВ лаборатории
СаС2 + 2Н2О → НС ≡ СН + Са(ОН)2
7.
Применение ацетиленаАцетилен
8.
Вычислите, какой объём ацетилена С2Н2 (н.у.) образуется врезультате взаимодействия с водой 100 г технического
карбида кальция, содержащего 4% примесей.
Дано:
m(CaC2) = 100 г
ω(примесей) = 4%
V(C2H2) – ?
Решение:
1,5 моль
х моль
СаС2 + 2Н2О → НС ≡ СН + Са(ОН)2
1 моль
1 моль
ω(CaC2 чист.) = 100 – 4 = 96%
m(CaC2) чист. = 0,96 · 100 = 96 г
n(CaC2) =
M(CaC2) = 40 + 12 · 2 = 64 г/моль
Ответ: V(C2H2) = 33,6 л
V(C2H2) = 1,5 моль · 22,4 л/моль = 33,6 л






 Химия
Химия








