Похожие презентации:
Коррозия металлов
1.
2.
Коррозия — это самопроизвольноеразрушение металлов и сплавов в результате
их взаимодействия с веществами
окружающей среды.
3.
Коррозия металла0
–
Fe – 2e → Fe
2+
4.
5.
6.
Коррозия металлов может привестик экологическим проблемам: из-за
повреждения трубопровода в
результате коррозии может
произойти утечка газа, нефти и
других опасных химических
продуктов.
7.
КоррозияХимическая
Электрохимическая
8.
Химическая коррозия — это разрушениеметаллов в результате их химического
взаимодействия с веществами
окружающей среды.
9.
10.
Электрохимическая коррозия — эторазрушение металлов, которое
сопровождается возникновением
электрического тока.
11.
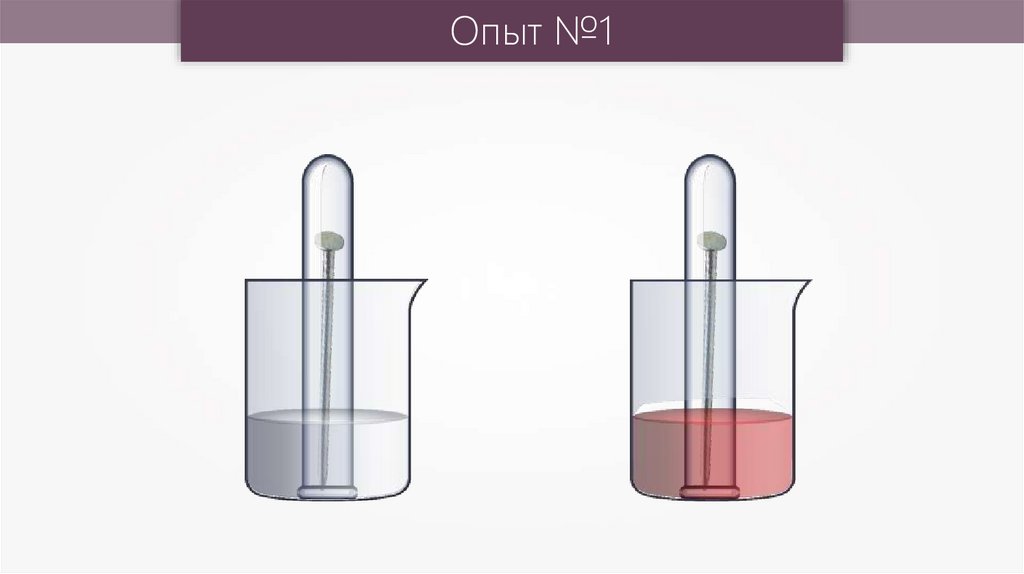
Опыт №112.
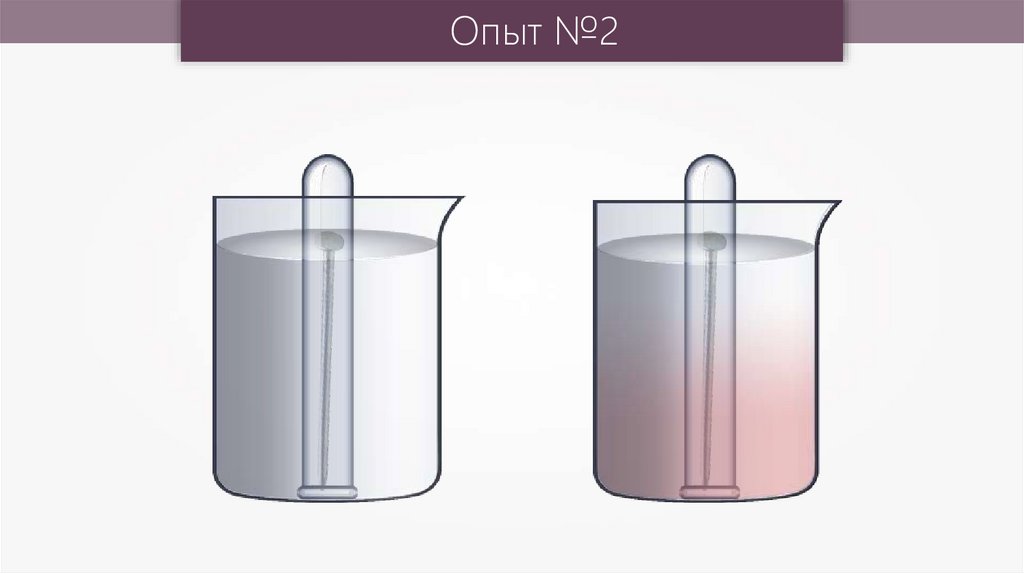
Опыт №213.
Опыт №314.
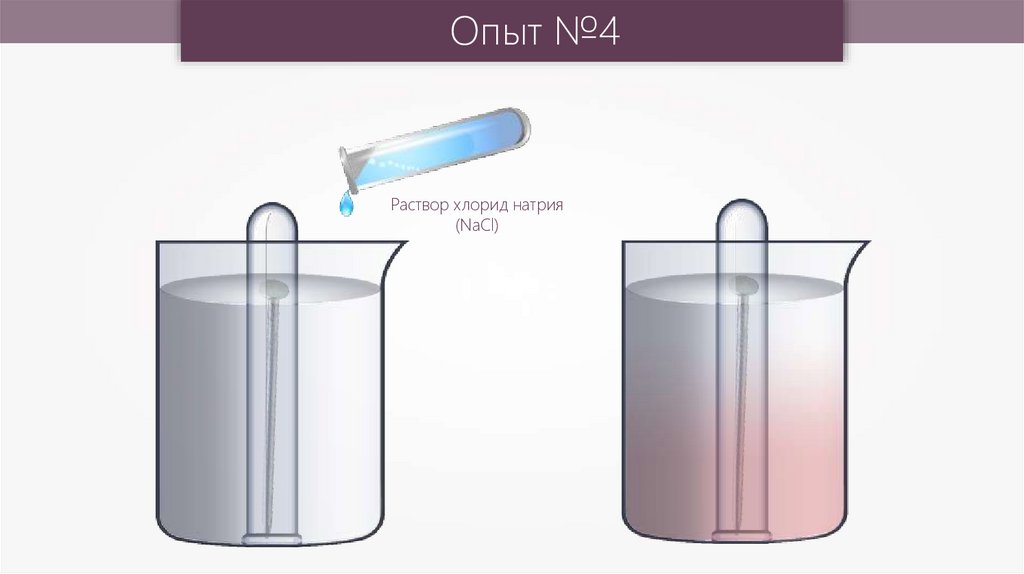
Опыт №4Раствор хлорид натрия
(NaCl)
15.
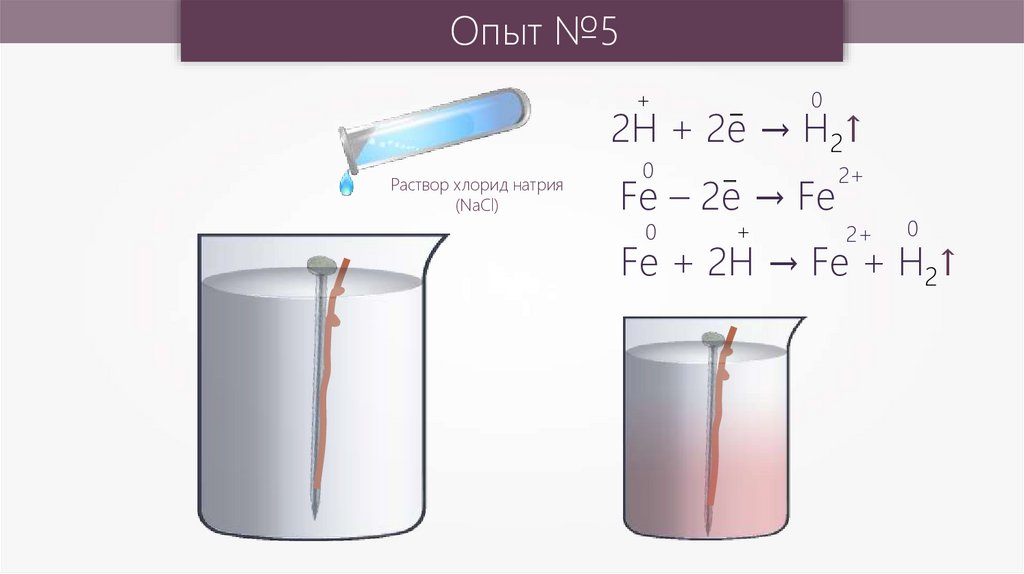
Опыт №5+
–
0
2H + 2e → H2↑
Раствор хлорид натрия
(NaCl)
0
–
Fe – 2e → Fe
0
+
2+
2+
0
Fe + 2H → Fe + H2↑
16.
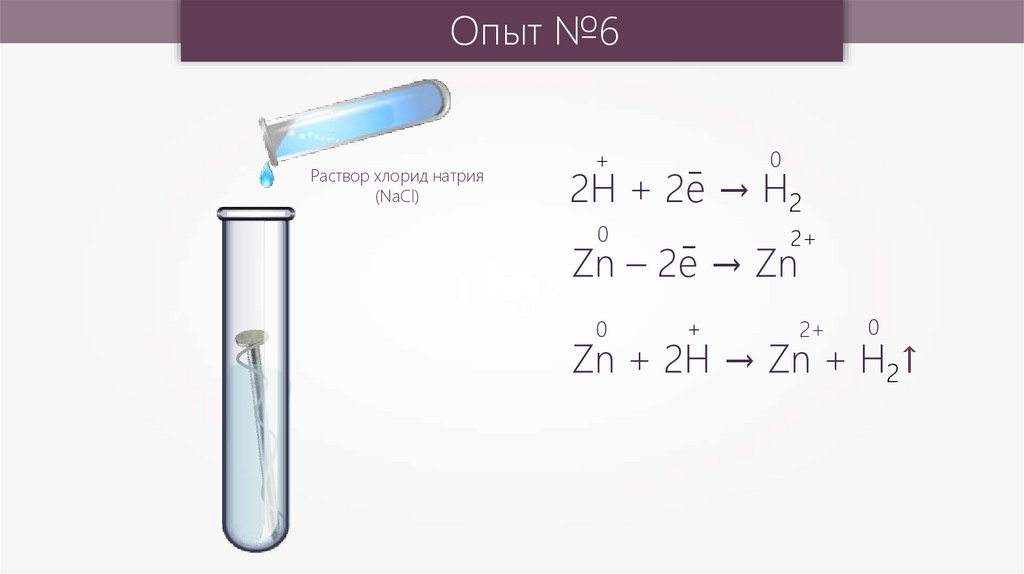
Опыт №6Раствор хлорид натрия
(NaCl)
+
–
0
2H + 2e → H2
0
–
2+
Zn – 2e → Zn
0
+
2+
0
Zn + 2H → Zn + H2↑
17.
При коррозии металлов и сплавовпротекают окислительновосстановительные реакции, в
результате которых атомы металла
взаимодействуют с компонентами
окружающей среды и окисляются.
Коррозия металла усиливается при
соприкосновении его с менее
активным металлом и замедляется,
если металл соприкасается с металлом
более активным.
18.
Методы защиты металлов от коррозии19.
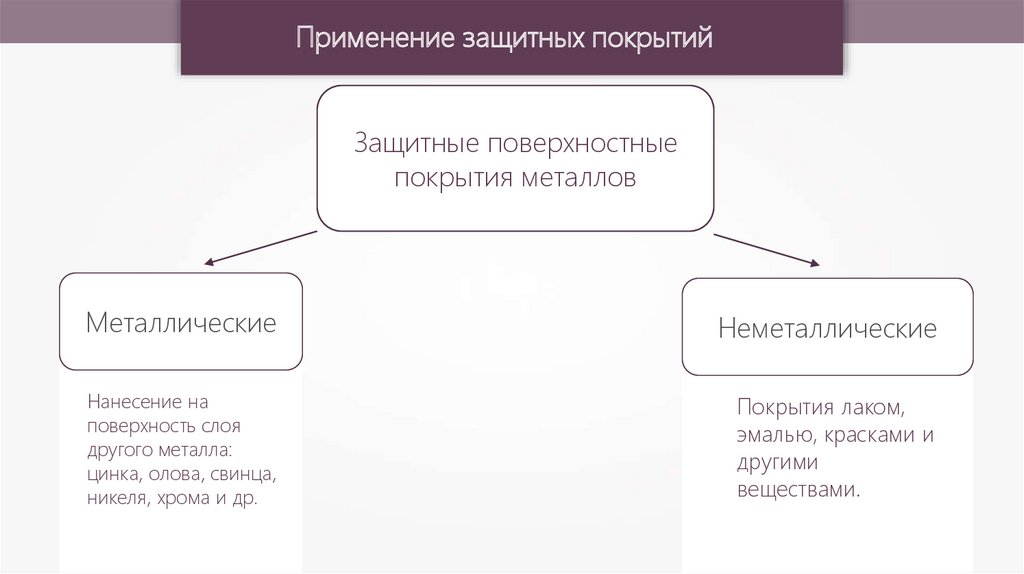
Применение защитных покрытийЗащитные поверхностные
покрытия металлов
Металлические
Неметаллические
Нанесение на
поверхность слоя
другого металла:
цинка, олова, свинца,
никеля, хрома и др.
Покрытия лаком,
эмалью, красками и
другими
веществами.
20.
Применение защитных покрытийКровельное железо
21.
Покрытие железныхизделий никелем, хромом,
помимо защиты от
коррозии, придаёт им
красивый внешний вид.
22.
Создание сплавов с антикоррозионными свойствами23.
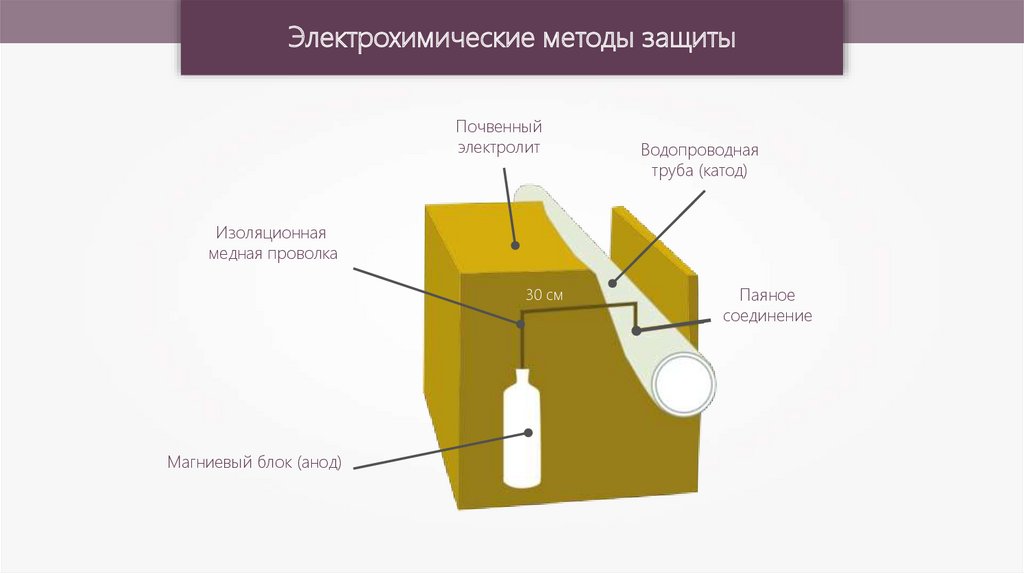
Электрохимические методы защитыПочвенный
электролит
Водопроводная
труба (катод)
Изоляционная
медная проволка
30 см
Магниевый блок (анод)
Паяное
соединение
24.
Введение в рабочую среду,веществ, которые уменьшают агрессивность среды

















 Химия
Химия








