Похожие презентации:
Аналитическая химия
1. Аналитическая химия
наука об определении химического состава веществ.- Отбор аналитических проб
- Составлении схемы анализа и выборе методов
анализа
- Анализ вещества
- Статистическая обработка результатов
Методы основаны на получении и измерении аналитического
сигнала, то есть любого проявления химических и физических
свойств вещества, фиксируемых прибором, которое можно
использовать для его обнаружения или количественного
определения.
2.
Качественныйанализ
Идентификация
веществ, т.е.
обнаружение
элементов в
соединениях и
химических
соединений в
смесях
Количественный
анализ
Определение
относительного
количества
(концентрации или
массы) элементов в
соединениях и
химических
соединений в смесях
3.
Качественный анализ4.
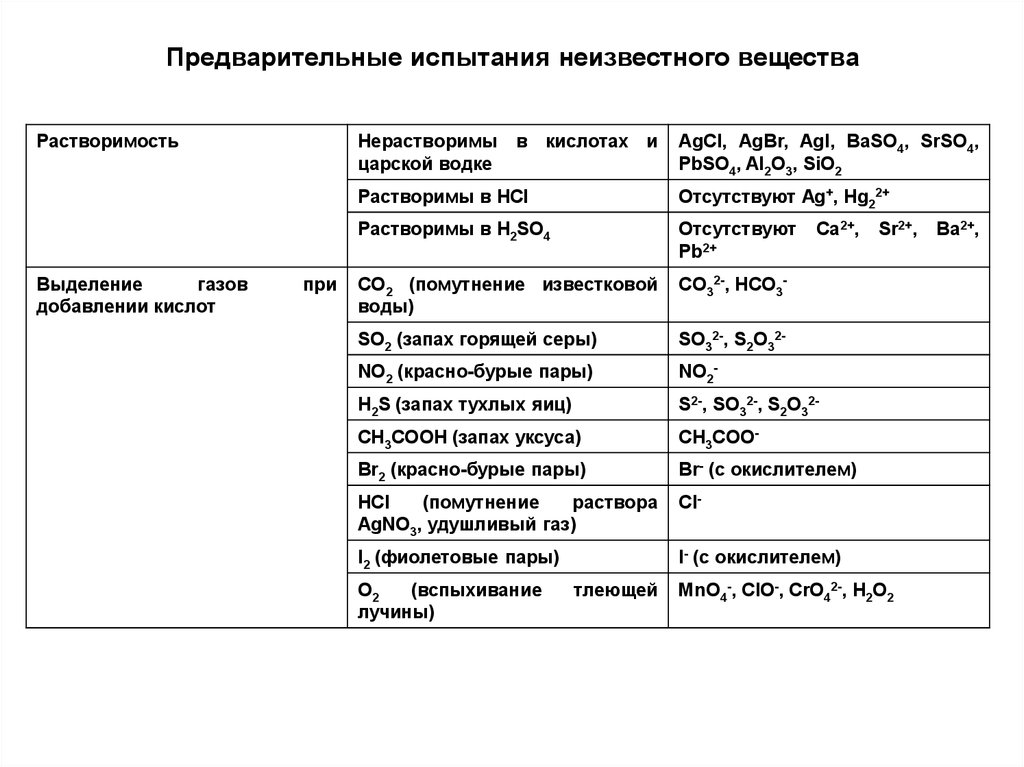
Предварительные испытания неизвестного веществаРастворимость
Выделение
газов
добавлении кислот
при
Нерастворимы в кислотах и
царской водке
AgCl, AgBr, AgI, BaSO4, SrSO4,
PbSO4, Al2O3, SiO2
Растворимы в HCl
Отсутствуют Ag+, Hg22+
Растворимы в H2SO4
Отсутствуют
Pb2+
CO2 (помутнение известковой
воды)
CO32-, HCO3-
SO2 (запах горящей серы)
SO32-, S2O32-
NO2 (красно-бурые пары)
NO2-
H2S (запах тухлых яиц)
S2-, SO32-, S2O32-
CH3COOH (запах уксуса)
CH3COO-
Br2 (красно-бурые пары)
Br- (с окислителем)
HCl
(помутнение
раствора
AgNO3, удушливый газ)
Cl-
I2 (фиолетовые пары)
I- (с окислителем)
O2
(вспыхивание
лучины)
тлеющей
Ca2+,
Sr2+,
MnO4-, ClO-, CrO42-, H2O2
Ba2+,
5.
К+Ca+
Cu+
Na+
6.
7.
Определение рН раствора8.
Ионы Fe2+ в кислой среде сгексацианоферратом (III) калия образуют синий
осадок – калия-железа (II) гексацианоферрат (III)
(турнбулева синь):
Fe2+ + K+ + [Fe(CN)6]3- → KFe[Fe(CN)6]
Реакция с роданидом аммония, NH4SCN,
или роданидом калия, KSCN. Ионы Fe3+ в кислой
среде (pH = 2) с роданидом аммония или калия
образуют комплексное соединение, которое
окрашивает раствор в кроваво-красный цвет:
Fe3+ + 6 SCN- → [Fe(SCN)6]3-
9.
Реакция Ni2+ с диметилглиоксимом (реактивом Чугаева),C4H8N2O2. Катионы Ni2+ в аммиачной среде (рН = 9) образуют с
диметилглиоксимом малорастворимую внутрикомплексную соль
яркого розового цвета:
Ni2+ + 2 C4H8N2O2 + 2 NH3 [Ni(C4H7N2O2)2] + 2 NH4+
10.
11.
12.
Инструментальные методыОптические методы анализа - основаны на измерении оптических
показателей анализируемых веществ на изучении взаимодействия
электромагнитного излучения с атомами и молекулами вещества,
сопровождающегося излучением, поглощением или отражением
лучистой энергии.
- эмиссионный спектральный анализ основан на изучении
спектров испускания (излучения) или эмиссионных спектров
различных веществ
- абсорбционный спектральный анализ: основан на изучении
спектров поглощения лучей анализируемых веществ.
- люминесцентный (флуоресцентный) анализ использует свечение
исследуемого объекта, возникающего под действием
ультрафиолетовых лучей, источником которых служит ртутная
кварцевая лампа, рентгеновских или радиоактивных лучей.
-рентгеноспектральный анализ
-магнитная спектроскопия (ядерный магнитный резонанс,
электронный парамагнитный резонанс)
- инфракрасная спектроскопия.
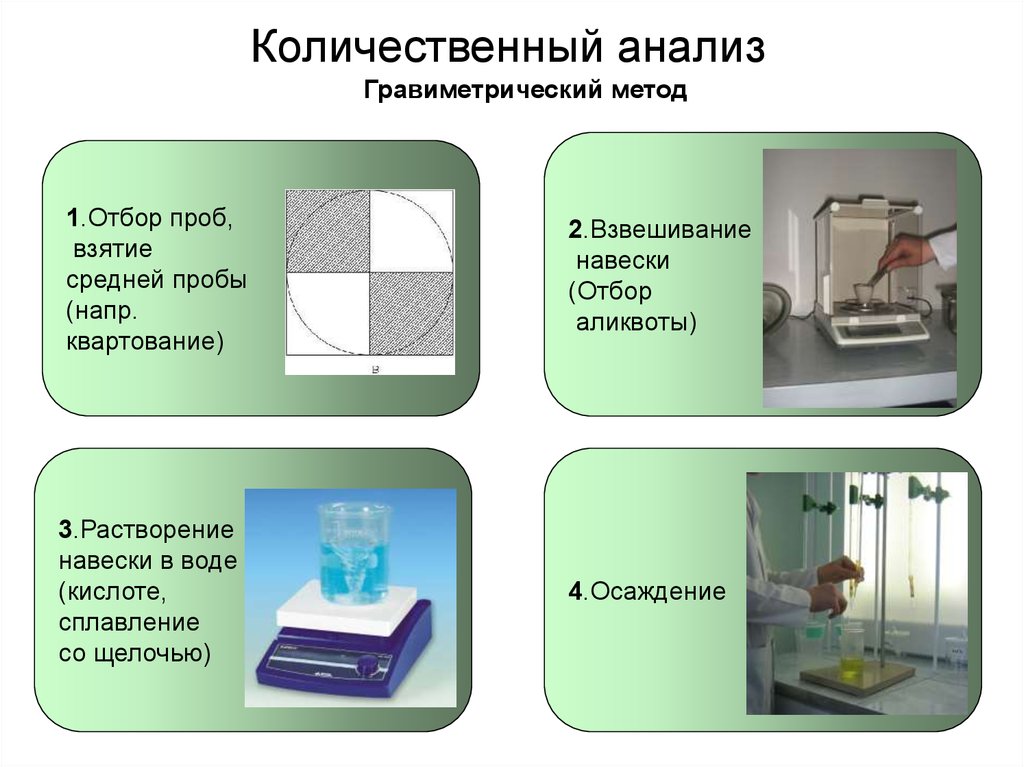
13. Количественный анализ
Гравиметрический метод1.Отбор проб,
взятие
средней пробы
(напр.
квартование)
2.Взвешивание
навески
(Отбор
аликвоты)
3.Растворение
навески в воде
(кислоте,
сплавление
со щелочью)
4.Осаждение
14.
5.Фильтрованиеи
промывание
осадка
6.Высушивание
осадка
7. Прокаливание до
постоянного веса
8.Обработка результатов
15.
Титриметрический анализ16.
Методы титрования17.
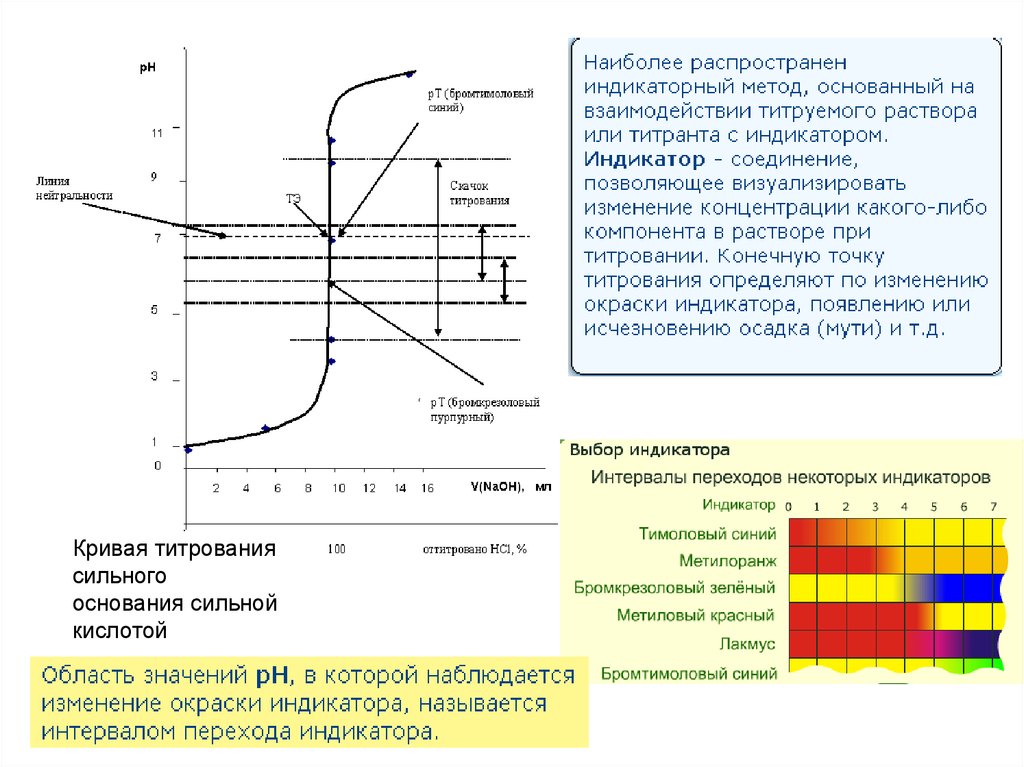
Кривая титрованиясильного
основания сильной
кислотой
18.
Инструментальные (физические и физико-химические) методыанализа – методы, основанные на использовании зависимостей
между измеряемыми физическими свойствами веществ и их
качественным и количественным составом.
Потенциометрическое
φ ~ ln C
Фотометри
ческое
D~C
Кондуктометрический метод
основан на том, что при
определëнной температуре
электрическая проводимость
разбавленных растворов
пропорциональна концентрации
электролитов.
Кулонометрическое т.
концентрация расчитывается
количеству электричества,
израсходованного на
генерацию необходимого для
реакции с анализируемым
веществом
количества титранта.
19.
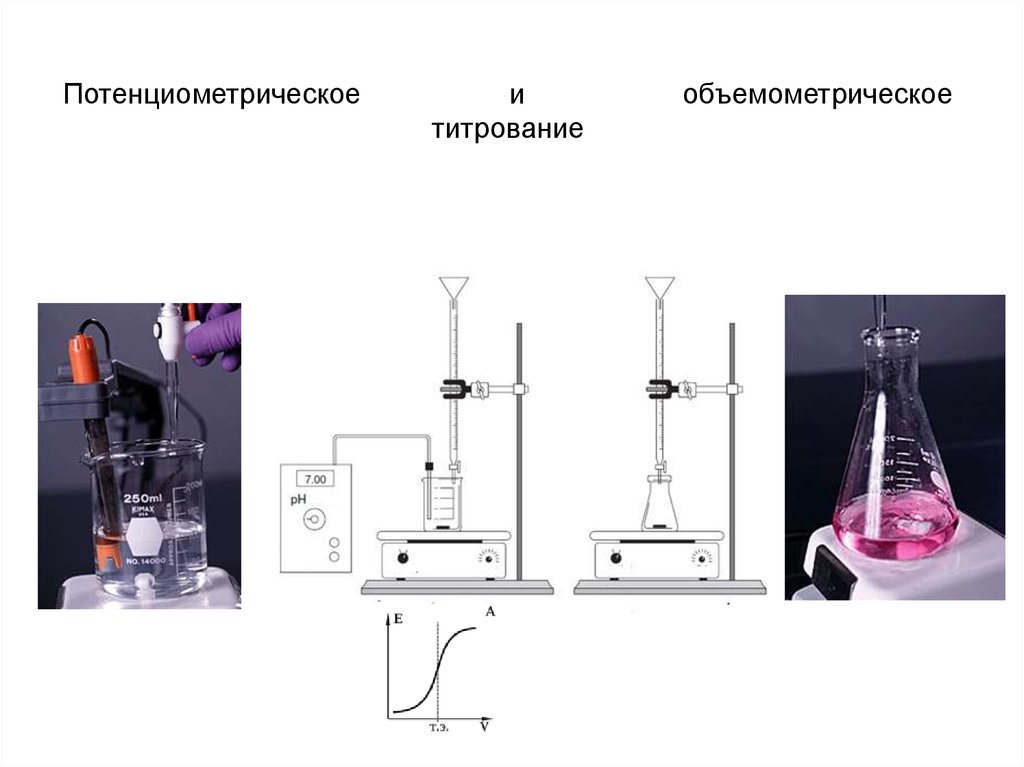
Потенциометрическоеи
титрование
объемометрическое
20.
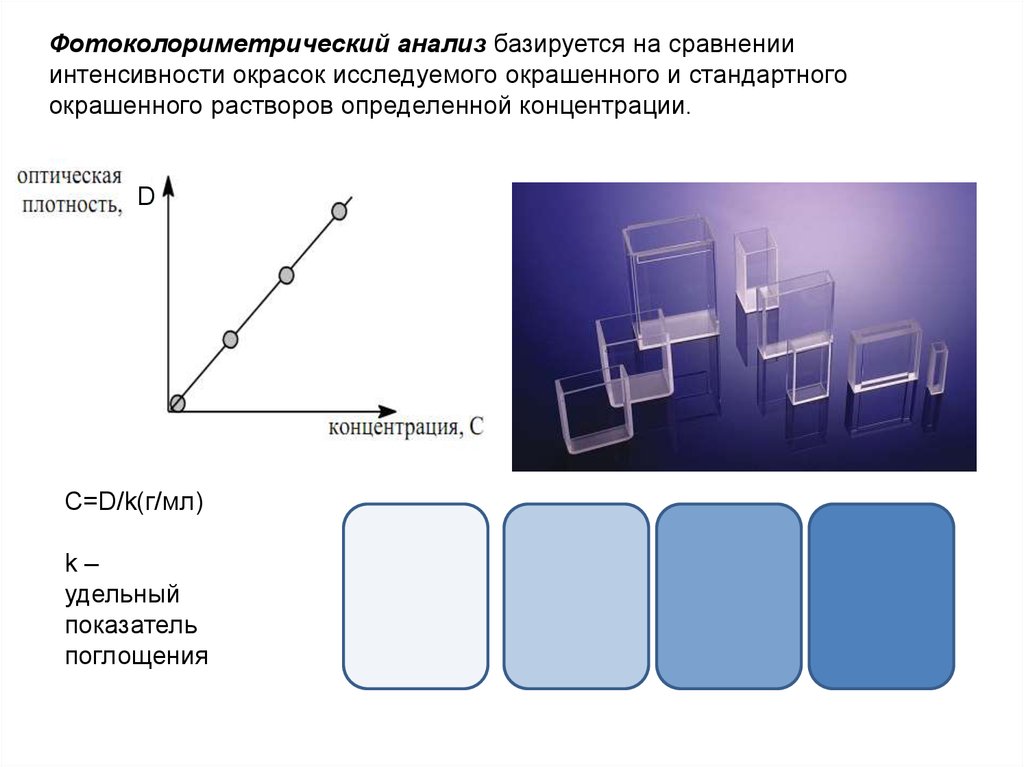
Фотоколориметрический анализ базируется на сравненииинтенсивности окрасок исследуемого окрашенного и стандартного
окрашенного растворов определенной концентрации.
D
C=D/k(г/мл)
k–
удельный
показатель
поглощения
21.
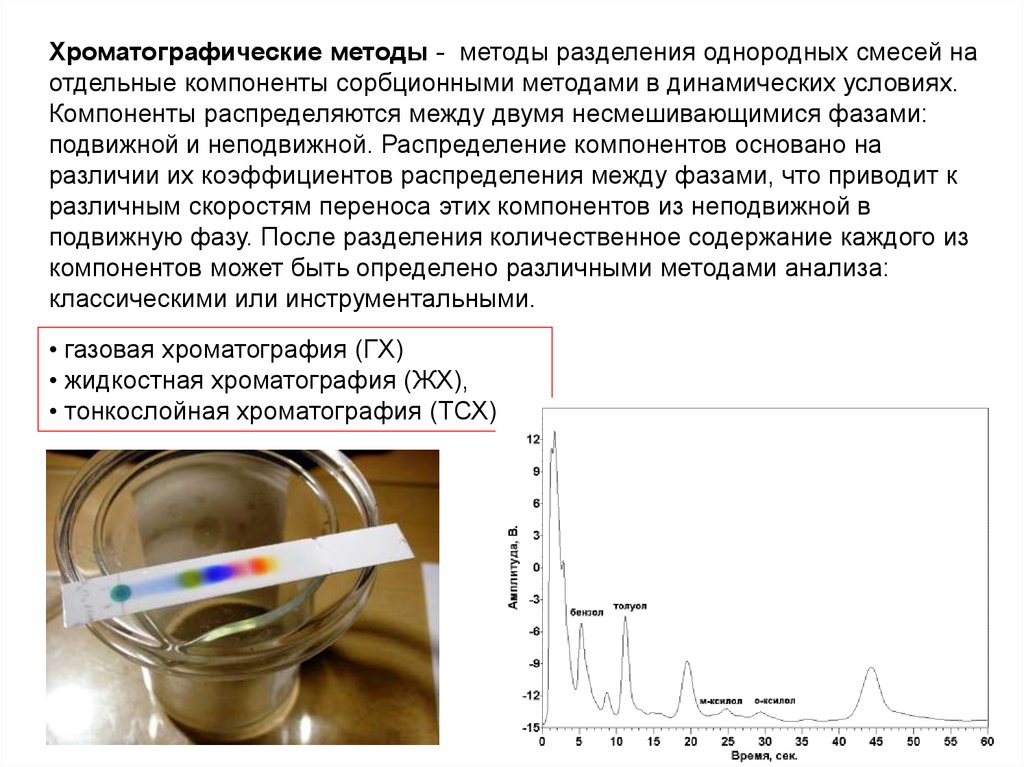
Хроматографические методы - методы разделения однородных смесей наотдельные компоненты сорбционными методами в динамических условиях.
Компоненты распределяются между двумя несмешивающимися фазами:
подвижной и неподвижной. Распределение компонентов основано на
различии их коэффициентов распределения между фазами, что приводит к
различным скоростям переноса этих компонентов из неподвижной в
подвижную фазу. После разделения количественное содержание каждого из
компонентов может быть определено различными методами анализа:
классическими или инструментальными.
• газовая хроматография (ГХ)
• жидкостная хроматография (ЖХ),
• тонкослойная хроматография (ТСХ)













 Химия
Химия








