Похожие презентации:
Делимость электрического заряда. Электрон. Строение атомов
1. Делимость электрического заряда. Электрон. Строение атомов.
2.
1. Когда тело считается наэлектризованным?2. Какие существуют два рода зарядов?
3. Как взаимодействуют заряды?
4. Что такое электроскоп?
3.
Делимость электрического зарядаПроведем эксперимент!
4.
Существует ли пределделения заряда?
5. Опыты Иоффе и Милликена
В своих опытах ониэлектризовали мелкие
пылинки цинка. Заряд
пылинок меняли и
вычисляли. При этом заряд
оказывался каждый раз
другим. Но все его изменения
были в целое число раз (т. е. в
2, 3, 4 и т. д.) больше
некоторого определённого
наименьшего заряда. Этот
заряд дальше уже не делится.
Частицу, имеющую самый
маленький заряд, назвали электроном.
Милликен Роберт
(1868—1953)
Американский физик-экспериментатор.
Опытным путём доказал существование
частиц с наименьшим зарядом. Лауреат
Нобелевской премии
Иоффе Абрам Фёдорович
(1880-1960)
Российский физик, академик.
Создатель российской научной
школы. Проводил исследования по
измерению заряда электрона.
6. Опыт Иоффе
Опыт Милликена7.
Выводы:В природе существует наименьший
электрический заряд, который уже нельзя
разделить.
Наименьший электрический заряд называется
ЭЛЕМЕНТАРНЫМ зарядом
Частица, обладающая отрицательным
элементарным зарядом называется
ЭЛЕКТРОНОМ
8.
Электрический зарядЭлектрический заряд
Электрический заряд-это
физическая величина.
Она обозначается буквой
q. За единицу
электрического заряда
принят кулон(Кл).
9.
ЭЛЕКТРОН- частица с наименьшимотрицательным зарядом.
Электрический заряд – одно из основных
свойств электрона .Этот заряд нельзя
«снять» с электрона.
Пример: Крылышко мухи имеет массу ,
примерно в 5*1022 большую, чем
масса электрона.
10.
СТРОЕНИЕ АТОМОВ11.
«Пудинг с изюмом»Атом, по мысли английского ученого Дж. Томсона,
очень похож на пудинг с изюмом: электроны, как
"изюминки", а «пудинг" - положительно заряженное
вещество атома.
12.
Другие учёные считали, что атомнапоминает орех: есть скорлупа,
внутри
которой
находятся
положительные
и
отрицательные
заряженные
частицы .
13.
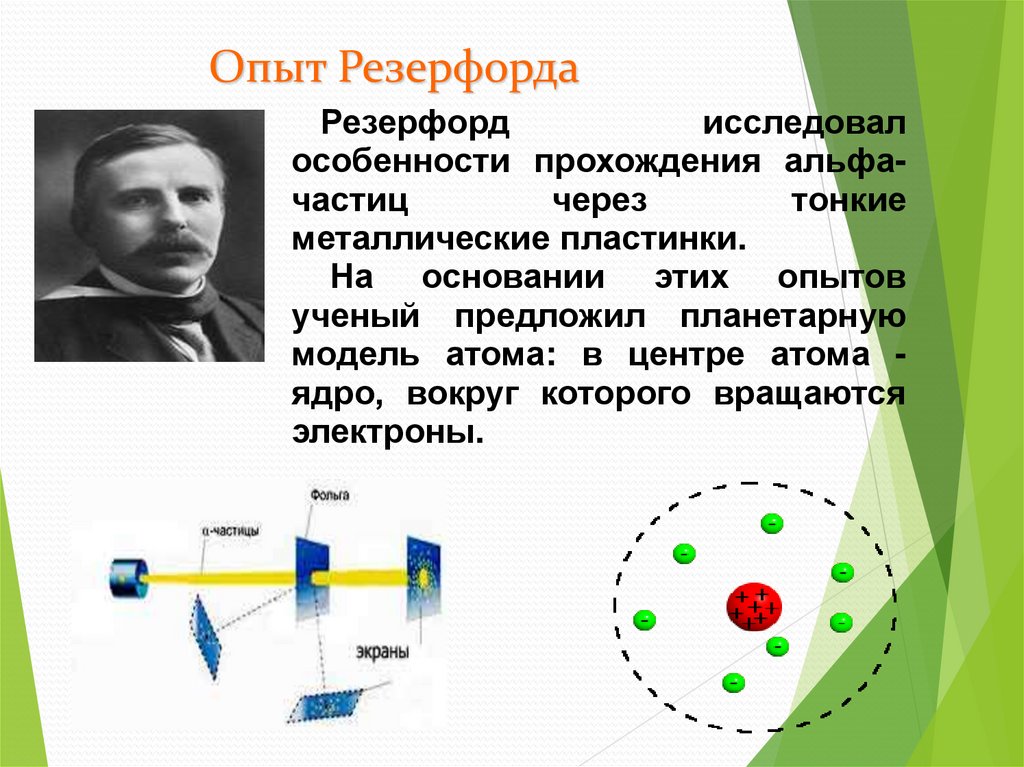
Опыт РезерфордаРезерфорд
исследовал
особенности прохождения альфачастиц
через
тонкие
металлические пластинки.
На основании этих опытов
ученый предложил планетарную
модель атома: в центре атома ядро, вокруг которого вращаются
электроны.
14.
Боровская модель атомаБо́ровская моде́ль а́тома - в этой
модели отрицательно заряженный
электрон
вращается
вокруг
позитивно
заряженного
ядра
атома, предложенная Нильсом
Бором . За основу он взял
планетарную
модель
атома Резерфорда.
Однако Бор ввел допущение, суть
которого заключается в том, что
электроны
в
атоме
могут
двигаться
только
по
определенным орбитам.
15.
По строению атом похож…на Солнечную систему!
16.
Строение атомаСтроение атома таково:
В центре атома находится ядро, состоящее из протонов и
нейтронов, а вокруг ядра движутся электроны. Вся масса атома
сосредоточена в ядре. Атом в целом не имеет заряда, он
нейтрален, потому что положительный заряд ядра равен
отрицательному заряду всех его электронов.
17.
Атомные частицы и их свойстваАтом состоит из трёх видов частиц:
1) Электрон - (е) - заряд отрицательный,
q=-1,6 . 10-19Кл,масса mе =9,1.10-31кг
2) Протон – (р)- заряд положительный,
q = 1,6 . 10-19Кл, масса mр =1,67. 10-27кг=
1840 mе
3) Нейтрон –(n)- не заряжен, масса mn≈ mр
.
18.
19. Модели атомов
а — водорода; б — гелия; в — лития20. Модель атома водорода
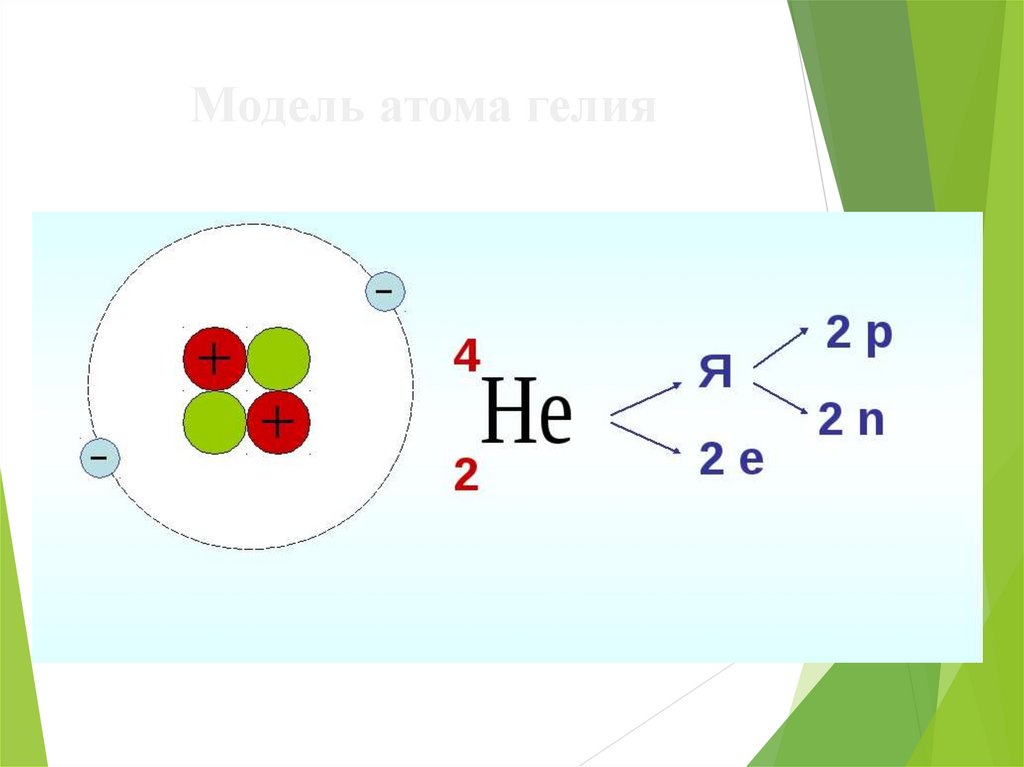
21. Модель атома гелия
22.
Атом не имеет заряда, т.к. количество электронов ватоме равно количеству протонов.
Атом, потерявший один или несколько электронов,
называют положительным ионом.
Атом, к которому присоединился один или несколько
электронов, называется отрицательным ионом.
Нейтральный атом
Отрицательный ион
Число протонов и
электронов одинаково
Число электронов
больше числа протонов
Положительный ион
Число электронов
меньше числа протонов
23.
24.
Домашнее заданиеСпасибо за урок!





















 Физика
Физика








