Похожие презентации:
Алюминий, его физические и химические свойства
1.
Алюминий, егофизические и
химические
свойства
Черногорова Лариса Викторовна
МБОУ СШ № 31 г. Липецка
2. Цели урока:
--
-
Надо знать
Положение х.э. Al в
ПСХЭ;
Распространение х.э. Al
в природе;
Особенности строения
атома Al и его
важнейшие св-ва;
Физические и
химические свойства
вещества;
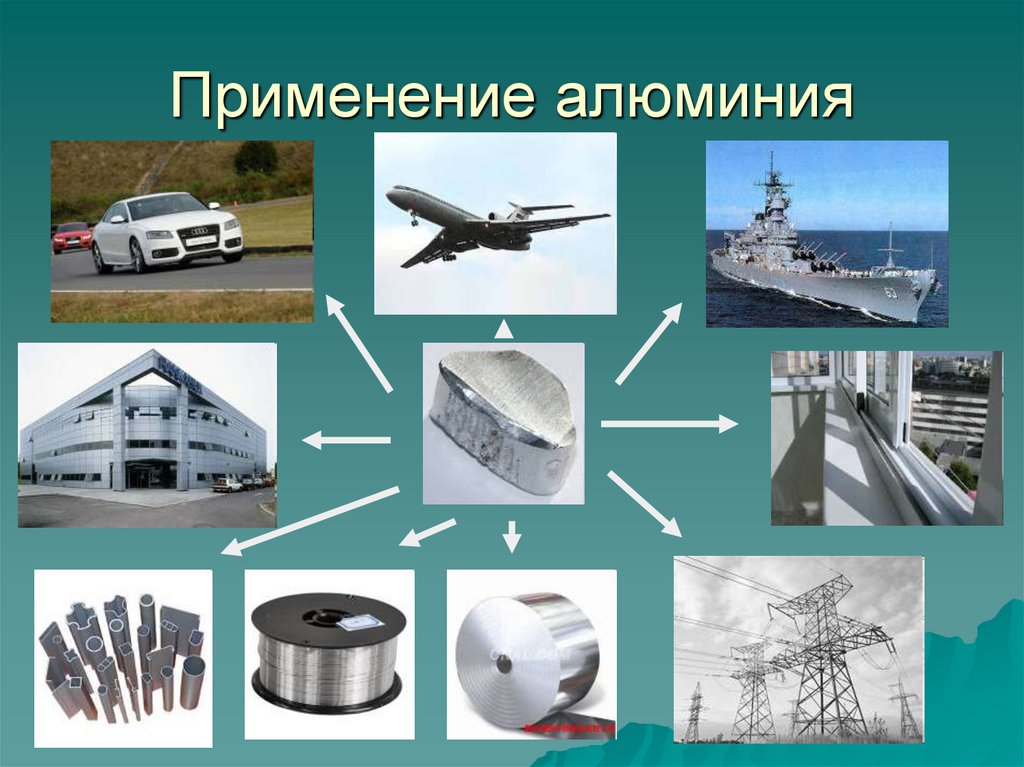
Области применения
алюминия;
Способы получения
алюминия;
Надо уметь
-описывать положение
х.э.
Al в ПСХЭ;
-объяснять особенности
строения атома Al и его
важнейшие св-ва;
-характеризовать
физические и
химические свойства Al ;
-характеризовать способы
получения и области
применения Al ;
3. Положение Al в ПСХЭ
ПериодРяд
–
–
Группа –
Подгруппа –
Порядковый номер –
Относительная атомная масса -
4. Положение Al в ПСХЭ
ПериодРяд
–3 (малый)
–3
Группа – III
Подгруппа –главная
Порядковый номер – 13
Относительная атомная масса -27
5. Алюминий в природе
6. Природные соединения алюминия
АЛ
Ю
М
О
С
И
Л
И
К
А
Т
Алюмосиликат
натрия и кальция
Алюмосиликат
кальция и магния
ы
Турмалин
Б
О
К
С
И
Т
ы
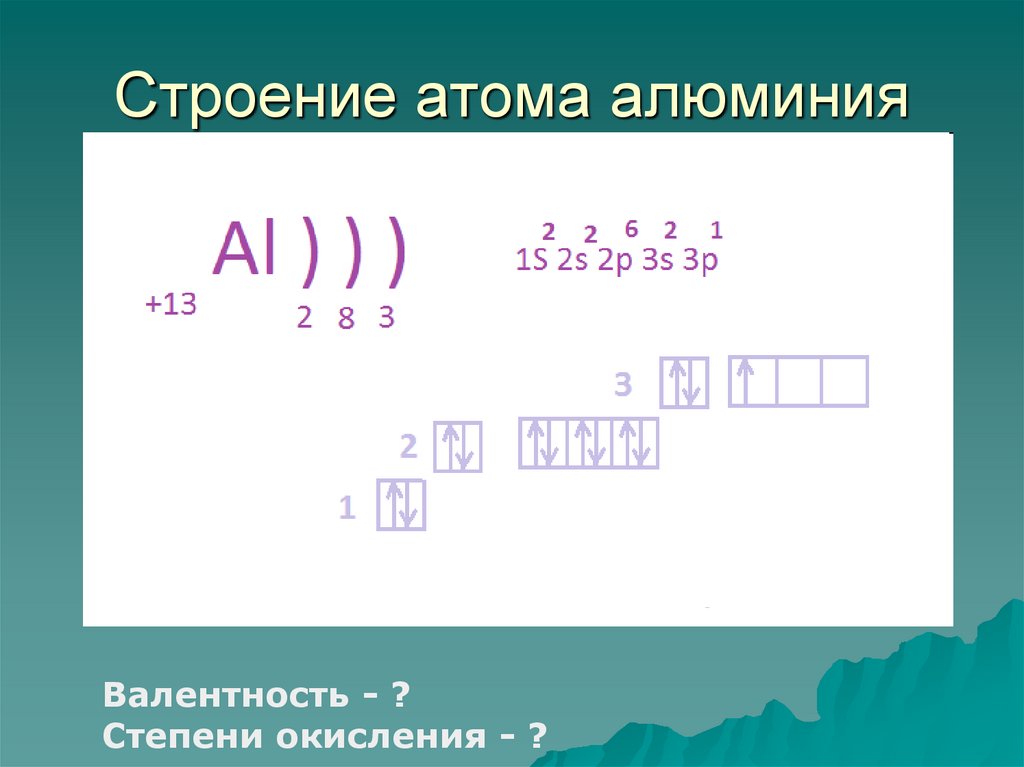
7. Строение атома алюминия
Валентность - ?Степени окисления - ?
8.
КорундРубин
Сапфир
Бирюза
9. Физические свойства
10. Химические свойства
Реагирует с простыми веществами( при нагревании):
Al
Al
Al
Al
Al
+
+
+
+
+
O2 =
Cl2 =
S=
N2 =
C=
11.
Химические свойства алюминия12.
13.
14.
15.
1)Al + HCl =2)Al + HNO3 (p-p) =
3)Al + H2SO4 (конц.) =
4)Al + H3PO4 =
5)Al + H2SO4(р-р) =
6)Al + HNO3(конц.) =
16. Алюминотермия
Al + Fe2O3 =Al + Cr2O3 =
Al + SnO2 =
Al + BaO =

















 Химия
Химия








