Похожие презентации:
Контекстные задачи как способ формирования у школьников навыков решения практических проблем
1. Контекстные задачи как способ формирования у школьников навыков решения практических проблем и функциональных умений Русакова
Е.В.2. Перечень умений и навыков школьников в развитии естественнонаучной функциональной грамотности
1. Использовать естественнонаучные знания вжизненных ситуациях.
2. Делать выводы, формулировать ответ в
понятной форме.
3. Уметь описывать, объяснять и прогнозировать
естественнонаучные явления.
4. Уметь интерпретировать научную
аргументацию и выводы.
5. Понимать методы научных исследований.
6.Перечислять явления, факты, события.
3. Перечень умений и навыков школьников в развитии естественнонаучной функциональной грамотности
7. Сравнивать объекты, события,факты.
8. Объяснять явления, события,
факты, анализировать их и
характеризовать.
9. Составлять конспект, план и т. д….
4. Основные этапы формирования любого умения:
Первый этап: ученику предлагается попробоватьсделать то, что он никогда раньше не делал. При
этом приобретается первичный опыт
выполнения какого-либо нового действия.
Второй этап: формируется новое знание (способ
действия) и осуществляется тренировка его в
применении.
Третий этап: контролируется правильность
применения нового знания и устанавливается
его связь с имеющимися знаниями.
5.
• Мне нравится использовать контекстныезадачи на уроках и внеурочной
деятельности, которые формируют у
школьников навыки решения реальных
практических проблем и функциональных
умений, открывают возможности для
оценивания уровня развития творческого
потенциала личности. Такие задачи
отражают реальные ситуации из бытовой,
производственной, общественной жизни;
при этом основной единицей их
содержания является проблема
6.
Контекстные задачи, которые яиспользую в своей
деятельности, способствуют
формированию у школьников
навыков решения
практических проблем и
функциональных умений.
7.
Контекстные задачи открываютширокие возможности для
оценивания уровня развития
творческого потенциала личности,
учат генерировать мысли,
работать в команде, связывать
теоретические знания и
практическое применение этих
знаний
8. Принципы разработки контекстных задач
1.Принцип доступности.2.Принцип актуальности.
3.Принцип учёта возрастных
особенностей учащихся.
9.
Занятие элективногокурса в 11 классе по
теме: «Применение
производных
карбоновых кислот»
10. Разминка
1.Какая карбоновая кислотанаходится в сливочном масле в
виде сложного эфира с
глицерином, выделяется в
свободном виде при
«прогоркании» масла, обладает
резким запахом и неприятна на
вкус?
11. Это масляная кислота!
CH3-(CH2)2-COOHНазвание по международной
систематической
номенклатуре - бутановая
кислота.
12.
2.Назовитекарбоновую кислоту,
которая содержится в
жире козьего молока.
13.
Это капроновая кислота!CH3-(CH2)4-COOH
Название «капроновая» эта
кислота получила от латинского
слова «Capra» – коза. Название
по международной
систематической номенклатуре
- гексановая кислота.
14.
3.Какая кислота имеет формулуC6H8O6 и является
водорастворимым витамином,
участвующим в биохимических
окислительновосстановительных процессах
человеческого организма? Что
это за витамин?
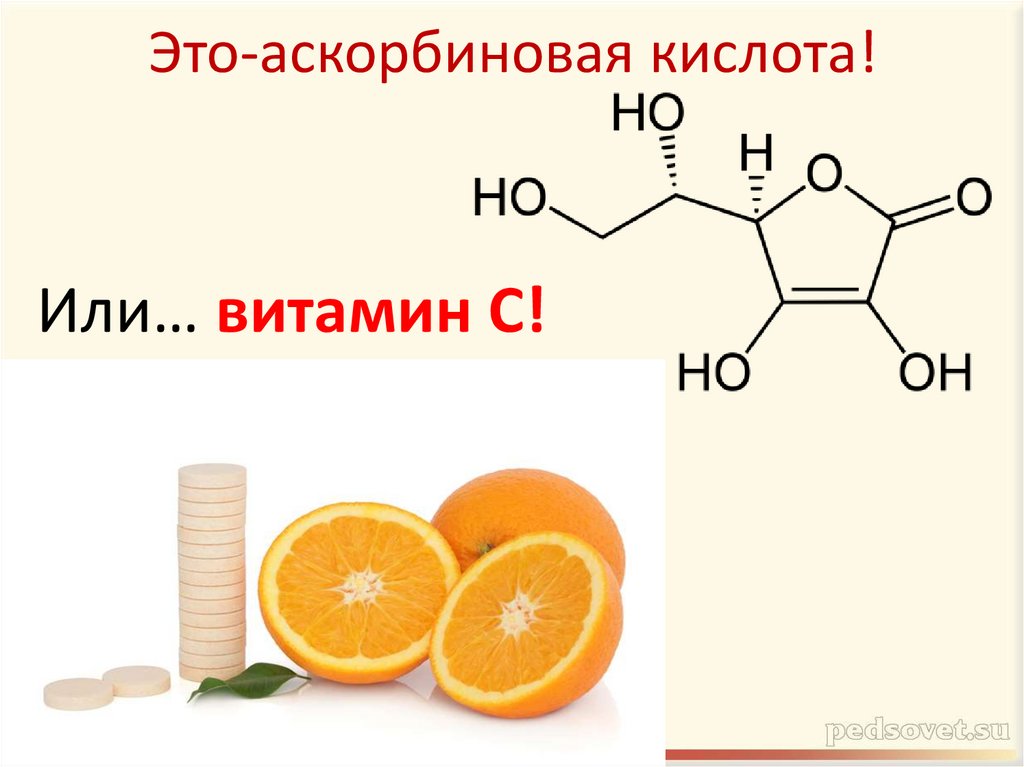
15. Это-аскорбиновая кислота!
Или… витамин С!16.
4. В 1714г по указу Петра I в Петербурге былзаложен аптекарский сад. Там выращивали
лекарственные растения. Листья одного из таких
растений, помещённые в молоко, предохраняют
его от скисания. Из его корней можно получить
жёлтый краситель, а из волокон-сети, не
гниющие в воде. Листья используются для
приготовления здоровой и полезной пищи.
Личный опыт с этим растением способен довести
до слёз. Кислоту, содержащуюся в этом
растении, также входит состав жгучих выделений
муравьёв, пчёл, медуз. Что это за растение? Что
это за кислота? Где её используют?
17. Это крапива! Кислота-муравьиная (метановая). Используют её:
HCOOH1. как пищевая добавка-консервант
E236;
2.как антиобледенитель;
3. при дублении/выделке
натуральных кож и изделий из них;
4.как протравливающий агент при
финишном окрашивании тканей в
текстильной промышленности;
6. в техпроцессах производства
различных резин в качестве
коагулянта.
18.
5.Какие функциональныепроизводные карбоновых
кислот являются
ацилирующими агентами и
применяются для
получения ацетилцеллюлозы, винилацетата,
красителей, лекарств,
синтетических полимеров,
карбоксилатных каучуков?
19. Это- ангидриды карбоновых кислот!
СИНТЕТИЧЕСКИЕКРАСИТЕЛИ
КАУЧУКИ
ЛЕКАРСТВА
20. Исследование продолжается!
Ребята, вы разделены на две группы: группа №1 игруппа №2. Вам необходимо:
1. Выбрать руководителя группы (у вас 10 секунд).
2. Выбрать представителя группы, который будет
искать информацию в Интернете для всей группы
согласно индивидуальному заданию (у вас 10
секунд). 3. Распределить обязанности в группе: кто
будет записывать уравнения химических
реакций на доске, кто будет отвечать на
вопросы задачи перед всеми участниками
и кто будет проводить эксперимент и
демонстрировать его результаты ( у вас 30 секунд).
21.
3. Решить задачу, выполнив все задания к ней.(у вас на это будет 10 минут).
4. Записать уравнения соответствующих реакций
на доске.
5. Продемонстрировать результаты
эксперимента и прокомментировать их.
6. Ответить на все вопросы задачи.
7. Заслушать информацию по индивидуальным заданиям.
5. Проанализировать правильность
своих ответов и оценить свою работу.
22. Индивидуальные задания
Для группы №1: найти в сети Интернетинформацию «История возникновения
химических волокон. Полиэфирные
волокна»
Для группы №2: найти в сети Интернет
информацию о применении нитрилов
и амидов как производных
карбоновых кислот.
Ответы запишите в программе
Microsoft Word. (используйте картинки)
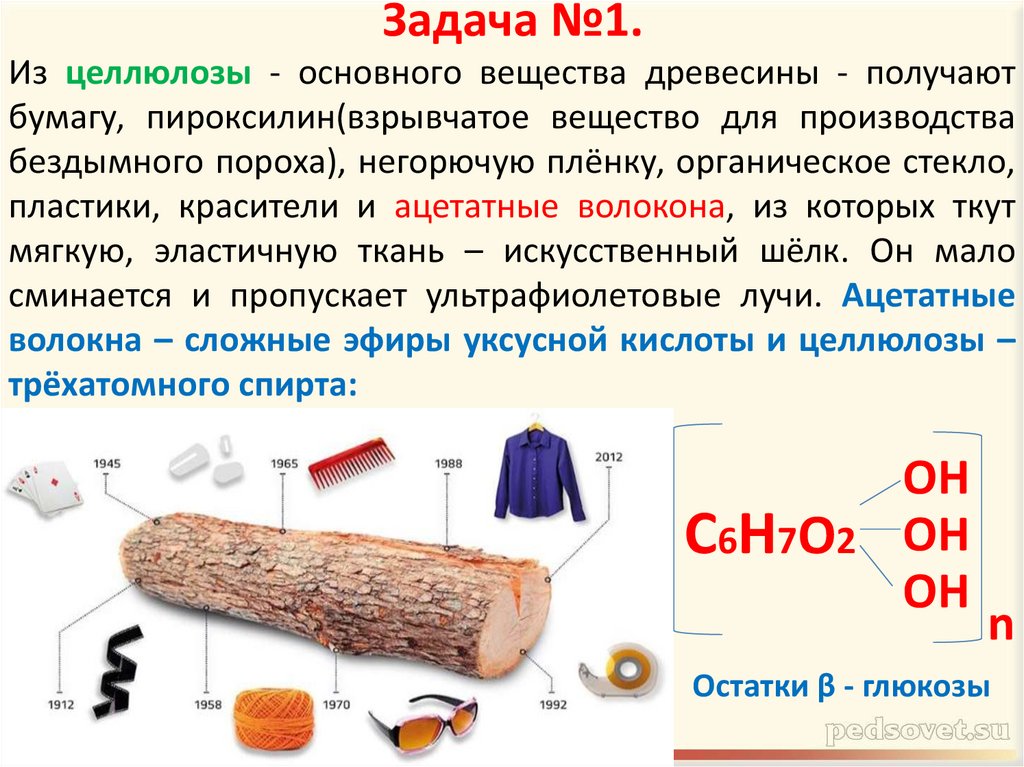
23. Задача №1.
Из целлюлозы - основного вещества древесины - получаютбумагу, пироксилин(взрывчатое вещество для производства
бездымного пороха), негорючую плёнку, органическое стекло,
пластики, красители и ацетатные волокона, из которых ткут
мягкую, эластичную ткань – искусственный шёлк. Он мало
сминается и пропускает ультрафиолетовые лучи. Ацетатные
волокна – сложные эфиры уксусной кислоты и целлюлозы –
трёхатомного спирта:
C6H7O2
ОН
ОН
ОН
n
Остатки β - глюкозы
24. Задания:
1. Запишите уравнения реакции полученияангидрида уксусной кислоты.
2. Запишите уравнения реакции
взаимодействия целлюлозы с уксусным
ангидридом с образованием
диацетилцеллюлозы для производства
ацетатного волокна и негорючей кино- и
рентген - пленок )
3. Запишите уравнения реакции
взаимодействия целлюлозы с уксусным
ангидридом с образованием
триацетилцеллюлозы ( для получения
прочных пластмасс, красителей,
электроизоляционных пленок лаков и т.д.)
25.
4. Исследуйте ацетатное волокнона устойчивость к растворам
кислот и щелочей и характер
горения:
4.1. Повторите правила безопасной работы
в кабинете химии (см. таблицу на столе)
4.2. Закрепите в держателе пробирок
несколько ацетатных волокон и
исследуйте а) скорость горения, запах
продуктов горения, какой характер
имеет остаток после сгорания.
4.2. Проанализируйте действие конц.
растворов кислот и щелочей на волокно:
26.
2 часа назад ваш учительпоместила несколько волокон в
пробирку №1 с
концентрированным раствором
серной кислоты и несколько
волокон в пробирку №2 с
концентрированным раствором
щёлочи. Отметьте
наличие(отсутствие) изменений.
Соблюдайте технику
безопасности!
Запишите уравнения реакций на
доске.
27. Задача №2.
Ежедневно миллионы людей пользуются мылом,ставшим необходимым атрибутом жизни современного
человека. Мыло было «изобретено» в Вавилоне
приблизительно шесть тысяч лет назад, но кем и когда –
точно неизвестно.
28.
По видам мыло бывает глицериновое,детское, жидкое туалетное, кусковое, лечебнокосметическое, прозрачное, твердое туалетное,
хозяйственное.
Считается,
что
лучший
антисептик – это хозяйственное мыло. Мыласмеси растворимых (натриевых, калиевых,
аммонийных) солей высших карбоновых
кислот. Пример состава мыла:
C17H35COONa
(СТЕАРАТ НАТРИЯ)
29. Задания:
1. Объясните, почему у женщин, изображённых на картинефранцузского художника Жана Франсуа Милле «Прачки», красные руки?
2. Напишите уравнение реакции гидролиза мыла, предположив,
что прачки пользовались твёрдым, натриевым, мылом.
3. Ответить на вопрос:
в чем преимущества
использования
синтетических
моющих средств
по сравнению с мылом?
30. 4.Проведите опыт: «Получение нерастворимых солей жирных кислот»
4.1. Повторите правила безопасной работы вкабинете химии (см. таблицу на столе)
4.2. В пробирку поместите кусочек твердого
мыла, прилейте к нему 8–10 мл
дистиллированной воды, взболтайте и
подогрейте полученный раствор. Разделите
раствор по двум пробиркам, добавьте в
первую – раствор хлорида кальция, во
вторую – раствор сульфата меди.
4.3. Объясните изменения, происходящие в
каждой пробирке.
Соблюдайте технику безопасности!
Запишите уравнения реакций на доске.
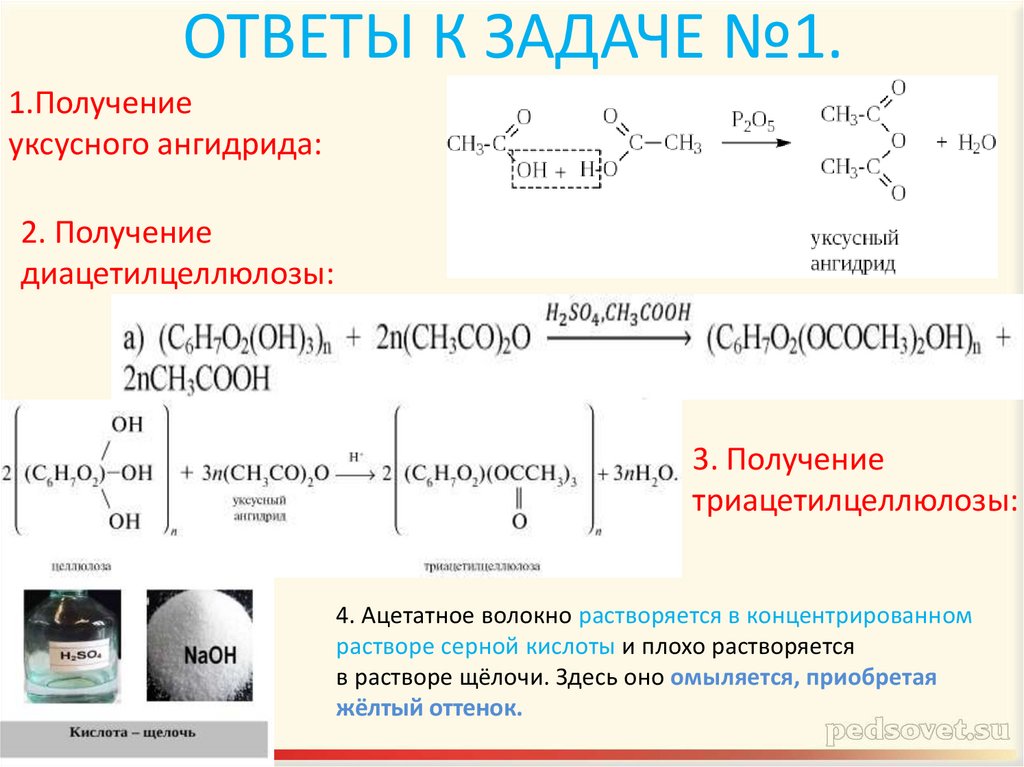
31. ОТВЕТЫ К ЗАДАЧЕ №1.
1.Получениеуксусного ангидрида:
2. Получение
диацетилцеллюлозы:
3. Получение
триацетилцеллюлозы:
4. Ацетатное волокно растворяется в концентрированном
растворе серной кислоты и плохо растворяется
в растворе щёлочи. Здесь оно омыляется, приобретая
жёлтый оттенок.
32.
Ацетатное волокно горит желтым пламенем,распространяя специфический кисловатый
запах и образуя наплыв темного цвета,
который после охлаждения легко
раздавливается пальцами. Если пламя
погасить, то волокно медленно тлеет с
выделением струйки дыма.
33. Ответ 1 группы на индивидуальное задание
34.
Полиэфирные волокнаПолиэфи́ ры (или полиэ́стеры) — высокомолекулярные
соединения, получаемые поликонденсацией многоосновных
кислот или их ангидридов с многоатомными спиртами.
Известны природные (янтарь, древесная смола, шеллак и др.)
и искусственные полиэфиры. Практическое применение
получили глифталевые смолы, полиэтилентерефталат,
полиэфирмалеинаты и полиэфиракрилаты.
полиэфирные волокна - синтетические волокна,
формуемые из расплава полиэтилентерефталата. К
полиэфирным волокнам относится лавсан. Превосходят по
термостойкости большинство натуральных и химических
волокон: при 180°С они сохраняют прочность на 50%.
Полиэфирные волокна сравнительно атмосферостойки.
Полиэфирные волокна устойчивы к действию ацетона,
четырёххлористого углерода, дихлорэтана и др. растворителей,
микроорганизмов, моли, плесени, коврового жучка.
35.
36. ОТВЕТЫ К ЗАДАЧЕ №2.
1. В горячей воде происходит гидролиз солейкарбоновых кислот с образованием щёлочи,
которая и раздражает руки.
2. Гидролиз стеарата натрия:
3. Преимущества синтетически моющих средств:
они не теряют своей моющей способности
даже в жесткой и морской водах, так как их
кальциевые и магниевые соли растворимы.
Также, среда их водных растворов-нейтральна
(в отличие от растворов мыла - щелочной)
37.
4. Образуются стеараты кальция (осадок белогоцвета) и меди (бирюзово-зелёного цвета):
2С17Н35COONa+CaCl2
(С17Н35COO)2Са+2NaCl
2С17Н35COONa+CuCl2
(С17Н35COO)2Cu+2NaCl
СТЕАРАТ КАЛЬЦИЯ
СТЕАРАТ МЕДИ