Похожие презентации:
Гидролиз
1.
Презентация к уроку химии по теме:«Гидролиз»
Выполнила: Кренинг А.
Группа: ФО-03-21
2 курс фармации
Приняла: Дильдабекова Л.А.
2.
Гидролизhydro – вода, lysis - распад
Гидролиз – это реакция
обменного разложения веществ водой.
• Частицы растворенного вещества в воде окружены
гидратной оболочкой. В некоторых случаях это приводит
к химическому взаимодействию с образованием новых
веществ, к реакции гидролиза.
3.
ГидролизОрганических
веществ
Неорганических
веществ
Солей
4.
Гидролизорганических
веществ
Белков
Галогеноалканов
Сложных
эфиров
(жиров)
Углеводов
5.
ГидролизГидролиз галогеноводородов:
t, OH
R-Cl + H2O ↔ R-OH + HCl
Гидролиз сложных эфиров:
О
О
H,t
∕∕
∕∕
R1-C
+ H2O ↔ R2-OH + R1- C
O-R2
OH
6.
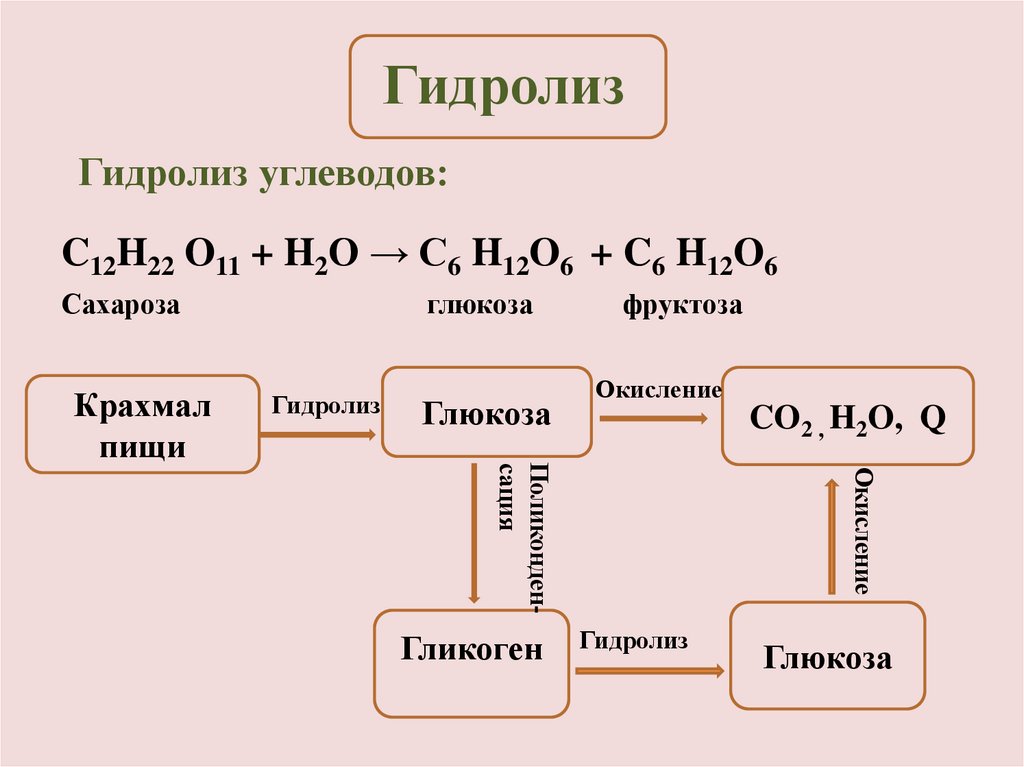
ГидролизГидролиз углеводов:
C12H22 O11 + H2O → C6 H12O6 + C6 H12O6
Сахароза
Гидролиз
Глюкоза
фруктоза
Окисление
CO2 , H2O, Q
Гликоген
Окисление
Поликонденсация
Крахмал
пищи
глюкоза
Гидролиз
Глюкоза
7.
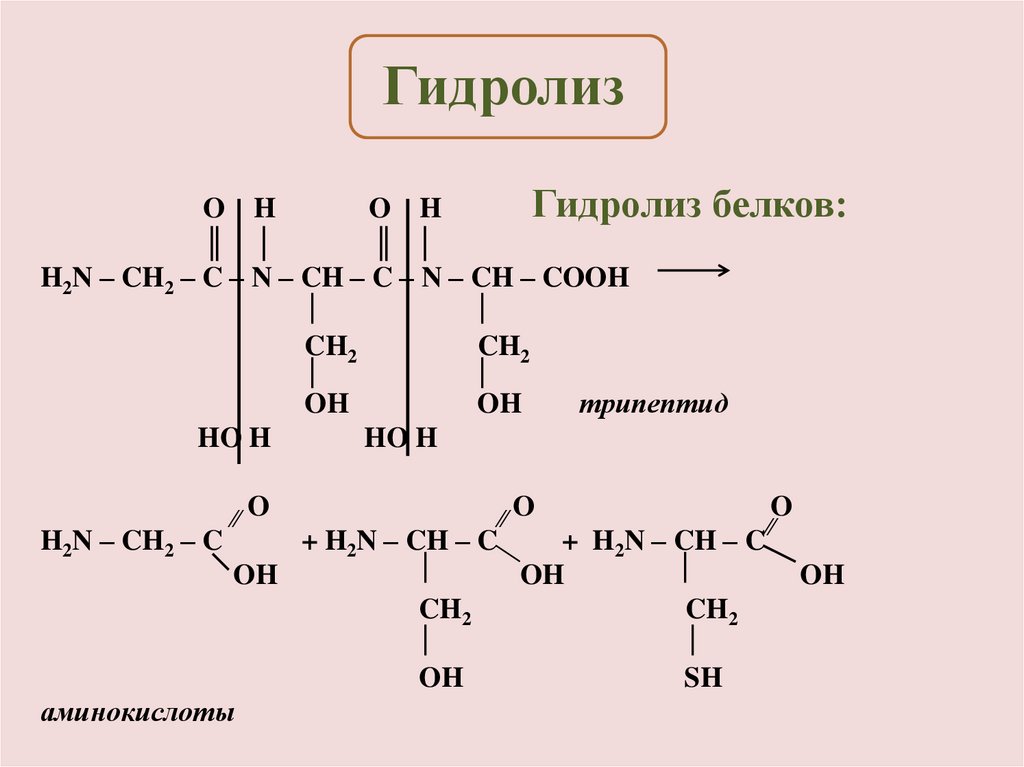
ГидролизГидролиз белков:
O H
O H
║ │
║ │
H2N – CH2 – C – N – CH – C – N – CH – COOH
HO H
H2N – CH2 – C
∕∕ O
OH
│
│
CH2
CH2
│
│
OH
OH
HO H
+ H2N – CH – C
│
CH2
│
OH
аминокислоты
трипептид
∕∕ O
O
∕∕
+ H2N – CH – C
│
OH
CH2
│
SH
OH
8.
Гидролиз солей• Сущность гидролиза сводится к обменному
химическому взаимодействию катионов или
анионов соли с молекулами воды. В результате
образуется слабый электролит.
• Любая соль – это продукт взаимодействия
основания с кислотой. В зависимости от силы
основания и кислоты выделяют 4 типа солей.
9.
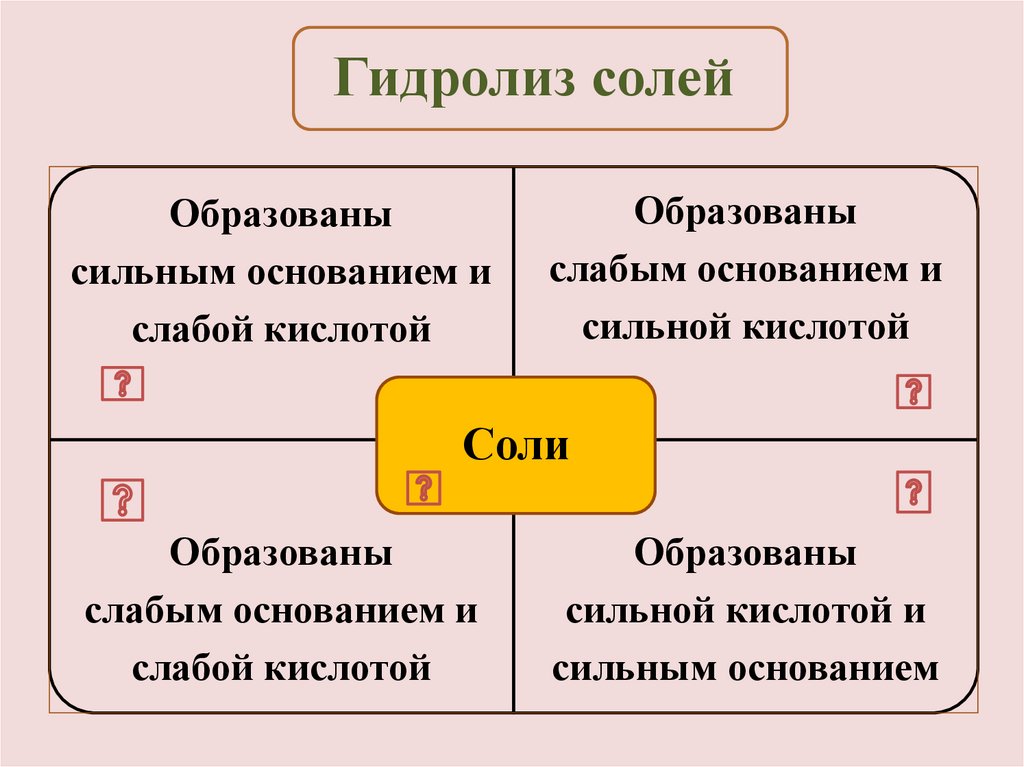
Гидролиз солейОбразованы
сильным основанием и
слабой кислотой
Образованы
слабым основанием и
сильной кислотой
Соли
Образованы
слабым основанием и
слабой кислотой
Образованы
сильной кислотой и
сильным основанием
10.
Диссоциация кислотСильные электролиты
Слабые электролиты
H2SO4 → 2H+ + SO42-
H2CO3 ↔ H+ + HCO3-
HNO3 → H+ + NO3-
H2SO3 ↔ H+ + HSO3-
HCl → H+ + Cl-
H2SiO3↔ H+ + HSiO3H2S ↔ H+ + HSОрганические кислоты:
CH3COOH ; HCOOH
11.
Диссоциация основанийСильные электролиты
Щелочи
NaOH → Na+ + OHKOH → K+ + OHLiOH → Li+ + OHBa(OH)2→ Ba2++ 2OH-
Слабые электролиты
Нерастворимые
основания
Mg(OH)2
Zn(OH)2
Cu(OH)2
Fe(OH)2
Fe(OH)3 и другие
NH3•H2O
12.
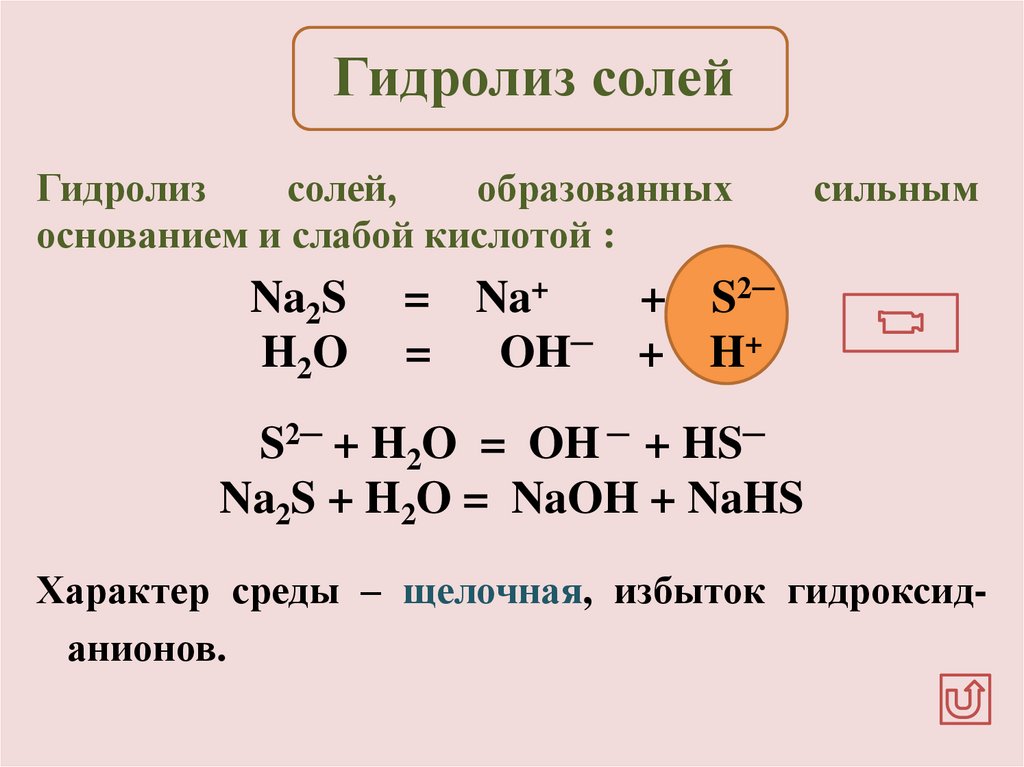
Гидролиз солейГидролиз
солей,
образованных
основанием и слабой кислотой :
Na2S
H2O
сильным
= Na+
+ S2─
=
OH─ + H+
S2─ + H2O = OH ─ + HS─
Na2S + H2O = NaOH + NaHS
Характер среды – щелочная, избыток гидроксиданионов.
13.
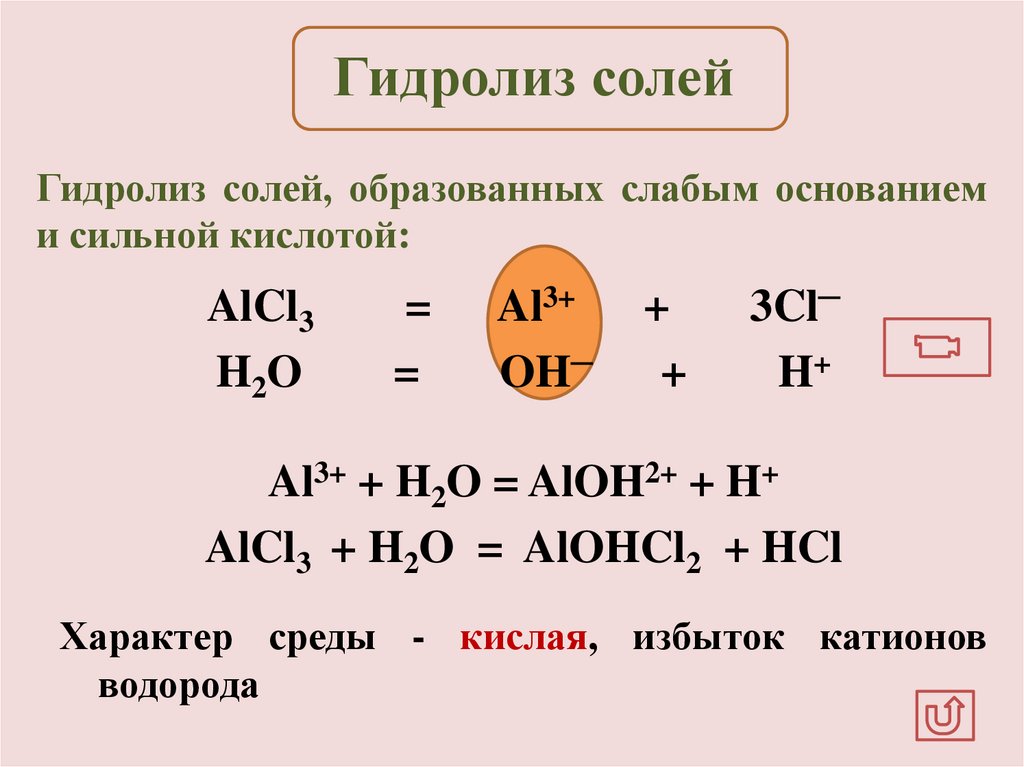
Гидролиз солейГидролиз солей, образованных слабым основанием
и сильной кислотой:
AlCl3
H2O
=
=
Al3+
OH─
+
+
3Cl─
H+
Al3+ + H2O = AlOH2+ + H+
AlCl3 + H2O = AlOHCl2 + HCl
Характер среды - кислая, избыток катионов
водорода
14.
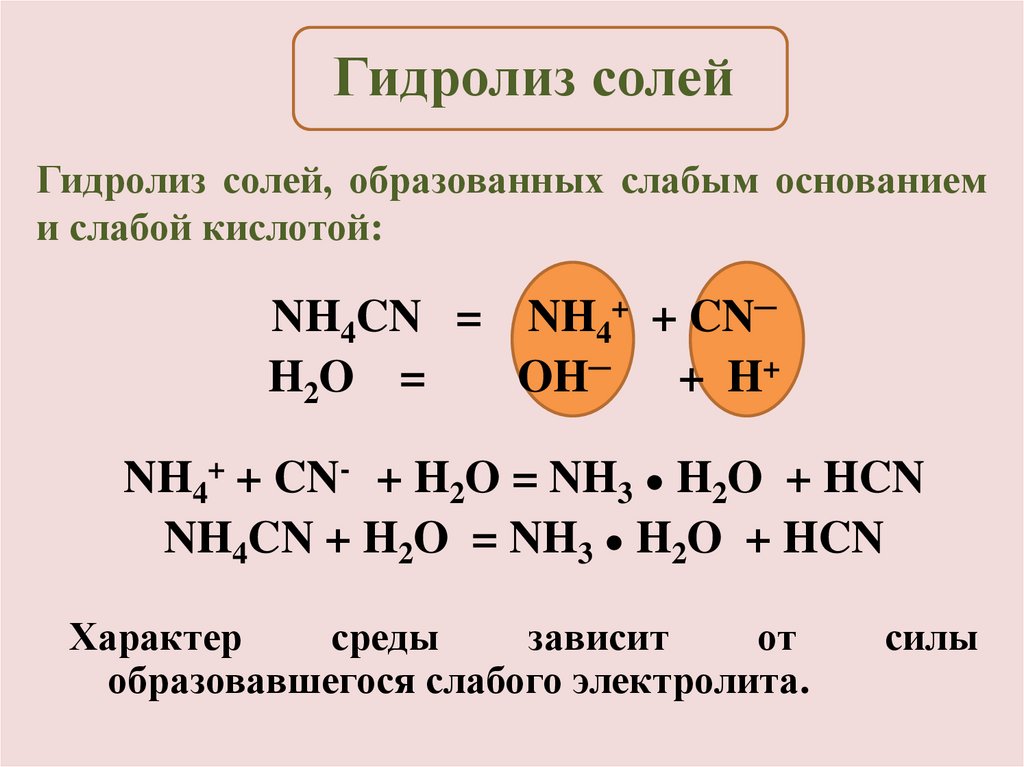
Гидролиз солейГидролиз солей, образованных слабым основанием
и слабой кислотой:
NH4CN = NH4+ + CN─
H2O =
OH─ + H+
NH4+ + CN- + H2O = NH3 ● H2O + HCN
NH4CN + H2O = NH3 ● H2O + HCN
Характер
среды
зависит
от
образовавшегося слабого электролита.
силы
15.
Гидролиз солейНеобратимый гидролиз солей, образованных
слабым основанием и слабой кислотой:
Например, соли, которые нельзя получить реакцией обмена
между водными растворами двух солей (в ТР – разлагаются в
водной среде) Fe2(CO3)3
2FeCl3 + 3Na2CO3 + 3H2O =2Fe(OH)3↓ +3CO2↑+ 6NaCl
Fe2(CO3)3 + 3H2O = 2Fe(OH)3↓ +3CO2↑
Реакция между двумя растворами (FeCl3 и Na2CO3) будет
необратимой, а карбонат железа (+3) не образуется.
16.
Гидролиз солейГидролиз
солей,
образованных
основанием и сильной кислотой:
сильным
KCl = K+ + ClСлабых ионов нет, гидролиз не идет, среда
нейтральная.
17.
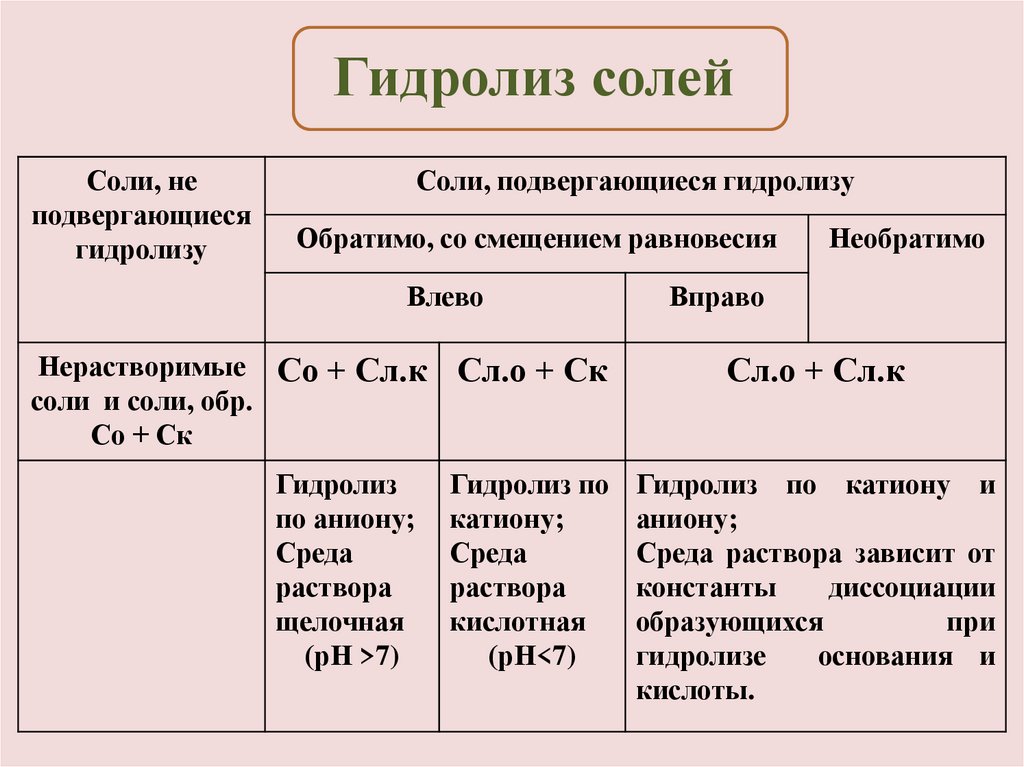
Гидролиз солейСоли, не
подвергающиеся
гидролизу
Соли, подвергающиеся гидролизу
Обратимо, со смещением равновесия
Влево
Необратимо
Вправо
Нерастворимые Со + Сл.к
соли и соли, обр.
Со + Ск
Сл.о + Ск
Сл.о + Сл.к
Гидролиз
по аниону;
Среда
раствора
щелочная
(рН >7)
Гидролиз по
катиону;
Среда
раствора
кислотная
(рН<7)
Гидролиз по катиону и
аниону;
Среда раствора зависит от
константы
диссоциации
образующихся
при
гидролизе
основания и
кислоты.
18.
Гидролиз солейУсловия смещения реакций обратимого гидролиза
(согласно принципу Ле Шателье).
Усилить гидролиз соли можно следующими способами:
1.Добавить воды (уменьшить концентрацию раствора;
2. Нагреть раствор;
3.
Связать
один
из
продуктов
гидролиза
в
труднорастворимое соединение или удалить
один из
продуктов в газовую фазу.
19.
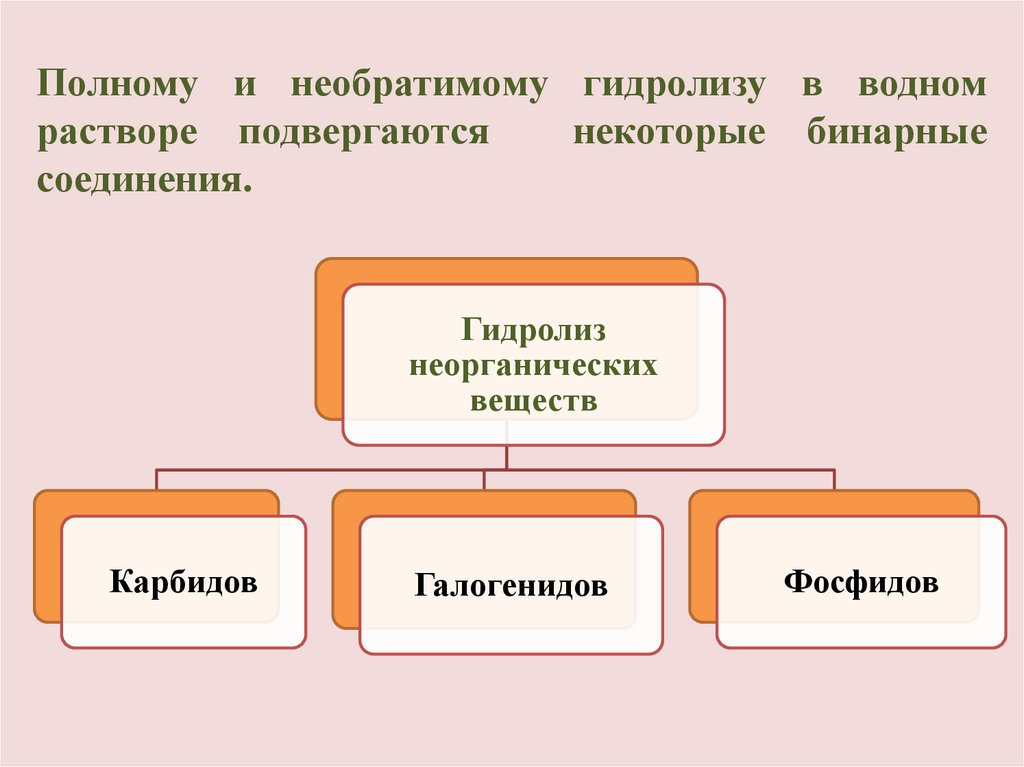
Полному и необратимому гидролизу в водномрастворе подвергаются
некоторые бинарные
соединения.
Гидролиз
неорганических
веществ
Карбидов
Галогенидов
Фосфидов
20.
ГидролизГидролиз карбидов:
CaC2 + 2H2O = Ca(OH)2 + C2 H2↑
Карбид
кальция
ацетилен
Al4C3 + 12H2O = 4Al(OH)3 + 3CH4↑
Карбид
алюминия
метан
21.
ГидролизГидролиз галогенидов:
SiCl4 + 3H2O = H2SiO4↓ + 4HСl
хлорид
кремния (+4)
кремниевая
кислота
Гидролиз фосфидов:
Са3P2 + 6H2O = 3Са(OH)2 + 2PH3↑
фосфид
кальция
фосфин
22.
ГидролизРоль гидролиза:
В природе: преобразование земной коры; обеспечение
слабощелочной среды морской воды.
В
народном
хозяйстве:
порча
производственного
оборудования; выработка из непищевого сырья ценных
продуктов (бумага, мыло, спирт, глюкоза, белковые
дрожжи); очистка промышленных стоков и питьевой воды;
подготовка тканей к окрашиванию; известкование почв.
В повседневной жизни: стирка; мытье посуды; умывание с
мылом; процессы пищеварения.
23.
Список использованной литературы1. О.С. Габриелян. Учебник для общеобразовательных
учреждений. ХИМИЯ. Базовый уровень. 11 класс. – М.: Дрофа,
2007
2. О. С. Габриелян, А. В. Яшукова. Химия. 11 класс. Базовый
уровень. Методическое пособие. – М.: Дрофа, 2009.
3. О. С. Габриелян, И. Г. Остроумов. Химия 11 класс: настольная
книга учителя. – М.: Дрофа, 2005
Используемые интернет-ресурсы
http://school-sector.relarn.ru/nsm/
http://school-collection.edu.ru/collection/chemistry/
http://www.alhimik.ru
http://all-met.narod.ru













 Химия
Химия








