Похожие презентации:
РНК-геномні віруси, ортоміксовіруси, параміксовіруси, рабдовіруси
1.
Кафедра мікробіології, вірусологіїта імунології
РНК-ГЕНОМНІ ВІРУСИ
ОРТОМІКСОВІРУСИ,
ПАРАМІКСОВІРУСИ, РАБДОВІРУСИ.
2.
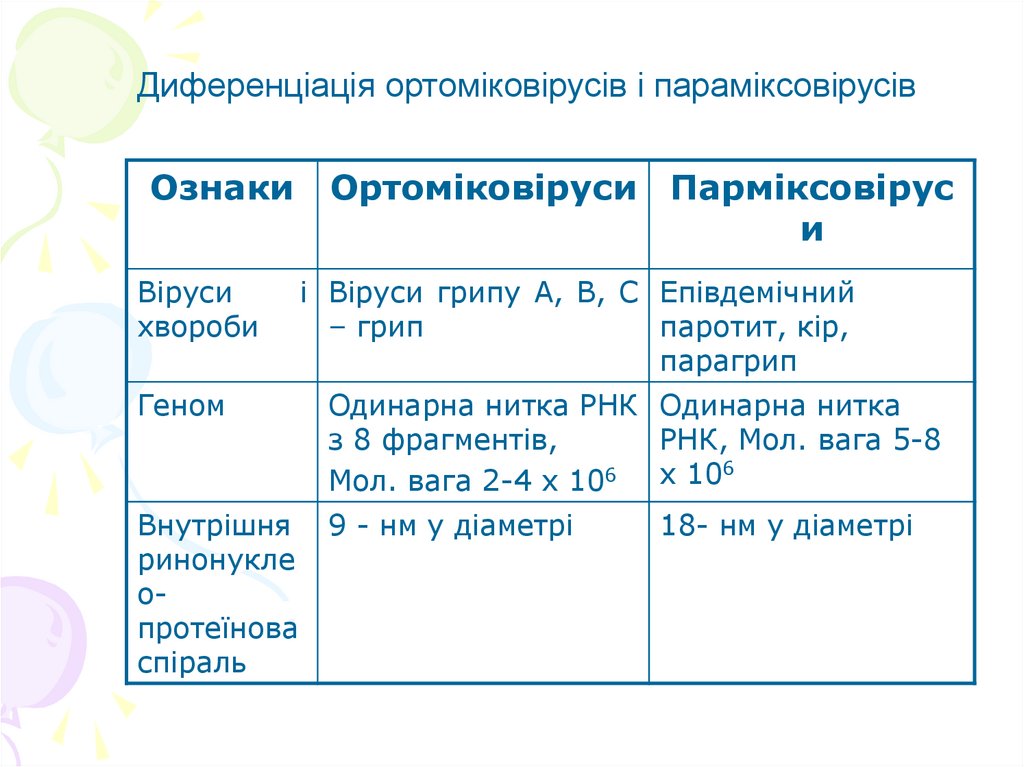
Диференціація ортоміковірусів і параміксовірусівОзнаки
Віруси
хвороби
Ортоміковіруси Парміксовірус
и
і Віруси грипу А, В, С Епівдемічний
– грип
паротит, кір,
парагрип
Геном
Одинарна нитка РНК Одинарна нитка
з 8 фрагментів,
РНК, Мол. вага 5-8
6
Мол. вага 2-4 х 106 х 10
Внутрішня
ринонукле
опротеїнова
спіраль
9 - нм у діаметрі
18- нм у діаметрі
3.
4.
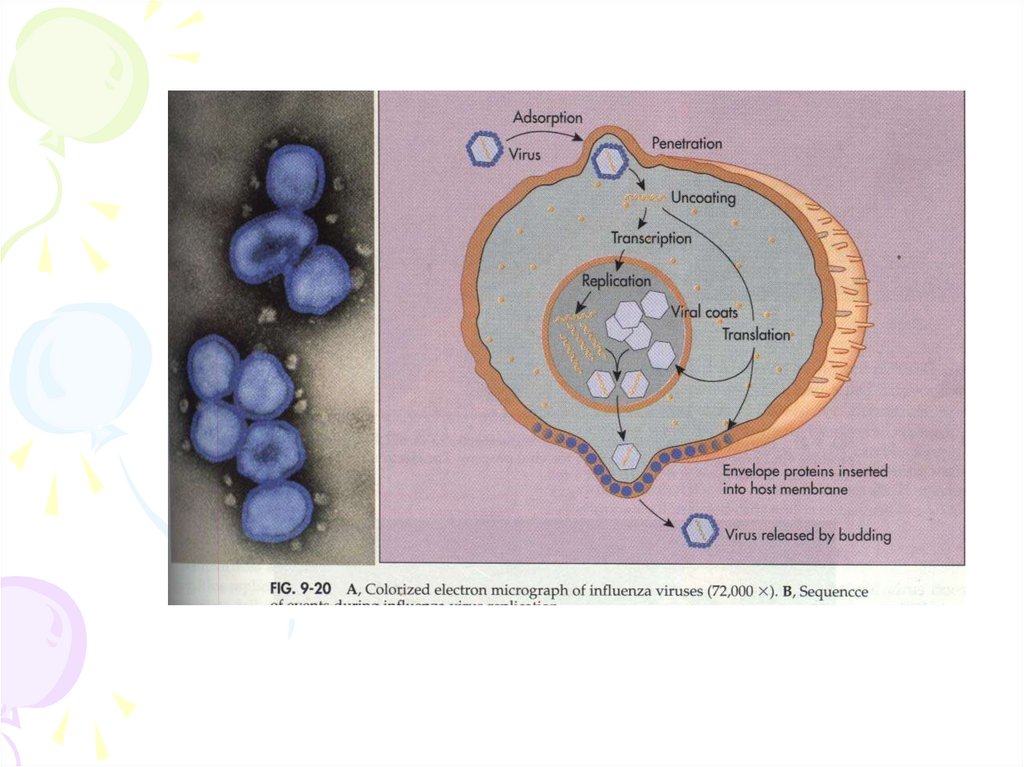
Нуклеокапсид складається з 8 фрагментів вРНК ікасидних білків, які утворюють спіралеподібний
тяж.
Кожний фрагмент транскрибується та реплікується
самостійно .
5.
6.
Гемаглютинін – тример з м.м. 225 кД (Н1-Р13)Функції:
-розпізнає клітинний рецептор – мукопептид,
який має N-ацетилнейрамінову (сіалову)
кислоту;
- забезпечує злиття мембрани віруса з
мембраною клітини та мембранами лізосом;
-визначає пандемічність вірусу (зміна
гемаглютиніну – причина пандемій, його
мінливість – епідемій грипу);
-- має виражені протективні властивості,
тобто сприяє формуванню імунітету.
7.
Нейрамінідаза (N) – тетрамер з м.в. 200-250 кД.(N1-N10)
Функції:
-забезпечує диссемінацію вірусів, відщеплюючи
нейрамінову кислоту від новосинтезованих
віріонів і мембрани клітини;
-- разом з гемаглютиніном забезпечує
пандемічні та ендемічні властивості вірусу;
--
8.
9.
10.
Антигенна мінливість вірусів грипу1. Дрейф-варіації. Відбувається селективний
відбір штамів із
зміненою антигенною
структурою (гемаглютиніну і нейрамінідази), які
продовжують викликати спалахи, доки до них не
з’являться антитіла. Такий дрейф підтримує
неперервність епідемій.
2. Шифт мінливість. Повна зміна гемаглютиніну
або нейрамінідази на інший.
Всі пандемії були викликані вірусам грипу А, у
яких відбулись шифт-зміни.
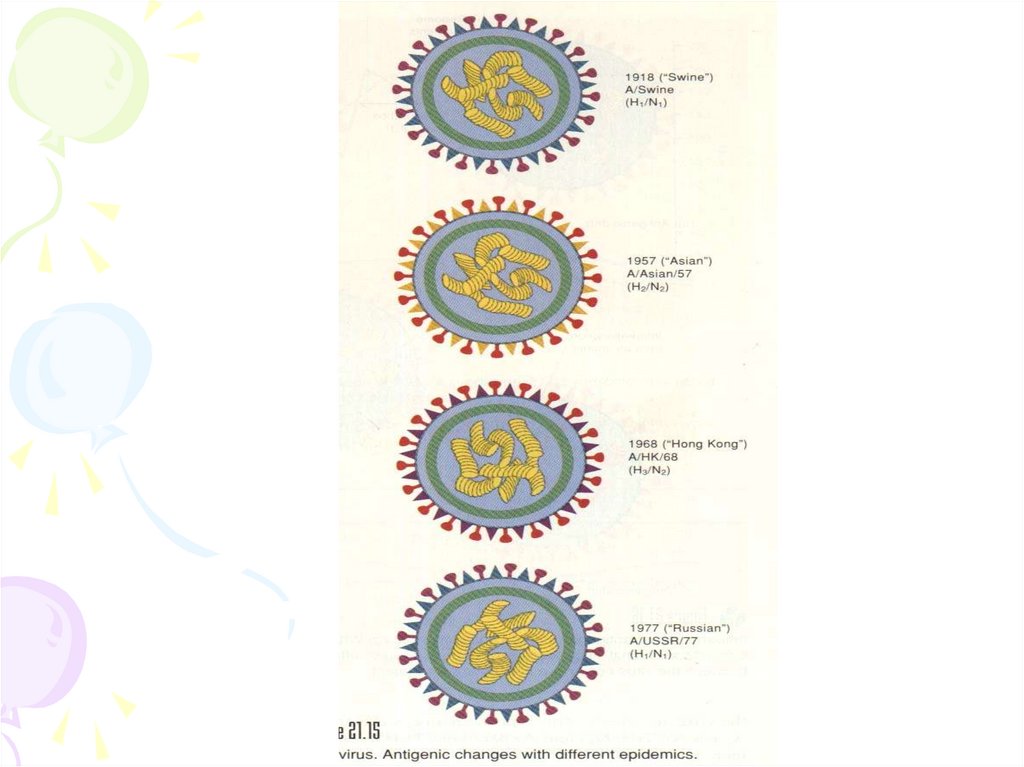
11.
1918 p. – N1H1 (загинуло 20 млн. чоловік)1957 – H2N2 (перехворіло понад ½ наседення
планети).
1968 р. – H3N2/
Встановлено, що грип у людини викликають віруси
із фенотипом H1N1, H2N2, H3N2/
Антигенні дрейфи та шифти – перешкода на шляху
створення вакцин.
Курячий грип – H5N1.
12.
13.
14.
15.
Лабораторна діагностика1. Вірусологічнй
(зараження
10-11 денних
курячих ембріонів (ідентифікація – РЗК. РГГА).
2. Імунофлуоресцентний метод (мазки-відбитки із
слизової носа і в змивах з ротоглотки).
3. ІФА для виявлення вірусних антигенів, ЛПР.
4. Серологічний метод (зростання титру антитіл у
парних сироватках – РЗК, РГГА, ІФА).
5. Визначення секреторних IgA в слині.
16.
Специфічна профілактика1. Жива вакцина з атенуйованих вірусів.
2. Вбита цільновіріонна вакцина.
3. Субвіріонна вакцина (із розщеплених
віріонів.
4. 4. Субодинична вакцина (містить тільки
гемаглютинін і нейрамінідазу
17.
Віруси грипу ВГеном складається з 8 фрагментів, які кодують 3
неструктурних і 7 структурних білків.
У наявності гемаглютинін і нейрамінідаза.
Віруси грипу С
Геном складається із
7 фрагментів. Кодує 2
неструктурних і 6 структурних білків.
Відсутня нейрамінідаза. Тому на поверхні один тип
шипів, які складаються з глікозованого пептиду gp88.
Він має дві функції: гемаглютиніну і нейрамінат-Оацетилестерази. Розпізнається іншими рецепторами
(мукопептидом з N-ацетил-9-О-ацетилнейраміновою
кислотою)
18.
Родини ParamyxoviridaeРоди: Paramyxovirus, Morbillivirus, Pneumovirus
Paramyxovirusus включає збудник епідемічного
паротиту, кору,віруси парагрипу, респіраторносинцитіальний вірус
19.
20.
ПараміксовірусиВіріони сферичної форми, діаметром 150-200 нм.
Геном
представлений
однонитковою
нефрагментованою негативною РНК з м.в. 5.6 МД, яка
складається із 6 генів.
З віріонною РНК пов’язаний білок NP і полімеразні білки
P і L. У їх складі є транскриптаза.
Є матричний білок.
Суперкапсид складається з ліпідного бішару та
глікозованих білків NP і F (fusion – злиття), які
виступають у вигляді шипів.
Білок NP має гемаглютинуючу та нейрамінідазну
активність, відповідаючи за зв’язування з клітинними
рецепторами.
21.
Білок F опосередкує три види активності:- гемоліз еритроцитів;
-злиття мембрани віруса з мембраною клітини та
її лізосомами;
- злиття клітин (за рахунок утворення синцитію
вірус розповсюджується з клітини до клітини).
-Віруси
не
потребують
для
транскрипції
затравочної мРНК, тому не проникають в ядро
клітини.
-Погано розмножуються в курячих ембріонах.
22.
Репродукуються в первинно трипсинізованихкультурах клітин, в яких виявляються з
допомогою феномену гемадсорбції.
Не мають спільного антигену для всієї родини
ВПГЛ
23.
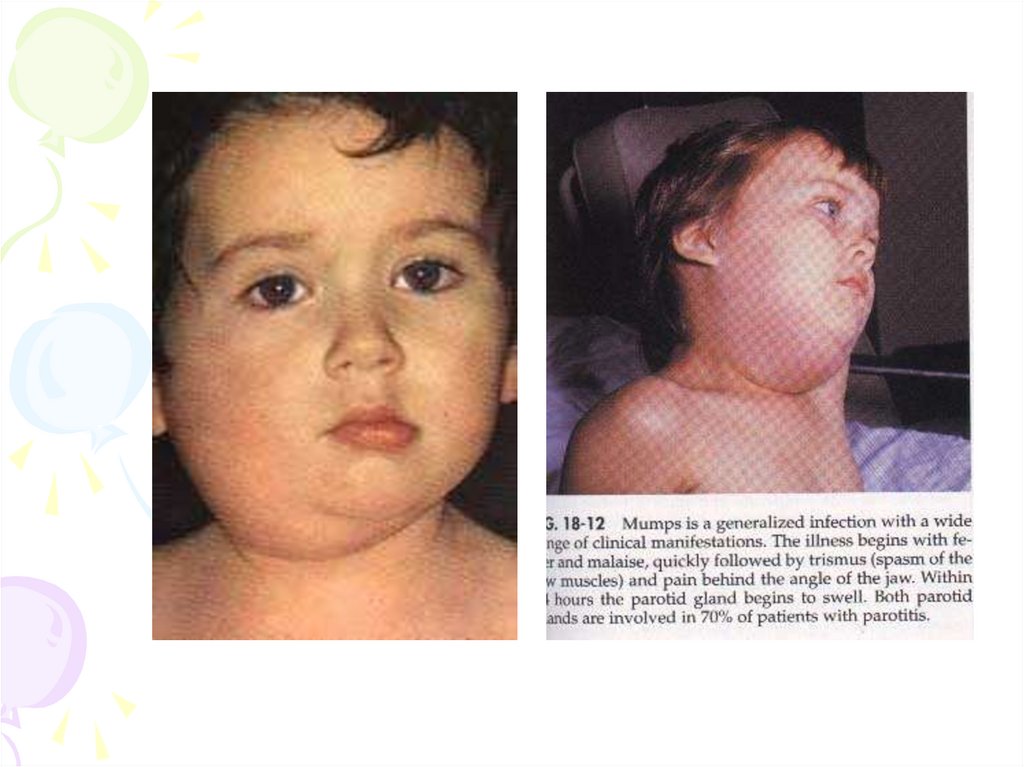
Вірус епідемічного паротитуЕпідемічний паротит – гостре інфекційне захворювання, яке
характеризується ураженням однієї або обидвох слинних
Властивості віруса
Складний вірус. Геном представлений нефрагментованою,
однонитковою, “мінус”-ниткою РНК, м.в. 8 МД.
У складі віріону 8 білків. Суперкапсидні білки HN i F виконують ті
ж самі функції, що й в інших параміксовірусів.
Вірус має гемаглютинуючу, гемолітичну, нейрамінідазну та
симпластоутворюючу активність.
24.
Багатоядерні клітини (синцитій)25.
Особливості епідеміологіїДжерело інфекції – хвора людина
Механізм зараження – повітряно-краплинний
Інкубаційний період – 14-21 день
Вірус проникає з порожнини рота через стенонову
протоку в навколовушну слинну залозу, де він
репродукується
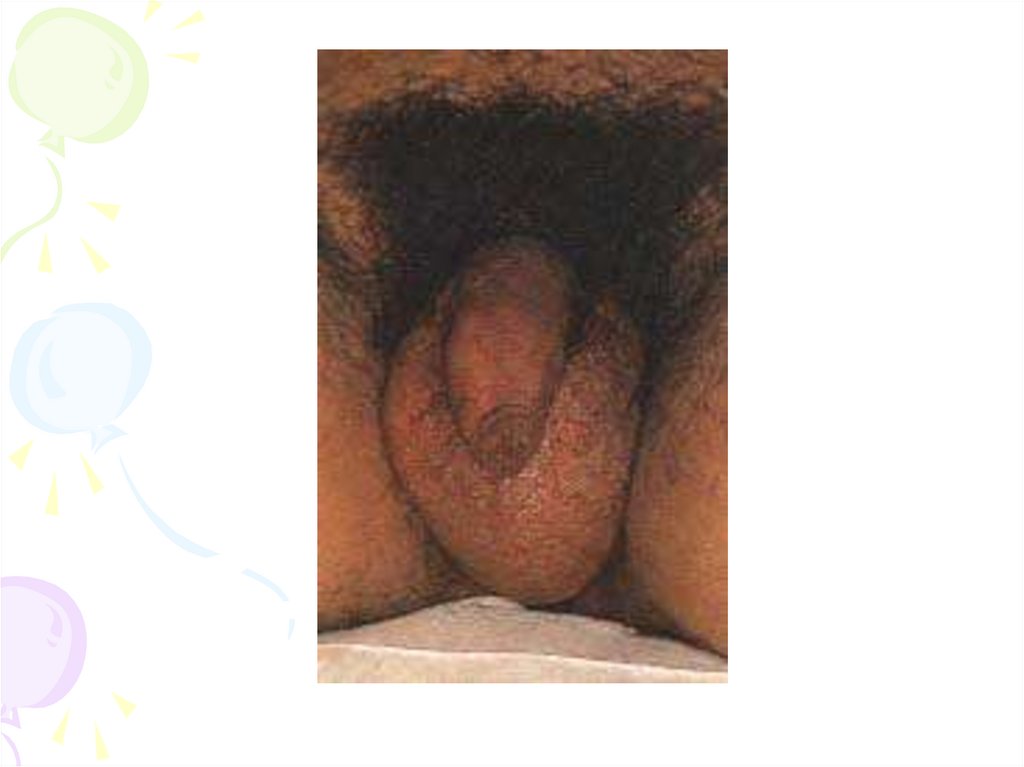
Поступаючи у кров, може проникнути в різні органи
(яєчки, яйники, підшдункову та щитоподібну
залозу, мозок), викликаючи орхіт, менінгіт,
менінгоенцефаліт, тиреоїдит, поліартрит, нефрит,
панкреатит.
26.
27.
28.
Лабораторна діагностика:Вірусологічна: матеріал -слина, сеча,
спиномозкова рідина, пунктат залоз; заражають
7-8 денні курячі ембріони.
Вірус типують у РГГА (РГГад), ІФА,
імунофлуоресценції, нейтралізації, РЗК.
Серологічна: матеріал – парні сироватки.
РГГА, РЗК.
29.
Специфічна профілактика – жива атенуйована(пасажі на курячих ембріонах) вакцина
30.
Віруси парагрипуСферична форма. Діаметр 150-200 нм.
Геном представлено однонитковою нефрагментованою
негативною ниткою РНК, м.м. 5,6 МД. Геном
складається із 6 генів.
З віріонною РНК пов’язаний білок NP і полімеразні білки
P і L. У їх складі є транскриптаза.
Є матричний білок.
Суперкапсид складається з ліпідного бішару та
глікозованих білків NP і F (fusion – злиття), які
виступають у вигляді шипів.
Білок NP має гемаглютинуючу та нейрамінідазну
активність, відповідаючи за зв’язування з клітинними
рецепторами.
31.
Parainfluenza 1Включає вірус Сендай, патогенний для новонароджених і
свиней) і гемадсорбуючий вірус типу 2 (НА-2).
Спричиняють круп (ларинготрахеїт) у дітей, гострий риніт,
бронхіт, фарингіт, бронхіоліт, пневмонію.
Parainfluenza 2
Викликають круп у дітей.
Parainfluenza 3
Гемадсорбуючий вірсу типу 1
ураження дихальної системи,
пневмонію.
(НА-1). Спичиняє
круп, бронхіоліт,
32.
Parainfluenzavirus 4 і 5Поки не доведена їх остаточна роль у виникненні
захворювань у людини.
33.
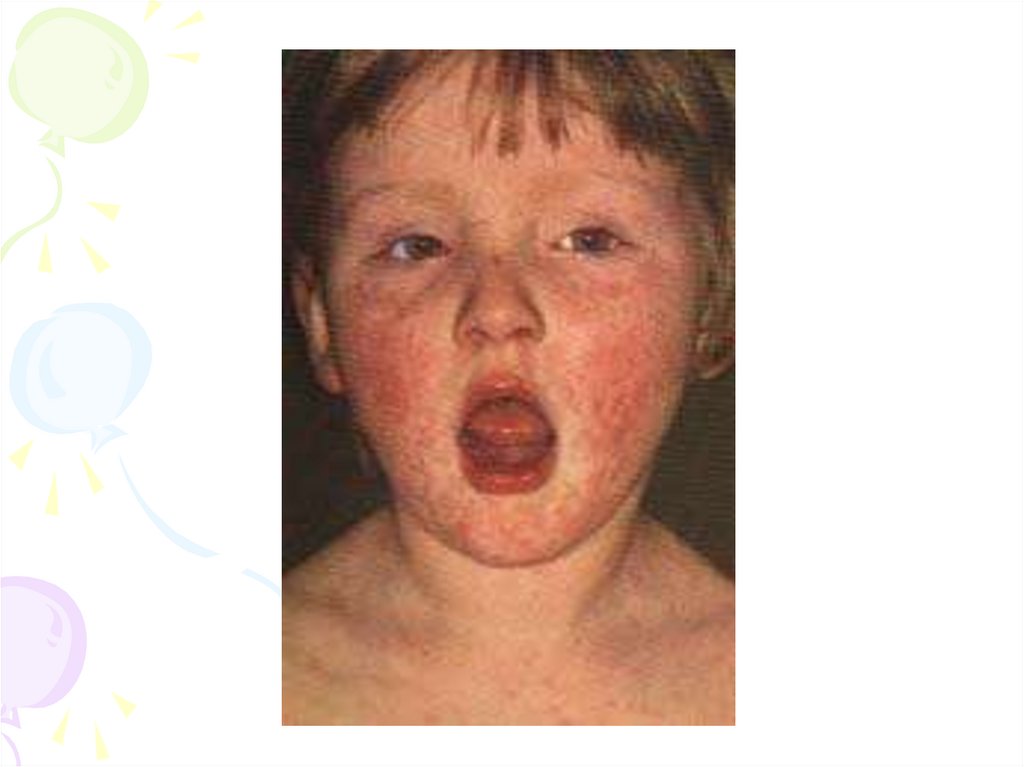
Віруси коруКір
гостре
інфекційне
захворювання,
яке
характеризується інтоксикацією, макуло-папулярною
висипкою, гарячкою та респіраторними симптомами
Властивості вірусу
Діаметр віріону 150-250 нм.
Геном представлено негативною однонитковою РНК.,
яка кодує 6 стректурних білків: білки нуклеокапсиду NP, P, L (білки полімеразного комплексу з
транскриптазою), М-білок, два глікозованих білка, які
входять до складу суперкапсиду – Н (гемаглютинін) і F
(білок злиття, гемолізин).
Вірус
має
гемаглютинуючу,
симпластоутворюючу активність.
Не має нейрамінідази.
гемолітичну,
34.
35.
Гемаглютинін,гемолізин,
нуклеопротеїд,
матриксний білок розрізняються за антигенною
специфічністю та імуногенністю.
Найвища імуногенність у гемаглютиніну.
Він має спільні антигенні детермінанти з вірусами
чуми собак, і чуми великої рогатої худоби.
36.
У курячих ембріонах розмножується погано.Культивування: певинно-трипсинізовані клітини
нирок мавп, ембріону людини.
Вірус викликає характерну цитопатичну дію:
утворення гігантських багатоядерних клітин –
симпластів і синцитіїв – та зернисті включення в
цитоплазмі та ядрі.
Може спричиняти мутагенну дію на хромосоми
клітин.
37.
Особливості патогенезу і клініки коруІнкубаційний період – біля 10 днів.
Джерело інфекції – хвора людина
Механізм зараження – повітряно-краплинний. Може бути
трансплацентарний механізм.
Вірус розмножується в епітеліальних клітинах слизової
носоглотки, трахеї, бронхів. Проникаючи в кров, викликає
появу висипки.
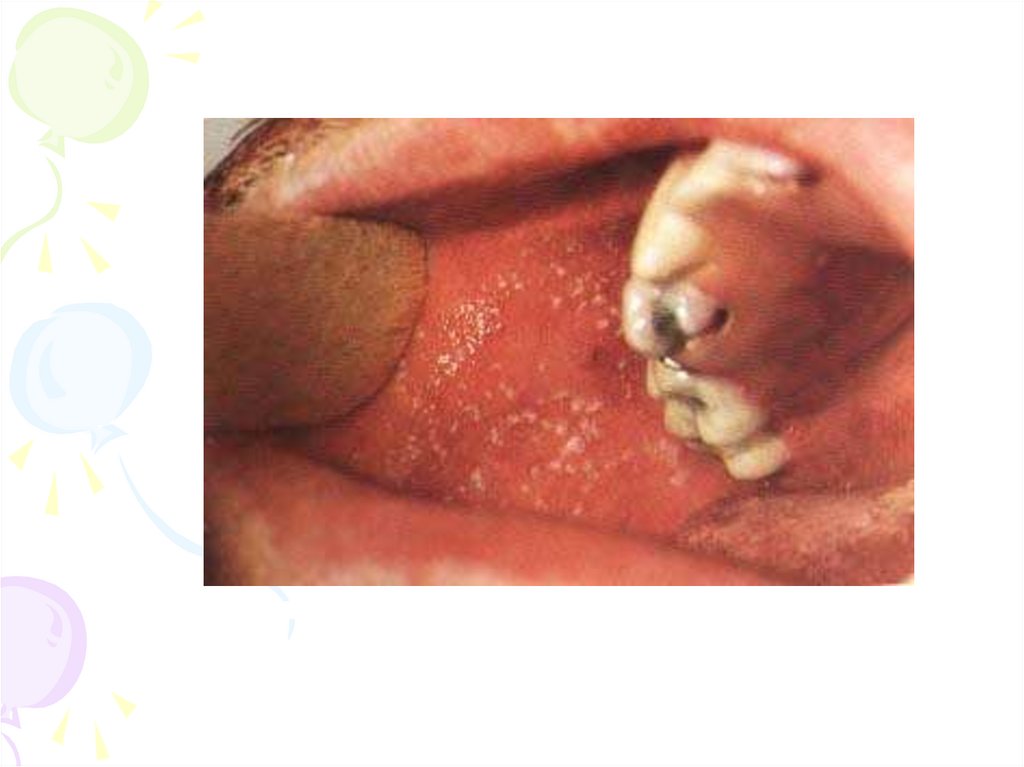
На слизовій щік – плями Копліка-Філатова.
У продромальному періоді – явища ГРЗ (риніт, фарингіт,
кон’юнктивіт.
Ускладнення – пневмонія, набряк гортані, рідко гострий
коровий енцефаліт.
У результаті демієлінізації нервових волокон – підгострий
склерозуючий паненцефаліт.
38.
Специфічна профілактика: жива вакцина затенуйованих штамів (Л-16). Проводять
одноразово, підшкірно на 1-ому році життя.
Імуноглобулін.
39.
40.
41.
42.
43.
44.
Респіратрно-синцитіальний вірусСферична форма, діаметр 120-200 нм.
Геном представлено однонитковою,
нефрагментованою, негативною РНК, м.в. – 5,6МД.
Несе 10 генів, які кодують 10 вірусспецифічних білків,
з яких 7 входять до складу віріону, решта –
неструктурні.
Віруси не мають гемаглютиніну, нейрамінідази,
гемолітичної активності
45.
Вірус гарно розмножується в клітинах HeLA, Hep-2та ін. з появою цитопатичної дії, а ткаж з
формуванням біляшок.
Не культивується в курячих ембріонах.
46.
ЕпідеміологіяДжерело інфекції - хвора людина.
Механізм зараження – повітряно-краплинний
Інкубаційний період - 3-5 днів.
Вірус розмножується в епітеліальних клітинах
верхніх дихальних шляхів.
Особливо небезпечний для дітей перших 6 місяців
життя, викликаючи бронхіт, бронхіоліт, пневмонію.
47.
48. ЧОМУ ПЕЧІНКА ТАКА ВАЖЛИВА ДЛЯ ОРГАНІЗМУ? Розкладає і видаляє з організму шкідливі субстанції, такі як алкоголь або хімічні
отрутиВиробляє холестерин
Синтезує хімічні субстанції, які спричиняють
згортання крові
Виробляє жовч, яка допомагає в травленні
Синтезує нові білки ( необхідні для приросту
тіла і загального здоров’я)
Контролює об'єм крові
Містить і контролює резервний запас заліза,
вітамінів, цукру, жирів та інших
мінералів, які ми споживаємо з їжею і робить
їх доступними для організму при необхідності
Печінка це головне джерело тепла організму
49. РодинаPicornaviridae Вірус гепатиту А 27 нм +РНК Нуклеокапсид кубічного типу симетрії, містить 60 капсомерів, суперкапсид
HAV+РНК
КАПСИД
РодинаPicornaviridae
Вірус гепатиту А 27 нм
+РНК
Нуклеокапсид кубічного типу
симетрії, містить 60 капсомерів,
суперкапсид відсутній, стійкий до
ефіру, органічних розчинників
Єдиний вірус гепатиту, що
культивується на культурах
клітин людини і мавп.
Дуже резистентний. Витримує
нагрівання при 60 °С протягом
години, формальдегід 1:4000 –
72 год, інактивується при
кип’ятінні через 1 хв.
50.
Джерело інфекції: хворалюдина, вірусоносій
Шлях передачі: фекальноСпецифічнимиоральний
кінцевими факторами
передачі збудника є харчові продукти (м’ясні,
молочні, хлібні) та вода.
Проміжними факторами можуть бути мухи,
забруднена фекаліями вода, що використовується
для миття посуду, руки людей, які готують їжу.
Інкубаційний період: 2-6 тижні
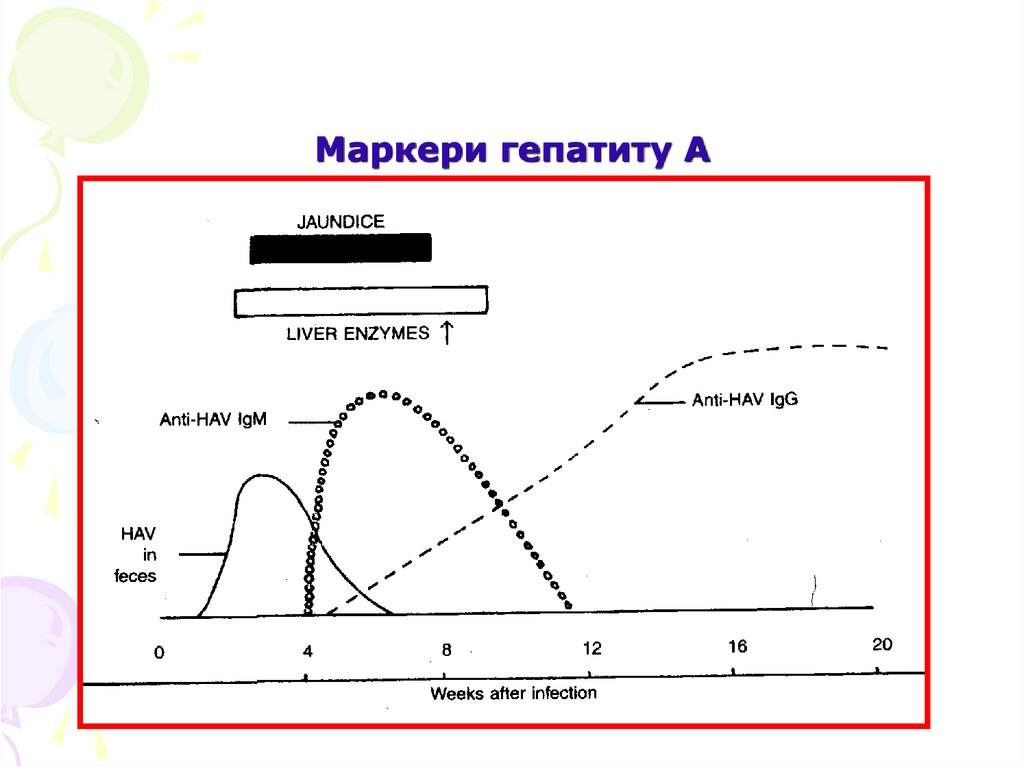
51. Маркери гепатиту А
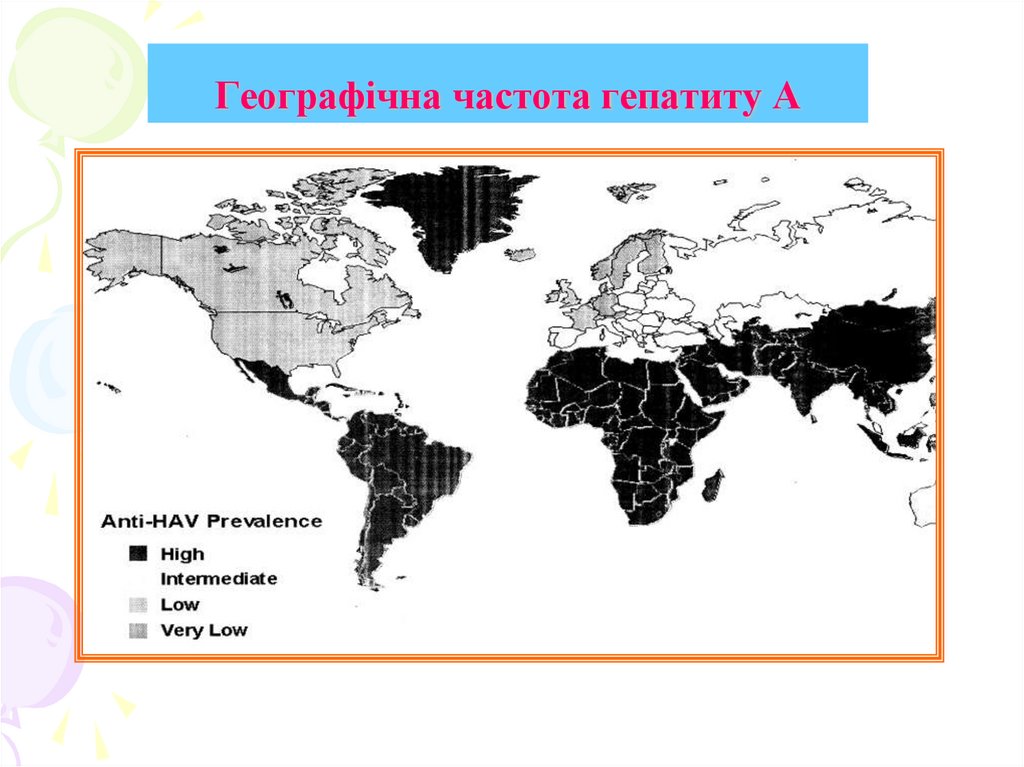
52. Географічна частота гепатиту А
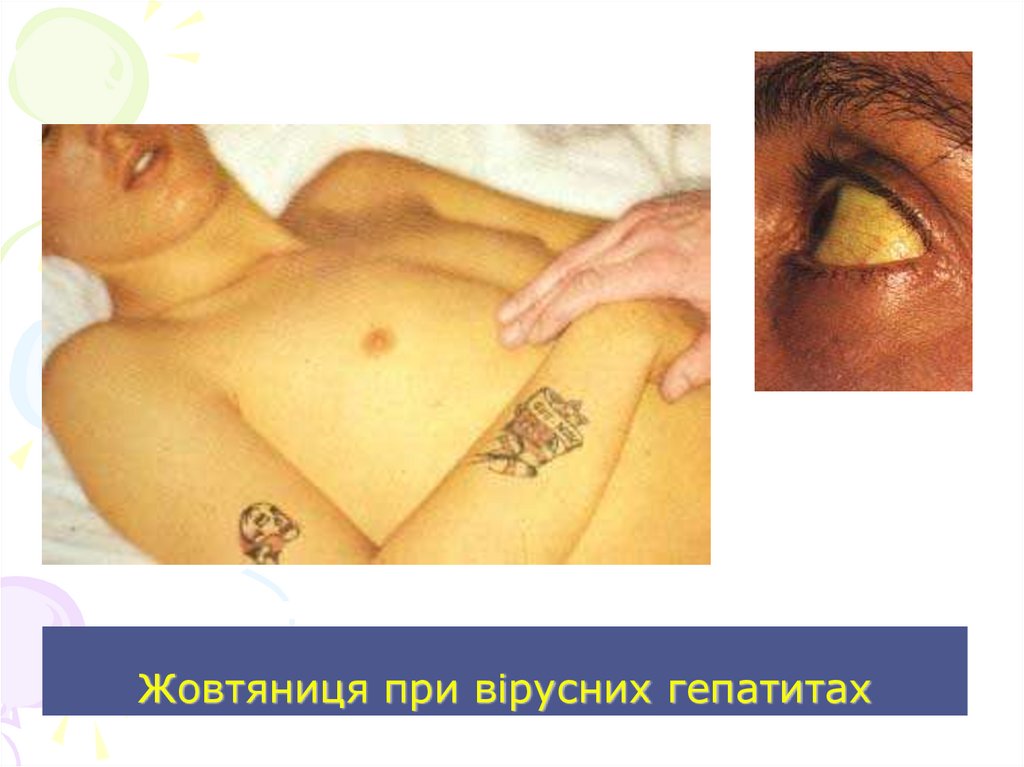
53. Жовтяниця при вірусних гепатитах
54. Вірусологічна діагностика і специфічна профілактика
• Вірус можна виявити у пізньому інкубаційномуперіоді і в преіктеричній стадії, рідко пізніше,
використовуючи ІЕМ екстрактів фекалій.
• Практичні лабораторії, в основному,
використовують ІФА для виявлення анти-ГАВ IgM i
анти-ГАВ IgG.
• Для пасивної специфічної профілактики вживають
нормальний людський імуноглобулін до зараження
або в ранньому інкубаційному періоді.
• Для специфічної активної профілактики
використовують інактивовану формаліном,
адсорбовану на гідроокису алюмінію вакцину,
вирощену на людській диплоїдній культурі клітин
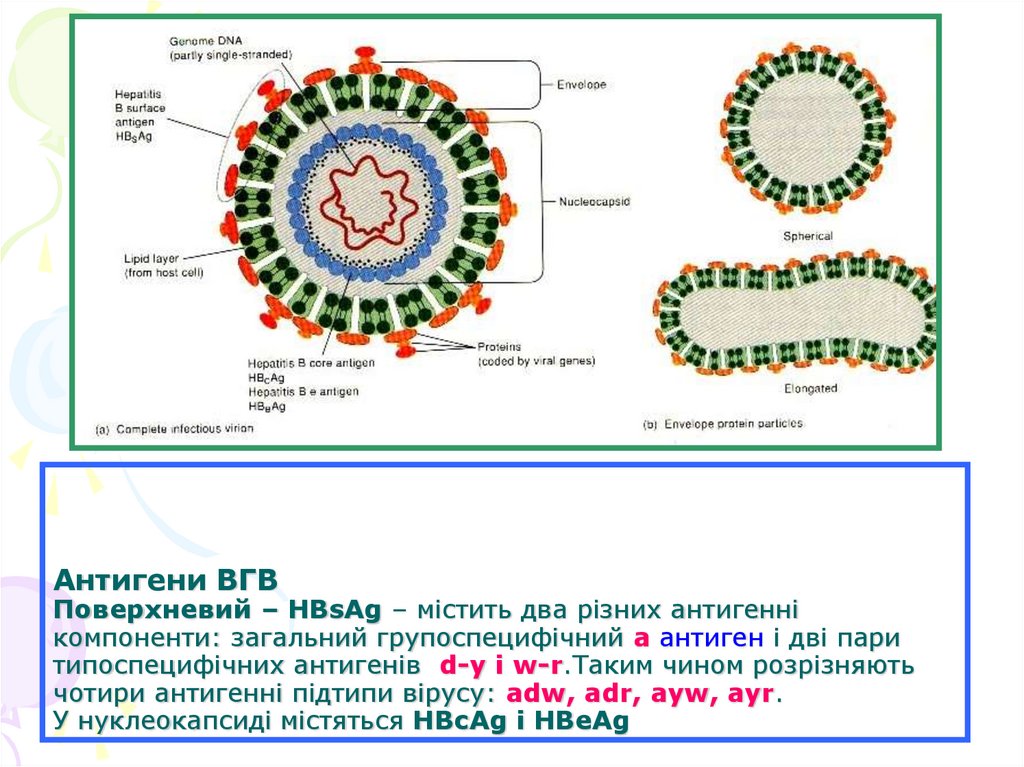
55. Родина Hepadnaviridae Вірус гепатиту В
Під електронним мікроскопом розрізняють три типи віруснихчасточок: сферичні діаметром 22 нм і тубулярні діаметром 22 нм,
але різної довжини. Антигенно вони ідентичні – містять
поверхневий антиген вірусу.
Третій тип це повноцінний вірус, який має нуклеокапсид і
суперкапсид. Його діаметр - 42 нм.
ДНК – циркулярної конфігурації, один - зовнішній мінус ланцюг
кільцевий, другий - внутрішній плюс ланцюг, короткий, має
розрив, з ним пов’язана вірусна ДНК полімераза, яка володіє ДНК
залежною ДНК полімеразною і РНК залежною зворотньою
транскриптазною функціями.
Вона відновлює розірвану ділянку ДНК, яка стає повноцінною
двохспіральною ДНК.
56. Антигени ВГВ Поверхневий – HBsAg – містить два різних антигенні компоненти: загальний групоспецифічний a антиген і дві пари
типоспецифічних антигенів d-y і w-r.Таким чином розрізняютьчотири антигенні підтипи вірусу: adw, adr, ayw, ayr.
У нуклеокапсиді містяться HBсAg і HBеAg
57.
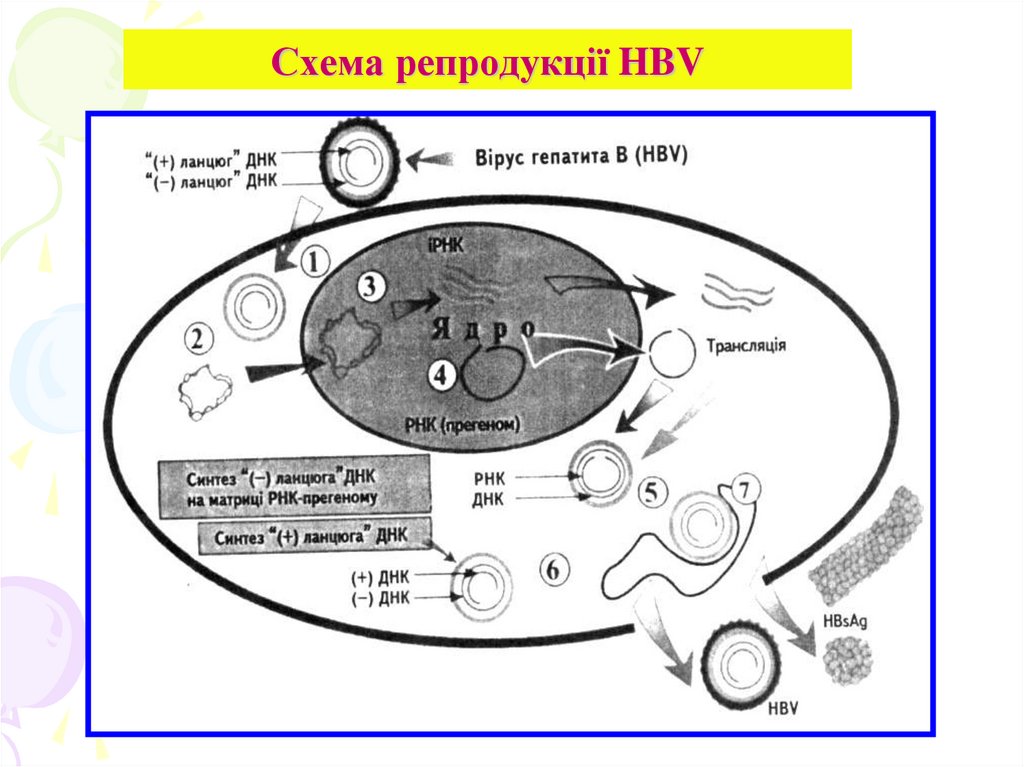
Основні гени вірусу: S, С, Х, Р.Ген S кодує поліпептиди HBsAg
Ген С кодує білки нуклеокапсиду HBсAg і HBеAg
Ген Х є активатором усіх генів ГБВ, а також клітинних
промоторів, кодує білок Х. Ген Х був знайдений в
ядрах клітин гепатокарциноми. У цих хворих
виявляють і антитіла до білку гена Х.
Ген Р, який охоплює 80 % “ - ланцюга геному і
частково перекриває усі інші гени, кодує полімеразу,
якій притаманні три ензиматичні функції (ДНК
полімерази,
зворотньої
транскриптази
і
рибонуклеази).
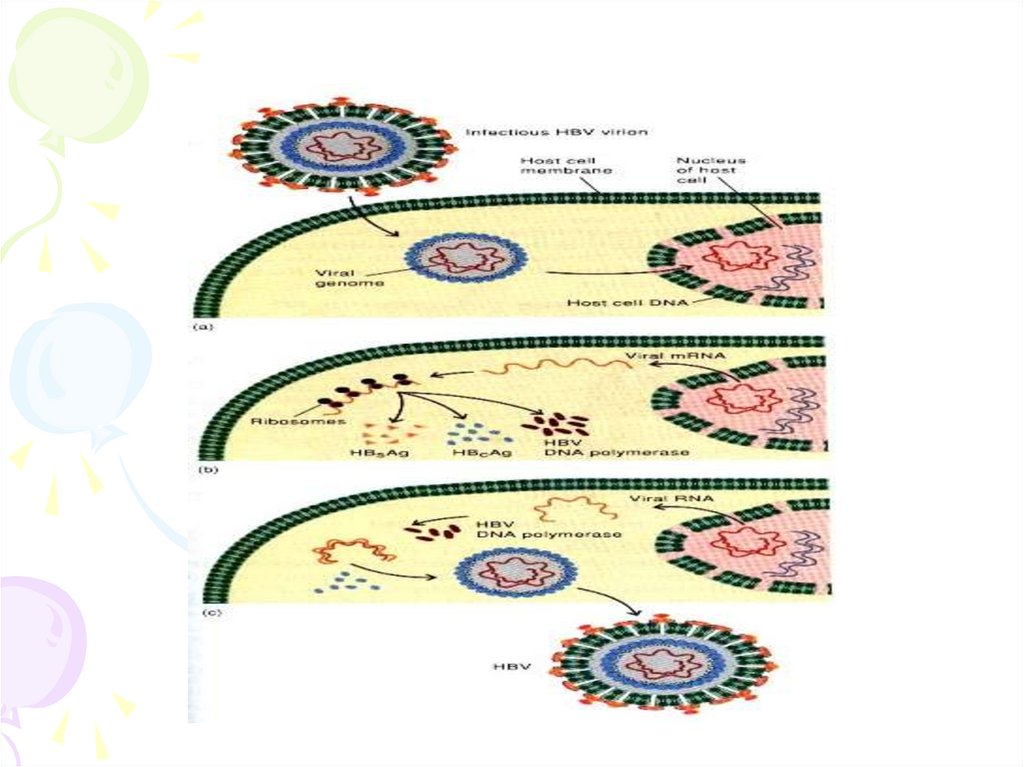
58. Схема репродукції HBV
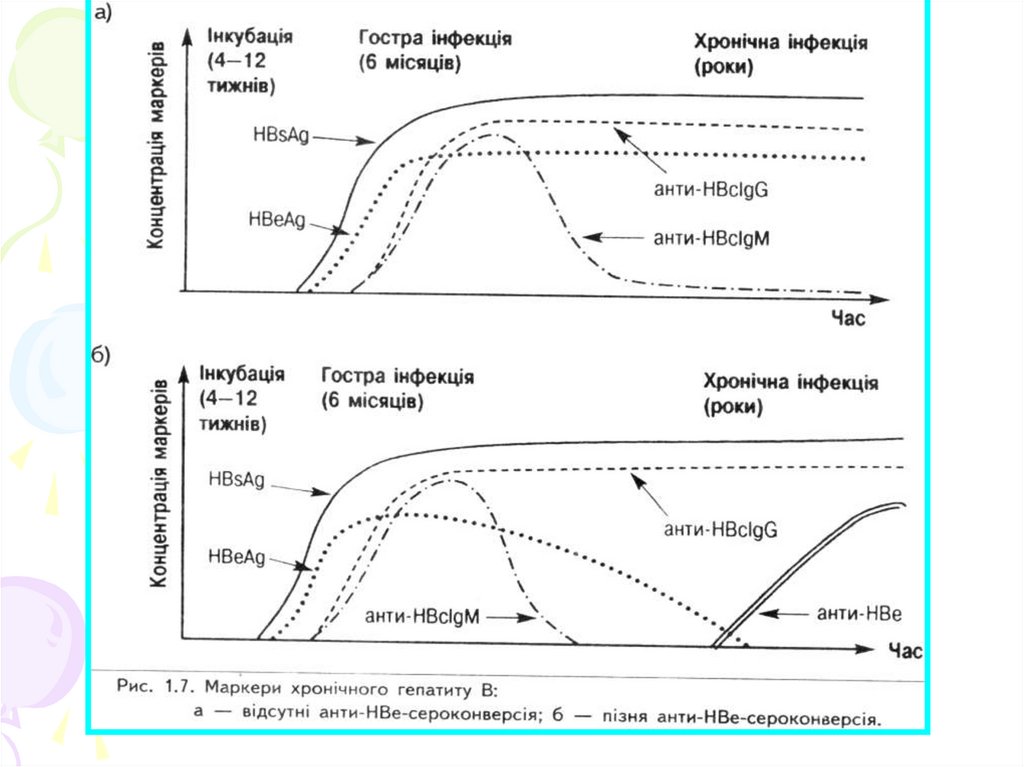
59.
60.
61.
62. Шляхи інфікування HBV в США
63. Гепатит В в Україні (на 100 тис. населення)
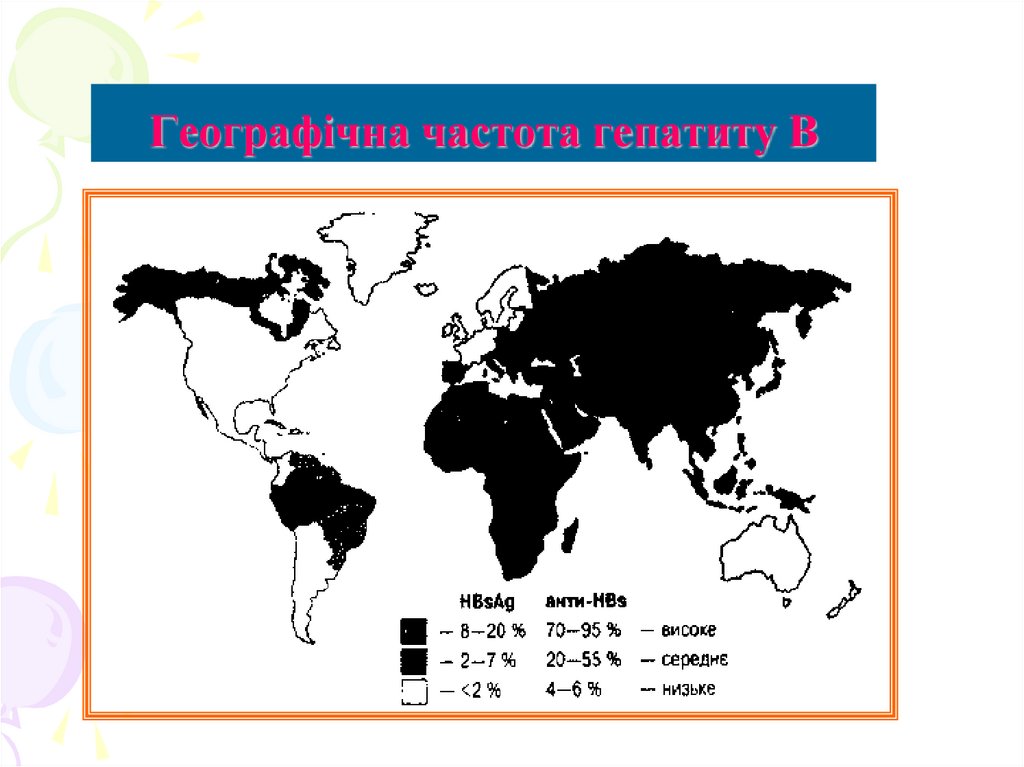
64. Географічна частота гепатиту В
65.
• Руйнування інфікованих гепатоцитіввідбувається, основним чином, за
допомогою клітинних імунних реакцій,
опосередкованих Т-лімфоцитами,
природними кілерами (NK і К клітинами) апоптоз, макрофагами та за допомогою
різноманітних цитокінів. Лізис інфікованих
вірусом гепатоцитів Т – лімфоцитами є
тільки першою ланкою в складному
комплексі ураження печінки.
• В процесі руйнування інфікованих
гепатоцитів з них виходять вірусні
антигени (HBcAg, HBeAg, HBsAg), які, в
свою чергу, стимулюють імунну систему до
утворення специфічних антитіл (анти-HBc
IgM,анти-HBc IgG, анти-HBe, анти-HBs).
66.
ПрисутністьHBeAg у вільному стані
пригнічує як клітинний, так і гуморальний
імунітет. Блокуючи утворення гамаінтерферону, він тим самим гальмує
пізнання Т-клітинами вірусних антигенів та
утворення специфічних антитіл Влімфоцитами. Це, в свою чергу, затримує
швидке виведення HBV із організму.
Звільнення гепатоциту від вірусу
відбувається шляхом його руйнування. З
появою специфічних антитіл утворюються
імунні комплекси, які захоплюються
макрофагами і виводяться нирками.
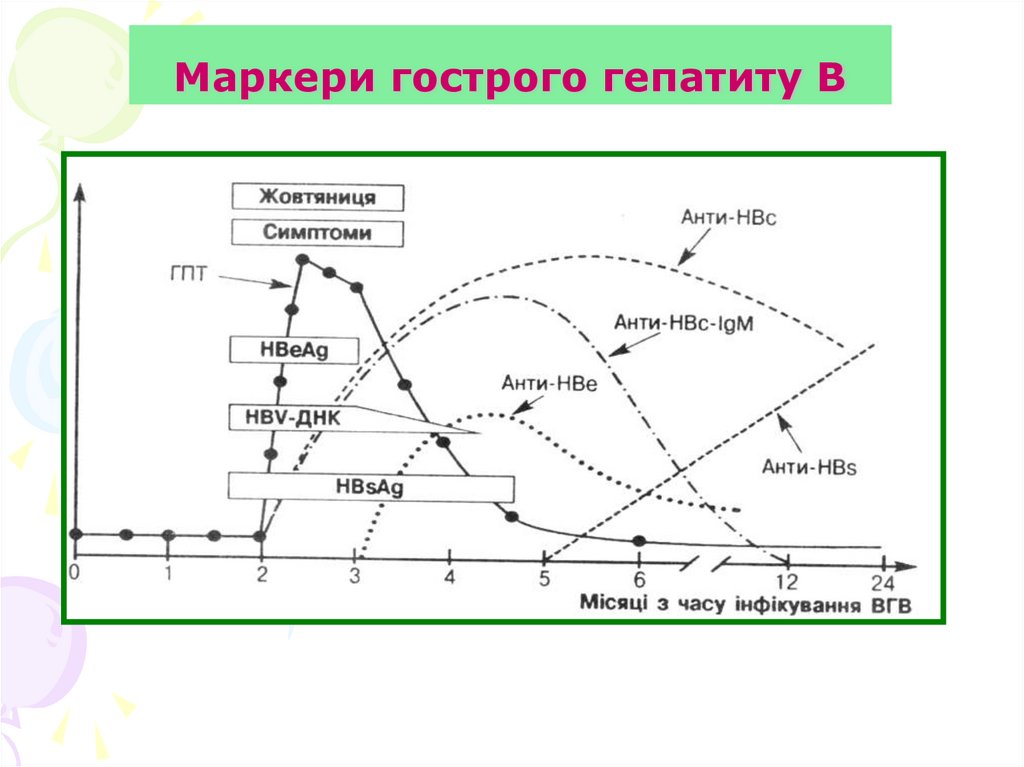
67. Маркери гострого гепатиту В
68.
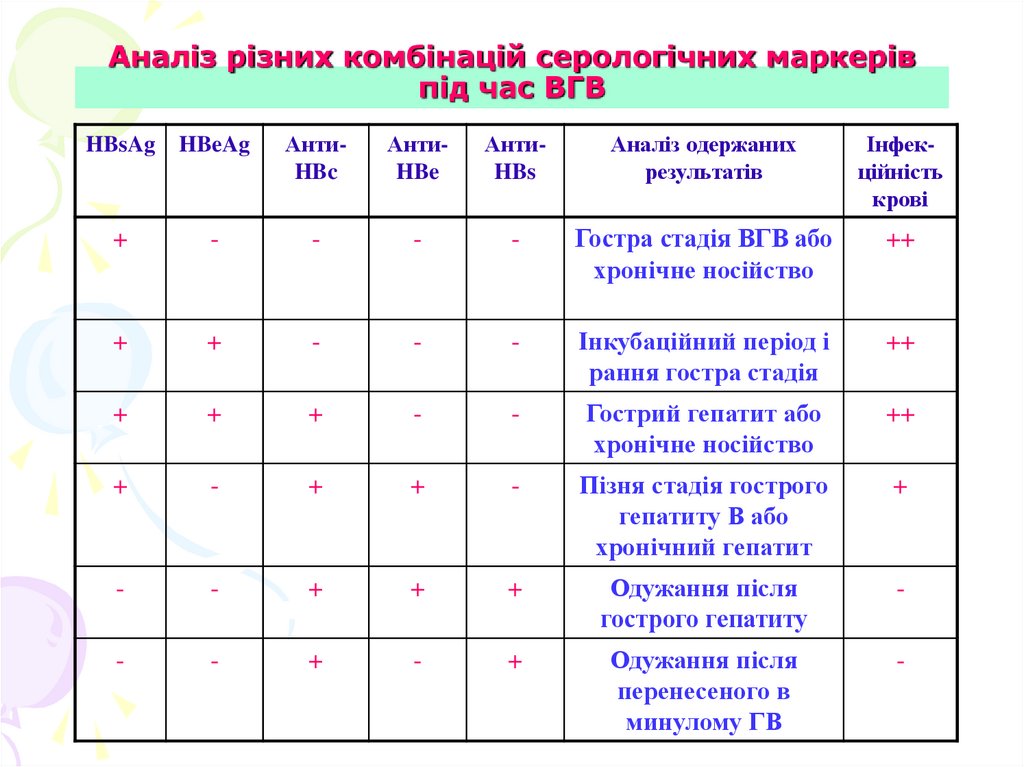
69. Аналіз різних комбінацій серологічних маркерів під час ВГВ
HBsAgHBeAg
АнтиHBc
АнтиHBe
АнтиHBs
Аналіз одержаних
результатів
Інфекційність
крові
+
-
-
-
-
Гостра стадія ВГВ або
хронічне носійство
++
+
+
-
-
-
Інкубаційний період і
рання гостра стадія
++
+
+
+
-
-
Гострий гепатит або
хронічне носійство
++
+
-
+
+
-
Пізня стадія гострого
гепатиту В або
хронічний гепатит
+
-
-
+
+
+
Одужання після
гострого гепатиту
-
-
-
+
-
+
Одужання після
перенесеного в
минулому ГВ
-
70. Ознаки імунітету до HBV
71. Характеристика комбінованих вакцин проти гепатиту В, зареєстрованих в Україні
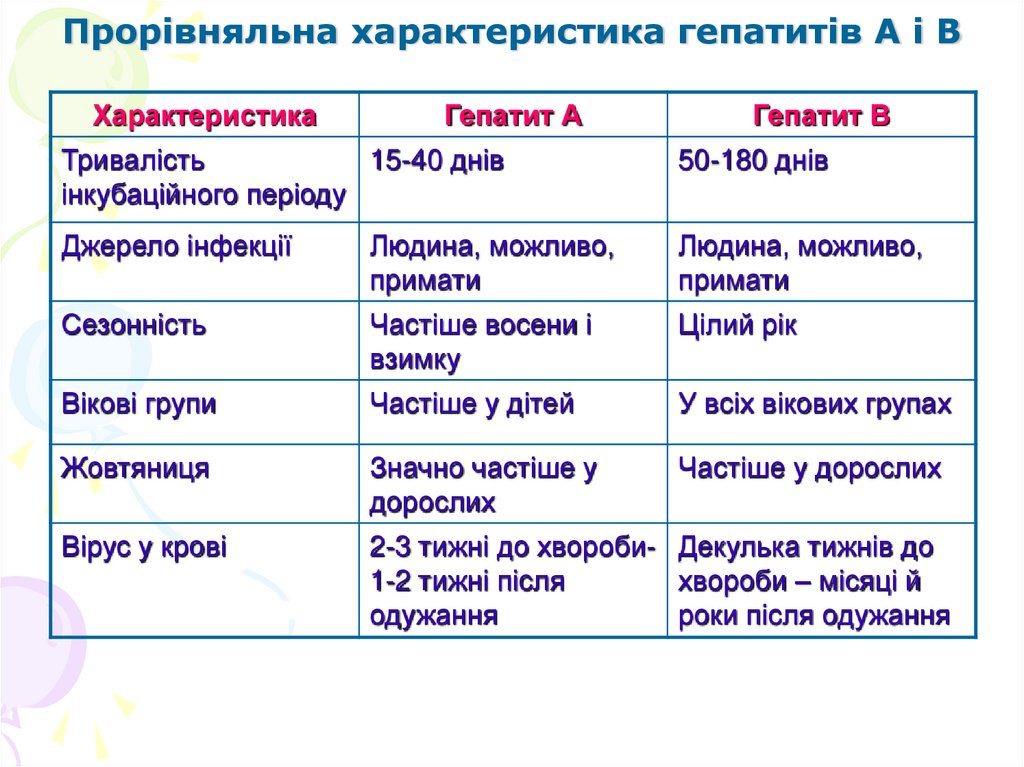
72. Прорівняльна характеристика гепатитів А і В
ХарактеристикаГепатит А
Гепатит В
Тривалість
15-40 днів
інкубаційного періоду
50-180 днів
Джерело інфекції
Людина, можливо,
примати
Людина, можливо,
примати
Сезонність
Частіше восени і
взимку
Цілий рік
Вікові групи
Частіше у дітей
У всіх вікових групах
Жовтяниця
Значно частіше у
дорослих
Частіше у дорослих
Вірус у крові
2-3 тижні до хвороби- Декулька тижнів до
1-2 тижні після
хвороби – місяці й
одужання
роки після одужання
73.
ХарактеристикаГепатит А
Гепатит В
Вірус у фекаліях
2-3 тижні до
хвороби- 1-2
тижні після
одужання
Рідко присутній
або у невеликій
кількості
Розмір вірусу
27-32 нм
42 нм
Діагностика
базується на
Тести
функціонального
стану печінки,
клінічні
симпитоми,
анамнез
Тести
функціонального
стану печінки,
клінічні
симпитоми,
анамнез, наявність
HBsAg у крові
Ефективна
вакцина
Немає
Є
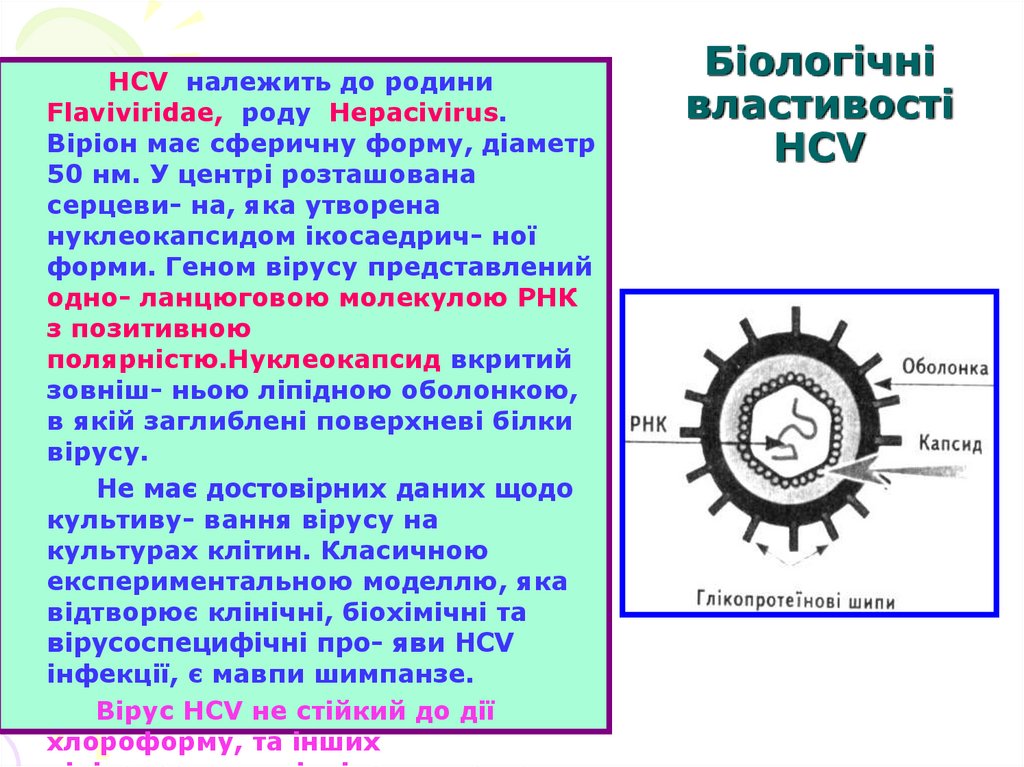
74. Біологічні властивості HCV
HCV належить до родиниFlaviviridae, роду Hepacivirus.
Віріон має сферичну форму, діаметр
50 нм. У центрі розташована
серцеви- на, яка утворена
нуклеокапсидом ікосаедрич- ної
форми. Геном вірусу представлений
одно- ланцюговою молекулою РНК
з позитивною
полярністю.Нуклеокапсид вкритий
зовніш- ньою ліпідною оболонкою,
в якій заглиблені поверхневі білки
вірусу.
Не має достовірних даних щодо
культиву- вання вірусу на
культурах клітин. Класичною
експериментальною моделлю, яка
відтворює клінічні, біохімічні та
вірусоспецифічні про- яви HCV
інфекції, є мавпи шимпанзе.
Вірус HCV не стійкий до дії
хлороформу, та інших
Біологічні
властивості
HCV
75. Вірус гепатиту C
76. Маркери вірусного гепатиту С
77.
• Основним джерелом цієї інфекції є хворі нагострий гепатит С з безжовтяничним
перебігом та хворі на хронічний гепатит С.
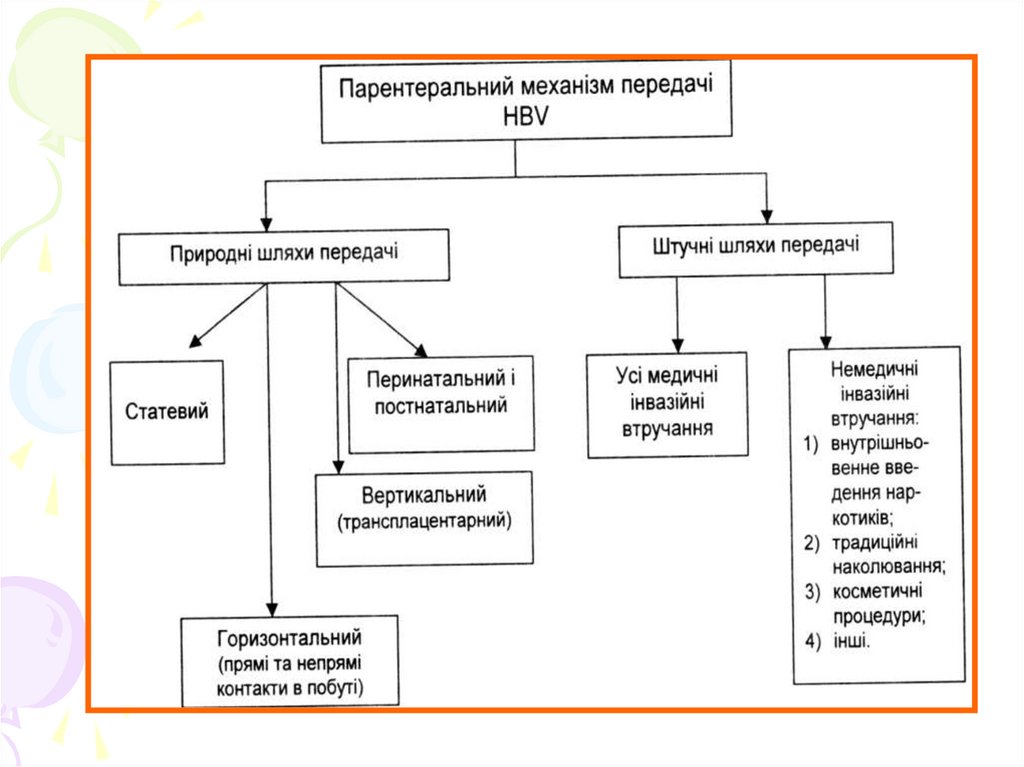
• Основний шлях передачі – парентеральний.
Це хвороба ін’єкційних споживачів
психотропних наркотичних препаратів;
хворих, які потребують переливання крові
та її препаратів; хворих, що перебувають на
гемодіалізі тощо.
78. Чинники ризику інфікування у хворих на хронічний гепатит С у Росії
79.
• HСV характеризується безмежною мінливістюсвоєї антигенної структури, що лежить в основі
хронізації хвороби.
• Еволюція наслідків інфікування HСV не
оптимістична: гострий гепатит з жовтяницею
спостерігають у 10-20% хворих, в інших випадках
його не діагностують у зв’язку з легким
безжовтяничним перебігом, але майже у 80% осіб
розвивається хронічний гепатит з прогресуванням
фіброзу у 30-40% хворих. Останній закінчується
розвитком цирозу печінки (у 20-30% осіб) та
гепатоцелюлярної карциноми у кожного третього
з хворих на цироз.
80.
Лабораторна діагностика гепатиту С базуєтьсяна виявленні підвищеного рівня біохімічних
показників (АлАт) та виявленні специфічних
маркерів інфікування: анти НСV у ІФА та РНК
НСV у ПЛР.
Лікування: пролонгований альфа-інтерферон
(Пегасис) у комбінації з рибавірином.
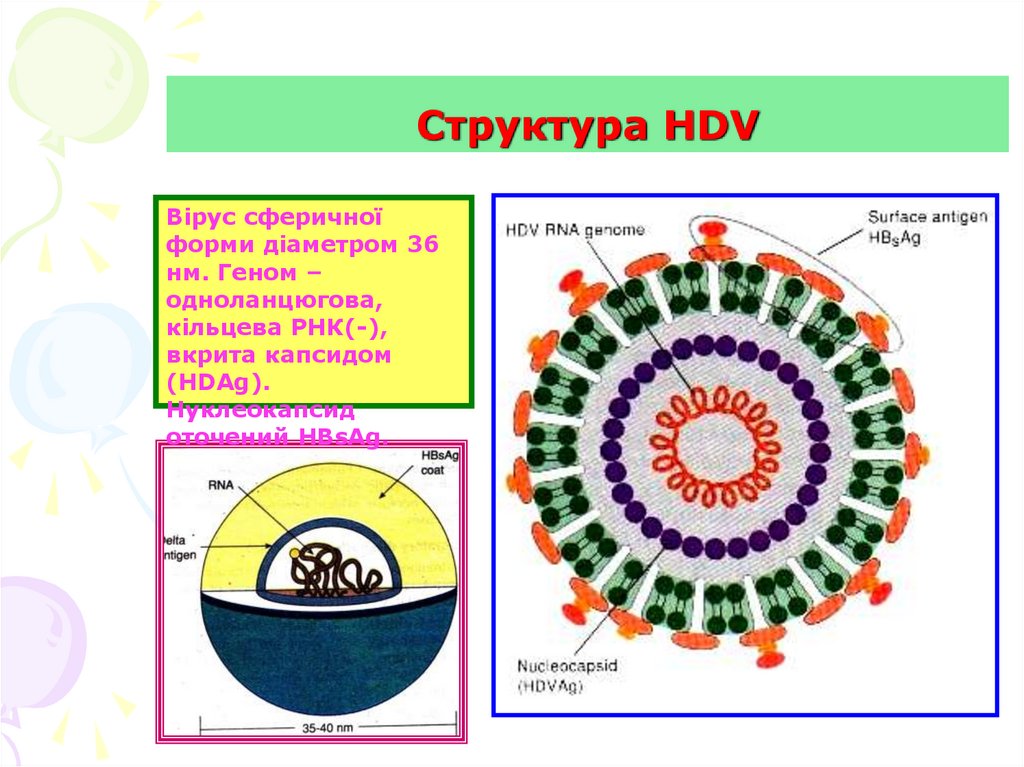
81. Cтруктура HDV
Вірус сферичноїформи діаметром 36
нм. Геном –
одноланцюгова,
кільцева РНК(-),
вкрита капсидом
(HDAg).
Нуклеокапсид
оточений HBsAg.
82. Джерелом інфекції є інфікована HDV людина (хвора на гостру чи хронічну форму HDV-HBV інфекції. Шляхи передачі HDV тісно
Вірус гепатиту D відносно стійкий до впливуфізико-хімічних чинників. Так він стійкий до дії
кислот, нуклеаз, сечовини, нагрівання і руйнується
під дією лугів та протеаз. За своєю стійкістю
близький до HBV.
HDV не культивується в клітинних культурах,
проте є дані про можливість культивування його в
клітинах гепатоми людини, клітинах мавп’ячих
нирок після інфікування їх РНК HDV. Вірус може
культивуватись на людиноподібних мавпах –
носіях HBsAg.
Джерелом інфекції є інфікована HDV людина
(хвора на гостру чи хронічну форму HDV-HBV
інфекції.
Шляхи передачі HDV тісно пов’язані з HBV, як
вірусом помічником. Головним механізмом
передачі HDV є парентеральний (природний і
штучний). Статевий шлях можливий у осіб, які
мають чисельні статеві контакти з багатьма
партнерами.
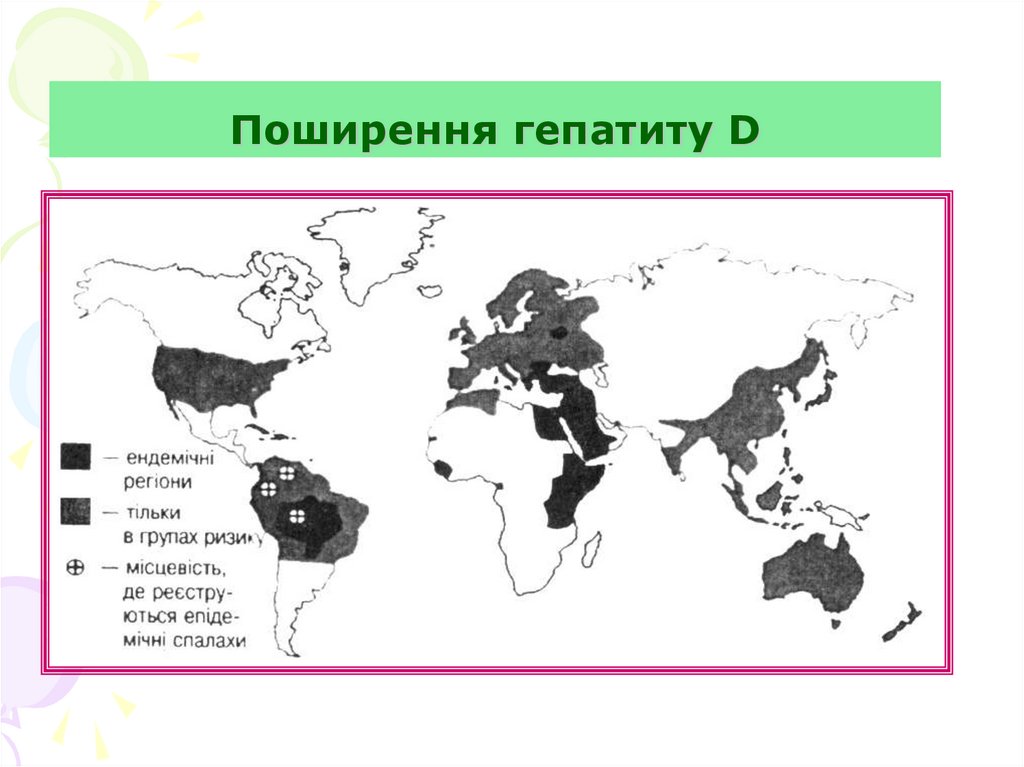
83. Поширення гепатиту D
84. Маркери гострого гепатиту D (коінфекція)
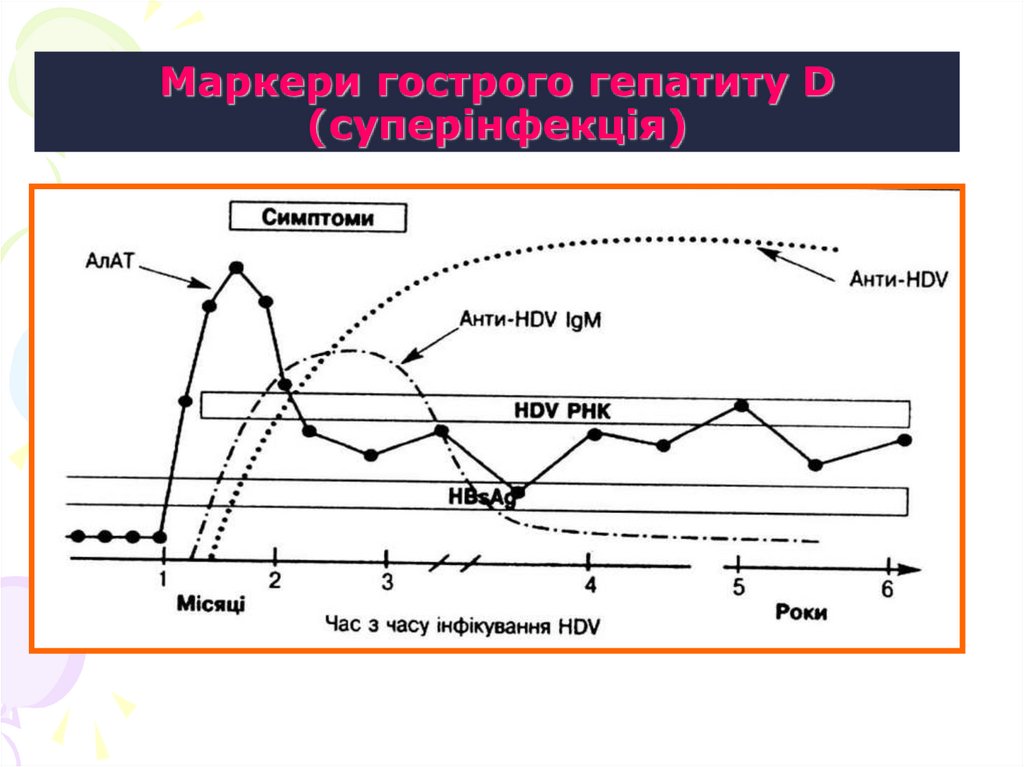
85. Маркери гострого гепатиту D (суперінфекція)
86. ВІРУС ГЕПАТИТУ Е
HEV належить до родиниCaliciviridae
Має круглу форму, діаметр
віріона - 32-34 нм.
Геном вірусу представлено
однонитковою РНК, яка
зверху оточена
капсидом.
Вірус не культивується у
клітинних культурах.
РНК
87.
Вірус передається, як і HАV, за допомогоюфекально-орального
механізму,
найчастіше
з
питною водою, забрудненою стоками. Доведено, що
він
може
передаватись
під
час
побутового
спілкування людей.
Епідеміологічна
особливість
цього
вірусу
полягає в тому, що він уражає здебільшого людей
молодого і середнього віку, тоді як HАV - дітей до
14 років. Епідемічний гепатит Е спостерігається в
тих регіонах земної кулі, де більшість мешканців
інфікується ВГА ще у перші роки життя. Клінічна
особливість ГЕ - важкий перебіг хвороби з високою
летальністю
(20-40 %) серед вагітних жінок,
особливо
в
останньому
триместрі
вагітності.
Характерною ознакою хвороби на відміну від інших
гепатитів є холестаз.
HEV розповсюджується від людини до людини
при контакті з меншою вірогідністю, ніж гепатит А.
Для попередження спалахів гепатиту Е, як правило,
88. Вірус гепатиту G - HGV
Родина Flaviviridaeрід Hepacivirus
Форма сферична,
діаметр – 40-50 нм, + РНК
Тип симетрії - ікосаедричний
Суперкапсид, покритий
шипиками.
Вірус не культивується на
культурах клітин, в організмі
лабораторних тварин.
Шимпанзе не сприйнятливі до
HGV
Гепатит G – антропонозна кров’яна інфекція. Джерело
інфекції є хворі на гострий або хронічний гепатит та здорові
вірусоносії. РНК HGV виявляється в сироватці та плазмі крові,
в мононуклеарних клітинах крові, слині, спермі. Основний
шлях передачі – парентеральний. Основні чинники передачі
89.
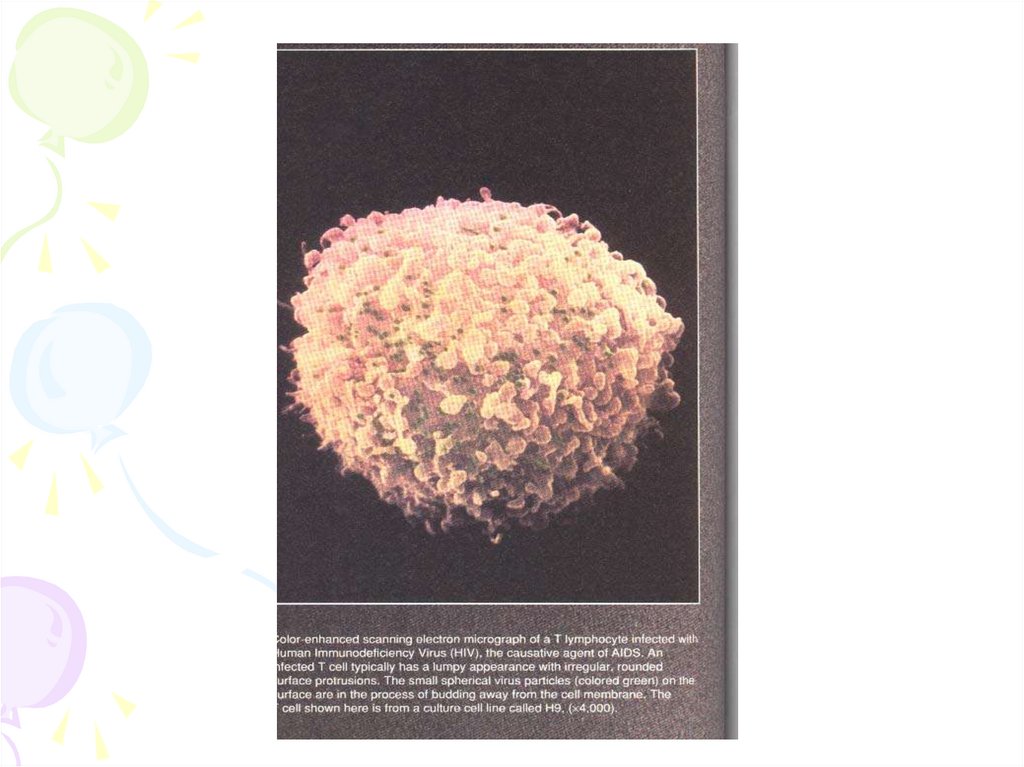
ВІРУС ІМУНОДЕФІЦИТУЛЮДИНИ (ВІЛ)
У середині 1981 р. Центр по контролю захворюваності США одержав
повідомлення, що за 8 місяців в Лос-Анжелесі діагностовано 5 випадків
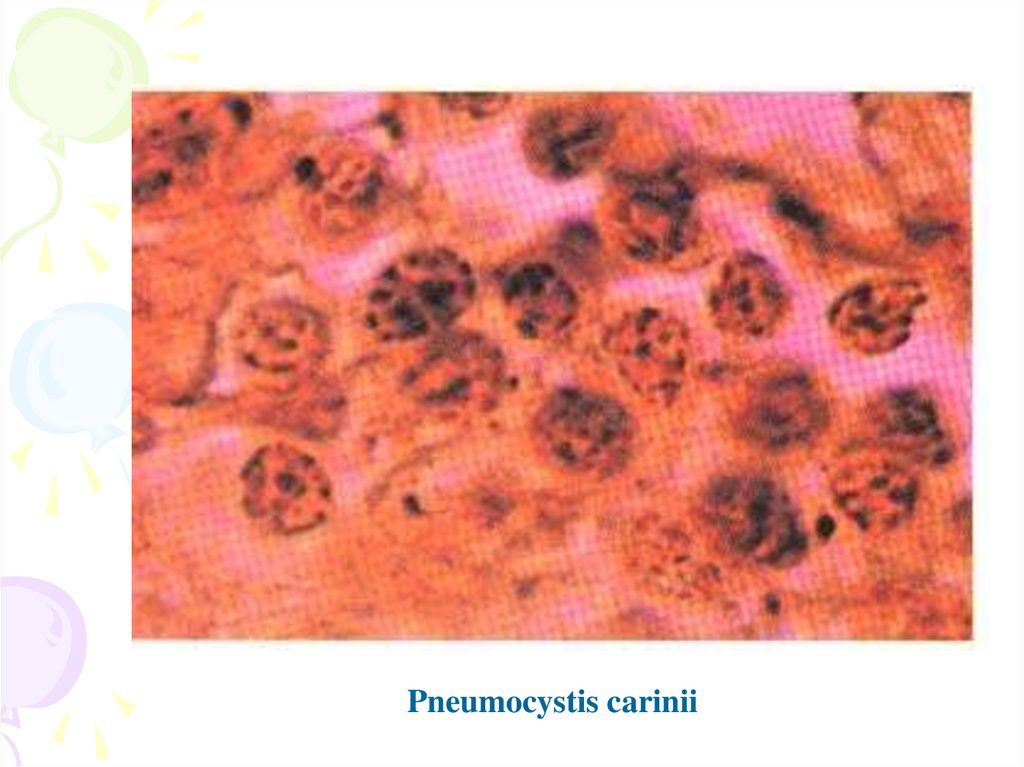
пневмоцистоза - рідкісного типу пневмонії, яка викликається Pneumocystis
carinii.
До цього часу захворювання зустрічалось рідко, тому ліки для нього були
експериментальними і призначались тільки ЦКЗ.
90.
ЦКЗодержав
повідомлення
про
збільшення
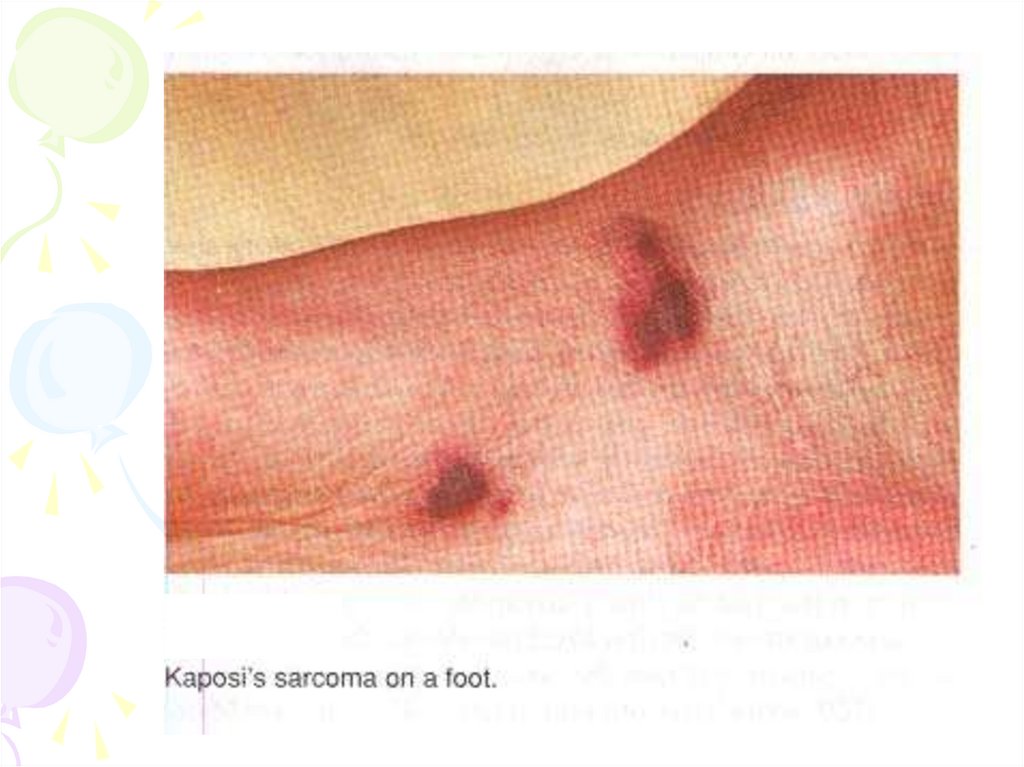
захворюваності одним видом раку - саркомою Капоші.
До цього часу це захворювання рідко зустрічалось в
США - і головним чином серед мужчин похилого віку,
які приймали препарати, що пригнічують дію імунної
системи.
Однак зараз протягом 30 місяців було зареєстровано 26
випадків саркоми, і знову таки у молодих мужчин
гомосексуалістів у Нью-Йорку. У деяких з них також
була пневмонія (P. carinii) та інші тяжкі опортуністичні
хвороби.
91.
92.
Pneumocystis carinii93.
Пізніше клініцисти та епідеміологи помітилизбільшення
числа
випадків
у
мужчингомосексуалістів двох явищ, які не можна було
пояснити:
- хронічної лімфаденопатії
- досить рідкої недиференційованої неходжкінської
лімфоми.
В основі цих зрушень лежали тяжкі ураження
імунної системи.
94.
Цей клінічний комплекс було класифіковано якабсолютно новий синдром, який в 1982 році
одержав назву СНІДу (AIDS).
Було встановлено, що у хворих виснажується
популяція певних лімфоцитів, зокрема СD4
клітини.
95.
У 1983 р. Р. Галло виділив ретровірус людини з кровіхворих на СНІД - Т лімфотропний вірус людини типу
ІІІ (HTLV - ІІІ - human T-lymphоtropic virus type ІІI).
Дещо раніше були описані подібні до нього віруси
HTLV – І і ІІ. Вони уражають Т-лімфоцити і викликають
досить агресивний рак (Т клітинний лейкоз), який
ендемічний для Японії, Африки, країн Карибського
басейну та інших регіонів. Тільки в Японії
нараховується понад 1,5 млн носіїв цього вірусу. Він
може передаватись від матері до дитини, а також при
переливання крові, статевих контактах. Захворювання
проявляється неврологічною симптоматикою, хронічною
мієлопатією, дисфункцією сфінктерів. Захворювання
подібно до розсіяного склерозу та бокового
аміотрофічного склерозу.
96.
У 1983 р. Люк Монтан’є після культивуваннязбільшеного лімфовузла молодого гомосексуаліста через
15 днів в культуральній рідині знайшов фермент транскриптазу. Отже, там був вірус. Він мав особливі
властивості - викликав симпластоутворення, але по
морфологіїі і серологічним ознакам відрізнявся від
HTLV-I i HTLV-II. Потім: в великих кількостях
накопичувався в культурах клітин В лімфоцитів,
попередньо трансформованих вірусом Епштейн-Бар
(герпес вірус), були серологічні перехрести з
поверхневими білками HTLV I.
Його позначали як LAV (lymphadenopathy associated
virus), він розмножувався в Т4, але не в Т 8 клітинах .
Вдалось ідентифікувати вірусний білок р25 (або р24).
97.
98.
99.
Збудники СНІДу належать до родини Retroviridae,підродини Lentiviridae, куди входять віруси вісни, меді
(вісна - демієлінізуюча хронічна інфекція у вівців, меді прогресуюча пневмонія у вівців).
100.
101.
Чутливість до дії різних факторів довкілляВірус високочутливий до нагрівання (при 56 С
протягом 30 хв його активність зменшується в 100 раз)
і до широкозастосовуваних дезинфектантів навіть в
концентраціях менших, ніж звичайно.
Вірус інактивується ефіром, ацетоном, етанолом
(20%),
гіпохлоритом
натрію
(0,2%),
бетапропіолактоном 0,25 % (1:400), перекисом водню
0,3 %, глютаральдегідом (0,0125 %).
Однак він відносно резистентний до УФО, іонізуючої
радіації.
Довше зберігає свої патогенні властивості при
кімнатній температурі, ніж решта ретровірусів.
102.
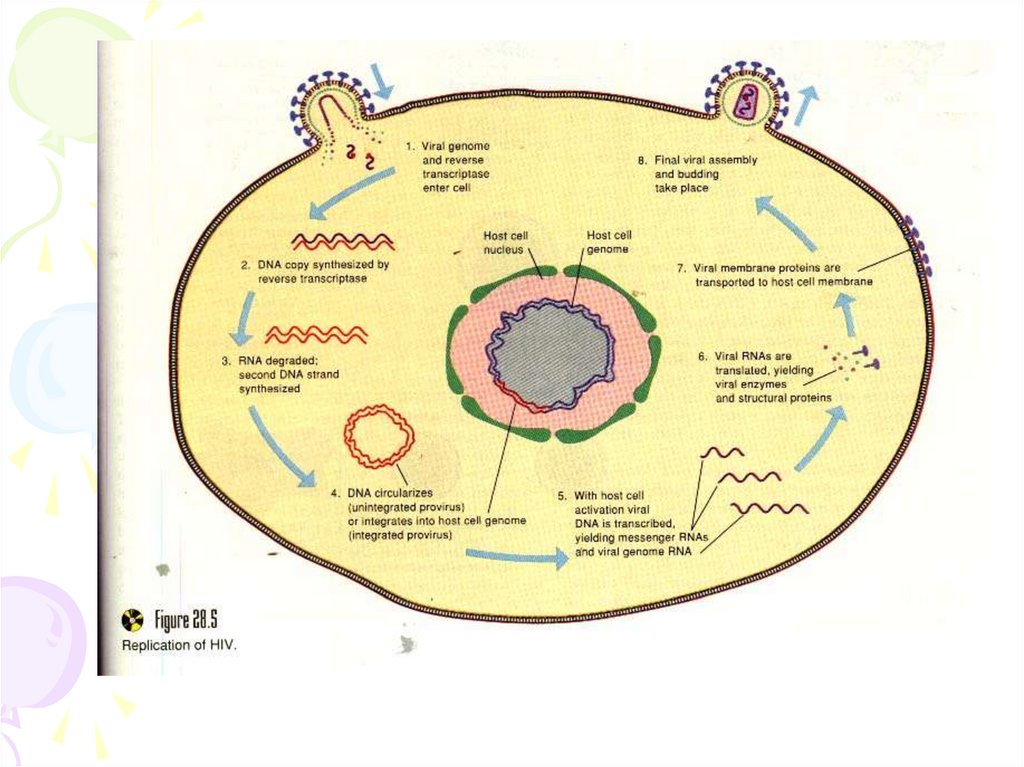
Молекулярна біологія ВІЧГеном - двониткова РНК з коефіцентом седиментації 35
S. Геном містить 9213 нуклеотидів і має 9 генів.
Основні гени: gag - кодує білки серцевини, pol ферменти, env - білки оболонки. Ці гени є у всіх вірусів
раку і лейкозу.
Крім того, у віруса є ряд генів-регуляторів: tat позитивний регулятор, rev (art, trs) - вибірковий
регулятор, vif (sor, A, P, Q) - фактор інфекційності,
vpr, vpn- функція їх невідома, nef (3’orf, B, E, F) негативний регулятор.
103.
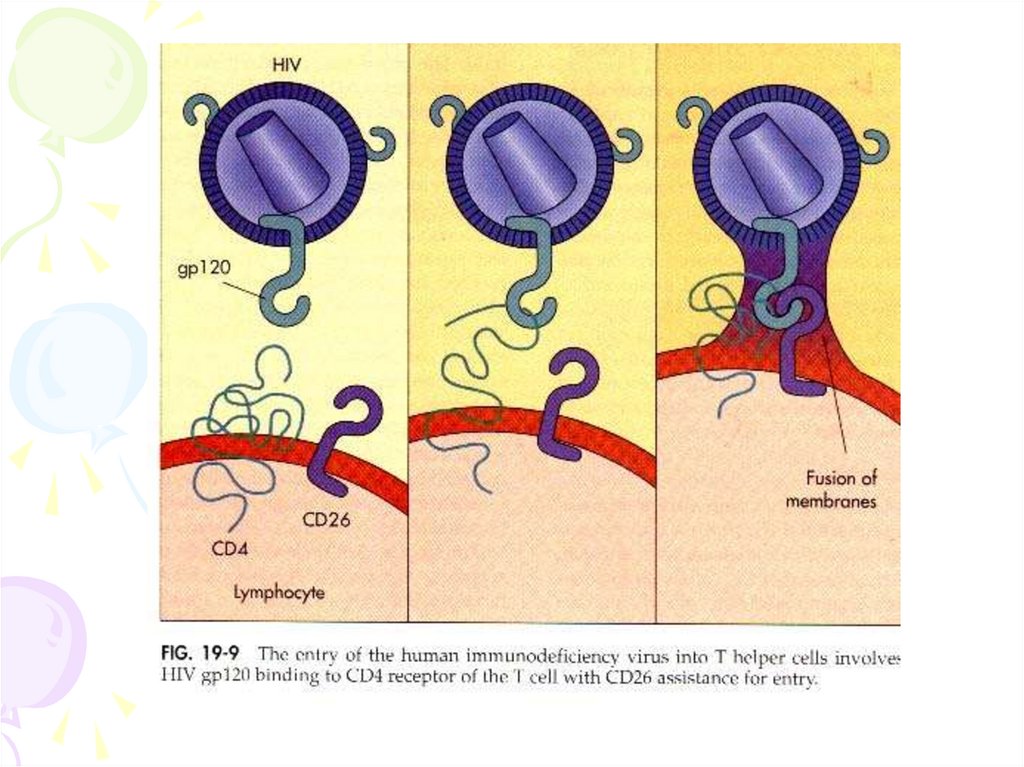
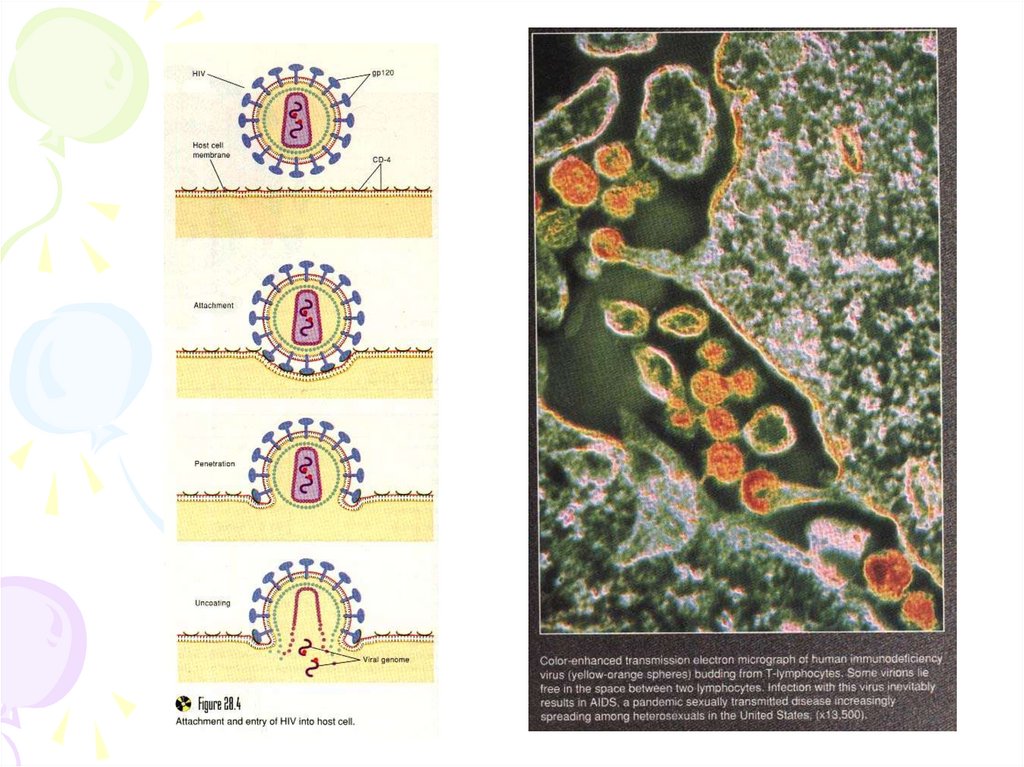
Взаємодія вірусів з клітиноюВірус проникає в клітину двома шляхами: за допомогою
злиття мембран при звільненні gp41 (інтегрує в стінку
лімфоциту) або ендоцитозом.
104.
105.
106.
107.
108.
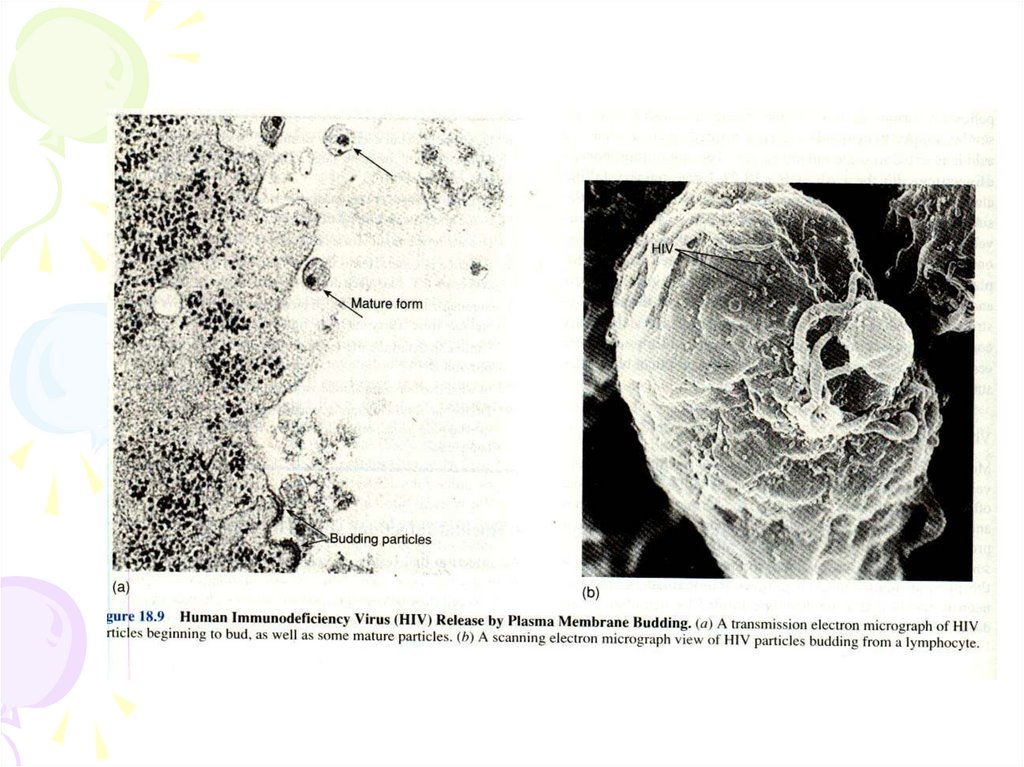
Загибель лімфоцитів може відбуватись за різнимимеханізмами:
А) HIV розриває клітину, виходячи з неї після реплікації;
Б) На поверхні заражених клітин знаходиться gp120, а
він взаємодіючи з незараженими клітинами, викликає
злиття їх мембран і утворення функціонально
скомпрометованого синцитію.
В) Вірус викликає нормальну імунну відповідь, і
цитотоксичні клітини (NK) або Т8-лейкоцити (Т-кілери)
знищують заражені клітини, на поверхні яких є вірусні
білки;
Г) У крові циркулює вільний gp120, він здатний
адсорбуватись на клітинах з рецепторами CD4, а імунна
система знищує їх.
Д) Клітини гинуть внаслідок дії імуноглобулінів, які
з’єднуються з антигенами на поверхні клітини,
приєднують комплемент і викликають лізис клітини.
109.
ПАТОГЕНЕЗРецептор для вірусів - CD4 антиген:
- T4 лімфоцити (хелпери/індуктори);
- 3 – 10 % B лімфоцитів;
-10-20 % моноцитів і макрофагів; серед них альфеолярні
макрофаги,клітини Лангенгарса шкіри;
- гліальні
клітини і макроглія ЦНС.
Фолікулярні дендритні клітини мигдаликів
інфікуватись без участі CD4 рецепторів.
можуть
Специфічна взаємодія забезпечується суперкапсидними
глікопротеїнами gp120. Злиття мембран забезпечує
трансмембранний gp41.
110.
Провідна роль у відповіді і регуляції імунологічнихфункцій належить Т-лімфоцитам. Т-хелпери регуляторні клітини, допомагають розвитку імунної
відповіді; іх різновид -Т-індуктори сприяють активації
та взаємодії Т-ефекторів (Т-кілерів) та Т-супресорів; Тсупресори (регуляторні клітини) - на певній стадії
подавляють імунну відповідь; Т-кілери здатні до
цитотоксичної дії (приймають участь в забезпеченні
протипухлинного, противірусного, трансплантаційного
імунітету, гіперчутливості сповільненого типу).
111.
У хворих спостерігається 8-10-кратне зниженняциркулюючих хелперів (в нормі в крові знаходиться до
800 клітин на 1 мкл). Співвідношення між Т-хелперами і
Т-супресорами знижується до 0,2-0,5, в той час як у
здорових людей воно сягає 1,9-2,4.
Розвивається порушення всіх ланцюгів, де задіяні
клітини Т4. Відбувається інгібування цитотоксичних Тлімфоцитів, які нездатні виявляти активність відносно
клітин-мішенів, що заражені вірусами. Порушується
функція Т-супресорів, і, відповідно, зменшується їх
регулюючий вплив на клітинний і гуморальний імунітет.
112.
Характерноює
неспецифічна
поліклональна
активація В-лімфоцитів. Вона веде до збільшення
синтезу імуноглобулінів G, A, D і нормальних антитіл.
Абсолютна кількість В-лімфоцитів при цьому не
змінюється, що веде до виснаження їх пулу.
Пояснюється
це
тривалою
антигенною
дією
активізованої опортуністичної інфекції (мікрофлори,
вірусів герпесу, ЦМВ, ВЕБ).
Знижується продукція ІЛ-2, інтерферону та інших
лімфокінів, що в свою чергу спричиняє зниження
кількості макрофагів, моноцитів, а це веде до зниження
секреції ІЛ-І. Таким чином, порушуються всі ланцюги
імунної відповіді.
113.
Періоди розвитку і клініка захворюванняКлініка СНІДу - це айсберг, значна частина якого
схована від уважного ока клініциста.
Під час інкубаційного періоду у 50 % інфікованих
розвивається мононуклеозоподібний синдром, який
виникає через 2-4 тижні після зараження. Триває він 24 тижні, в цей час спостерігається субфибрильна
температура,
ангіна,
фарингіт,
збільшуються
лімфовузли, розвивається гепатолієнальний синдром,
з’являється головний біль,
артралгія,
міалгія,
розвивається лімфопенія.
Безсимптомне носійство може тривати роками.
114.
Іінкубаційнийперіод
змінюється
синдромом
генералізованої лімфаденопатії, який також може
тривати роками.
У цей час спостерігається збільшення лімфовузлів
двох і більше груп, не рахуючи пахові (завушні,
підщелепні, надключичні, кубітальні, підколінні,
стегнові) тривалістю три і більше місяців, з’являється
діарея (1 місяць), знижується маса тіла (понад 10% ).
Проте спостерігаются тривалі ремісії.
115.
Наступний період - снідасоційований комплекс.При
ньому
спостерігаються
генералізована
лімфаденопатія, втрата маси тіла, пітливість,
гарячка, кашель, розлади шлунково-кишкового
тракту, лейко-, лімфо-, тромбоцитопенія, ознаки
порушення клітинного
імунітету. З’являються
опортуністичні інфекції. Часто розвиваються
характерні порушення ЦНС, які проявляються у
вигляді деменції. Однак і під час цього періоду
деколи спостерігаються ремісії.
116.
Четвертий період - це безпосередньо СНІД.117.
КЛАСИФІКАЦІЯ ВООЗ (ВІЛ/СНІД)Клінічна стадія І
1. Асимптоматична
2. Переметуюча генералізована лімфаденопатія
Клінічна стадія II
3. Втрата ваги, < 10% від маси тіла
4. Мінімальні шкірно-слизові прояви (себорейний
дерматит, грибкове ураження нігтів, повторні
виразки порожнини рота, хейліт)
Герпес Зостер протягом останніх 5 років
Повторні інфекції верхніх дихальних шляхів
(включаючи бактеріальні синусити)
118.
Клінічна стадія III1. Втрата ваги, > 10% від маси тіла
2. Непояснена хронічна діарея, > 1 місяця
3. Непояснена тривала лихоманка (інтермітуюча чи
постійна), > 1 місяця
4. Кандидоз порожнини рота
5. Волосата лейкоплакія
6. Туберкульоз легень протягом останнього року
7. Тяжкі бактеріальні інфекції (пневмонії, гнійні
міозити)
119.
Клінічна стадія IV1. Синдром виснаження, асоційований із ВІЛ (по визначенню CDC)
2. Пневмонія, викликана P. Carinii
3. Токсоплазмоз мозку
4. Криптоспоридіоз з діареєю > 1 місяця
5. Позалегеневий криптококкоз
6. CMV інфекція (за винятком враження печінки, селезінки або л/у)
7. HSV інфекція при враженні шкірно-слизових оболонок > 1
місяця або вісцеральна
будь-якої тривалості
8. Прогресуюча мультифокальна лейкоенцефалопатія
9. Будь-який дисемінований ендемічний мікоз (гістоплазмоз,
коккцидіомікоз)
10. Кандидоз стравоходу, трахеї, бронхів або легень
11. Атиповий мікобактеріоз розповсюджений
12. Сальмонельозна септицемія (крім спричиненої S. typhimurium)
13. Позалегеневий туберкульоз
14. Лімфома
15. Саркома Капоші
16. ВІЛ-асоційована енцефалопатія (по визначенню CDC)
120.
Захворювання, які дозволяють запідозрити СНІД улюдини.
А. Злоякісні новоутворення
- саркома Капоші;
лімфома, яка локалізується в головному мозку.
Б. Опортуністичні інфекції.
І - протозойні та гельмінтні:
- пневмонія (P. carinii);
- токсоплазмоз (пневмонія);
- криптоспоридіоз (кишкова форма);
- стронгілоїдоз.
121.
122.
ІІ - грибкові:- кандидоз;
- аспергільоз;
- криптококоз.
ІІІ - бактеріальні:
мікобактеріози
(викликаються
атиповими
мікобактеріями, крім M. tuberculosis, M. bovis, M.
africans, M. leprae);
IV -вірусні:
- цитомегаловірусна інфекція (ураження легень,
шлунково-кишкового тракту, центральної нервової
системи);
- герпесінфекції;
- паповаінфекція (прогресуюча
лейкоенцефалопатія).
багатовогнищева
123. Хворі на СНІД
124.
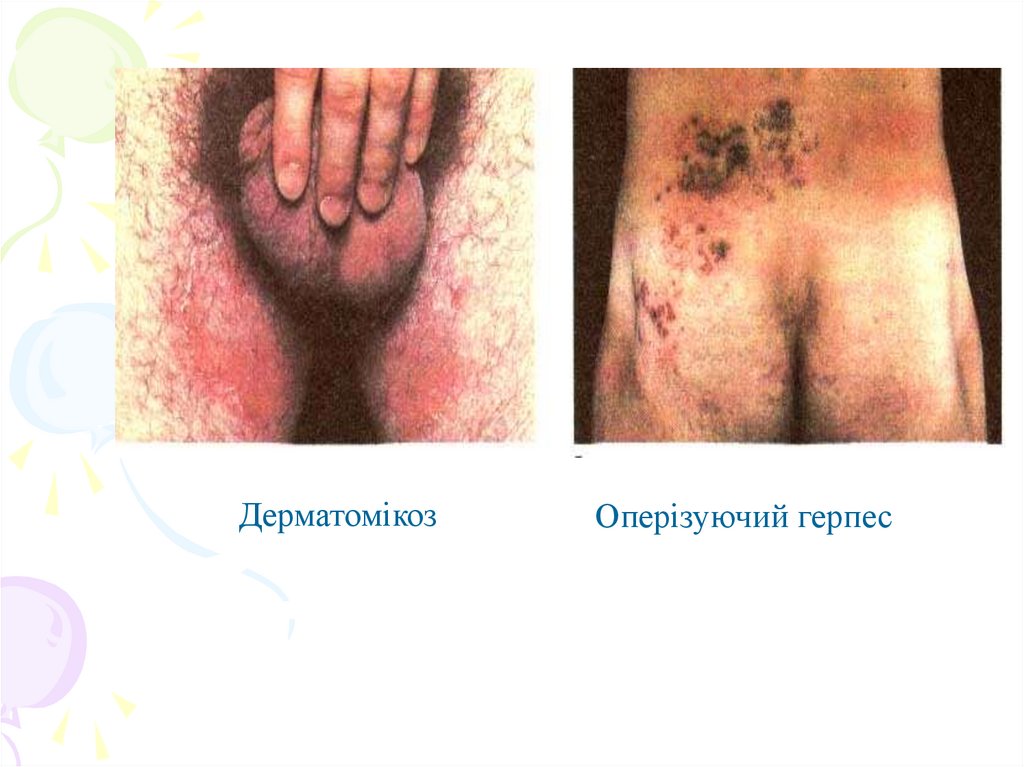
ДерматомікозОперізуючий герпес
125.
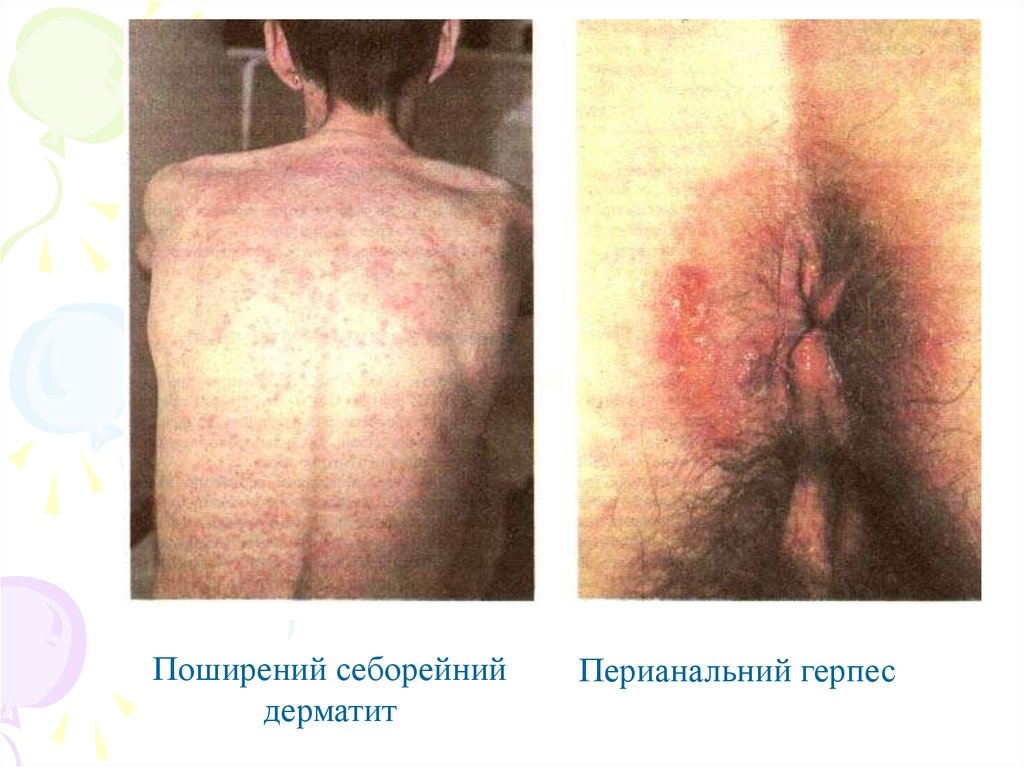
Поширений себорейнийдерматит
Перианальний герпес
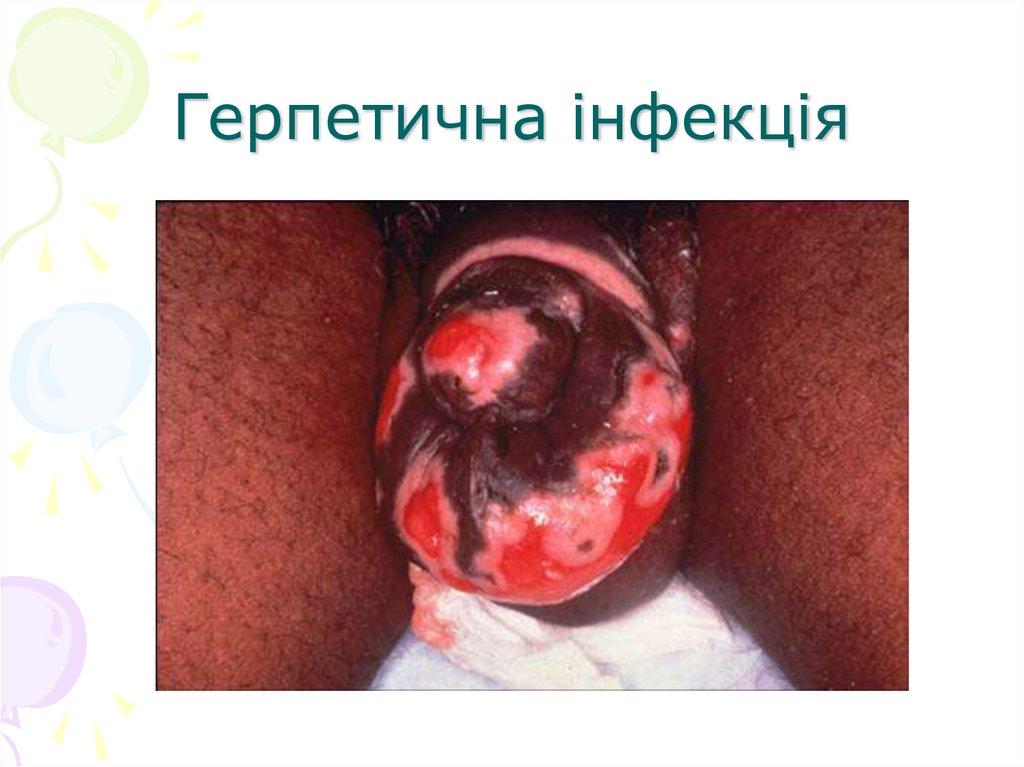
126. Герпетична інфекція
127.
Саркома КапошіСаркома Капоші у
хворого, який отримує
імуносупресивну
терапію
128.
129.
Histoplasma capsulatum130.
Candidiasis131.
Cryptosporidium (intestinal epithelium)132.
Cryptococcus neoformans (nervous system)133.
134.
Сипмптоми, які дозволяють запідозрити СНІД улюдини
І. Серйозні:
- зниження маси тіла на 10 %;
- хронічна діарея понад 1 місяць;
- гарячка тривалістю понад 1 місяць (постійна або
інтермітуюча);
2. Незначні;
- кашель понад 1 місяць;
- генералізований багатовогнищевий дерматит;
- рецидивуючий H. zoster;
- кандидоз порожнини рота, глотки;
- хронічний прогресуючий
простий герпес;
- генералізована лімфаденопатія.
герпес,
десимінований
135.
У дітей такі симптоми:І. Серйозні:
- зниження маси тіла на 10 %;
- хронічна діарея понад 1 місяць;
- гарячка тривалістю понад 1 місяць (постійна або
інтермітуюча);
2. Незначні;
- генералізована аденопатія;
- кандидоз порожнини рота, глотки;
- звичайні рецидивуючі інфекції (отити, фарингіти);
- стійкий кашель;
- генералізований дерматит;
- підтвердження СНІДу у матері.
136.
Епідеміологія СНІДуЄдиним джерелом інфекції є хвора людина або
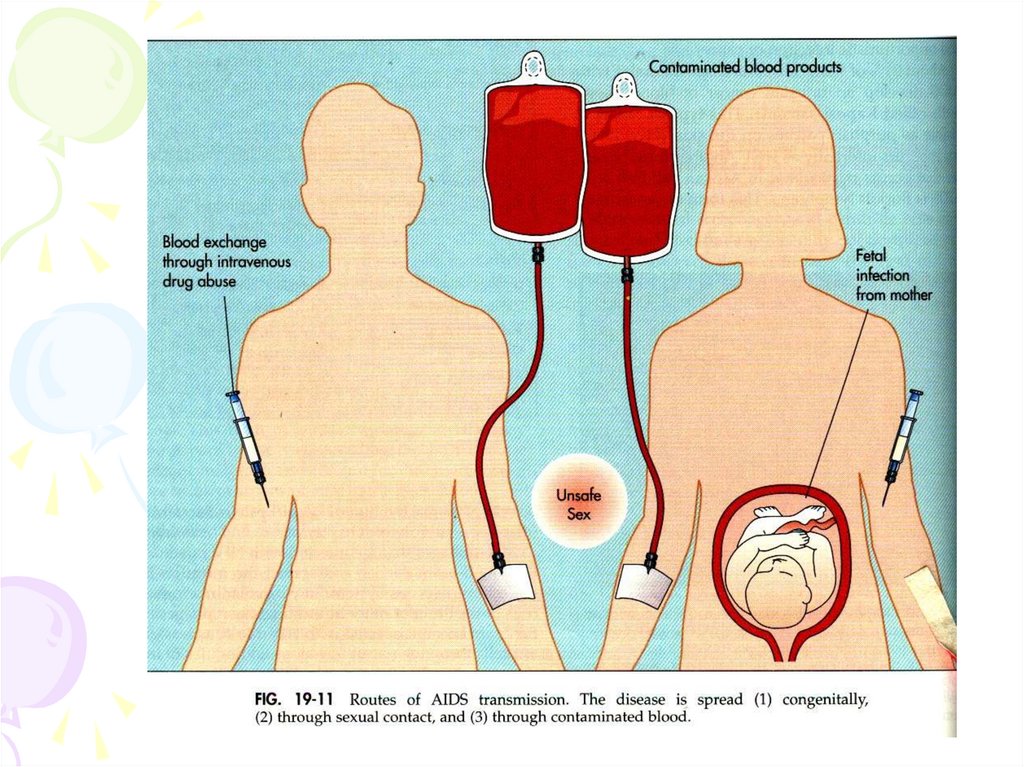
вірусоносій. Вірус може проникати в організм різними
шляхами.
До 1995 р. в Україні домінував статевий шлях
передачі, з 1995 - парентеральний:
- парентеральний - 68,5 %;
- статевий - 21 %;
- мати - дитина (вертикальний) - 6 %;
- не встановлений - 4,5 %.
137.
138.
Групи високого ризику щодо ВІЛ інфікування1. Гомосексуалісти та чоловіки бісексуали.
2. Наркомани, які використовують спільні голки.
3.
Люди, яким багаторазово переливали кров або
продукти крові в період між 1978 – 1985 роками.
4. Сексуально нерозбірливі чоловіки і жінки, особливо
повії.
5. Люди, які перенесли гепатит B, сифіліс та інші
хвороби, що передаються статевим шляхом.
139.
У всьому світі склалась двоетапналабораторної діагностики ВІЛ-інфекції.
система
На першому етапі проводять скринінг сироватки
крові на антитіла до ВІЛ за допомогою різних тестсистем імуноферментного аналізу (ІФА). Кров
донорів досліджують у лабораторіях з діагностики
СНІДу, розгорнутих на базі станцій (відділень)
переливання крові, а кров осіб, які належать до групи
ризику, - у лабораторіях з діагностики СНІДу різних
медичних закладів (диспансери. СЕС, протичумні
станції, лікарні, поліклініки, діагностичні центри
тощо). Крім того, дослідження сироватки крові в ІФА
на антитіла до ВІЛ частково проводять у лабораторіях
клінічної імунології, розгорнутих на базі інфекційних
лікарень.
140.
141.
142.
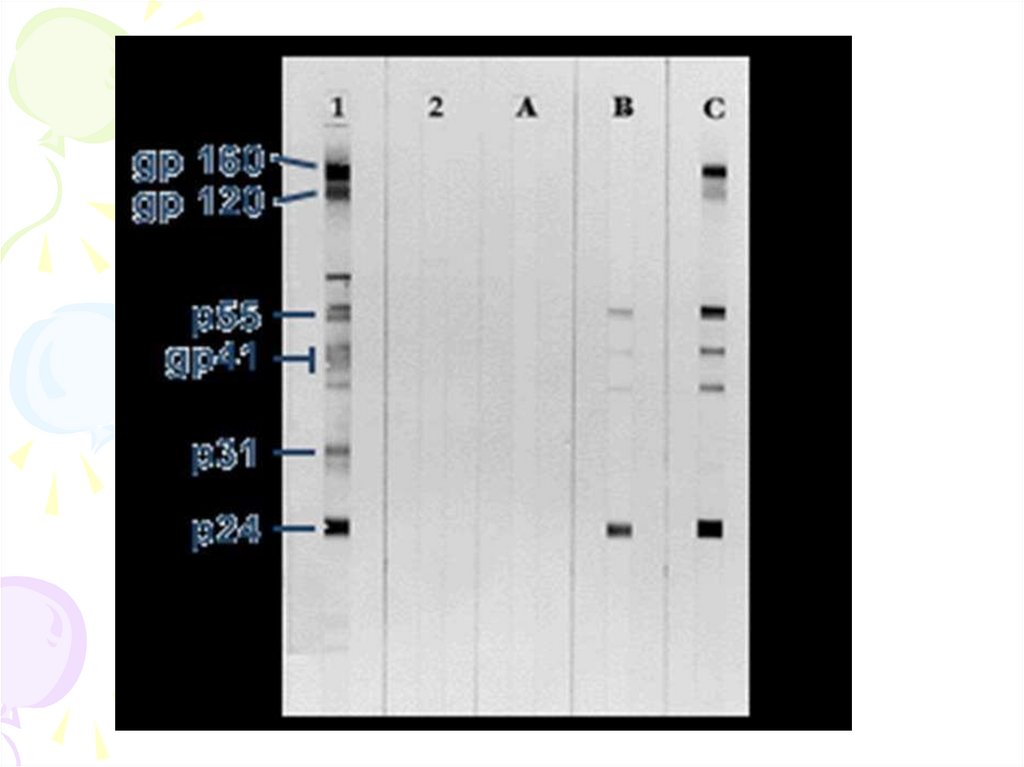
На другому етапі сироватки крові, позитивні в ІФА(два позитивні результати з двох або трьох досліджень),
направляють у лабораторії спеціалізованих НДІ,
діагностичні центри для дослідження за допомогою
підтверджуючих тестів: імуноблоту (вестерн-блоту),
тесту радіоімунної преципітації (РІП) і реакції
непрямої імунофлуоресценції (РНІФ).
Одержання
позитивного
результату
під
час
дослідження методом імуноблоту або РІП, тобто
виявлення антитіл до певних структурних білків
ВІЛ, дає змогу зробити позитивний висновок про
янаявність ВІЛ-інфекції, хоча можливі випадки
несправжньопозитивних
реакцій.
Аналогічний
висновок можна зробити також у разі одержання
позитивних результатів дослідження сироваток крові на
антитіла до ВІЛ у РНІФ, використовуючи культури Тлімфоцитів, інфікованих ВІЛ, тобто ті, що містять
вірусний антиген.
143. ІФА
144.
145.
Крім зазначеної поетапної схеми лабораторноїдіагностики ВІЛ-інфекції на підставі виявленння
противірусних
антитіл
застосовують
також
альтернативні методи вірусологічної діагностики:
виявлення антигену ВІЛ у сироватці крові
допомогою ІФА та інших тестів;
за
виділення ВІЛ у культурах лімфоцитів із подальшою
індикацією вірусу за ЦПД
(утворення синцитіїв),
ревертазною активністю та детекцією вірусного
антигену (або провірусу в молекулярній гібридизації in
situ);
визначення провірусу в лімфоцитах периферичної
крові у тесті молекулярної гібридизації.
146.
Лікування СНІДу - надзвичайно важлива проблема,яка, на жаль, далека від остаточного розв’язання. У
залежності від особливостей репродукції вірусів можна
передбачити різні способи втручання в його життєвий
цикл.
Для блокування його зв’язування з клітиною метою
можна використати:
а) декстрансульфат;
б) антитіла до gp 120, які блокують рецептори CD4;
в) розчинний CD4;
г) антиідіотипічні імуноглобуліни проти CD4,які будуть
з’єднуватись з gp120.
д) химерні молекули імуноглобулінів, у яких варіабельні
частини представлено ділянками CD4 .
147.
Порушення вивільнення вірусної РНК з білковоїоболонки забезпечують антитіла проти gp41, який
забезпечує злиття мембрани вірусу з клітиною.
Основний шлях, що дозволяє загальмувати цикл
репродукції вірусів - блокада феременту зворотної
транскриптази. Для цього використовуються препарати
дидезоксицитидин, дидозоксиаденозин, фосфоноформіат азидотимідин та інші дидезоксинуклеотиди.
Препаратом вибору в лікуванні СНІДу є азидотимідин
(ретровір) аналог тиміну. Він відрізняється від тиміну
наявністю групи - ОН замість - N3 в положенні 3’. При
синтезі нуклеїнової кислоти він заміщує тимін і в зв’язку
з відсутністю гідроксильних груп неможливе приєднання
інших нуклеотидів. Отже, блокується синтез ДНК.
148.
V. Використання імплантованих генів.Приклад: 1. У клітини кісткового мозку від хворого на
СНІД інтегрується лабораторно зконструйований ген, який
перешкоджає активації провіруса. Клітини вводять в організм
хворого, де вони розмножуються, забезпечуючи популяцію
клітин, які не можуть продукувати інфекційний ВІЛ.
Ця ідея відпрацьована на попередженні експериментальної
інфекції, що викликаєть вірусом простого герпесу у мишей.
VI. Підвищити чутливість вірусу до ультрафіолетового
опромінення.
Приклад: 1. Хворий на СНІД отримує препарати, які
підвищують чутливість уражених ВІЛ клітин до дії УФО.
Мононуклеарні клітини видаляються з організму,
опромінюються і вводяться назад в організм хворого.
Інфіковані опромінені клітини руйнуються в організмі.
149.
VII. Використання імуностумуляторів.Приклади: 1. Інтерферон, синтезований in vitro, який
вводиться в організм хворого в малих дозах, блокує
вивільнення вірусів з інфікованих клітин. Це істотно
підсилює ефект zidovudine.
α-інтерферон також ефективний проти багатьох
випадків саркоми Kaпоші.
2. Ditiocarb, який хімічний подібний до одного
із сільськогосполарських фунгіцидних препаратів,
збільшує опір резистентність до вторинних інфекцій.
Воно може також призначатись разом із зідовудином.
150.
АНТИРЕТРОВІРУСНІ ПРЕПАРАТИАнтиретровірусні препарати застосовують для терапії і
профілактики ВІЛ-інфекції/ СНІДу. Існує 3 класи АРВП:
1) нуклеозидні інгібітори зворотної транскриптази ВІЛ (Nucleoside
Analog Reverse Transcriptase Inhibitors —NARTIs).
2) ненуклеозидні інгібітори зворотної транскриптази ВІЛ (NonNucleoside Reverse Transcriptase Inhibitors — NNTRIs);
3) інгібітори протеази ВІЛ.
НУКЛЕОЗИДНІ ІНГІБІТОРИ
ЗВОРОТНОЇ ТРАНСКРІПТАЗИ ВІЛ
До даного класу АРВП належать:
аналоги тимідину — зидовудин, фосфазид, ставудин;
аналог аденіну — диданозин;
аналоги цитидину— залцитабін, ламівудин;
аналог гуаніну — абакавір.
151.
НЕНУКЛЕОЗИДНІ ІНГІБІТОРИ ЗВОРОТНОЇТРАНСКРІПТАЗИ ВІЛ
Невірапін
Делавердин
Іфавіренц.
Вони інгібують ЗТ і, відповідно, стадію зворотної
транскрипції при реподукції ВІЛ. Високоспецифічні до ЗТ ВІЛ
і не блокують ДНК-поліиеразу людини.
ІНГІБІТОРИ ПРОТЕАЗИ ВІЛ
До інгібіторів протеази ВІЛ належать
саквінавір, індинавір, ритонавір, нелфінавір і
ампренавірі
152.
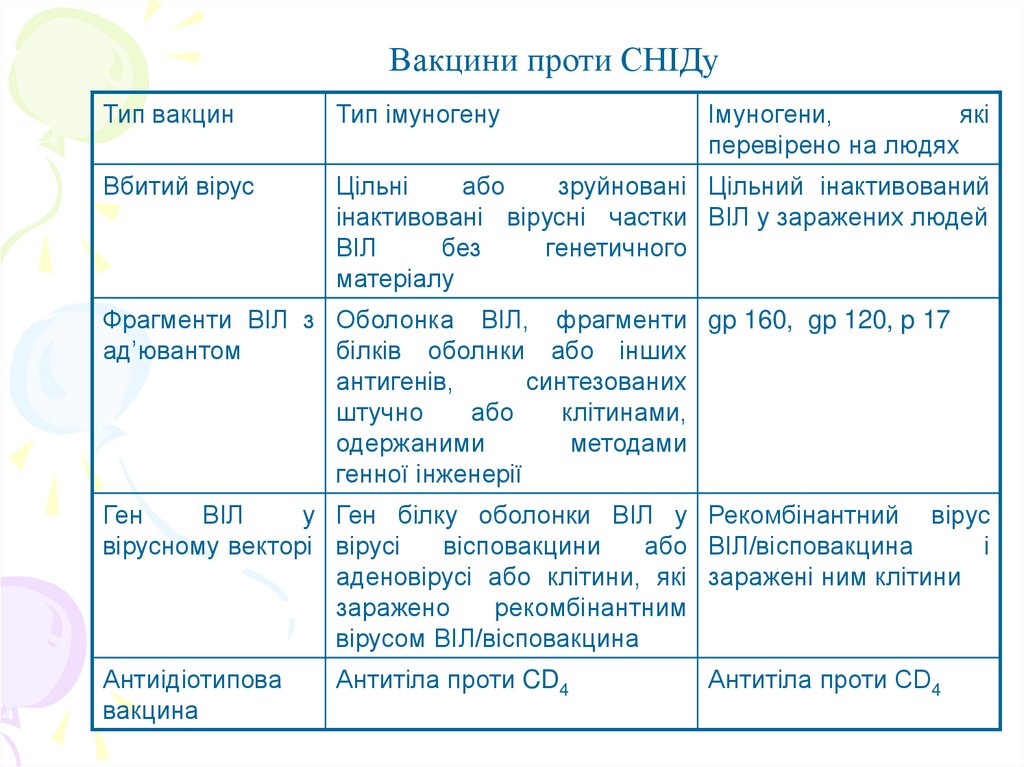
Вакцини проти СНІДуТип вакцин
Тип імуногену
Імуногени,
які
перевірено на людях
Вбитий вірус
Цільні
або
зруйновані Цільний інактивований
інактивовані вірусні частки ВІЛ у заражених людей
ВІЛ
без
генетичного
матеріалу
Фрагменти ВІЛ з Оболонка ВІЛ, фрагменти gp 160, gp 120, p 17
ад’ювантом
білків оболнки або інших
антигенів,
синтезованих
штучно
або
клітинами,
одержаними
методами
генної інженерії
Ген
ВІЛ
у Ген білку оболонки ВІЛ у Рекомбінантний вірус
вірусному векторі вірусі
вісповакцини
або ВІЛ/вісповакцина
і
аденовірусі або клітини, які заражені ним клітини
заражено
рекомбінантним
вірусом ВІЛ/вісповакцина
Антиідіотипова
вакцина
Антитіла проти CD4
Антитіла проти CD4
153.
Деякі шляхи зменшення ризику зараження на СНІД1. Утримання від сексуального стосунків – ефективний,
але не широко використовуваний засіб.
2. Залишайтеся з одним вірним сексуальним
партнером. Використовуйте свою енергію в близьких
стосунках з однією персоною, замість багаторазових
поверхневих взаємин.
3. Використовуйте латексні презервативи із
спермицидною активністю. Не використовуйте інших
видів презервативів. Презервативи істотно зменшують,
але не виключають ризик зараження ВІЛ.
4.
Не займайтесь анальним сексом. Він особливо
ризикований.
154.
5.Уникайте травм статевих органів і прямої кишки.
Маленькі розриви шкіри і слизових оболонок сприяють
передачі ВІЛ.
6.
Уникайте голок та інших об'єктів, забруднених
кров’ю когось-іншого.
7. Відстрочите вагітність на невизначений термін, якщо
ви жінка, заражена ВІЛ. Якщо ви не впевнені,
обов’язково здайте кров для виключення інфікування ВІЛ
перед вагітністю. Біля 30% малюків, народжених до
заражених ВІЛ матерів, помре СНІДу.
8.
Не майте статевих контактів з особою, яку ви
погано знаєте.
9.
Не майте статевого контакту з особою, яка
знаходиться в групі ризику.
10.
Не майте статевих контактів з особами, у яких є
виразки ураження від вірусу простого герпесу або з
інших причин. Вони сприяють передачі ВІЛ.

















































































































 Медицина
Медицина








