Похожие презентации:
Биохимия, как наука. Виды биологического материала для биохимических исследований
1.
Биохимия, как наука.Виды биологического
материала для биохимических
исследований
Преподаватель:
Черных Наталья
Валерьевна
2.
ЛитератураЛюбимова, Бабкина, Тимофеев: Теория и
практика лабораторных биохимических
исследований
А.А. Кишкун «Руководство по лабораторным
методам диагностики»
Дополнительная литература:
Е.С. Северин «Биохимия»
3.
В рамках дисциплины мы будем изучать:- задачи, структуру, оборудование, правила работы и техники
безопасности в биохимической лаборатории;
- особенности подготовки пациента
лабораторным исследованиям;
к
биохимическим
- основные методы и диагностическое значение биохимических
исследований крови, мочи, ликвора и так далее;
4.
- основы гомеостаза,гомеостаза;
биохимические
механизмы
сохранения
- нормальную физиологию обмена белков, углеводов, липидов,
ферментов, гормонов, водно-минерального обмена, кислотноосновного состояния;
- причины и виды патологии обменных процессов;
- основные методы исследования обмена веществ, гормонального
профиля, ферментов
5.
Биологическая химия (биохимия) – наука, изучающая химический(молекулярный) состав живых организмов и протекающие в них
химические реакции, которые лежат в основе жизнедеятельности.
Объекты изучения - вирусы, бактерии, растения, животные и организм
человека.
6.
История развития биохимииСтановление биохимии как науки произошло на рубеже XIX и XX веков;
термин "биохимия" предложил в 1903 К. Нейберг.
Первый период – с древних времен до эпохи Возрождения (XV в.):
человечество эмпирически пользовалось биохимическими процессами
(изготовление хлеба, сыра, вина и т.д.)
Карл Нейберг
немецкий биохимик
Второй период (XVв. –первая половина XIXв.):
М.В. Ломоносов – закон сохранения массы вещества
Ван Гельмонт
Ю. Либих – метод количественного химического анализа вещества
К. Шееле – выделил молочную, яблочную кислоты, глицерин, казеин молока
А.М. Бутлеров – теория строения органического вещества
А. Кольбе – синтезировал уксусную кислоту
М. Бертло – синтезировал триглицериды
А.М. Бутлеров
7.
Третий период (вторая половина XIXв.- первая половина XXв.):И.М.Сеченов изучал физиологию и биохимию дыхания
Л.П. Мархлевский и С.В. Салазкин изучали строение гемоглобина и
хлорофилла
Н.И.Лунин открыл витамины
Д.И. Ивановский открыл вирусы
Э. Фишер сформулировал основные положения пространственной
структуры белков
Дж. Самнер получил в кристаллическом виде первый фермент уреазу
Г.Кребс открыл и подробно изучил цикл мочевины и цикл трикарбоновых
кислот
8.
Четвертый период (вторая половина XXв.-XXIв.)• 1953 г. - Дж. Уотсон и Ф. Крик предложили модель двойной спирали строения ДНК.
• 1953 г. - Ф. Сенгер впервые расшифровал аминокислотную последовательность белка инсулина.
• 1961 г. - М. Ниренберг расшифровал первую «букву» кода белкового синтеза - триплет ДНК, соответствующий
фенилаланину.
• 1966 г. - П. Митчелл сформулировал хемиосмотическую теорию сопряжения дыхания и окислительногофосфорилирования.
• 1969 г. - Р. Мерифильд химическим путем синтезировал фермент рибонуклеазу.
• 1971 г. - в совместной работе двух лабораторий, руководимых Ю. А. Овчинниковым и А. Е. Браунштейном,
установлена первичная структура аспартатаминотрансферазы - белка из 412 аминокислот.
• 1977 г. - Ф. Сенгер впервые полностью расшифровал первичную структуру молекулы ДНК
1988 г . Колин Питчфорк стал первым человеком, осужденным за убийство на основе доказательств,
полученных в результате ДНК-дактилоскопии, и первым преступником, пойманным в результате массового
применения процедуры дактилоскопии.
9.
Разделы биохимииСтатическая биохимия изучает химический состав организмов и
структуру
составляющих
их
молекул
(белков,
аминокислот,
нуклеиновых кислот, нуклеотидов, углеводов и их производных,
липидов, витаминов, гормонов).
Динамическая
биохимия
представляющие
обмен
изучает
веществ
химические
(метаболизм),
а
реакции,
именно
пути
превращения молекул и механизмы происходящих между ними реакций.
10.
Функциональная биохимия изучает биохимические реакции, лежащие воснове физиологических функций. Она изучает биохимические основы
переваривания
механизмы
питательных
мышечного
веществ
сокращения,
в
желудочно-кишечном
проведения
нервного
тракте;
импульса,
дыхательной функции крови, регуляции кислотно-щелочного равновесия,
функции печени и почек, иммунной системы и др.
Биохимия человека или медицинская биохимия – это раздел биохимии,
который изучает закономерности обмена веществ в человеческом организме, в
том числе и при заболеваниях.
11.
Задачи биохимии человека:1. Изучение строения и функций биомолекул, входящих в состав тканей
организма
2. Изучение механизмов поступления пластических и биологически
активных веществ во внутреннюю среду организма
3. Изучение механизмов превращения поступивших мономеров в
биополимеры, специфичные для данного организма
12.
4. Изучение механизмов высвобождения, накопления и использованияэнергии в клетке
5. Изучение механизмов образования и выведения конечных продуктов
распада веществ в организме
6. Изучение механизмов воспроизведения и передачи наследственных
признаков организма
13.
Биомолекулы и клеточные структурыБиомолекулы – органические соединения, входящие в состав организмов,
образующие клеточные структуры и участвующие в биохимических реакциях
обмена веществ.
Функции биомолекул в живых организмах:
а) участие в реакциях обмена веществ в роли промежуточных продуктов
(метаболитов). Например, аминокислоты, моносахариды, жирные кислоты и
др.
б) участие в образовании сложных молекул (белков, нуклеиновых кислот,
липидов, полисахаридов) или биологических структур (мембран, рибосом,
ядерного хроматина и др.).
в) участие в регуляции биохимических процессов и функций отдельных
клеток и организма в целом (витамины, гормоны, циклические нуклеотиды
цАМФ, цГМФ и др.).
14.
Основные классы биомолекул:- Белки и аминокислоты
Белки – протеины (protos - первый, значимый), важнейший класс
биомолекул, с наличием которых связывают существование жизни в
условиях Земли. Белки являются молекулами, в состав которых входят 20
аминокислот.
- Нуклеиновые кислоты и нуклеотиды
Дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК) кислоты –
биополимеры,
состоящие
из
пуриновых
и
пиримидиновых
нуклеотидов. Они являются носителями генетической информации у всех
живых организмов.
15.
• Углеводы - молекулы, состоящие из моносахаридов и их производных(дисахаридов, гомо- и гетерополисахаридов). В животных организмах
моносахариды и гомополисахарид гликоген в основном исполняют
энергетические функции, а гетерополисахариды принимают участие в
образовании мембран, соединительной ткани и т.д.
• Липиды- молекулы, особенностью которых является гидрофобная
природа. Липиды выступают как энергетический материал
(нейтральные жиры), являются структурными компонентами мембран
(фосфолипиды, гликолипиды) и биорегуляторами (стероидные гормоны,
эйкозаноиды, жирорастворимые витамины).
16.
Витамины- соединения с различным химическим строением, не синтезирующиесяв животных организмах, но необходимые для их жизнедеятельности. Они должны
постоянно поступать в организм с продуктами питания, обеспечивая
нормальное течение метаболических процессов, так как являются компонентами
ферментных систем.
Гормоны и медиаторы- молекулы, передающие химические сигналы. Благодаря
регуляторному действию гормонов и медиаторов нервной системы происходит
интеграция
отдельных
анатомо-физиологических
систем
в
целостный
многоклеточный организм.
Кроме того в организме имеются свободные аминокислоты, азотистые соединения,
нуклеотиды, низкомолекулярные моно-, ди- и трикарбоновые кислоты, спирты,
амины, являющиеся промежуточными продуктами метаболизма.
17.
Согласно существующим представлениям, образование биомолекул ипервых примитивных живых клеток происходило на Земле под действием
физических факторов атмосферы приблизительно 3 млрд. лет тому назад
по схеме:
Неорганические молекулы атмосферы и океана – метан, аммиак, вода
Первичные биомолекулы – аминокислоты, нуклеотиды
Протоклетки (первичные клетки)
18.
Стенли Миллер (1953г.), обнаружил возможность образованияаминокислот при действии электрических разрядов на смесь метана,
аммиака, водорода и водяного пара. В этих реакциях синтеза
центральное место занимает цианистый водород – НСN, который может
образовываться в реакции: CH4 + NH3 →→→→ HCN + 3H2
В дальнейшем цианистый водород превращается в цианамид, нитрит и
цианоацетилен – предшественники аминокислот, пуринов, пиримидинов,
порфиринов.
19.
Принципы организации живой материи1. Принцип молекулярной экономии – комбинация небольшого
числа молекул дает бесконечное множество макромолекул.
Например, миллионы белков составлены из набора 20
аминокислот, а в состав ДНК входят в основном 4 азотистых
основания.
2. Принцип простой сложности – все биомолекулы состоят из
нескольких элементов – органогенов (С, Н, О, N, S, P).
3. Принцип
комплементарности
–
необходимость
пространственного соответствия отдельных частей биомолекул
при их образовании (например, для ДНК – это расположение
азотистых оснований по правилам Чаргаффа), а также при
взаимодействии макромолекул (например, комплексы антигенантитело, фермент-субстрат и т.д.) по типу «ключ-замок».
20.
Принципы функционирования живой материи1. Все реакции в живых организмах подчиняются ІІ закону
термодинамики и происходят по закону действующих масс
2. Большинство реакций в живых организмах являются
ферментативными, то есть протекают при участии ферментов –
катализаторов белковой природы
3. Все реакции в живых организмах протекают в водной среде, в том
числе и реакции окисления, при относительно невысоких
температурах.
4. Энергия в организмах выделяется при окислении питательных
веществ (углеводов, белков, жиров) и значительная ее часть
аккумулируется в виде макроэргических связей АТФ.
21.
Биохимические методыисследования
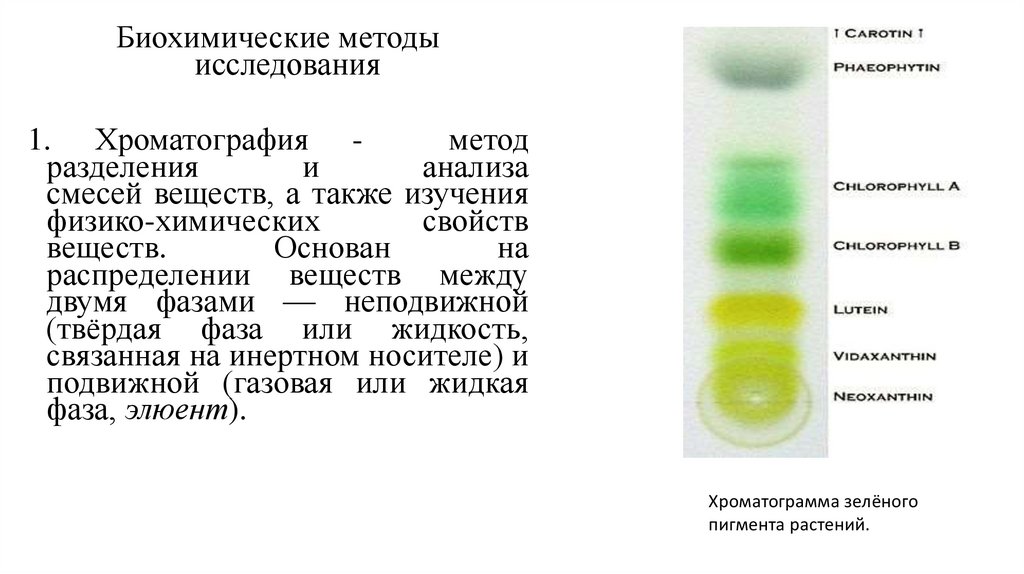
1. Хроматография метод
разделения
и
анализа
смесей веществ, а также изучения
физико-химических
свойств
веществ.
Основан
на
распределении веществ между
двумя фазами — неподвижной
(твёрдая фаза или жидкость,
связанная на инертном носителе) и
подвижной (газовая или жидкая
фаза, элюент).
Хроматограмма зелёного
пигмента растений.
22.
• Колонка — содержит хроматографический сорбент, выполняет функциюразделения смеси на индивидуальные компоненты.
• Элюент — подвижная фаза (растворитель или смесь растворителей): газ,
жидкость или (реже) сверхкритический флюид.
• Неподвижная фаза — твёрдая фаза или жидкость, связанная на инертном
носителе, в адсорбционной хроматографии — сорбент.
• Хроматограмма — результат регистрирования зависимости концентрации
компонентов на выходе из колонки от времени.
• Детектор — устройство для регистрации концентрации компонентов смеси
на выходе из колонки.
• Хроматограф — прибор для проведения хроматографии.
23.
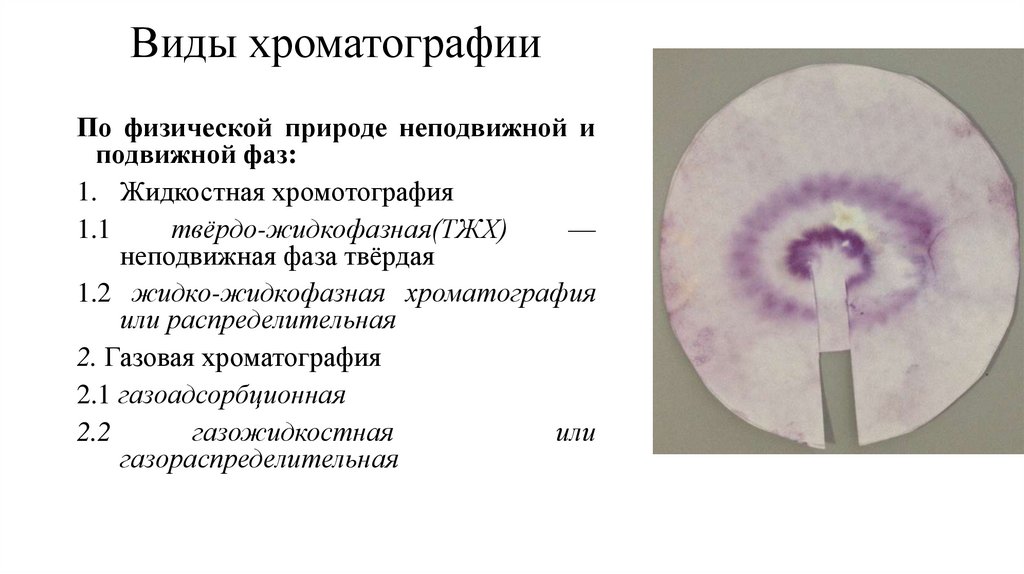
Виды хроматографииПо физической природе неподвижной и
подвижной фаз:
1. Жидкостная хромотография
1.1
твёрдо-жидкофазная(ТЖХ)
—
неподвижная фаза твёрдая
1.2 жидко-жидкофазная хроматография
или распределительная
2. Газовая хроматография
2.1 газоадсорбционная
2.2
газожидкостная
или
газораспределительная
24.
В зависимости от природы процесса, обусловливающегораспределение сорбатов между подвижной и неподвижной фазами:
• Адсорбционная
хроматография
—
разделение
за
счёт адсорбции основано на различии адсорбируемости компонентов
смеси на данном адсорбенте.
• Распределительная хроматография — разделение основано на
различии в растворимости сорбатов в подвижной и неподвижной фазах
или на различии в стабильности образующихся комплексов.
• Ионообменная хроматография — разделение основано на различии
констант ионообменного равновесия.
25.
• Осадочная хроматография — разделение основано на различнойрастворимости осадков в подвижной фазе.
• Аффинная хроматография — основана на биоспецифическом
взаимодействии компонентов с аффинным лигандом;
• Эксклюзионная хроматография — разделение основано на различии и
проницаемости молекул разделяемых веществ в неподвижную фазу.
Компоненты элюируются в порядке уменьшения их молекулярной
массы.
26.
По технике выполнения (характеру процесса)разделяют хроматографию на:
• Колоночную (неподвижная фаза находится в
колонке).
• Плоскостную (планарную) — бумажную и
тонкослойную (неподвижная фаза — лист бумаги
или тонкий слой сорбента на стеклянной или
металлической пластинке)
• Капиллярную (разделение происходит в плёнке
жидкости или слое сорбента, размещённом на
внутренней стенке трубки)
• Хроматографию
в
полях
(электрических,
магнитных, центробежных и других сил).
Жидкостный хроматограф Varian «ProStar 500
Series» (ВЭЖХ) с блоком предколоночной
дериватизации на базе автосамплера Varian
«410»
27.
2. Центрифугирование - разделение неоднородных систем на фракции поплотности при помощи центробежных сил. Центрифугирование применяется
для отделения осадка от раствора, для отделения загрязненных жидкостей, и
т.д.
28.
3.Электрофорез
способ
пространственного
разделения
молекул, имеющих разный заряд
и размеры, путем помещения их в
электрическое поле.
Виды электрофореза:
Гель-электрофорез
Иммуноэлектрофорез
Изоэлектрическое фокусирование в
градиенте рН
Белки дрожжей, разделённые с
помощью электрофореза в
полиакриламидном геле
29.
4. Потенциометрические методы– основаны на измерении разности
потенциалов
между
парой
подходящих
электродов,
погруженных в анализируемый
раствор.
30.
5.Фотоэлектроколориметрические методы анализа основаны насравнении интенсивности окраски исследуемого раствора с окраской
раствора,
концентрация
которого
известна
(стандарт).
При
колориметрических определениях используют реакции, в результате
которых определяемое вещество переводят в окрашенное соединение.
Интенсивность
окраски определяют на
фотоэлектроколориметре
(ФЭКе). Она прямо пропорциональна концентрации окрашенного
раствора
и
толщине
рассматриваемого
слоя.
Чем
больше
интенсивность окраски, тем выше оптическая плотность.
Фотоколориметр КФК-3
Кювета
для ФЭка
31.
6. Спектрофотометричекие методы анализа –определение количества вещества в растворе
или
твердой
среде
светопоглощения
вол
по
измерению
строго
определенной
длины.
Светопоглощение
измеряют
фотоэлемента
по
изменению
силы
тока,
возникающего
в
нем,
падении
на
при
с
помощью
фотоэлемент светового потока, прошедшего
через контрольный, а затем через исследуемый
образец. Измерение проводится в приборе
спектрофотометре.
Спектрофотометр UNICO 2150.
32.
Биохимический анализатор — это прибор для биохимическихисследований различных веществ: электролитов, ферментов,
гормонов и прочее. Он способен определить концентрацию и
наличие этих веществ практически в любых видах
биологического материала.
2 вида: автоматические и полуавтоматические
33.
Автоматические выполняют большой спектр операций: отборматериалов и реагентов, их смешивание и нагрев, анализ,
обработка и печать полученной информации, автоматическое
промывание прибора.
На полуавтоматических анализаторах процесс подготовки
анализируемых веществ оператор производит вручную, что
крайне неудобно для крупных лабораторий.
34.
Для более быстрой и удобной работы системы биохимическиеанализаторы могут быть оснащены:
• автоматическими манипуляторами,
• центрифугами для пробирок,
• специальным программным обеспечением
результатов пациентов.
для
обработки
35.
Полуавтоматический биохимическийанализатор
осуществляет
автоматическую
калибровку,
выдает
запрос
о
необходимости
добавления
следующей пробы. Расчет результатов
исследования
производится
по
выбранному оператором алгоритму и
отображается на дисплее прибора. В
некоторых модификациях приборов
предусмотрены
дополнительные
опции, позволяющие производить
сравнения результатов и определить
их адекватность по бланку, изменению
оптической плотности или значению.
Возможно
несколько
вариантов
предоставления
информации:
в
электронном виде (вывод результатов
на экране монитора либо сохранение
на записывающем устройстве), печать
на бумаге.
36.
Автоматические биохимические анализаторыТребуют минимального участия оператора. Оператор выбирает профиль
работы прибора в соответствии с порядком определения параметров и
количеством анализируемых проб. Все остальные действия по подготовке
пробы (выбор и смешивание реагентов, расчет результатов и др.)
осуществляются в автоматическом режиме.
37.
Преимущества автоматических анализаторов:• Высокая производительность, быстрота в обработке проб и
результатов анализов.
• Минимальные затраты на расходные материалы за счёт
автоматического смешивания, подачи реагентов и промывки
системы.
• Удобство и простота в управлении за счет современного
программного обеспечения с возможность подключения к
внешнему ПК и передачи данных в общелабораторную
компьютерную сеть.
• Опционально предусмотрена система охлаждения блока хранения
реагентов.
38.
Различают два типа автоматических биохимических анализаторов:«открытый» и «закрытый».
Закрытый
тип
анализаторов
предполагает
использование
ограниченного числа реагентов, предусмотренных производителем. В
систему изначально внесены контрольные и калибровочные данные, а
информация о применяемых реагентах в данном конкретном
исследовании заносится в прибор посредством считывания штрих-кода с
их упаковки. Ограниченность выбора реагентов является минусом
данного анализатора. Как правило, заявленные производителем реагенты
достаточно дорогостоящие, заменить их более дешевыми аналогами
нельзя, так как это может привести к некорректной работе самого
анализатора. К плюсам анализатора данного типа можно отнести
стабильность результатов калибрования.
39.
Биохимический анализатор BS-12040.
Открытыйтип
анализаторов
предполагает
возможность
использования реагентов практически любого производителя
благодаря встроенному набору светофильтров для проведения
наиболее распространенных методик анализа. В остальном работа
систем открытого и закрытого типа одинакова.
41.
Взависимости
от
потенциальных
возможностей
приборов
биохимические автоанализаторы подразделяют на:
1) малые (обладающие производительностью примерно 100— 120
анализов/ч);
2) средние (180—250 анализов/ч);
3) современные большие многоканальные (позволяющие выполнять 400—
600—800 и более анализов/ч).
В зависимости от габаритов и массы приборов различают:
1) настольные автоанализаторы (малогабаритные приборы, не требующие
дополнительной водоподготовки);
2) напольные автоанализаторы с системой водоочистки (иногда
нуждающиеся в расположении в отдельной комнате, оснащенной
кондиционером).
42.
Материалом для биохимических исследований в КДЛ могут быть:Биологические жидкости внутренних сред организма:
- цельная кровь
- сыворотка и плазма крови
- спинномозговая жидкость,
- лимфа и др.
Биологические выделения:
- моча
- желчь
- слюна
- желудочный и кишечный соки
- кал и др.
43.
Методы забора биологического материала:1. Безинструментальный – так собирают мочу, кал, мокроту, слюну и
т.д.
2. Пункционный – материал берут с помощью игл из вены, артерий,
спинного мозга, суставов.
3. Прокол иглой – кровь из пальца.
4. Пункционная биопсия – пункция из внутренних органов.
5. Зондовый метод – сбор желудочного сока, мочи и т.д.
6. Промывание легких, мочевого пузыря и т.д.
7.Мазки и соскобы из носовой полости, зева, слизистой матки.
8. Отпечатки с ран, свищей, эрозий.










































 Биология
Биология Химия
Химия








