Похожие презентации:
Кислород, его характеристика, получение и свойства
1.
«Кислород – это та ось, вокругкоторой вращается химия»
А.Берцелиус
2.
План урока1. Нахождение кислорода в природе.
2. История открытия кислорода.
3. Кислород, как элемент
4. Свойства кислорода.
5. Получение кислорода в лаборатории.
6. Применение кислорода.
7. Домашнее задание
8. Закрепление
3.
1. Нахождениекислорода в природе.
4.
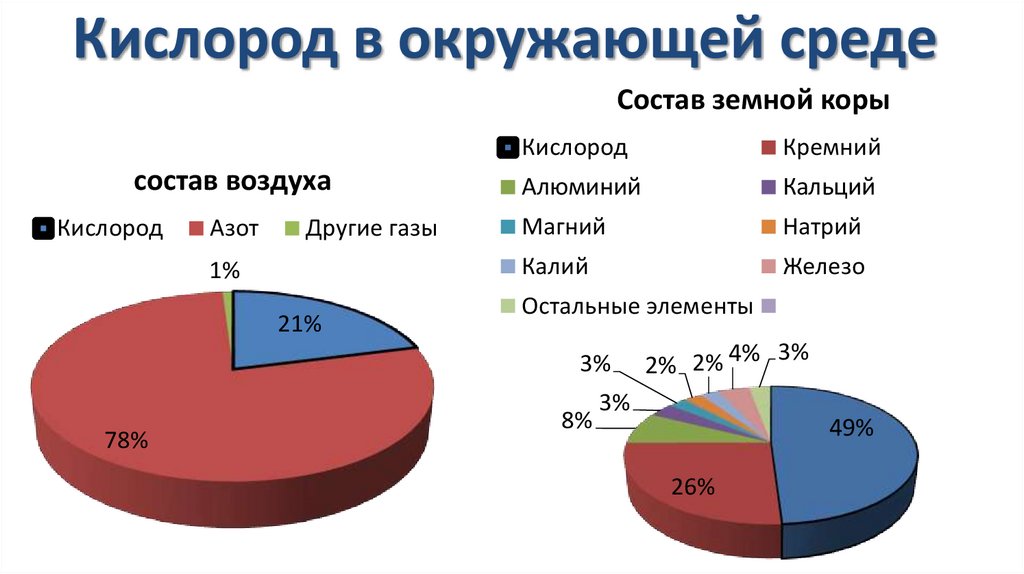
Кислород в окружающей средеСостав земной коры
состав воздуха
Кислород
Азот
Другие газы
1%
21%
78%
Кислород
Кремний
Алюминий
Кальций
Магний
Натрий
Калий
Железо
Остальные элементы
3% 2% 2% 4% 3%
3%
8%
49%
26%
5.
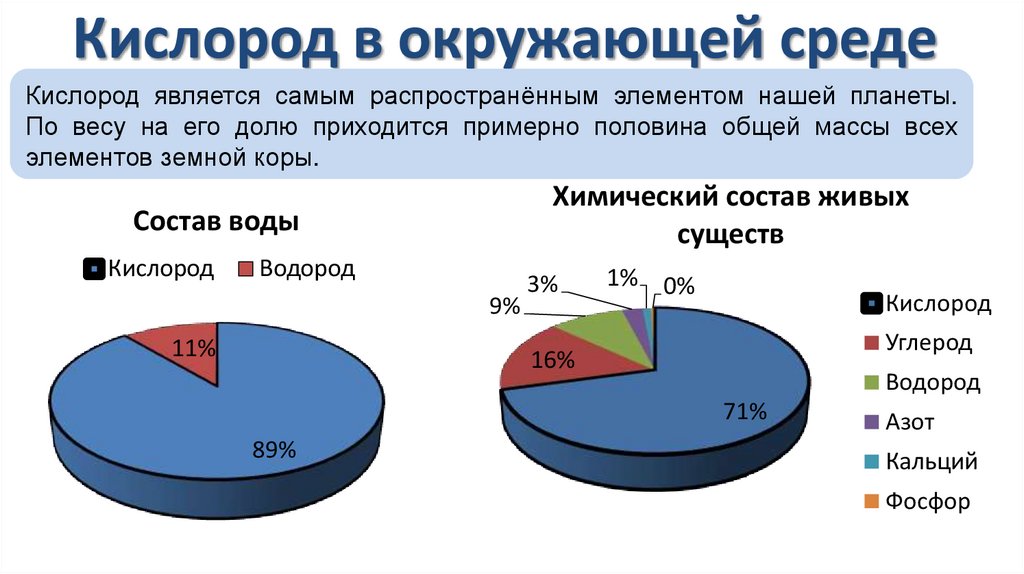
Кислород в окружающей средеКислород является самым распространённым элементом нашей планеты.
По весу на его долю приходится примерно половина общей массы всех
элементов земной коры.
Химический состав живых
существ
Состав воды
Кислород
Водород
9%
11%
3%
1% 0%
Кислород
Углерод
16%
Водород
71%
89%
Азот
Кальций
Фосфор
6.
2. История открытиякислорода.
7.
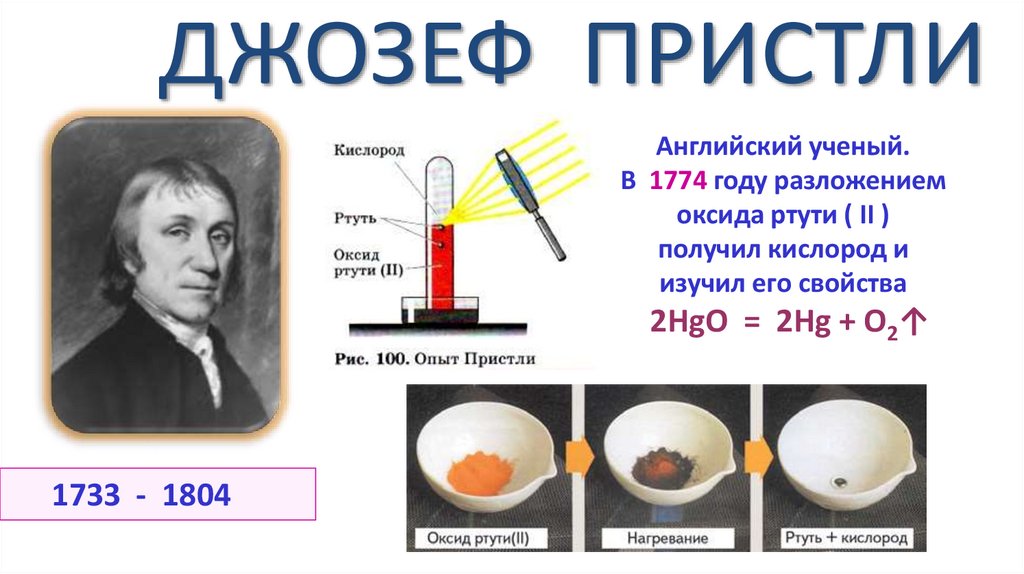
Английский ученый.В 1774 году разложением
oксида ртути ( II )
получил кислород и
изучил его свойства
2HgO = 2Hg + O2↑
1733 - 1804
8.
глицеринхлор
молибден
барий
1742 - 1786
Шведский ученый.
В 1771 году провел опыты
по разложению
оксида ртути ( II ),
изучил свойства
образующегося газа.
Однако результаты
его исследований
были опубликованы
лишь в 1777 году.
9.
С целью проверки опытов Шееле и Пристлив 1774 году получил кислород, установил его
природу и изучил его способность соединяться
с фосфором и серой при горении и металлами
при обжиге. Изучил состав атмосферного воздуха.
Создал кислородную теорию горения. Совместно с
Ж. Менье установил сложный состав воды и получил
воду из кислорода и водорода.
2H2 + O2 = 2H2O
Лавуазье показал, что процесс дыхания
подобен процессу горения.
1743 - 1794
Название кислороду Oxygenium дал А. Лавуазье
10.
Голландский алхимик и технолог. Получил кислородпримерно за 150 лет до Пристли и Шееле при
нагревании нитрата калия:
2КNO3 = 2KNO2 + O2 ↑ Его открытие было
засекречено, т.к. использование полученного газа
предполагалось для дыхания людей
на
подводных лодках
1572 - 1633
11.
3. Кислород, какэлемент
12.
Кислород как элемент.В какой группе, подгруппе и периоде находится элемент кислород?
Какой он имеет порядковый номер?
Какая атомная масса кислорода?
Какая валентность?
В состав каких
веществ и соединений
входит кислород?
13.
Кислород как элемент.1.
2.
3.
4.
5.
Элемент кислород находится в VI группе, главной
подгруппе, II периоде,
порядковый номер №8,
Ar = 16.
валентность II
Входит в состав оксидов, оснований, солей, кислот,
органических веществ, в том числе живых организмовдо 65% по массе.
14.
4. Свойства кислорода.15.
Физические свойстваГаз - без цвета, вкуса и запаха; в 100V H2O растворяется 3V O2 (н.у.);
t кип= -183 С; t пл = -219 C; d по воздуху = 1,1.
При давлении 760 мм. рт.ст. и температуре
–183 С кислород сжижается
3
2
Сосуд Дьюара
16.
Химические свойстваВзаимодействие веществ с кислородом называется окислением.
С кислородом реагируют все элементы, кроме Au, Pt, He, Ne и Ar, во всех
реакциях (кроме взаимодействия со фтором) кислород - окислитель.
С неметаллами
Со сложными веществами
4FeS2 + 11O2 2Fe2O3 + 8SO2
2H2S + 3O2 2SO2 + 2H2O
CH4 + 2O2 CO2 + 2H2O
C + O2 CO2
S + O2 SO2
2H2 + O2 2H2O
С металлами
2Mg + O2 2MgO
2Cu + O2 –t 2CuO
17.
5. Получениекислорода в
лаборатории.
18.
Способы получения кислорода1) разложение перманганата калия
2KMnO4 = K2MnO4 + MnO2 + O2↑
19.
2) разложение пероксида водорода2H2O2 = 2H2O + O2↑
Катализаторы – это вещества, которые ускоряют ход химической реакции, но сами
при этом не расходуются.
Пример: MnO2 ускоряет процесс разложения перекиси водорода.
20.
3) разложение хлората калия2KClO3 = 2KCl + 3O2↑
4) разложение оксида ртути (II)
2HgO = 2Hg + O2↑
5)электролиз воды
2H2O = 2H2↑ + O2↑
21.
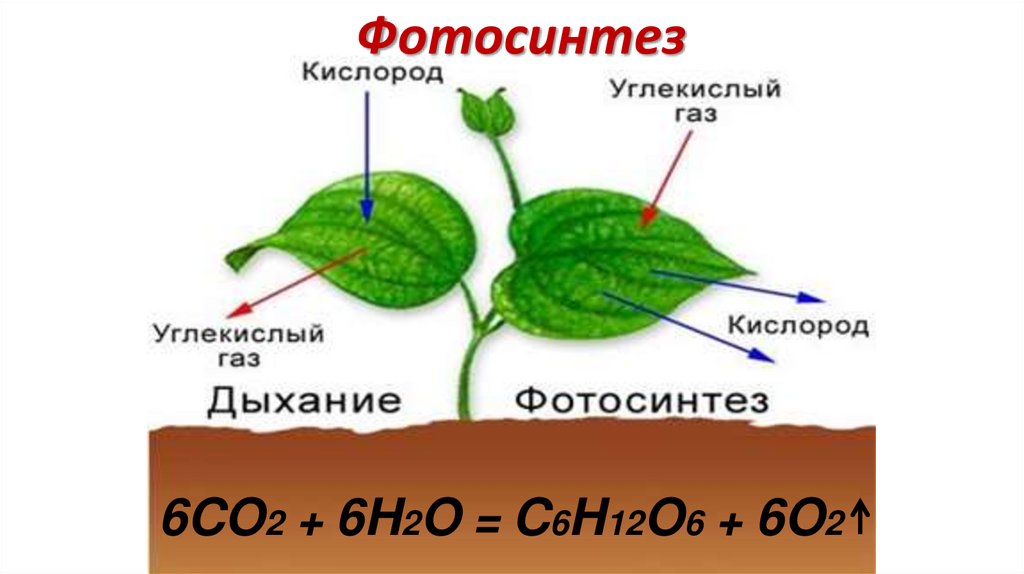
Фотосинтез6CO2 + 6H2O = C6H12O6 + 6O2
22.
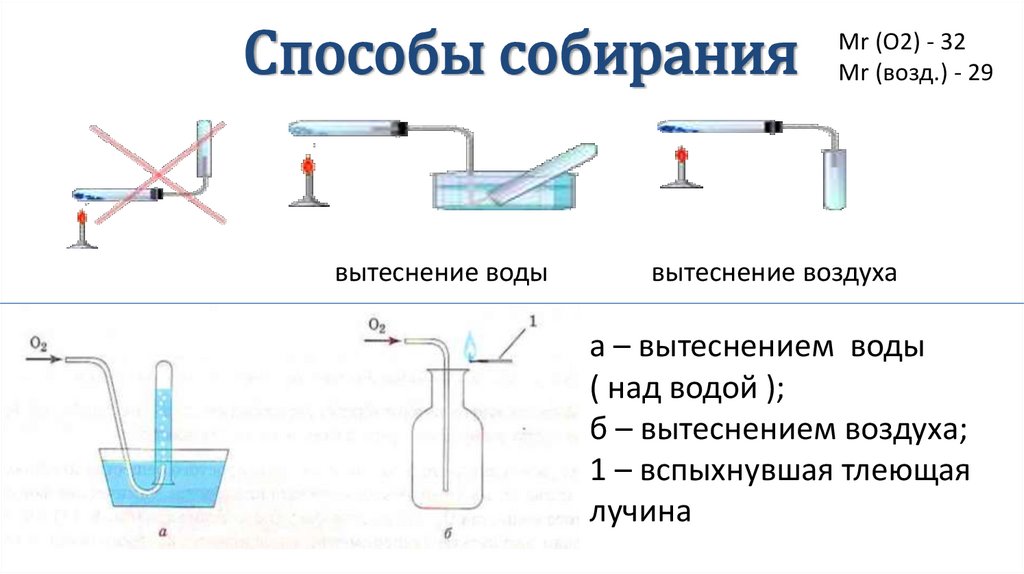
Способы собираниявытеснение воды
Mr (O2) - 32
Mr (возд.) - 29
вытеснение воздуха
а – вытеснением воды
( над водой );
б – вытеснением воздуха;
1 – вспыхнувшая тлеющая
лучина
23.
6. Применениекислорода.
24.
Применение кислорода:Находит широкое применение в медицине
и промышленности.
При высотных полётах лётчиков снабжают
специальными приборами с кислородом.
При многих лёгочных и сердечных
заболеваниях, а также при операциях дают
вдыхать кислород из кислородных
подушек.
Кислородом в баллонах снабжают
подводные лодки.
Горение рыхлого горючего материала,
пропитанного жидким кислородом,
сопровождается взрывом, что даёт
возможность применять кислород при
взрывных работах.
Жидкий кислород применяют в реактивных
двигателях, в автогенной сварке и резке
металлов, даже под водой.
25.
7. Домашнее заданиеконспект данной
информации!
26.
8. Закрепление27.
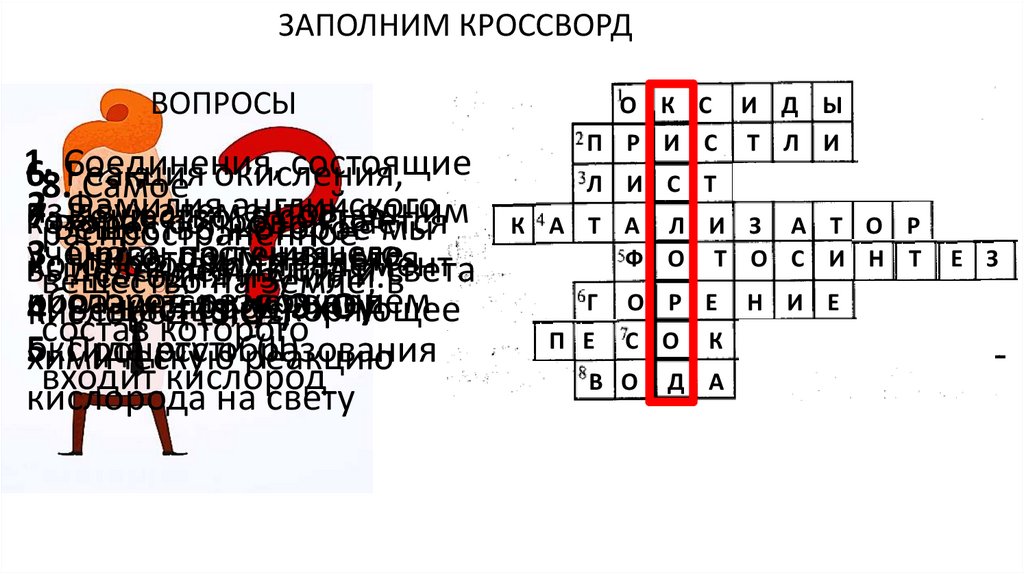
ЗАПОЛНИМ КРОССВОРДВОПРОСЫ
1.
состоящие
6.8.Соединения,
Реакция
окисления,
Самое
2.
Фамилия
английского
из
двух
элементов,
одним
7.распространенное
Вещество,
в состав
которая
сопровождается
Вещество, которое
мы
ученого,
получившего
3.
Орган
растения,
где
изсегодня
которых
является
которого
входит
элемент
выделением
тепла
и всвета
вещество наизучили.
Земле,
кислород
разложением
образуется
кислород
кислород
4.
Вещество,
ускоряющее
кислород
(SiO
2)ЭхОу
состав которого
оксида
ртути
(II)
5.
Процесс
образования
химическую
реакцию
входит кислород
кислорода на свету
О К С И Д Ы
П Р И С Т Л И
Л И С Т
К А Т А Л И З А Т О Р
Ф О Т О С И Н Т
Г
П Е
О Р Е Н И Е
С О К
В О
Д А
Е З






















 Химия
Химия








