Похожие презентации:
Класифікація неорганічних сполук. Оксиди
1.
Класифікаціянеорганічних сполук.
Оксиди
2.
Неорганічні сполуки – це сполуки, які утворюються всіма хімічнимиелементами (крім більшості органічних сполук Карбону),
хімічні речовини не рослинного і не тваринного походження
Прості речовини утворені атомами одного хімічного елемента:
неметали
aлюміній Al
сірка S
ртуть Hg
кисень O2
залізо Fe
метали
гелій He
3.
Складні речовини утворені атомами різних хімічних елементів:Оксиди
Кислоти
oртофосфатна
H3PO4
Основи
натрій
гідроксид
NaOH
силіцій (ІV) оксид
SiO2
кальцій карбонат СаСО3
ферум (ІІІ) гідроксид
Fe(OH)3
ферум (ІІІ) оксид Fe2O3
Солі
хлоридна HCl
натрій хлорид
NaCl
4.
Оксиди - складні речовини, які складаютьсяз двох хімічних елементів, один з яких є Оксиген
Алгоритм складання формули оксиду:
1. Записуємо два елементи, символ Оксигену
завжди пишеться на другому місці.
2. Над символами елементів ставимо валентності.
ІІІ
ІІ
Al O
5.
Алгоритм складання формули оксиду:1. Записуємо два елементи, символ Оксигену
завжди пишеться на другому місці.
2. Над символами елементів ставимо валентності.
3. Знаходимо найменше спільне кратне для значень
валентностей.
4. Знаходимо число атомів елементів, поділивши
найменше спільне кратне на значення валентностей.
6
ІІІ
ІІ
Al O
2
3
6.
Назви оксидів:1. Для елементів зі сталою валентністю:
назва елемента + слово «оксид»
Al2O3 – алюміній оксид, СаО – кальцій оксид
2. Для елементів зі змінною валентністю:
назва елемента + валентність + слово «оксид»
CO – карбон (ІІ) оксид, SO2 – сульфур (ІV) оксид
7.
8.
Кислотні оксиди – такі, яким відповідають кислотиSO3
Н2SO4
сульфур (VІ) оксид
сульфатна кислота
N2O5
НNO3
нітроген (V) оксид
нітратна кислота
- більшість оксидів неметалічних елементів:
SO2, CO2, Р2O5
- оксиди металічних елементів зі ступенем окиснення, більшим +3:
CrO3, Mn2O7
9.
Основні оксиди – такі, яким відповідають основиNa2O
NaOH
натрій оксид
натрій гідроксид
FeO
Fе(OН)2
ферум (ІІ) оксид
ферум (ІІ) гідроксид
- оксиди металічних елементів зі ступенем окиснення +1,+2,
рідко +3:
CaO, Na2O, MgO, BaO, FeO
10.
Амфотерні оксиди – оксиди, що виявляютьвластивості як кислотних, так і основних оксидів
ZnO
цинк оксид
Al2O3
алюміній оксид
Zn(OН)2 цинк гідроксид
Н2ZnO2 цинкатна кислота
Al(OН)3 алюміній гідроксид
Н3AlO3 алюмінатна кислота
До амфотерних оксидів належать:
BeO, ZnO, PbO, Al2O3, Fe2O3, Cr2O3
11.
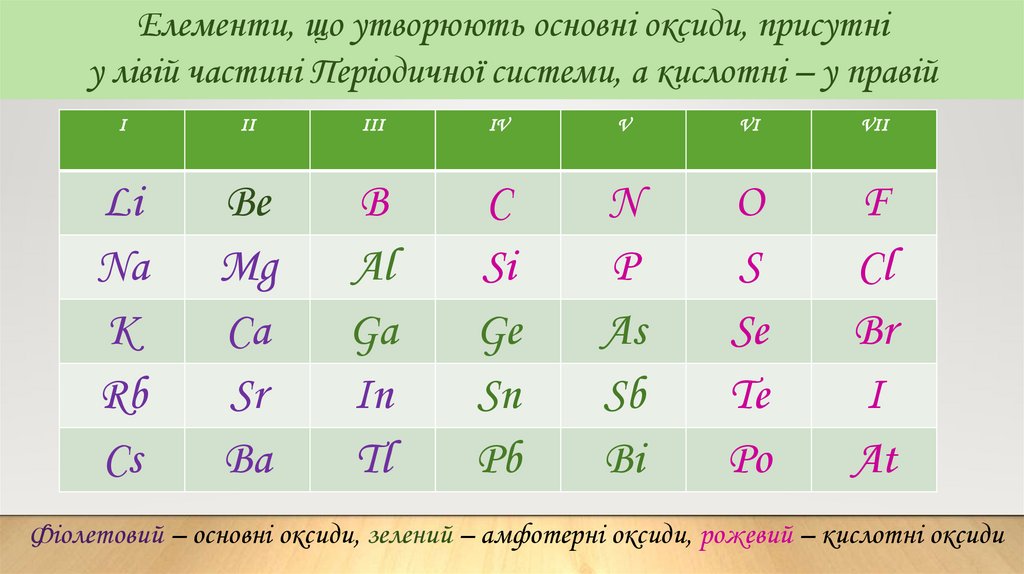
Елементи, що утворюють основні оксиди, присутніу лівій частині Періодичної системи, а кислотні – у правій
І
ІІ
ІІІ
ІV
V
VI
VII
Li
Na
K
Rb
Cs
Be
Mg
Ca
Sr
Ba
B
Al
Ga
In
Tl
C
Si
Ge
Sn
Pb
N
P
As
Sb
Bi
O
S
Se
Te
Po
F
Cl
Br
I
At
Фіолетовий – основні оксиди, зелений – амфотерні оксиди, рожевий – кислотні оксиди
12.
Фізичні властивості і значення оксидівОсновні та амфотерні оксиди
при кімнатній температурі –
це тверді речовини
СаО
Оксиди металів можуть бути забарвлені
у різні кольори
Cu2O
К2О
Fe2О3
Cr2O3
HgO
13.
Фізичні властивості і значення оксидівСеред кислотних оксидів є тверді речовини, рідини, газоподібні
Cl2O7
Р2O5
SiO2
Кристали SO3 при +17 °C стають рідиною
SO2
NO2
14.
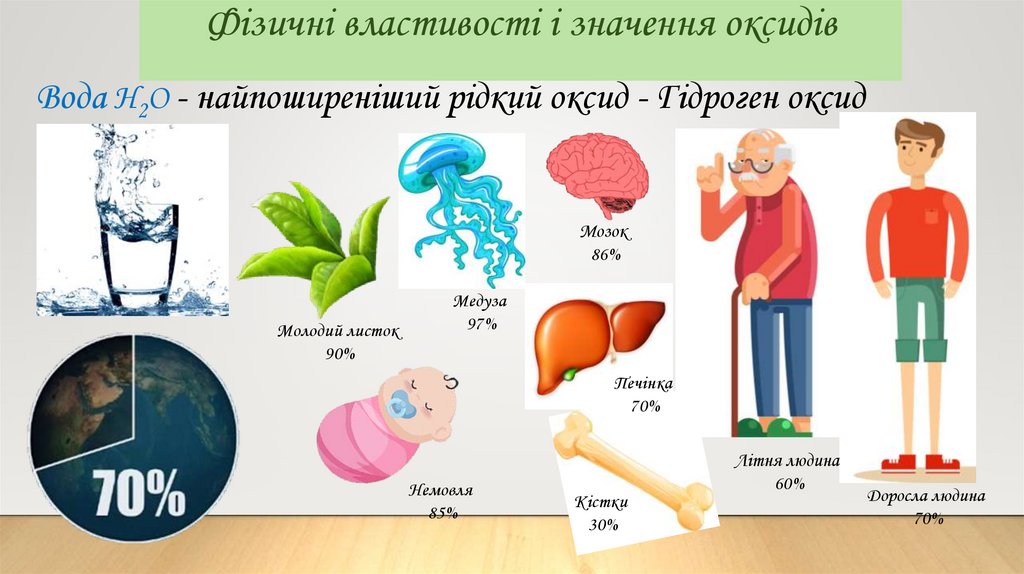
Фізичні властивості і значення оксидівВода Н2O - найпоширеніший рідкий оксид - Гідроген оксид
Мозок
86%
Молодий листок
90%
Медуза
97%
Печінка
70%
Немовля
85%
Кістки
30%
Літня людина
60%
Доросла людина
70%
15.
Фізичні властивості і значення оксидівСиліцій оксид SiO2 – найпоширеніший твердий оксид
Глина і пісок
атом Силіцію
атом Оксигену
Аметист
Гірський кришталь
Атоми Силіцію і Оксигену утворюють атомну кристалічну
гратку, тому кристали тверді, тугоплавкі, але крихкі
16.
Фізичні властивості і значення оксидівАлюміній оксид Al2O3 – поширений твердий оксид
Рубін – корунд,
забарвлений
сполуками Хрому
Al2O3
Корунд - мінерал,
кристалічний
алюміній оксид Al2O3
Сапфір – корунд,
забарвлений сполуками Титану
і Феруму
17.
Фізичні властивості і значення оксидівФерум оксид Fe2O3 надає характерного кольору піску, грунтам, іржі
Гематит
Магнетит
18.
Фізичні властивості і значення оксидівВуглекислий газ СO2 живі організми видихають в процесі дихання,
а рослини використовують для фотосинтезу
19.
Фізичні властивості і значення оксидівНітроген (ІІ) оксид NO
утворюється при електричних
розрядах під час грози
Найотруйнішим із оксидів є чадний газ СО,
що утворюється при нестачі кисню
Нітроген (IV) оксид NO2
- газ бурого кольору,
його ще називають
«лисячим» хвостом
20.
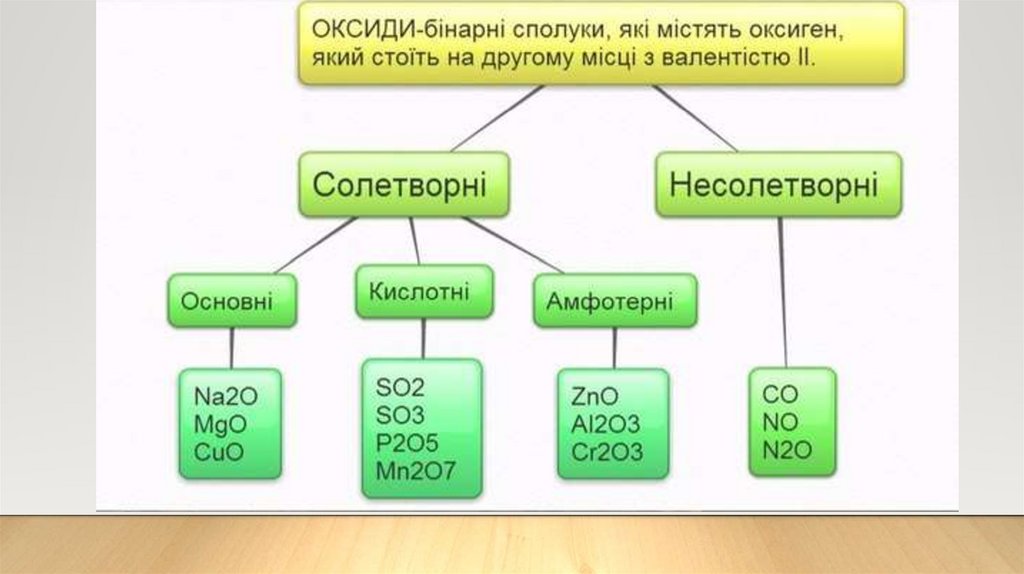
ПідсумкиОксиди – бінарні сполуки, які складаються з двох
хімічних елементів, один з яких є Оксиген.
Оксиди поділяються на солетворні та несолетворні.
Солетворні оксиди поділяють на групи:
- кислотні – їм відповідають кислоти,
- основні - їм відповідають основи,
- амфотерні - оксиди, що виявляють властивості
як кислотних, так і основних оксидів.
Найпоширенішим рідким оксидом є Гідроген оксид –
вода.
Силіцій оксид – найпоширеніший твердий оксид.

















 Химия
Химия








