Похожие презентации:
Рак тела матки
1.
РАК ТЕЛА МАТКИ(лекция)
Порханова Наталья Владимировна
2.
РТМ — самая частая ЗНО женских половыхорганов в развитых странах и 2-я по частоте
после рака шейки матки злокачественная
опухоль женских половых органов в мире
В структуре смертности от онкозаболеваний
в России в 2016 году среди женщин занимает
9 место (4,9%). Летальность на первом году с
момента установления диагноза составила
8,6%
3. Заболеваемость РТМ
Ежегодно в мире регистрируется189.000 новых случаев РТМ и 44.700 смертей.
В США в 2015 г.
выявлено 54 800
умерло 10 150 б-ных.
В России ежегодно выявлено 21 000
В структуре заболеваемости женского населения в
России в 2016 г. занимал 3-е ранговое место (7,7%)
По отношению к 2006 г. прирост составил 23,54%
Средний возраст - 62,6 года
Более 80% больных выявляется на ранних (I-II) стадиях
4. Морфологическая классификация злокачественных опухолей тела матки
Злокачественные эпителиальные опухоли:8380/3 Эндометриоидная аденокарцинома
8570/3 Вариант с плоскоклеточной метаплазией
8263/3 Виллогландулярный вариант
8382/3 Секреторный вариант
8480/3 Муцинозный рак
8441/2 Серозный эндометриальный интраэпителиальный
рак
8441/3 Серозный рак
8310/3 Светлоклеточный рак
5. Морфологическая классификация злокачественных опухолей тела матки
Нейроэндокринные опухолиС низкой степени злокачественности
8240/3 карциноид
С высокой степени злокачественности
8041/3 Мелкоклеточный нейроэндокринный рак
8013/3 Крупноклеточный нейроэндокринный рак
8323/3 Смешанная аденокарцинома;
8020/3 Недифференцированный рак
Злокачественные смешанные эпителиальные и
мезенхимальные опухоли:
8933/3 Аденосаркома;
8980/3 Карциносаркома.
6.
Стадии РТМ определяют по результатаминтраоперационной ревизии и результатов
послеоперационного гистологического
исследования с помощью классификации
TNM (UICC, 7-й пересмотр, 2009 г.) или
FIGO (2009 г.)
7. Классификации TNM (UICC, 7-й пересмотр, 2009 г.) или FIGO (2009 г.)
Тх Невозможно оценить состояние первичной опухолиT0 Первичная опухоль отсутствует
Tis Рак in situ
T1a IA Опухоль в пределах эндометрия или опухоль с инвазией
менее половины толщины миометрия
T1b IB Опухоль с инвазией более половины толщины
миометрия
T2 II Опухоль распространяется на строму шейки матки, но не
выходит за пределы матки
T3a IIIA Прорастание серозной оболочки матки, поражение
маточных труб или яичников (непосредственный переход
опухоли или метастазы)
T3b IIIB Поражение влагалища или параметриев
(непосредственный переход опухоли или метастазы)
8. Классификации TNM (UICC, 7-й пересмотр, 2009 г.) или FIGO (2009 г.)
T4 IVA Прорастание слизистой оболочки мочевого пузыря илипрямой кишки
NX Оценить состояние регионарных лимфатических узлов
невозможно
N0 Метастазов в регионарных лимфатических узлах (тазовых или
поясничных) нет
N1 IIIC Метастазы в регионарных лимфатических узлах (тазовых
или поясничных)
IIIC1 Метастазы в тазовых лимфатических узлах
IIIC2 Метастазы в поясничных лимфатических узлах
M0 Отдаленных метастазов нет
M1 IV Отдаленные метастазы (в том числе метастазы в паховых
лимфатических узлах и лимфатических узлах в пределах брюшной
полости, кроме тазовых или поясничных лимфатических узлов; за
исключением метастазов во влагалище, в придатках матки и по
тазовой брюшине)
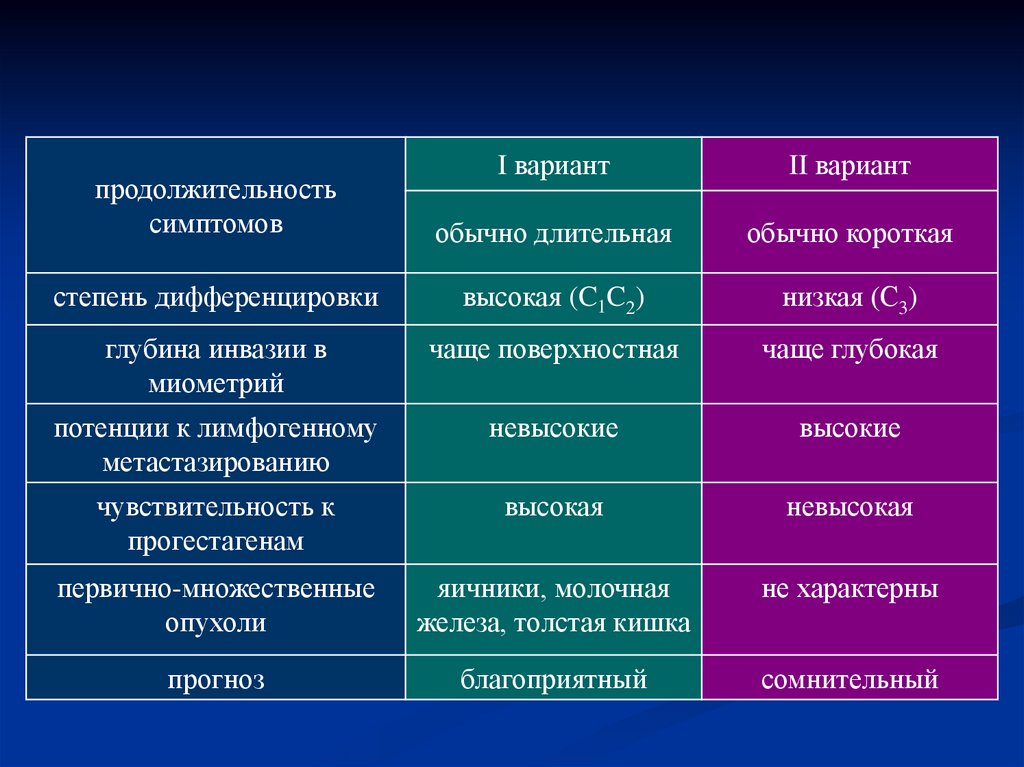
9.
продолжительностьсимптомов
I вариант
II вариант
обычно длительная
обычно короткая
степень дифференцировки
высокая (C1C2)
низкая (С3)
глубина инвазии в
миометрий
чаще поверхностная
чаще глубокая
потенции к лимфогенному
метастазированию
невысокие
высокие
чувствительность к
прогестагенам
высокая
невысокая
первично-множественные
опухоли
яичники, молочная
железа, толстая кишка
не характерны
прогноз
благоприятный
сомнительный
10. ФАКТОРЫ РИСКА.
Бесплодие и нарушение менструального цикла,связанное с
ановуляцией,
приводящей
к
гиперэстрогении на фоне снижения секреции
прогестерона.
Отсутствие родов, при этом риск развития PTМ в
2-3 раза выше, чем у рожавших.
Поздняя менопауза (после 52 лет) увеличивает
риск возникновения PTМ в 2,4 раза.
Это
объясняется увеличением с возрастом числа
ановуляторных циклов.
11.
2.Ожирение увеличивает риск возникновения
РТМ в 3 раза, если масса тела превышает
нормальную на 10-22 кг., и в 10 раз, если
превышает на 22 кг. (Это происходит в
результате более активного превращения
андростендиона
в
эстрон
в подкожной
клетчатке и,
следовательно
гиперэстрогении).
Синдром Штейна-Левенталя,
гормонопродуцирующие опухоли яичников,
наличие гормонозависимых опухолей в
анамнезе (при перенесенном ранее раке
молочной железы в 14 раз чаще встречается
РТМ.
12.
3.Неадекватная заместительная
гормонотерапия в постменопаузе без
прогестинов увеличивает риск
возникновения РТМ в 4-8 раз,
длительный прием эстрогенов - в 10-15
раз.
Прием тамоксифена - в 8 раз.
При сахарном диабете - в 3 раза.
Наследственный фактор.
13. Факторы риска
хронический эндометрит,кровотечение в постменопаузе,
аденомиоз в постменопаузе,
употребление в пищу большого
количества животных белков и
жиров.
14. Риск рака тела матки снижают:
комбинированные оральные контрацептивы:риск рака тела матки снижается на 11,7 % в год;
снижение риска сохраняется в течение более 15
лет после прекращения приема оральных
контрацептивов;
прием β-каротина, мононенасыщенных
жирных кислот, фруктов и овощей;
физическая активность;
умеренное потребление алкоголя (по
некоторым данным);
курение.
15. Этапы онкогенеза при РЭ
I.II.
III.
IV.
- функциональных нарушений (ановуляция,
гиперэстрогения);
- формирование морфологических нарушений,
расцениваемых как фоновые (диффузная и
очаговая гиперплазия эндометрия);
- формирование морфологических изменений,
расцениваемых как предраковые (слабо и умеренно
выраженные формы атипической гиперплазии);
- развитие злокачественной опухоли (фаза
преинвазивного рака - выраженная форма
атипической гиперплазии, рак в пределах
слизистой, рак с минимальной инвазией,
выраженные формы рака эндометрия).
16. Предопухолевая патология
При гиперплазии эндометрия (простая гиперплазияэндометрия и сложная гиперплазия эндометрия –
аденоматоз без атипии) малигнизация отмечается в 1-3%
наблюдений. Лечение гормональное, редко – оперативное.
Нельзя забывать о гормонопродуцирующих опухолях
яичников!
При атипической гиперплазии ( простая атипическая
гиперплазия и сложная атипическая гиперплазия –
аденоматоз с атипией) малигнизация отмечается в 30-50%
наблюдений. Лечение оперативное. По строго
индивидуальным показаниям молодым больным может
быть предпринята попытка гормонального лечения*.
(аблация и резекция эндометрия при АГ противопоказаны)
17. Патологическая анатомия
Формы роста РЭэкзофитная
эндофитная
смешанная
Локализация
в дне матки – 47,5%,
вся полость матки – 24,9%,
нижний сегмент – 27,6%.
Аденокарцинома представлена в 80% наблюдений.
а) Аденокарцинома эндометрия с плоскоклеточной метаплазией
встречается в 15-25% наблюдений.
б) Светлоклеточная ( мезонефроидная ) аденокарцинома
составляет менее 5% всех случаев РЭ, является одной из самых
агрессивных опухолей.
в) Истинный плоскоклеточный рак эндометрия – крайне редкая
форма опухоли, в мировой практике описано всего 70
наблюдений. Следует дифференцировать с плоскоклеточным
раком цервикального канала и аденокарциномой с
плоскоклеточной метаплазией. Прогноз крайне
неблагоприятный, даже при I стадии заболевания выживаемость
не превышает 36%.
18. Патологическая анатомия
г) Муцинозная аденокарцинома – также редкая форма ракаэндометрия, встречается у 5% больных данной патологией.
Чаще опухоли с высокой дифференцировкой, имеют
благоприятный клинический прогноз.
д) Папиллярная серозная аденокарцинома встречается в 34% наблюдений рака эндометрия. Морфологически имеет
сходство с серозным раком яичников и маточных труб.
Характеризуется очень быстрым лимфогенным и
гематогенным метастазированием, глубокой инвазией в
миометрий и диссеминацией по брюшной полости, как при
раке яичников. Прогноз неблагоприятный.
е) Недифференцированный рак встречается редко (6%),
чаще у пожилых больных, отличается агрессивным
течением.
ж) Синхронный рак эндометрия и яичников. Крайне
трудно провести дифференциальный диагноз между РЭ с
метастазами в яичники, метастазами рака яичников в
эндометрий и истинным синхронным заболеванием.
19. Патологическая анатомия
Кроме тоговстречаются
следующие формы патологии:
мелкоклеточная
нейроэндокринная карцинома,
переходноклеточная
карцинома,
смешанная карцинома
эндометрия.
20. Рак тела матки Регионарные лимфатические узлы
Регионарными лимфатическими узламиявляются тазовые
(подчревные, запирательные),
общие, внутренние и наружные
подвздошные,
расположенные около матки, крестцовые,
парааортальные.
21. Риск лимфогенной диссеминации зависит от:
гистологического типа опухоли,степени дифференцировки,
глубины инвазии,
размеров опухоли,
перехода опухоли на шейку матки,
распространение опухоли за пределы матки.
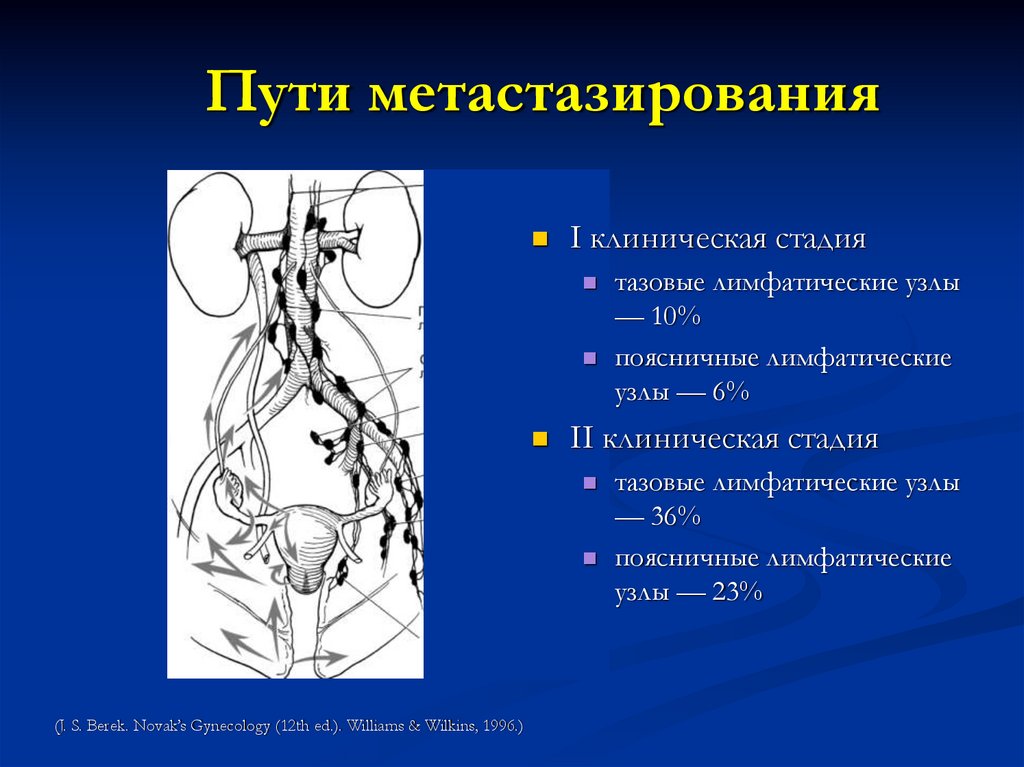
22. Пути метастазирования
I клиническая стадиятазовые лимфатические узлы
— 10%
поясничные лимфатические
узлы — 6%
II клиническая стадия
тазовые лимфатические узлы
— 36%
поясничные лимфатические
узлы — 23%
(J. S. Berek. Novak’s Gynecology (12th ed.). Williams & Wilkins, 1996.)
23. Метастазирование РЭ в лимфоузлы малого таза
• в зависимости от выраженности секреции в опухоли:выраженная секреция
- 5,0%
отсутствие секреци
- 16,7%
• от локализации опухоли:
в/з матки
- 2,1%
поражение всей матки
- 14,7%
переход на ц/канал
- 21%
• от глубины инвазии (при диаметре опухоли > 2 см)
до 0,5 см
- 5,1%
0,6 -1 см
- 6,7%
более 1 см
- 17,2%
• от диаметра опухоли
до 2 см
- 1%
2,1 - 3 см
- 6,2%
более 3 см
- 27,3%
24. Метастазирование РЭ в лимфоузлы малого таза
В зависимости от возраста:до 30 лет - метастазы не определялись
40-49 лет - 5,7%
старше 70 лет - 15,4%
при I патогенетическом варианте - 8,9%
при II патогенетическом варианте - 13,6%
В зависимости от степени дифференцировки опухоли
высокодифференцированная
- 4,5%
умереннодифференцированная - 10,1%
низкодифференцированная
- 16,1%
25. Метастазирование в лимфоузлы
Метастазытазовые л/у
поясничные л/у
Низкодифференцированная
опухоль (предоперационное
исследование)
18%
11%
Инвазия миометрия > ½
25%
17%
Распространение на шейку матки
15—30%
Поражение придатков матки или
брюшины
32%
20%
Опухолевые клетки в смывах
25%
19%
Опухоль > 2 см
15—35%
Boronow R.C. et al, 1984; Creasman W.T et al, 1987; Schink J.C. et al, 1987
26. Клиническая картина
Основное проявление рака тела матки -кровянистые выделения из половых путей и
маточные кровотечения:
наблюдаются у 70—90 % больных;
в репродуктивном периоде возможна менометроррагия;
в пременопаузе и постменопаузе наблюдаются
ациклические кровянистые выделения;
при стенозе цервикального канала выделений не бывает,
развивается гематометра;
27.
2.кровянистые выделения из влагалища в
постменопаузе - тревожный симптом, требующий
неотложного тщательного об
следования;
причиной кровянистых выделений далеко не всегда
бывает рак тела матки:
более частая причина — атрофия эндометрия в
постменопаузе;
заместительная гормонотерапия в постменопаузе,
полипы и
гиперплазия эндометрия являются причиной
кровянистых выделений в постменопаузе так же часто,
как рак тела матки.
28.
3.• При раке тела матки возможны гнойные
выделения из половых путей и пиометра:
- при пиометре в постменопаузе обязательно
исключают злокачественную опухоль матки.
• Боль:
схваткообразная — при скоплении крови в
полости матки:
тупая — при поражении нервных стволов за счет
сдавления опухолевым инфильтратом или
метастатически измененными лимфатическими
узлами.
29.
У 85—90 % больных распространенностьопухоли соответствует I—II стадии (FIGO).
Этот показатель остается достаточно
стабильным, что объясняется особенностями
клинической картины заболевания,
заставляющими больных рано обращаться к
врачу.
30. Диагностика
Анамнез.Осмотр.
Цитологическое исследование аспирата в 30% бывает
ложноотрицательным.
Аспирационная биопсия (эффект – 95%) с помощью
инструмента «Пайпель»
Гистероскопия.
Ультразвуковая томография коррелирует с
послеоперационными находками в 66-100% случаев.
Цистоскопия, ректороманоскопия, R0 легких,
сканирование скелета, КТ, МРТ, ПЭТ.
СА-125.
Bax, Bcl-2, P-16, P-27, p-53.
31. Для лечения больных РЭ необходимо учитывать:
пациента (общее состояние больной,сопутствующую патологию);
опухоль (характеристика опухоли);
учреждение, где будет лечиться больная
(важные не только хирургические
навыки, но и оснащенность учреждения).
32. Тактика лечения
Операция — первый этап лечения большинства больныхОтказ от операции оправдан только в тех случаях, когда
риск летального исхода во время и после нее превышает
риск смерти от прогрессирования рака тела матки
(Lurain J., 1996)
Частота рецидивов после лучевой терапии как
самостоятельного метода лечения составляет
10—15% (Lurain J., 1996)
В ведущих онкогинекологических клиниках не
подвергаются хирургическому лечению из-за тяжелых
сопутствующих заболеваний < 10% больных раком тела
матки ранних стадий (Marziale P., 1989)
Частые ошибки при определении клинической стадии,
приводят к неправильному планированию лечения
33. Лечение
При РЭ применяются хирургическое, лучевое, гормональное,лекарственное лечение и их комбинации.
ОПЕРАТИВНОЕ ЛЕЧЕНИЕ
Практически 90% больных РЭ на первом этапе подвергаются
оперативному лечению
Типичный объем – экстирпация матки с придатками
смывы с брюшины малого таза, боковых каналов, поддиафрагмальной
области
ревизия органов брюшной полости с пальпацией печени, большого
сальника, всех групп забрюшинных лимфоузлов
при поражении большого сальника и/или яичников показана
оментэктомия
после экстирпации матки с придатками производится вскрытие матки,
при котором оцениваются размеры опухоли, её локализация, инвазия
миометрия, переход на шейку матки
по показаниям - лимфаденэктомия
После хирургического стадирования у 10-25% больных с I-II
клинической стадией последняя повышается
34. Хирургическое лечение
Ранее считалось, что лимфаденэктомия при раке теламатки носит только диагностический характер
В последнее время появляются данные о том, что она
влияет на выживаемость больных раком тела матки
(Creasman W.T. et al., 2001; Mohan D.S. et a.l, 1998; Orr J.W. et
al., 1997; Van Trappen P.H. et al., 2001)
Удаление макрометастазов необходимо, поскольку
при макрометастазах малоэффективна лучевая терапия
выживаемость больных, которым выполнена
лимфаденэктомия, сравнима с таковой у больных с
микрометастазами
риск смерти в отсутствие удаления метастазов в
поясничных лимфатических узлах 6,85 (ретроспективные
данные, Havrilevsky, 2005)
35. Хирургическое лечение
Показания к лимфаденэктомиинизкодифференцированная аденокарцинома
инвазия миометрия более чем на половину
его толщины
переход опухоли на перешеек или шейку
матки
распространение опухоли за пределы матки
опухоль более 2 см
светлоклеточный, папиллярный серозный,
плоскоклеточный и недифференцированный
рак
36. Хирургическое лечение
FIGO IA—IBFIGO IC
Низкий риск
Промежуточный
риск
Эндометриоидная
аденокарцинома G3
Промежуточный
риск
Высокий риск
Светлоклеточный или
папиллярный серозный
рак
Высокий риск
Высокий риск
Эндометриоидная
аденокарцинома G1—2
Анеуплоидия повышает риск на 1 уровень
Fuller A.F., Jr., ESGO Meeting, 2005
37. Хирургическое лечение
Низкий рискЭкстирпация матки с
придатками, смывы из
брюшной полости
Промежуточный риск
+ тазовая
лимфаденэктомия
Высокий риск
+ поясничная
лимфаденэктомия
Fuller A.F., Jr., ESGO Meeting, 2005
38. Хирургическое лечение
Цели лимфаденэктомииуточнение стадии
улучшение выживаемости
определение тактики дальнейшего
лечения (возможность отказа от
послеоперационной лучевой терапии)
39. Расширенные операции
Операция Вертгейма при раке тела матки Iстадии не показана. Она не улучшает
выживаемости больных, увеличивая число
осложнений.
В 1962 г. Я. В. Бохман разработал
модификацию расширенной экстирпации
матки с придатками для лечения больных раком
тела матки.
Отличия расширенной экстирпации матки с
придатками по Я. В. Бохману от операции
Вертгейма:
не резецируются кардинальные связки;
не выполняется туннелирование мочеточников;
не удаляется верхняя треть влагалища.
40. Влагалищная экстирпация матки
При раке тела матки выполняется редко.Влагалищный доступ обычно применяют
при:
выраженном ожирении;
тяжелых сопутствующих заболеваниях;
выпадении матки.
Недостатки влагалищного доступа:
сложность удаления придатков матки;
невозможность ревизии брюшной полости;
невозможность биопсии лимфатических узлов.
41. Прогностические факторы
возрастстадия
гистологический тип
(светлоклеточный и
серозно-папиллярный
рак)
степень
дифференцировки
глубина инвазии
лимфоваскулярная
инвазия
перитонеальная
цитология
поражение лимфоузлов
рецепторный статус
плоидность
Her-2-neu, K-kras, P-53
Наиболее важные факторы
G3
инвазия >50% возраст > 60 лет
42. Лучевая терапия
Адъювантная лучевая терапия при ракетела матки все еще остается предметом
дискуссий (B.A. Jereczek-Fossa, 2001)
По данным ретроспективных
исследований, снижение частоты
рецидивов с 25% (у больных, которым
лучевая терапия не проводилась) до 5%
Не влияет на общую выживаемость
43.
Низкий риск (только наблюдение)I стадия G1,2, не серозно-папиллярныи и не
светлоклеточныи тип опухоли
инвазия < 1/2 миометрия
Средний риск
I стадия
G1-3
не серозно-папиллярный и не светлоклеточный рак
инвазия = 1/2 миометрия
Высокий риск (комплексное лечение)
Стадия Iс-Ш, анеуплодия, РЭ-РП-, мутация Р53
серозно-папиллярный и светлоклеточный рак
инвазия > 1/2 миометрия при любой G, G1 mts в
л/узлах, G3 при инвазии < 1/2 миометрия '
ESGO 2004
44. РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ РТМ ПРИ НИЗКОМ И СРЕДНЕМ РИСКЕ:
277 б-ных - только наблюдениеместные рецидивы
6,9%
5 летн. выживаемость 91%
263 б-ных - с адъювантной лучевой
терапией
местные рецидивы
1,9%
5 летн. выживаемость 89%
ESGO 2004
45. Лучевая терапия
Низкий риск прогрессирования — IA стадия, G1—2прогрессирование у 3—5% больных — ЛТ не показана
Промежуточный риск прогрессирования: IA стадия,
G3?, IB стадия, G1—2
прогрессирование: GOG 99 — у 10%, PORTEC 1 — у 14%
больных — возможна только внутриполостная ЛТ
Высокий риск прогрессирования — IC, IIA, IIB стадии,
G3 (кроме IA стадии), светлоклеточный и папиллярный
серозный рак
прогрессирование у 20—30% больных — сочетанная ЛТ
(Gerbaulet A., ESMO course “Gynecologic Tumors”, 2006)
46. Косвенные признаки гормоночувствительного рака эндометрия.
Гормоночувствительна Гормонорезистентнаяя опухоль
опухоль
Высоко- и умереннодифференцированный рак
Низкодифференцированный
рак
Высокое содержание
рецепторов прогестерона (PR+)
Низкое содержание рецепторов
прогестерона или их полное
отсутствие
(PR-)
Длительный безрецидивный
интервал
Короткий безрецидивный
интервал
Метастазы в легкие, влагалище,
лимфатические узлы
Рецидив в области малого таза
47. Рак эндометрия – прогестины
Более высокая эффективность у больныхс метастазами в легкие
Объем опухоли
Длительный безрецидивный период
Возраст
Эффект при рецидивах лучше, чем при
первично-распространенном процессе
Reifenstein E.C., 1997
48. Гормонотерапия
Гестоноронкапроат (депостат)по 200 мг в/м 1 раз в неделю, длительно
Медроксипрогестерон ацетат (провера)
по 200-400 мг внутрь ежедневно,
Депо-провера в/м по 500-1000 мг
еженедельно, длительно;
Мегестрол ацетат (мегейс)
по 160-320 мг в день длительно
49. Показания к органосохраняющему лечению минимального РЭ:
1. Молодой возраст пациентки, желание избежатьоперацию и сохранить детородную функцию, особенно
при предшествующем РЭ бесплодию.
2. Уверенность, что РЭ является у данной пациентки
минимальным, но не имеет формы малигнизированного
полипа, что достигается с помощью гистероскопии и
трансвагинальной эхографии.
3. Наличие высокодифференцированной диплоидной
аденокарциномы.
4. Возможность в данном лечебном учреждении
проведения многолетнего мониторинга за состоянием
больной.
5. Возможность определения рецепторного статуса
опухоли (содержание цитоплазматических рецепторов
эстрогенов и прогестерона).
50. Органосохраняющее лечение минимального РЭ у женщин молодого возраста
1 этап(1,2, 3-й мес.)
Высокие (насыщающие) дозы прогестагенов:
медроксипрогестерона ацетат (МПА, Депо-Провера)
500 мг через день + тамоксифен 40 мг ежедневно
Полный
регресс
опухоли
При нахождении элементов опухоли в аспирате или
при повторной биопсии — гистерэктомия с
придатками.
2 этап
(4, 5, 6-й мес.)
Продолжение гормонотерапии (МПА, Провера) 500 мг
внутрь 2 раза в неделю + тамоксифен 20 мг ежедневно
3 этап
(7, 8, 9-й мес.)
Индукция менструальноподобного цикла
эстрогенгестагенными препаратами по
контрацептивной схеме.
4 этап
(10,11,12-й мес.)
Индукция овуляции и двухфазного цикла:
кломифенцитрат; у пациенток с синдромом
поликистозных яичников - их клиновидная резекция.
51. Гормонотерапия распространенного рака эндометрия, его рецидивов и метастазов.
ПРОВЕРАпо 500 мг ежедневно 3 месяца
по 500 мг 3 раза в неделю 3 мес
по 500 2 раза в неделю 3 мес
в дальнейшем по 500 мг 1 раз в неделю пожизненно
+ ТАМОКСИФЕН
по 20 мг ежедневно
при необходимости на фоне гормонотерапии
проводится химиотерапия
Максимов С.Я.
Новикова Е.Г.
1999 г.
52. Химиотерапия
Активно изучается адъювантнаяхимиотерапия при раке тела матки
Наиболее активные препараты —
таксаны, антрациклины,
производные платины
(Burke T.W. et al., 2000)
53. Системная терапия
Нерешенные вопросы– эффективность адъювантной
химиотерапии при раке тела матки ранних
стадий
– эффективность адъювантной
химиотерапии при раке тела матки III—IV
стадий (GOG 122)
– выбор системной терапии (гормоно- или
химиотерапия) при прогрессировании
– сочетание системной и лучевой терапии
54. Базисные препараты для лекарственной терапии РТМ
Антранциклиныдоксорубицин,
эпирубицин(фармарубицин),
липосомальный доксорубицин (келикс)
Алкилирующие
агенты: препараты платины
(цисплатин, карбоплатин, оксалиплатин)
Ингибиторы митоза:
таксаны
(паклитаксел)
винкаалкалоиды (винорельбин)
Антиэстрогены ( тамоксифен, фазлодекс)
Прогестины (мегестрол, провера)
Ингибиторы ароматазы (фемара, аримидекс)
55. Показания для адъювантной химиотерапии
папиллярный серозный, светлоклеточный ианеуплоидный РТМ, не зависимо от инвазии и размеров
опухоли.
РТМ III—IV морфологических стадий (преимущества
перед ЛТ, GOG 122, 2006)
РТМ ранних стадий при наличии по крайней мере двух
из следующих факторов риска
низкая степень дифференцировки
глубокая инвазия миометрия
поражение стромы шейки матки
опухолевые эмболы в лимфатических и кровеносных
сосудах
(Fleming J. et al., ASCO 2006)
Необходимо помнить, что
светлоклеточная аденокарцинома
эндометрия
связана с повышенным риском венозных
тромбозов.
(Carret L., abs. 5597, ASCO 2007)
56. Показания к проведению химиотерапии при раке эндометрия.
отдаленные метастазырецидив заболевания
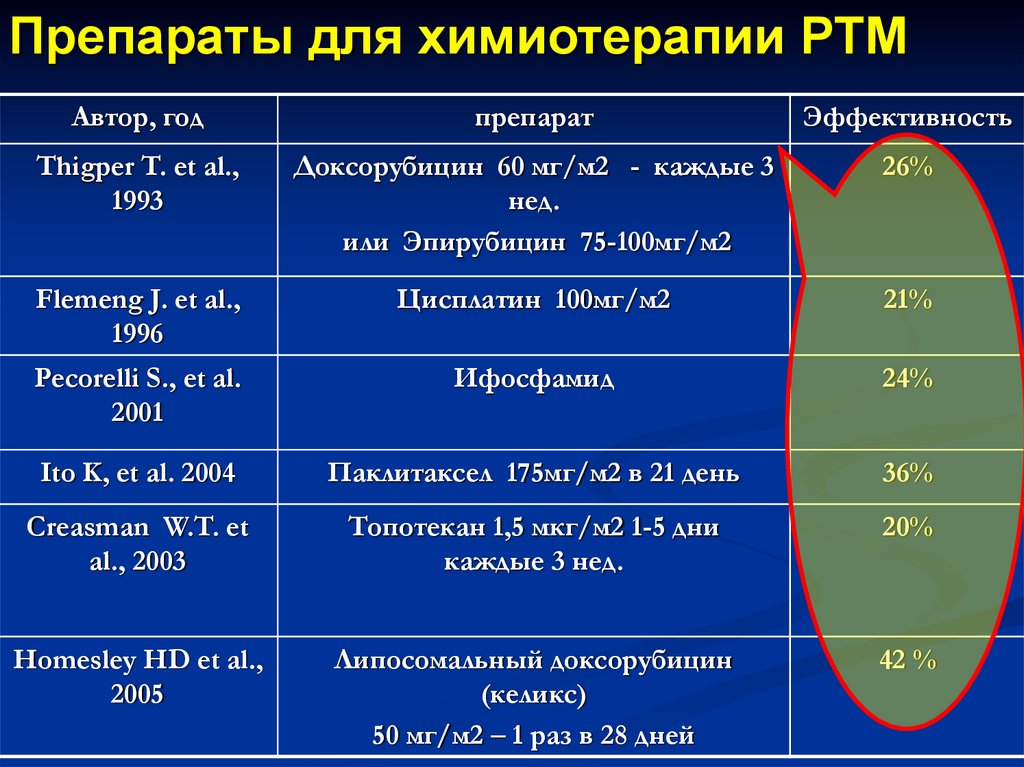
57.
Препараты для химиотерапии РТМАвтор, год
препарат
Эффективность
Thigper T. et al.,
1993
Доксорубицин 60 мг/м2 - каждые 3
нед.
или Эпирубицин 75-100мг/м2
26%
Flemeng J. et al.,
1996
Цисплатин 100мг/м2
21%
Pecorelli S., et al.
2001
Ифосфамид
24%
Ito K, et al. 2004
Паклитаксел 175мг/м2 в 21 день
36%
Creasman W.T. et
al., 2003
Топотекан 1,5 мкг/м2 1-5 дни
каждые 3 нед.
20%
Homesley HD et al.,
2005
Липосомальный доксорубицин
(келикс)
50 мг/м2 – 1 раз в 28 дней
42 %
58. Комбинированная химиотерапия
Автор, годпрепарат
Эффективность
Thigper T. et al., 1993
доксорубицин 50 мг/м2 + цисплатин 75
мг/м2 - каждые 3 нед.
33 - 47%
Flemeng J. et al., 2006
Hodberg T., 2007
паклитаксел 175мг/м2 +
карбоплатин AUC 5-6
52-56%
Hodberg T., et al. 2005
паклитаксел 135 мг/м2 – 24 часа +
цисплатин 75 мг/м2
48%
Oliva C. F.,et al. 2001
САР: Цисплатин 50мг/м2 + доксорубицин
50 мг/м2 + циклофосфан 500мг/м2 в 21д
46%
Orton J. et al., 2005
паклитаксел135 мг/м2 + доксорубицин 40
мг/м2 каждые 3 нед.
42%
Homesley HD et al.,
2007
Липосомальный доксорубицин 50 мг/м2 +
паклитаксел 135 мг/м2 – 24 часа 1 раз в 28
дней
54 %
59. Комбинированная терапия
Автор, годпрепарат
Эффективност
ь
Rosenberg P., et al.,
2006 (GOG 163)
паклитаксел 135 мг/м2 +
доксорубицин 40 мг/м2 +
цисплатин 60 мг/м2 - каждые
3 нед. + Г-КСФ
57%
Kim S., 2004
паклитаксел 175мг/м2 +
винорельбин 25мг/м2 1и 8 дни
57%, ПР -11%
Oliva C.F., 2006
эпирубицин 60 мг/м2+
паклитаксел 175 мг/м2
49%
60. Комбинированная химиотерапия больных раком тела матки с высоким риском рецидивов и метастазов (1-2 ст. G3, 3-4 ст.)
Цисплатин 50 мг/м2Вепезид 150 мг/м2
Доксорубицин 50 мг/м2
3-х летняя выживаемость 64%
K.L. Chan et all 2000
61. Химиотерапия местнораспространенного РЭ и его рецидивов (предварительные результаты)
Химиотерапия местнораспространенногоРЭ и его рецидивов
1.
(предварительные результаты)
СРАВНЕНИЕ 2-х РЕЖИМОВ АР и ТС
АР: доксорубицин 60 мг/м2
цисплатин 50 мг/м2
ТС: таксол 175 мг/м2
карбоплатин AUC-5
включено 70 больных, оценено 63
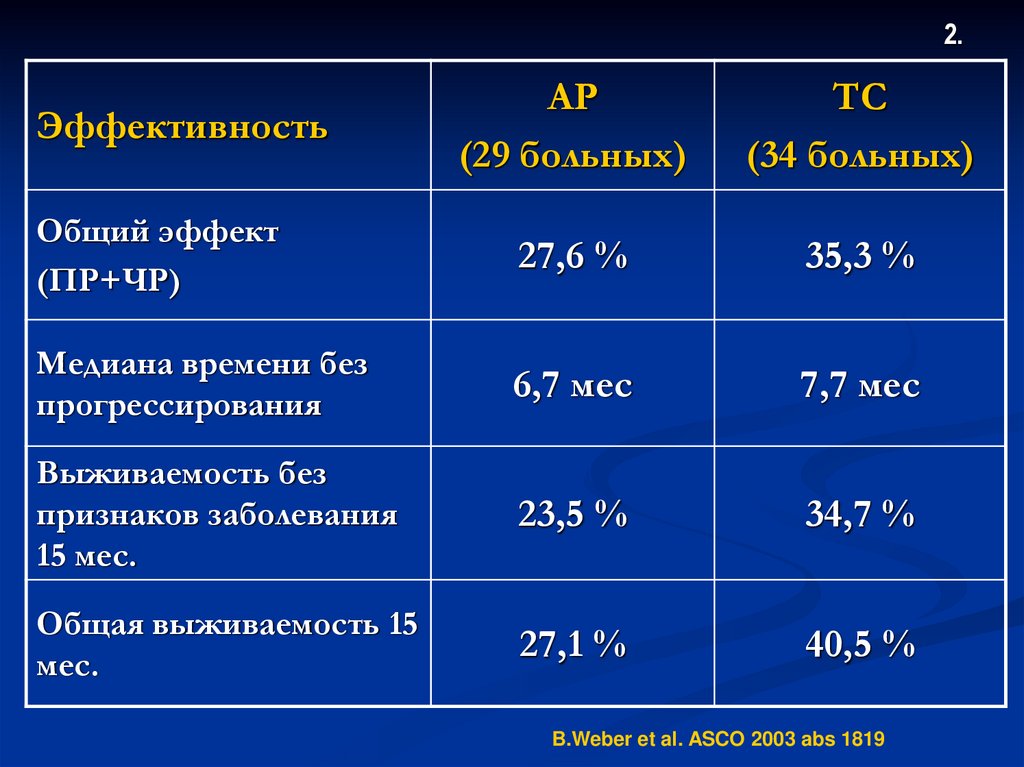
62.
2.АР
(29 больных)
ТС
(34 больных)
Общий эффект
(ПР+ЧР)
27,6 %
35,3 %
Медиана времени без
прогрессирования
6,7 мес
7,7 мес
Выживаемость без
признаков заболевания
15 мес.
23,5 %
34,7 %
Общая выживаемость 15
мес.
27,1 %
40,5 %
Эффективность
B.Weber et al. ASCO 2003 abs 1819
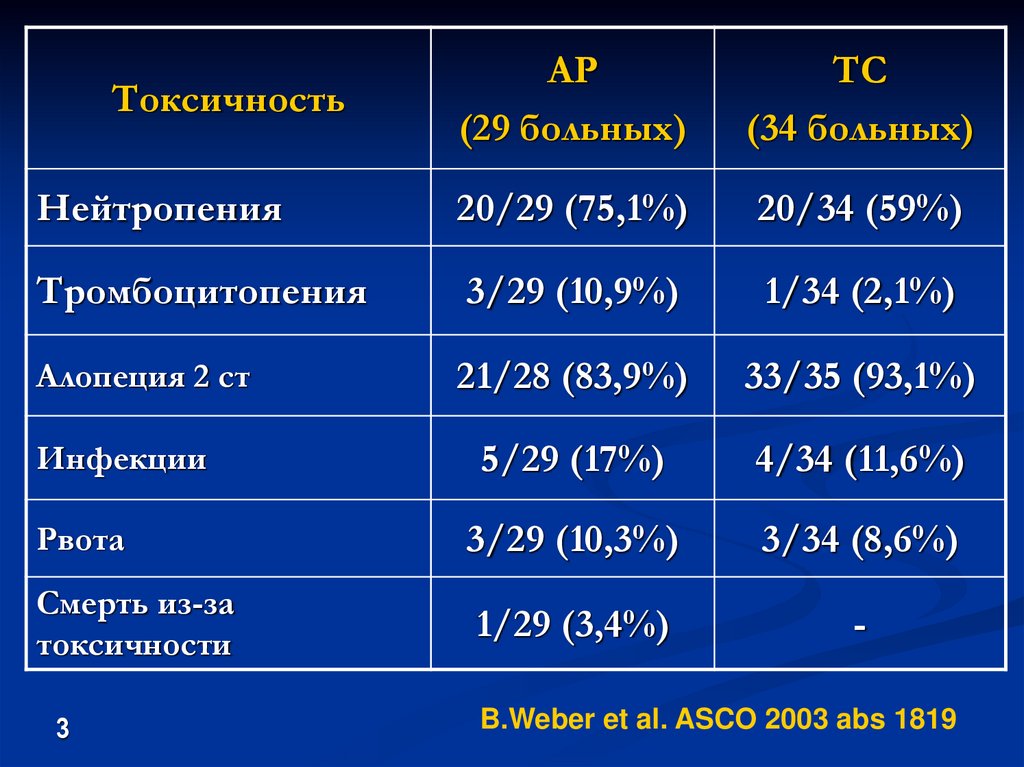
63.
АР(29 больных)
ТС
(34 больных)
Нейтропения
20/29 (75,1%)
20/34 (59%)
Тромбоцитопения
3/29 (10,9%)
1/34 (2,1%)
Алопеция 2 ст
21/28 (83,9%)
33/35 (93,1%)
Инфекции
5/29 (17%)
4/34 (11,6%)
Рвота
3/29 (10,3%)
3/34 (8,6%)
Смерть из-за
токсичности
1/29 (3,4%)
-
3
B.Weber et al. ASCO 2003 abs 1819
Токсичность
64.
При серознo-папиллярном раке(III-IVc.) высокоэффективно введение
карбоплатин AUC-7,5
таксол 175 мг/м2 Зх часовая инфузия
каждые 3-4 недели
(общая эффективность составила 82%;
причем полная ремиссия - 44%;
время без прогрессирования - 32 мес.
медиана выживаемости - 42 мес.)
(P. Sabbatini et all. 2001 г.)
65. ПАКЛИТАКСЕЛ, ЭПИРУБИЦИН и КАРБОПЛАТИН при лечении местнораспространенного РЭ и его рецидивов (предварительное сообщение) I/II
фаза28 больных, средний возраст 58 лет
(большая остаточная опухоль после операции,
метастазы в легкие, поражение > 2 тазовых л/узлов
и парааортальных, серозно-папиллярный,
светлоклеточный или недифференцированный рак)
КАРБОПЛАТИН AUC-4
ЭПИРУБИЦИН 50 мг/м2
ПАКЛИТАКСЕЛ 150 мг/м2
каждые 3-4 недели – 6 курсов
66. ПАКЛИТАКСЕЛ, ЭПИРУБИЦИН и КАРБОПЛАТИН при лечении местнораспространенного РЭ и его рецидивов (предварительное сообщение) I/II
фазаЭФФЕКТИВНОСТЬ
ОЭ – 75%
ПР – 15%
ЧР – 62%
Основная токсичность – гематологическая, которая
быстро купировалась.
Т.о. схема активна, с приемлемым уровнем токсичности.
Исследование продолжается
R.Nakashima et al.
ASCO 2003 abs 1963
67. КАРБОПЛАТИН + ПАКЛИТАКСЕЛ в лечении первичного местнораспространенного РЭ и его рецидивов (II фаза)
с 2000-2003г66 больных
18 - местнораспространенный РЭ
48 – рецидивы РЭ
КАРБОПЛАТИН AUC-5
ПАКЛИТАКСЕЛ 175 мг/м2
6 курсов
Общая эффективность – 67% (44 больных)
Полная ремиссия – 29% (19 больных)
Частичная ремиссия – 38% (25 больных)
при местнораспространенном РЭ
при рецидивах РЭ
ОЭ-86%
ОЭ-60%
2-летняя выживаемость – 57%
3-летняя выживаемость – 29%
Медиана общей выживаемости – 26,4 мес
68. КАРБОПЛАТИН + ПАКЛИТАКСЕЛ в лечении первичного местнораспространенного РЭ и его рецидивов (II фаза)
ТОКСИЧНОСТЬ:нейтропения 2/3 ст. – 12%
тромбоцитопения 1 ст. – редко
нейросенсорные симптомы
1ст. – 42%
2 ст. – 26%
3 ст. – 8%
двигательная нейротоксичность 2/3 ст. – 13%
Т.о. данная схема более эффективна, чем используемые ранее
режимы
B.Sorbe et al.
ASCO 2005 abs 5110
69.
70.
Цисплатин50 мг/м2 в/в капельно
Эпирубицин
60 мг/м2 в/в
Циклофосфан
600 мг/м2 в/в
в 1 и 21 день
одновременно с облучением малого таза до СОД
45-50 Гр. и зоны параортальных лимфоузлов
71. Возможно проведение химиотерапии в монорежиме (цисплатин по 40 мг/м2 или таксол по 60 мг/м2 еженедельно 5 недель) во время
проведенияадъювантнои лучевой терапии на
малый таз и/или зону парааортальных
лимфатических узлов,
т.е. химиолучевое лечение.
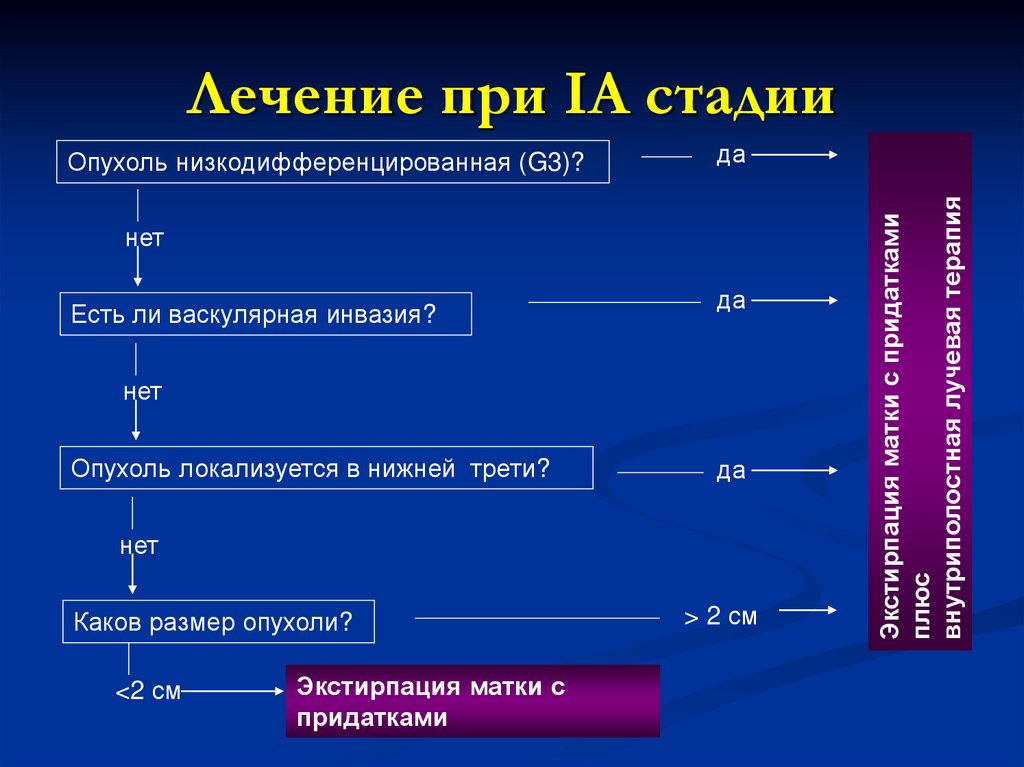
72. II клиническая стадия
Лечение при IА стадиида
нет
Есть ли васкулярная инвазия?
да
нет
Опухоль локализуется в нижней трети?
да
нет
Каков размер опухоли?
<2 см
Экстирпация матки с
придатками
> 2 см
Экстирпация матки с придатками
плюс
внутриполостная лучевая терапия
Опухоль низкодифференцированная (G3)?
73. III клиническая стадия
Лечение при IВ стадииОпухоль низкодифференцированная (G3)?
да
Экстирпация матки с
придатками плюс
нет
Опухоль локализуется в нижней трети?
да
лимфаденэктомия
Есть ли mts
в лимфоузлы?
нет
Есть ли васкулярная инвазия?
нет
да
да или неизвестно
Экстирпация
матки
с придатками
Экстирпация матки
с придатками плюс
внутриполостная
лучевая терапия
Сочетанная
лучевая терапия
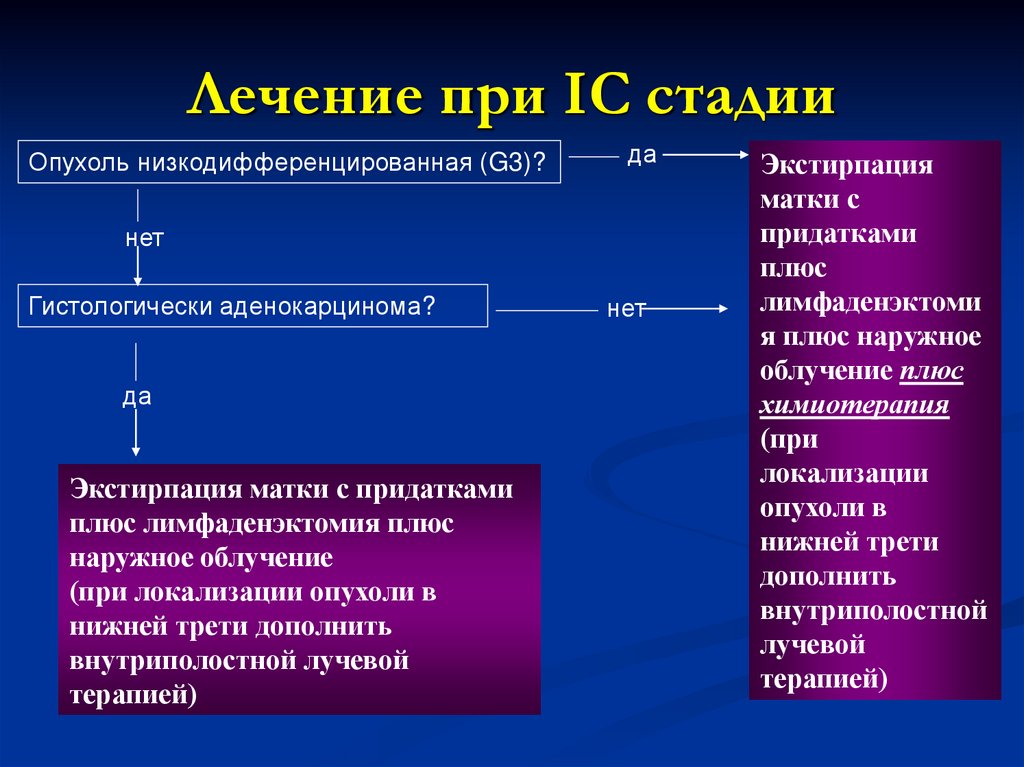
74. IIIA клиническая стадия
Лечение при IС стадииОпухоль низкодифференцированная (G3)?
да
нет
Гистологически аденокарцинома?
да
Экстирпация матки с придатками
плюс лимфаденэктомия плюс
наружное облучение
(при локализации опухоли в
нижней трети дополнить
внутриполостной лучевой
терапией)
нет
Экстирпация
матки с
придатками
плюс
лимфаденэктоми
я плюс наружное
облучение плюс
химиотерапия
(при
локализации
опухоли в
нижней трети
дополнить
внутриполостной
лучевой
терапией)
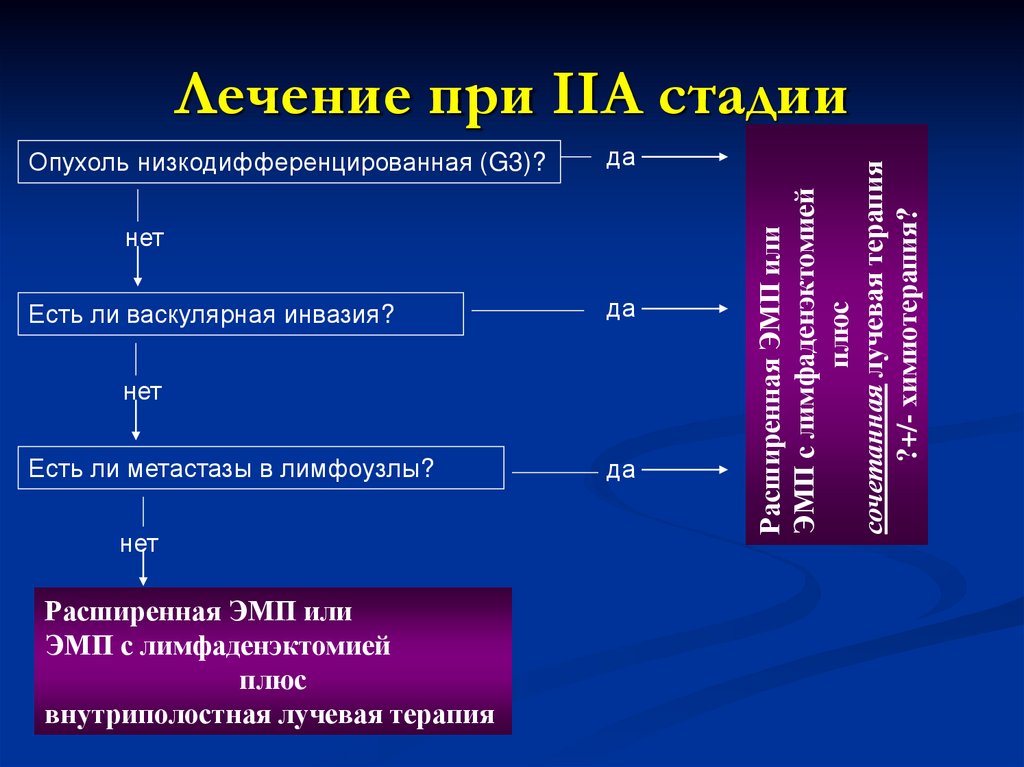
75. IIIB клиническая стадия
Опухоль низкодифференцированная (G3)?да
нет
Есть ли васкулярная инвазия?
да
нет
Есть ли метастазы в лимфоузлы?
нет
Расширенная ЭМП или
ЭМП с лимфаденэктомией
плюс
внутриполостная лучевая терапия
да
Расширенная ЭМП или
ЭМП с лимфаденэктомией
плюс
сочетанная лучевая терапия
?+/- химиотерапия?
Лечение при IIА стадии
76. IIIC клиническая стадия
Лечение при IIВ стадииОпухоль низкодифференцированная (G3)?
да
Расширенная ЭМП
нет
Есть ли васкулярная инвазия?
плюс
да
сочетанная лучевая
терапия
нет
?+/- химиотерапия?
Есть ли метастазы в лимфоузлы?
нет
Расширенная ЭМП
плюс
сочетанная лучевая
терапия
да
77. IV клиническая стадия
IIIA стадия (7-10% случаев)Наличие опухолевых клеток в
перитонеальной жидкости
и / или
Поражение серозной оболочки матки
и / или
Поражение яичников (прорастание или
метастазы)
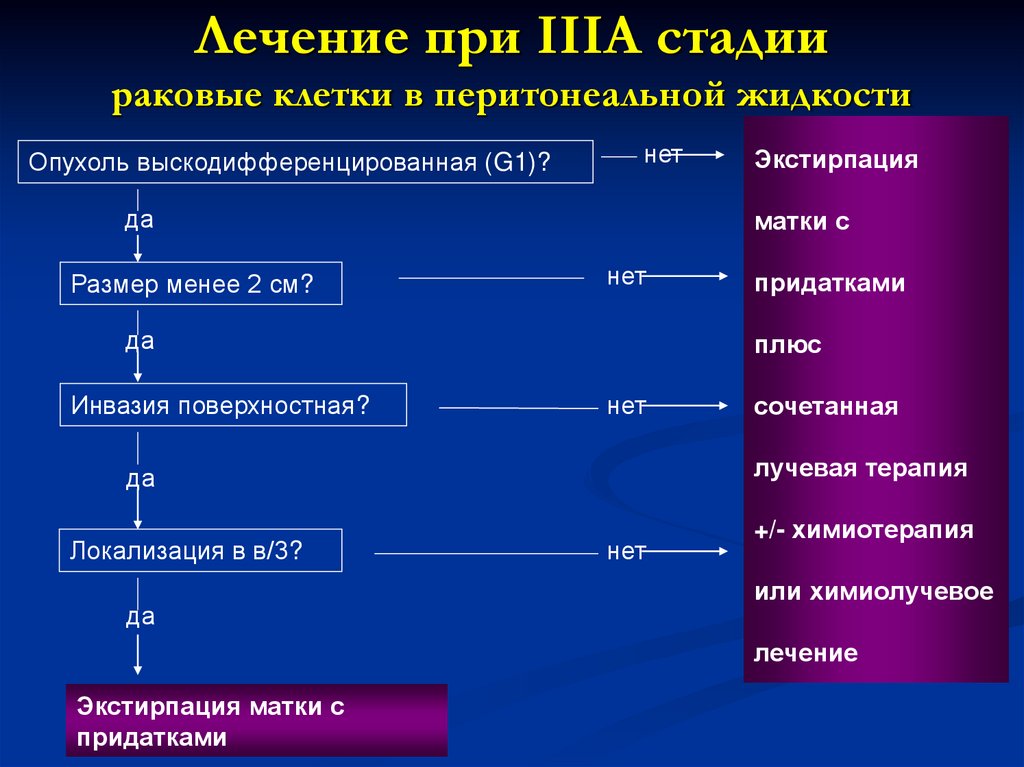
78. Лечение при IА стадии
Лечение при IIIA стадиираковые клетки в перитонеальной жидкости
Опухоль выскодифференцированная (G1)?
нет
да
Размер менее 2 см?
матки с
нет
да
Инвазия поверхностная?
да
придатками
плюс
нет
сочетанная
лучевая терапия
да
Локализация в в/3?
Экстирпация
нет
+/- химиотерапия
или химиолучевое
лечение
Экстирпация матки с
придатками
79. Лечение при IВ стадии
Лечение IIIA стадии(поражение серозной оболочки)
Экстирпация матки с придатками
плюс
Лимфаденэктомия
плюс
Сочетанная лучевая терапия
плюс / минус
Химиотерапия
80. Лечение при IС стадии
Лечение IIIA стадии(поражение яичников)
Экстирпация матки с придатками
плюс
лимфаденэктомия плюс оментэктомия
плюс
химиотерапия
опухоль
высокодифференцированная
опухоль низко- или умереннодифференцированная
Наружное облучение
плюс
прогестинотерапия
Сочетанная лучевая
терапия плюс
? прогестинотерапия ?
81. Лечение при IIА стадии
Лечение IIIВ стадииВопрос об оперативном вмешательстве
решается индивидуально
плюс
Сочетанная лучевая терапия
плюс
Химиотерапия
плюс / минус
Прогестинотерапия
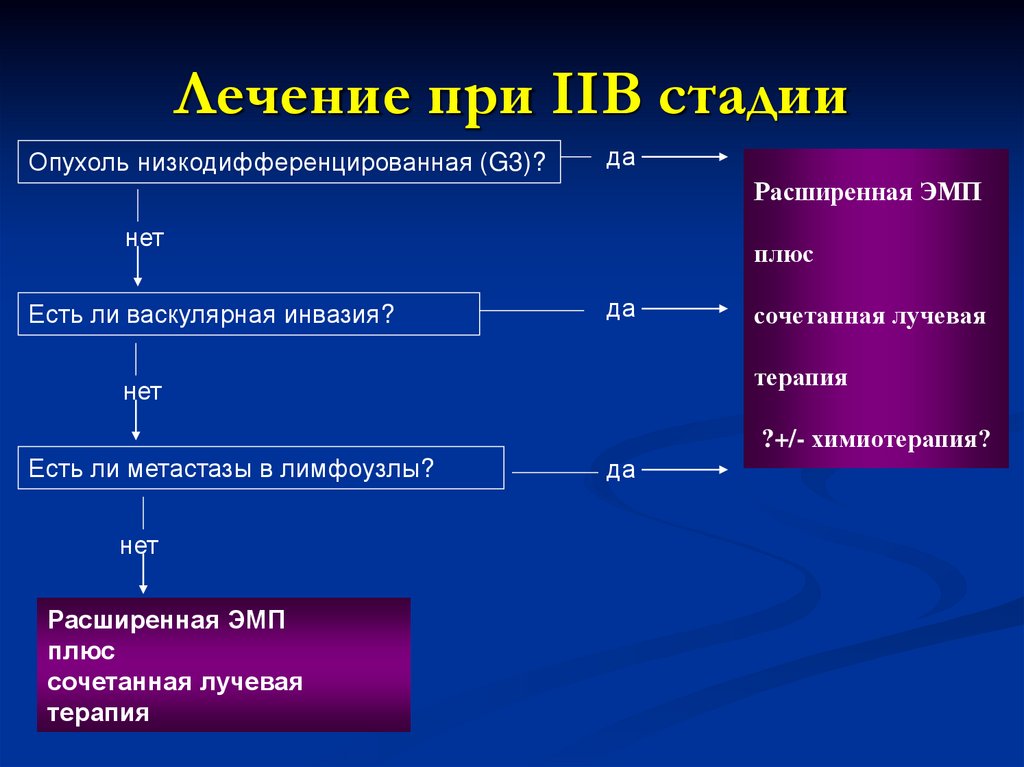
82. Лечение при IIВ стадии
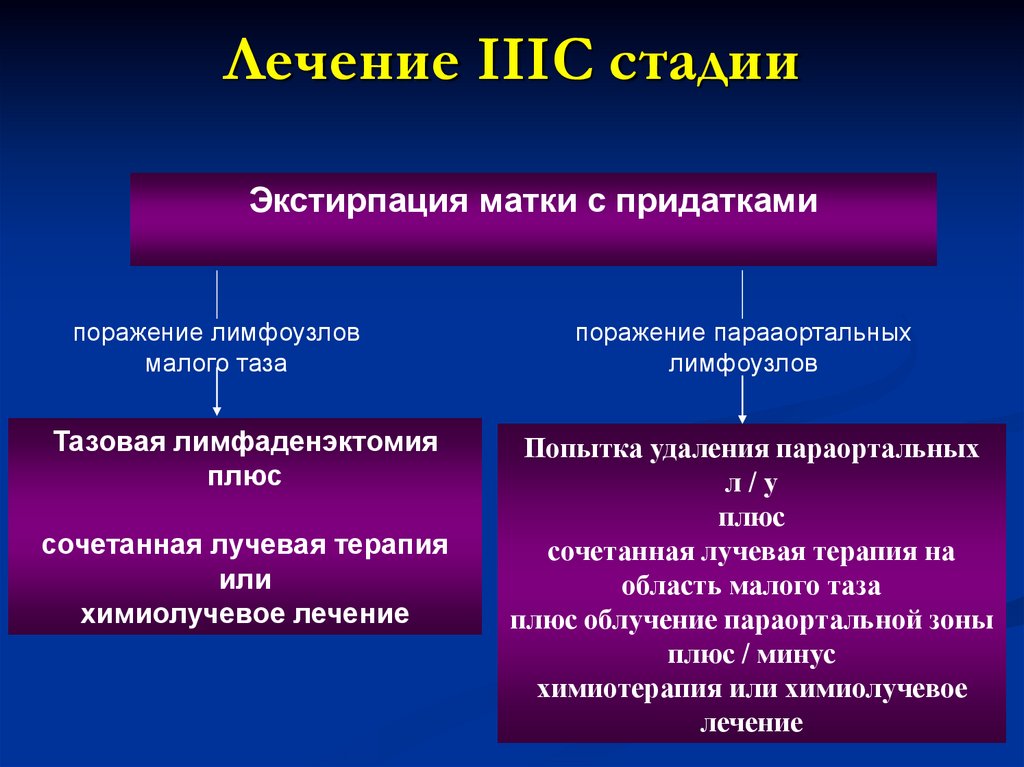
Лечение IIIС стадииЭкстирпация матки с придатками
поражение лимфоузлов
малого таза
Тазовая лимфаденэктомия
плюс
сочетанная лучевая терапия
или
химиолучевое лечение
поражение парааортальных
лимфоузлов
Попытка удаления параортальных
л/у
плюс
сочетанная лучевая терапия на
область малого таза
плюс облучение параортальной зоны
плюс / минус
химиотерапия или химиолучевое
лечение
83. IIIA стадия (7-10% случаев)
5 летние результаты лечения больных РЭв зависимости от патогенетического
варианта и вида оперативного
вмешательства.
I патогенетический вариант
экстирпация матки с придатками
расширенная экстирпация матки
с придатками
- 89%
- 82%
II патогенетический вариант
экстирпация матки с придатками
расширенная экстирпация
матки с придатками
- 47%
- 66%
84. Лечение при IIIA стадии раковые клетки в перитонеальной жидкости
Результаты лечения РЭ(5летняя выживаемость)
только операция
операция + лучевая
терапия
только лучевая терапия
I стадия
- 87,8%
- 88,7%
П стадия
78-85%
- 75%
53-65%
Рецидивы при лечении РЭ I стадии
только операция
операция + лучевая терапия
лучевая терапия + операция
- 12%
- 0%
-3%
85. Лечение IIIA стадии (поражение серозной оболочки)
5летняя выживаемость больных присочетанной лучевой терапии как
самостоятельном методе:
I-II стадии
- 61% - 88%
при
III-IV
- 14% - 49%
86. Лечение IIIA стадии (поражение яичников)
Выживаемость.При хирургическом и комбинированном
лечении в зависимости от степени
дифференцировки опухоли:
IА - 83-96%; IВ - 82-95%; IС - 73-90%;
IIА - 60-90%; IIВ - 55-75%;
III А - 59-72%; III В,С - 42-59%;
IV- 18-35%.
87. Лечение IIIВ стадии
5-летняя выживаемость больных раком темаматки в зависимости от клинической и
морфологической стадий (Кузнецов В.В. 2007)
Клиническая
стадия
Выживаемость, %
I
82
II
65
III
44
IV
15
Морфологическая
стадия
Выживаемость, %
IA
IB
IC
IIA
IIB
IIIA
IIIB
IIIC
IV
90
88
83
77
70
65
55
47
27
88. Лечение IIIС стадии
Факторы прогноза РТМ.5летняя выживаемость зависит от многих
факторов:
моложе 50 лет - 91,2%, старше - 70-60,9%;
при высокодифференцированном РТМ - 92%
умеренно- и низкодифференцированном 86% и
1.
64%;
при поверхностной инвазии миометрия - 80-90%,
при глубокой - 60%;
при отсутствии опухолевых эмболов в
лимфатических узлах при I стадии - 91%,
при наличии - 73%;
при отсутствии метастазов в лимфатических узлах 90%, при их наличии - 54%;
при отсутствии диссеминации по брюшине -88%,
при её наличии - 50%
89. 5 летние результаты лечения больных РЭ в зависимости от патогенетического варианта и вида оперативного вмешательства.
Факторы прогноза при РТМ.2.
Большое прогностическое значение имеют:
содержание рецепторов прогестерона и
эстрогенов в опухоли
плоидность опухолевых клеток и
пролиферативный индекс
содержание в опухоли простагландинов
серии Е
амплификация и экспрессия отдельных
онкогенов, в частности мутации гена Р53.
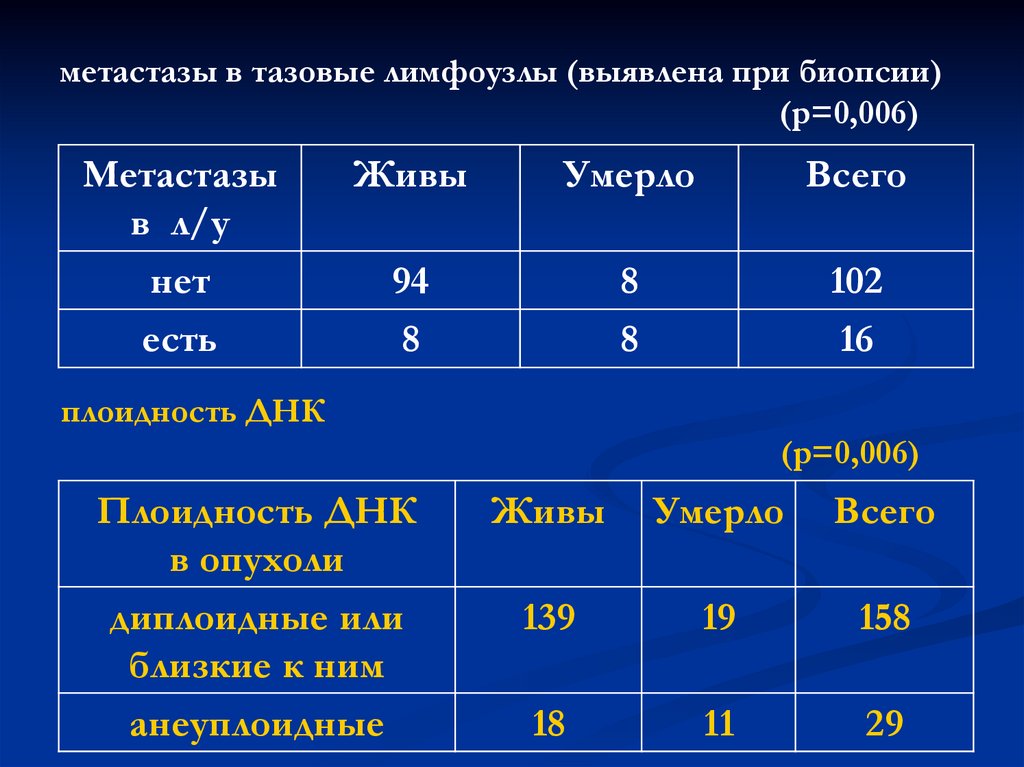
90. Результаты лечения РЭ (5летняя выживаемость)
метастазы в тазовые лимфоузлы (выявлена при биопсии)(р=0,006)
Метастазы
в л/у
нет
есть
Живы
Умерло
Всего
94
8
8
8
102
16
плоидность ДНК
(р=0,006)
Плоидность ДНК
в опухоли
диплоидные или
близкие к ним
анеуплоидные
Живы
Умерло
Всего
139
19
158
18
11
29
91.
НАБЛЮДЕНИЕБольные, получившие лечение по
поводу рака эндометрия подлежат
длительному наблюдению, особенно
в течение первых 2-3 лет, т.е. в
сроки наибольшей вероятности
развития рецидивов и метастазов
опухоли. Каждые 3-4 месяца
гинекологические осмотры, УЗТ.
Каждый год – R0 легких.
92. Выживаемость.
Заместительная терапия.Назначение эстроген/гестагенной терапии (индивина,
климодиен, ливиал) показано женщинам
пременопаузального возраста через 1-3 года после
окончания лечения, т.е. по завершении периода, в
течение которого чаще всего и возникают рецидивы и
метастазы. До этого, для уменьшения приливов
назначают прогестагены (медроксипрогестерона ацетат
по 10 мг/сут внутрь или по 150 мг в/м каждые 3 мес.) или
негормональные препараты белладонну/фенобарбитал/эрготамин, климаксан,
климадинон, феминал.
















































































 Медицина
Медицина








