Похожие презентации:
Кристалдық тор түрлері, байланыс типтері және заттардың қасиеттері арасындағы өзара байланыс. 8 сынып
1.
Берілген заттардағы химиялықбайланыс түрін анықтаңыз
Na2O, Mg, CsF, CaCl2, Cu, HCl,
Al2O3, Br2, MgI2, PH3, H2O, Fe,
I2, SiO2, Ca, F2, LiH, CO2
2.
МАТМЛИ «ОЗАТ»Тақырыбы: «Кристалдық тор түрлері, байланыс типтері
және заттардың қасиеттері арасындағы өзара байланыс»
8 сынып
Химия пәні мұғалімі: Ескатова Алтын Болатовна
3.
Оқу мақсаты• 8.1.4.3 -заттар қасиеттерінің кристалдық тор типтеріне
тәуелділігін түсіндіру
Бағалау критерийлері
• Байланыс түрлерін біледі.
• Кристалдық торлардың түрлері туралы түсінік береді.
• Кристалл тор түрлерін ажырата алады.
• Заттардың құрылымы мен қасиеттері арасындағы қатынас орнатады.
3
4.
Кристалдық тор түрлеріСабақ мақсаты: Иондық,
молекулалық,
макромолекулалық,
торларының қасиеттерін түсіну
металдық
кристалл
Кристалдық тордың зат қасиетіне қалай
әсер ететінін түсіндіре аламын.
Иондық, молекулалық, атомдық, металдық
кристалл торларының айырмашылықтарын
білемін.
Кристалдық тор түрлерін білемін.
5.
Тірек ұғымдар:Кристалдық торлар
Атомдық
Молекуалалық
Иондық
Металдық
Кристалдық торлар
Кристалдық тор – кристалл заттардағы атомдардың,
иондардың, молекулалардың белгілі бір ретпен орналасуы.
Бөлшектердің орналасқан нүктелері кристалдық тор түйіндері
деп аталады.
5
6.
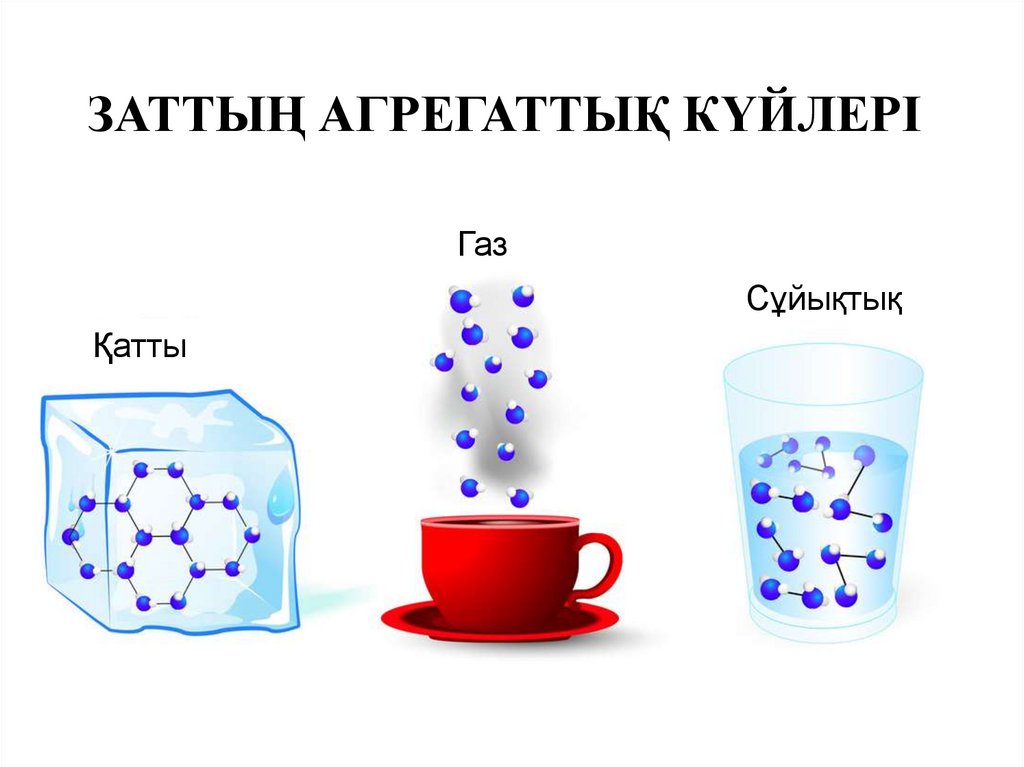
ЗАТТЫҢ АГРЕГАТТЫҚ КҮЙЛЕРІГаз
Сұйықтық
Қатты
7.
ҚАТТЫ ЗАТТАРКРИСТАЛДЫ
АМОРФТЫ
Кристалды заттардың аморфты заттардан
айырмашылығы қандай?
8.
Аморфты заттар9.
Кристалл заттар10.
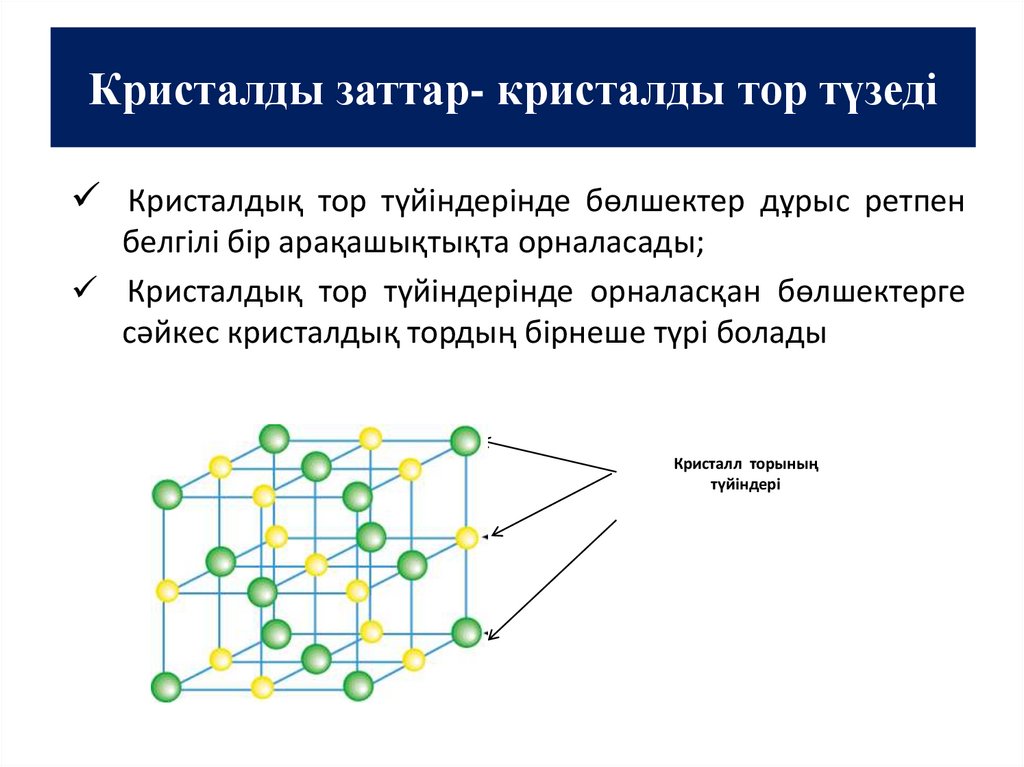
Кристалды заттар- кристалды тор түзедіКристалдық тор түйіндерінде бөлшектер дұрыс ретпен
белгілі бір арақашықтықта орналасады;
Кристалдық тор түйіндерінде орналасқан бөлшектерге
сәйкес кристалдық тордың бірнеше түрі болады
Кристалл торының
түйіндері
11.
Кристалдық тор – кристалл заттардағыатомдардың, иондардың, молекулалардың
белгілі бір ретпен орналасуы. Бөлшектердің
орналасқан нүктелері кристалдық тор
түйіндері деп аталады.
12.
Кристалдық тор типтеріф
Кристалдық торлар
Атомдық
Молекуалалық
Иондық
Металдық
12
13.
Кристалдық торларТорды
ң
типтер
і
Құрыл
ыс
белгіле
рі
Бөлшектер
дің
арасындағы
байланыс
типтері
Заттардың
қасиеттері
t0С
балқу
Ерігіштігі
Атомд
ық
Бейтар
ап
атомда
р
Ковалентті
Жоғар
ы
Ерімейді
Молеку Молеку Әлсіз
лалық лалар
молекула
аралық
байланыс
Төмен Органика
лық
еріткіште
р
мен суда
ериді
Мысалдар
С, Si, SiO2
Барлық заттар, жай
заттар, І2, Вr2,
қышқылдық
оксидтер,
қышқылдар,
органикалық заттар
13
14.
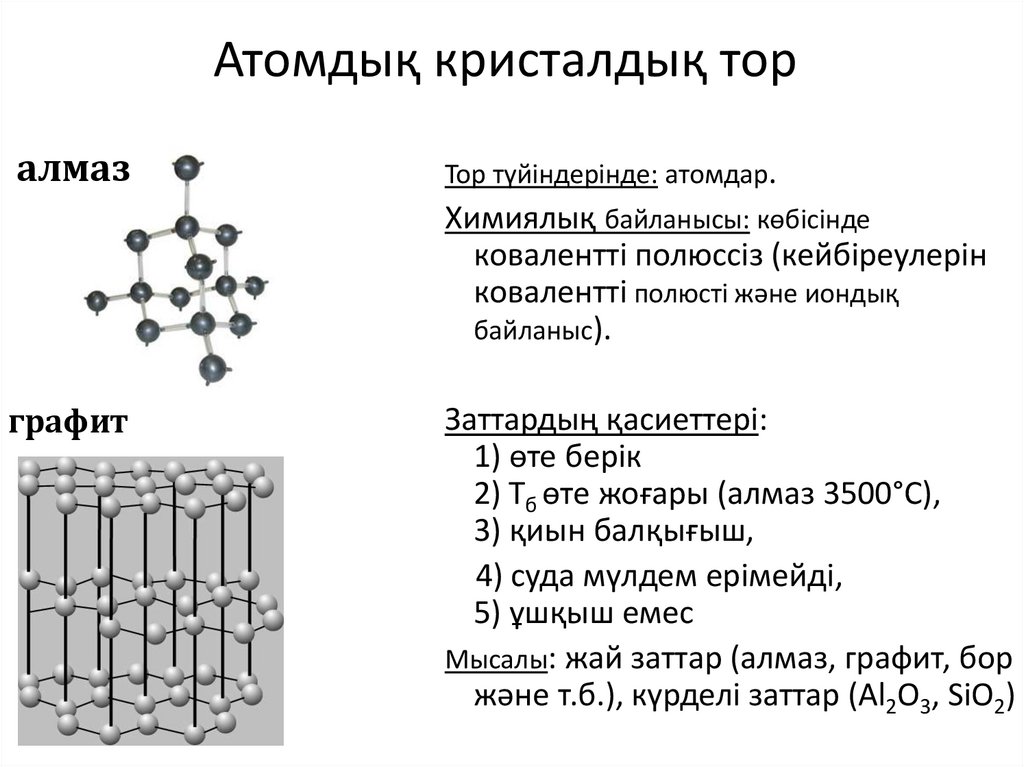
Атомдық кристалдық торалмаз
Тор түйіндерінде: атомдар.
Химиялық байланысы: көбісінде
ковалентті полюссіз (кейбіреулерін
ковалентті полюсті және иондық
байланыс).
графит
Заттардың қасиеттері:
1) өте берік
2) Тб өте жоғары (алмаз 3500°С),
3) қиын балқығыш,
4) суда мүлдем ерімейді,
5) ұшқыш емес
Мысалы: жай заттар (алмаз, графит, бор
және т.б.), күрделі заттар (Al2O3, SiO2)
15.
Атомдық кристалдық торларалмаз
Атомдық кристалдық торлардың
түйіндерінде коваленттік байланыспен
байланысқан жеке атомдар орналасқан.
Бор В, кремний Si, алмаз С, графит С
жай заттарға тән. Ал күрделі заттардан
кәдімгі өзен құмының SiO2 кристалдық
торы атомдық болады
графит
15
16.
Молекуалалық кристалдық тор типтеріТор түйіндерінде: молекулалар.
Химиялық байланысы: ковалентті полюсті және
полюссіз.
Заттардың қасиеттері:
Йод I2
Көмір қышқыл газы СО2
1) төмен беріктілік;
2) Тб және Тқ төмен;
3) Әдетте бөлме Т сұйық немесе газ;
4) ұшқыш.
Мысалы: жай заттар (H2, N2, O2, F2, P4, S8, Ne, He),
күрделі заттар (СО2, H2O, қант С12H22O11 және
т.б.)
16
17.
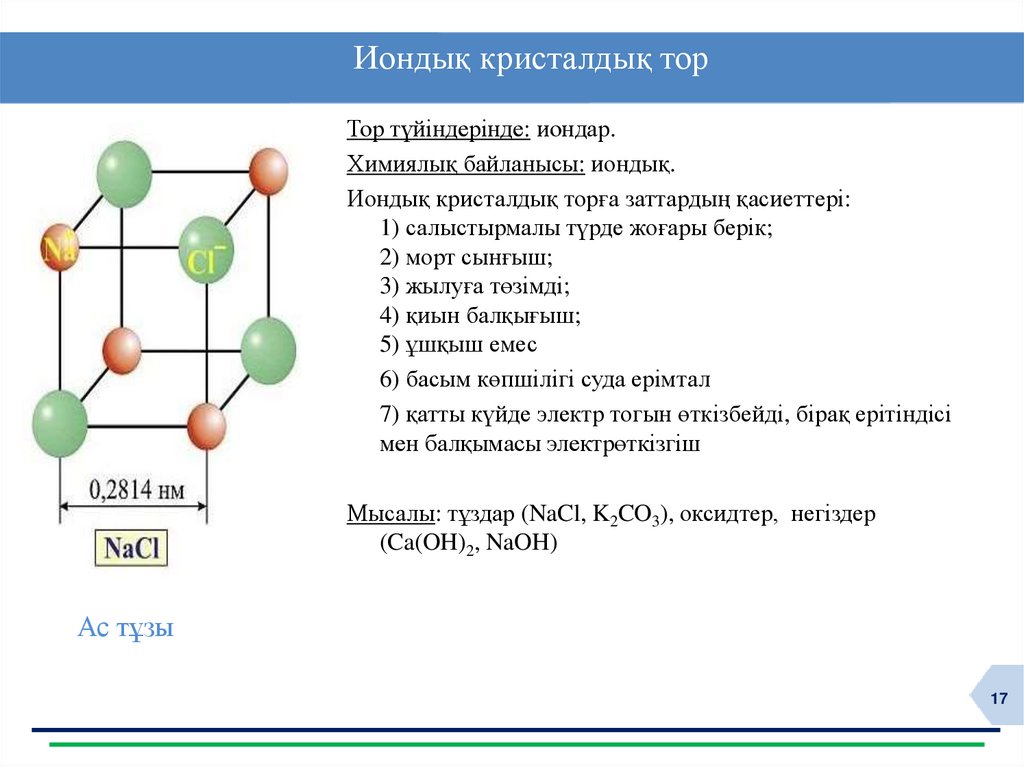
Иондық кристалдық торТор түйіндерінде: иондар.
Химиялық байланысы: иондық.
Иондық кристалдық торға заттардың қасиеттері:
1) салыстырмалы түрде жоғары берік;
2) морт сынғыш;
3) жылуға төзімді;
4) қиын балқығыш;
5) ұшқыш емес
6) басым көпшілігі суда ерімтал
7) қатты күйде электр тогын өткізбейді, бірақ ерітіндісі
мен балқымасы электрөткізгіш
Мысалы: тұздар (NaCl, K2CO3), оксидтер, негіздер
(Ca(OH)2, NaOH)
Ас тұзы
17
18.
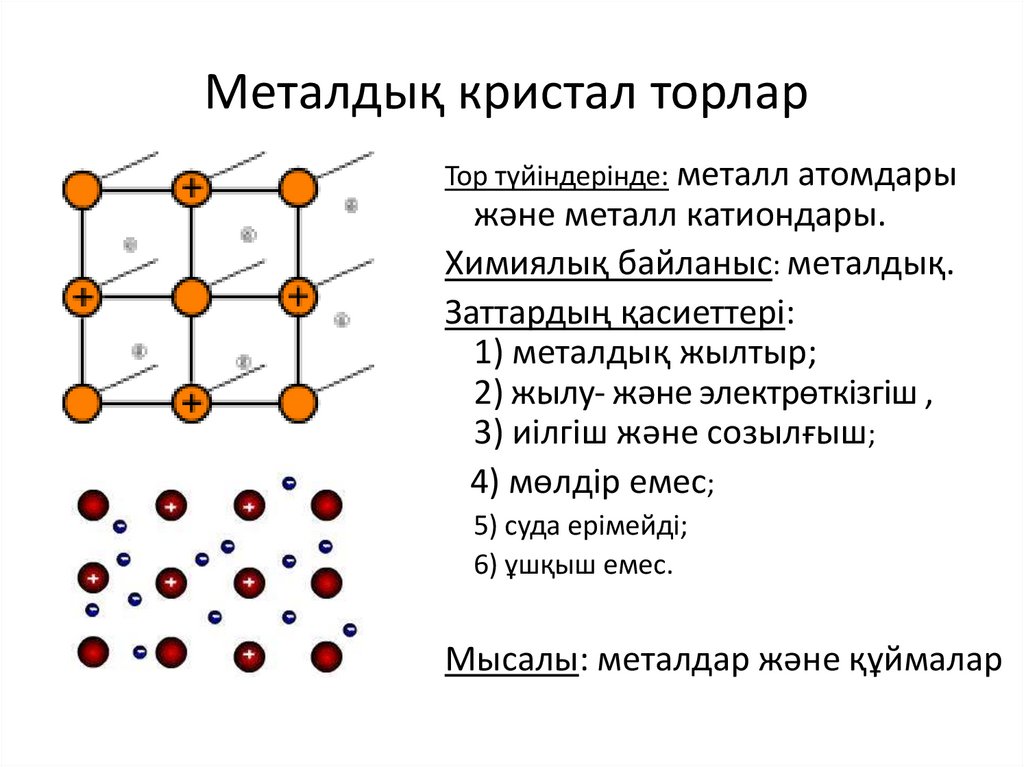
Металдық кристал торларТор түйіндерінде: металл атомдары
және металл катиондары.
Химиялық байланыс: металдық.
Заттардың қасиеттері:
1) металдық жылтыр;
2) жылу- және электрөткізгіш ,
3) иілгіш және созылғыш;
4) мөлдір емес;
5) суда ерімейді;
6) ұшқыш емес.
Мысалы: металдар және құймалар
19.
Барлық металдарда металдық байланыс боладыМеталл атомдарының сырқы
қабатындағы бос электрондар
Металдық байланыс –
металл катионы сыртқы
қабатындағы бос делокальданған
электрондардың тартылуы әсіренен
түзілетін байланыс.
Металл иондары
Металдық байланыс –металдарға тән қасиеттерді түсіндіреді
20.
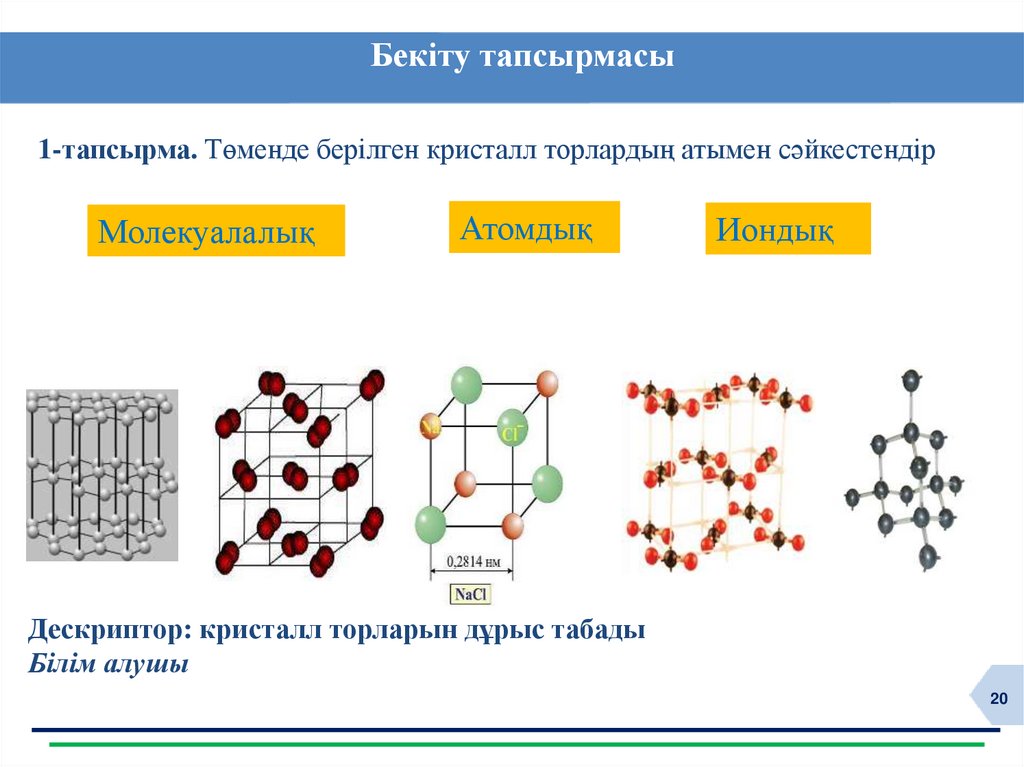
Бекіту тапсырмасы1-тапсырма. Төменде берілген кристалл торлардың атымен сәйкестендір
Молекуалалық
Атомдық
Иондық
Дескриптор: кристалл торларын дұрыс табады
Білім алушы
20
21.
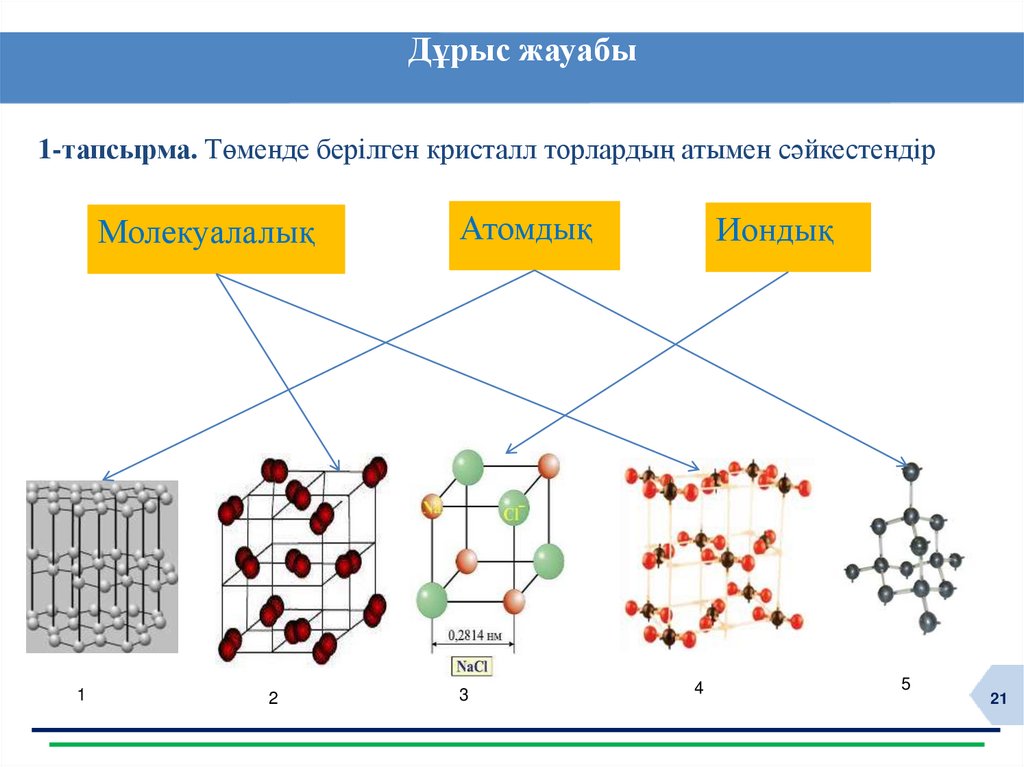
Дұрыс жауабы1-тапсырма. Төменде берілген кристалл торлардың атымен сәйкестендір
Молекуалалық
1
2
Атомдық
3
Иондық
4
5
21
22.
Бекіту тапсырмасы2-тапсырма. Кристалл торлары бірдей заттарды диагоналді, көлденең,
тігінен сызық жүргізіп белгілеп шығыңыз
NaCl N2O
H2
CO2
O2
NH3
Cl2
K2S
NaO
H
Дескриптор: кристалл торлары бірдей заттарды дұрыс табады.
Білім алушы
22
23.
Дұрыс жауабы2-тапсырма. Кристалл торлары бірдей заттарды диагоналді, көлденең,
тігінен сызық жүргізіп белгілеп шығыңыз
NaCl
N2O
H2
CO2
O2
NH3
Cl2
K2S NaOH
23
24.
Кейбір заттардың балқу температураларыЗаттар атаулары
Натрий фториді NaF
Балқу
температурасы (С)
905
Фторсутек HF
- 83
Фтор F2
- 220
Қорытынды
Заттардың физика-химиялық қасиеттері
торларының типтеріне тәуелді болады.
олардың
кристалдық
24
25.
Жеке жұмыс1.
2.
Периодтық кестенің көмегімен байланыс және кристалдық тор
типтерін анықтау үшін алгоритм құрастырыңыз.
Әр түрлі түспен көрсетілген элементтерден түзілген жай заттардың
физикалық қасиеттері, кристалдық торлар типтері туралы
ақпараттармен кестені толықтырыңыз.
Топ
Период
1
2
3
4
5
Кристалдық
торлар типтері
Физикалық
қасиеттері
I
Li
Na
K
Rb
II
Be
Mg
Ca
Sr
III
B
Al
Ga
In
IV
C
Si
Ge
Sn
V
N
P
As
Sb
VI
VII
VIII
O
S
Se
Te
Н
F
Cl
Br
I
He
Ne
Ar
Kr
Xe
26.
Металдық кристалдық торМеталдарда металдық байланыстар болады,
себебі кристалдық торларының түйіндеріне
металл атомдары мен иондар орналасқан , ал
металдың көлемінде электрон бұлттары еркін
қозғалып жүреді. Осы электорндар металдық
қасиеттерді анықтайды:
а) жоғары жылу және электрөткізгіштік
ә) металдық, жылтыр
б) созылғыштық, тапталғыштығы
27.
Тордың типіАтомдық
Молекулалық
Иондық
Металдық
Құрылыс
бірлігі
Бөлшектердің
арасындағы
байланыс типі
Балқу
температурас
ы
Ерігіштігі
Мысалдар
28.
Тордың типіҚүрылыс
бірлігі
Бөлшектердің
арасындағы
байланыс типі
Балқу
температурас
ы
Атомдық
Бейтарап
атомдар
Ковалентті
Жоғары
Молекулалық
Әлсіз
Молекулала
молекулааралық Төмен
р
байланыстар
Иондық
Иондар
Иондық
Жоғары
Металдық
Металл
атомдары
«Электрон» газы Әр түрлі
мен
катиондары
Ерігіштігі
Ерімейтін
Мысалдар
С, Si, SiO2
Барлық газдар, жай
Органикалық
заттар, І2, Вr2,
еріткіштер
қышқылдық оксидтер,
мен суда
қышқылдар,
ериді
органикалық заттар
Суда ерімтал
келеді
Металдар мен
бейметалдардан
түратын заттар,
гидроксидтер, тұздар
Ерімейтін
Металдар
Металдар
29.
ҚорытындыҚОЛДАНЫЛУЫ
ҚАСИЕТТЕРІ
КРИСТАЛДЫҚ
ТОР ТҮРІ
ХИМИЯЛЫҚ
БАЙЛАНЫС ТИПІ
ЗАТ
ҚҰРАМЫ
Заттың қасиеті химиялық байланыс типі мен
кристалдық тор құрылысына тәуелді
30.
Қорытынды:• Қатты күйдегі заттардың қасиеттері
кристалдық тор типіне тәуелді (ең
бірінші кезекте кристалл тор
түйінінде орналасқан бөлшекке
байланысты)
31.
Сабақ тақырыбы: Кристалдық тор түрлері, байланыстиптері және заттардың қасиеттері
арасындағы өзара байланыс
Сабақ мақсаты:
заттардың қасиеттері
кристалдық тор түрлері мен
байланыс типтеріне тәуелділігін зерттеу;
Fe
32.
Ойлан- жұптас-бөлісЙод не болды, ыстыққа шыдамай
жатырсынба?
Заттардың байланыс типін анықтаңыз, соған сәйкес қасиеттерін сипаттаңыз
33.
Кристалл торлары бірдей заттарды диагоналді, көлденең, тігіненсызық жүргізіп белгілеп шығыңыз
NaCl
N2O
Mg(OH)2
CO2
K2S
NH3
Cl2
O2
NaOH
34.
Кристалл торлары бірдей заттарды диагоналді, көлденең, тігіненсызық жүргізіп белгілеп шығыңыз
NaCl
N2O
Mg(OH)2
CO2
K2S
NH3
Cl2
O2
NaOH
35.
Берілген қосылыстардағы заттардыңбайланыс типі мен кристалдық тор түрін анықтаңыз
36.
Берілген қосылыстардағы заттардыңбайланыс типі мен кристалдық тор түрін анықтаңыз
3
37.
Берілген қосылыстардағы заттардыңбайланыс типі мен кристалдық тор түрін анықтаңыз
38.
Берілген қосылыстардағы заттардыңбайланыс типі мен кристалдық тор түрін анықтаңыз
39.
Берілген қосылыстардағы заттардыңбайланыс типі мен кристалдық тор түрін анықтаңыз
2
40.
КЕРІ БАЙЛАНЫС41.
Бүгінгі сабақта:•Байланыс түрлерін білемін.
• Кристалдық торлардың түрлері туралы түсінік беремін.
• Кристалл тор түрлерін ажырата аламын.
• Заттардың құрылымы мен қасиеттері арасындағы қатынас орнатамын.
Қосымша ресурстар
Химия оқулығы 8 сынып
Оспанова М.Қ., Белоусова Т.Г. Аухадиева.Қ.С
https://bilimland.kz/kk/subject/ximiya/8-synyp/
41
42.
• Номер: 641662• Прямая ссылка: https://www.Learnis.ru/641662/
42
43.
1-тапсырма• Келесі қосылыстардың ішінен нешеуі:
• 1. ковалентті полюсті
• 2. ковалентті полюссіз
• 3. иондық байланыстарға жататынын анықтаңдар.
Br2 , CO2, P2O5, HI, РH3 , NaCl , I2 , O3
43
44.
2-тапсырма• Күкірт ионының барлық электрондар саны
қанша?
44
45.
3-тапсырма• Льюис диаграммасын құру арқылы калий
сульфидінің түзілу механизмін көрсетіп,
күкірттің айналасындағы электрон санын
анықтаңдар.
45
46.
4-тапсырма• Период
бойынша солдан оңға қарай элементтердің
электртерістігінің мәні қалай өзгереді?
А)кемиді
Б)кемиді, сосын артады
С)өзгермейді
Д) артады
• Негізгі топшаларда жоғарыдан төмен қарай элементтердің
электртерістігінің мәні қалай өзгереді?
А) кемиді
Б) артады, сосын кемиді
С) өзгермейді
Д) артады
46
47.
Есептер:1. Мыс
сульфатының
қандай
мөлшерінде
38,4 г мыс болады?
M(CuSO4) = 64 + 32 + 16*4 = 160 г/моль
160 г CuSO4 ----- 64 г Cu
X г CuSO4 -------- 38,4 г Cu
X = 160*38,4 / 64 = 96 г
1. Мыс сульфатының ерітіндісіне 3,5 г темір ұнтағы
салынды. Неше грамм мыс бөлініп шықты?
3,5 г
хг
CuSO4 + Fe = FeSO4 + Cu
56 г
64 г
Х = 3,5*64 / 56 = 4 г
48.
Есептер:1.
Мыс сульфатының проценттік құрамы қандай?
CuSO4
W = N * Ar / Mr * 100 %
W(Cu) = 64 / 160 * 100 % = 40 %
W(S) = 32 / 160 * 100 % = 20 %
W(O) = 4 * 16 / 160 * 100 % = 40 %
Мырыш кендерінің ішіндегі ең маңыздысы - мырыш
алдамышы (ZnS). Осы кенді анализ жасап тексергенде,
оның 100 грамында 32,5 г мырыш бар екені анықталды.
Кендегі мырыш сульфидінің (ZnS) проценттік мөлшері
қандай?
M(ZnS) = 65 + 32 = 97 г/моль
97 г ------ 65 г Zn
Х г ------- 32,5 г Zn
X = 48,5 г ZnS
W(ZnS) = m(ZnS) / m(жалпы) * 100 % = 48,5 / 100 *100 % = 48,5 %
1.
49.
Есептер:5. Күкірт пен көмірдің 2 г қоспасын жаққанда,
күкірт (IV) оксиді (SO2) мен көміртегі (IV) оксидінің
(CO2) 6 г қоспасы шықты. Алғашқы қоспада неше
грамм көмір болғаны?
Xг
уг
C + O2 = CO2
12 г
44 г
У = 44х / 12 = 3,6 х
2–x
z
S + O2 = SO2
32 г
64 г
Z = 64 * (2-x) / 32 = 4-2x
3,6 x + 4 – 2x = 6
1,6 x = 2
X = 1,25 г С
50.
Есептер:5. Күкірт пен көмірдің 2 г қоспасын жаққанда,
күкірт
(IV) оксиді (SO2) мен көміртегі (IV)
оксидінің (CO2) 6 г қоспасы шықты. Алғашқы
қоспада неше грамм көмір болғаны?
6. Алюминий (ІІІ) оксидінің
құрамындағы
алюминийдің массалық үлесі?
7. 50 г мыс сульфатын
мыс гидроксидіне
айналдыру үшін қанша натрий гидроксиді керек?
51.
Есептер:1. Кальций нитратының 20,4 грамында қанша моль бар?
2. Кальций оксидінің 0,2 молінде қанша грамы бар?
3. Заттың құрамында 62,1 % көміртегі, 10,3 % сутегі, 27,6 %
оттегі
бар,
оның
мольдік
массасы 58. Заттың формуласын табыңыз.
52.
Есептер1.
31,8 г натрий карбонаты бар ерітіндіге 14,6 г тұз қышқылы бар
ерітінді құйылды. Қай зат және қандай мөлшерде артық қалды?
2.
Белгісіз заттың 6,8 г жаққанда 3,6 г су және 12,8 г күкірт (VІ)
оксиді түзілді. Осы заттың молекулалық формуласын табыңыз.
3.
Алюминотермия реакциясы кезінде 15 кг темір бөлінді. Оның ос
ы мөлшерін түзуге жұмсалған темір оксидінің және алюминийдіі
массасын табыңыз
53.
Есептер4. Хлорсутегінің 14,6 г мен аммиактың 8 г араластырылды. Қанша аммон
ий хлориді түзілді? Қай газ, қандай мөлшерде артық қалды?
5. Оттегі зертханада және өнеркәсіпте қалай алынады? 49 г бертолле
тұзы айырылғанда қанша көлем оттегі (қ.ж.) бөлінеді?
6. 16 г кальций оксиді суда ерітілді. Алынған гидроксидті толық
бейтараптау үшін қанша көлем (қ.ж.) көміртегі (VІ) оксиді керек?
54.
Есептер1. Судың айырылу реакциясын жазып, 90 г суды айырғанда түзілетін
оттектің массасын есептеңдер.
2. Массасы 3,2 г күкірт оттекпен әрекеттескенде түзілетін газдың көлемі
(қ.ж.)
3. 0,1 моль алюминиймен әрекеттесетін оттегінің (қ.ж.) көлемі
4. Сутек пероксидінен оттек алу реакциясының теңдеуін жазып, 16 г
оттек алу үшін қажетті сутек пероксидінің массасын есептеңдер.
5. Массасы 24,5 г калий хлоратын KClO3 айырғанда түзілетін оттектің
массасын есептеңдер.
55.
Есептер:1.
Мыс сульфатының қандай мөлшерінде 38,4 г мыс болады?
160 г CuSO4 ------ 64 г Cu
Х г CuSO4 -------- 38,4 г Сu
Х = 160*38,4 / 64 = 96 г СuSO4
1.
Мыс сульфатының ерітіндісіне 3,5 г темір ұнтағы салынды. Неше грамм
мыс бөлініп шықты?
3,5 г
хг
CuSO4 + Fe = Cu + FeSO4
56 г
64 г
Х = 3,5*64 / 56 = 4 г
1.
Мыс сульфатының проценттік құрамы қандай?
w = N * Ar / Mr *100 %
W(Cu) = 64 / 160 * 100% = 40%
W(S) = 32 / 160 *100% = 20%
W(O) = 4*16 / 160 *100% = 40%
1.
Мырыш кендерінің ішіндегі ең маңыздысы - мырыш алдамышы (ZnS).
Осы кенді анализ жасап тексергенде, оның 100 грамында 32,5 г мырыш
бар екені анықталды. Кендегі мырыш сульфидінің (ZnS) проценттік
мөлшері қандай?
M(ZnS) = 97 г/моль
97 г ZnS ---- 65 г Zn
Х г ZnS ----- 32,5 г Zn
X = 48,5 г (ZnS)
W = m (зат) / m (жалпы) = 48,5 / 100 *100% = 48,5 %
56.
Есептер:5. Күкірт пен көмірдің 2 г қоспасын жаққанда,
күкірт
(IV) оксиді (SO2) мен көміртегі (IV)
оксидінің (CO2) 6 г қоспасы шықты. Алғашқы
қоспада неше грамм көмір болғаны?
Хг
yг
С + О2 = СО2
12 г
44 г
У = 44х / 12 = 3,6 х
2-x г
zг
S + O2 = SO2
32 г
64 г
Z = 64*(2-x) / 32 = 4-2x
3,6х + 4-2x = 6
X=1,25 г (С)
2-1,25 = 0,75 г (S)
57.
Есептер:5. Күкірт пен көмірдің 2 г қоспасын жаққанда,
күкірт (IV) оксиді (SO2) мен көміртегі (IV) оксидінің
(CO2) 6 г қоспасы шықты. Алғашқы қоспада неше
грамм көмір болғаны?
6. Алюминий (ІІІ) оксидінің құрамындағы алюминийдің
массалық үлесі?
Mr (Al2O3) = 27*2 + 16*3 = 102 г/моль
w(Al) = N*Ar(Al) / Mr *100%= 2*27 / 102 *100% =52,94
%
w(O) = 3*16 / 102 * 100% = 47,06%
7. 50 г мыс сульфатын мыс гидроксидіне айналдыру
үшін қанша натрий гидроксиді керек?
58.
Есептер:7. 50 г мыс сульфатын
мыс гидроксидіне
айналдыру үшін қанша натрий гидроксиді керек?
50 г
хг
CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
160 г
80 г
Х = 50*80/160 = 25 г
Mr(CuSO4) = 64 + 32 + 16*4 = 160 г/моль
Mr(NaOH) = 23 + 16 + 1 = 40 г/моль
59.
Есептер:1. Кальций нитратының 20,4 грамында қанша моль бар?
n=m/M
n = N / Na
n = V / Vm
m(Ca(NO3)2) = 20,4 г
M(Ca(NO3)2) = 40 + (14+16*3)*2 = 164 г/моль
n = m / M = 20,4 г / 164 г/моль = 0,12 моль
1. Кальций оксидінің 0,2 молінде қанша грамы бар?
n(CaO) = 0,2 моль
M(CaO) = 40+16=56 г/моль
m(СаО) = n * M = 0,2 моль * 56 г/моль = 11,2 г
1. Заттың құрамында 62,1 % көміртегі, 10,3 % сутегі, 27,6 %
оттегі
бар,
оның
мольдік
60.
Есептер:Заттың құрамында 62,1 % көміртегі, 10,3 % сутегі, 27,6 %
оттегі бар, оның мольдік массасы 58. Заттың формуласын табыңыз.
W(C) = 62,1 %
W(H) = 10,3%
W(O) = 27,6 %
Mr = 58
W=






















































 Химия
Химия








