Похожие презентации:
Мікроклональне розмноження рослин
1.
НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ БІОРЕСУРСІВ ТА ПРИРОДОКОРИСТУВАННЯ УКРАЇНИМікроклональне
розмноження рослин
Лектор,
Доктор сільськогосподарських
наук
професор кафедри
екобіотехнології та
біорізноманіття Кляченко Оксана Леонідівна
2.
План• 1. Теорія і принципи мікроклонального розмноження
рослин.
• 2. Етапи мікроклонального розмноження рослин.
• 3.Фактори, які впливають на регенерацію рослин.
• 4. Умови культивування рослин-регенерантів.
• 5. Отримання безвірусного посадкового матеріалу
3.
Мікроклональне розмноження рослин – це неста-теве вегетативне розмноження, при якому отримують генетично ідентичні форми, що сприяє
збереженню генетично однорідного посадкового
матеріалу. В основі мікроклонального розмноження лежить процес регенерації, відновлення цілої
рослини із клітин, які знаходяться на різних
етапах онтогенезу,
життєвого циклу.
4.
Термін клон походить від грецького Κλών – паросток,пагін букв запропонований Робертом Джоном Вебером
у 1903 р. як назва для «групи рослин, котрі отримані з
використанням будь-якої вегетативної
частини рослини(наприклад, бульб чи цибулин) і є
частиною однієї і тієї ж особини.
5.
• Для такого розмноження використовуютьсячастини рослин (експланти), котрі вже
містять меристемні (твірні)
тканини чи меристемні групи клітин – зародок,
ембріоїди, різні види бруньок (верхівкові, пазушні,
сплячі тощо) або такі осередки індукуються в
процесі роботи
6.
• Вперше метод культури твірних тканин длямікроклонального розмноження застосував
французький дослідник Жан Морель у 1690
році для одного з виду орхідей –
цимбідіума Cymbidium. Протягом року йому
вдалося отримати з одного вихідного
експланта близько 4 млн рослин.
7.
Переваги мікроклонального розмноження рослин• значно вищий коефіцієнт розмноження. При мікроклональному
розмноженні можна отримати до 100000-1000000 мериклонів в
рік, тоді як при звичайному розмноженні - 5-100 рослин за той
же термін;
• - мініатюризація процесу, що призводить до економії площ, які
зайняті маточними та розмножуваними рослинами;
• - оздоровлення рослин від грибних і бактеріальних патогенів,
вірусів, мікоплазменних, віроїдних і нематодних інфекцій;
• - великою перевагою даної технології є те, що в умовах in vitro
часто розмножаються і укорінюються ті рослини, які зовсім не
розмножуються або погано розмножуються звичайним шляхом;
• Створення «банку» не інфікованого селекційного матеріалу;
• Можливість широкого обміну рослинним матеріалом між
регіонами і країнами.
8.
Основні типи мікророзмноження• Мікрочеренкування;
• Утворення мікробульб і мікроцибулин;
• Індукція адвентивних бруньок;
• Пригнічення апікального домінування і
розвиток пазушних бруньок;
• Розмноження в біореакторах
мікробульбами та мікроцибулинами
(картопля, гдадіолуси, нарціси, лілії
9.
Масштабність застосування МКР• Відповідно до кількості отриманої продукції, технології розмноження in vitro розподіляють на велико- і мало масштабні. Поділ
такий умовний тому, що він пов'язаний з метою досліджень та
сферою застосування.
• Створення потрібного числа копій цінних, унікальних для селекціонера генотипів (ліній, гібридів, мутантів, трансгенних рослин)
не потребує великих масштабів
• Швидке мікроклональне розмноження новостворених і існуючих
господарськоцінних сортів з метою масового отримання
посадкового матеріалу є великомасштабним процесом.
Масштаби застосування технологій визначаються потребою та
рентабельністю.
10.
Перспективні сфери застосуваннямікроклонального розмноження
• Швидке мікроклональне розмноження in vitro кращих
екземплярів дорослих деревних культур та їх «плюсових» форм,
особливо це стосується хвойних;
• Використання техніки in vitro для розмноження гетерозисних,
гібридів F1 покоління, в яких проходить розщеплення в
наступних поколіннях та гетерозиготних, що розщеплюються
при схрещуванні рослин;
• Збереження рідкісних та зникаючих видів рослин, їх
розмноження та повернення у відповідне природнє середовище;
• Розмноження сконструйованих генетично модифікованих
рослин.
11.
При мікроклональному розмноженні для отримання цілої рослиниможе бути використано два типи клітин:
• 1) ізольована клітина в стані активного ділення із ембріональної,
недиференційованої, неспеціалізованої меристемної тканини.
Такими тканинами є верхівкові (апікальні) меристеми пазушних
або сплячих бруньок стебла;
• 2) ізольовані спеціалізовані тканини, які пройшли процес
диференціації. Такі клітини складають спеціалізовані тканини
експлантату (мезодерміс, епідерміс). В цьому випадку виникають
in vitro ініціюючі меристемоїдні ембріональні клітини, проходить
соматичний ембріогенез, утворюються бруньки або ембріоїди із
яких формується рослина і здійснюється процес розмноження
рослин.
12.
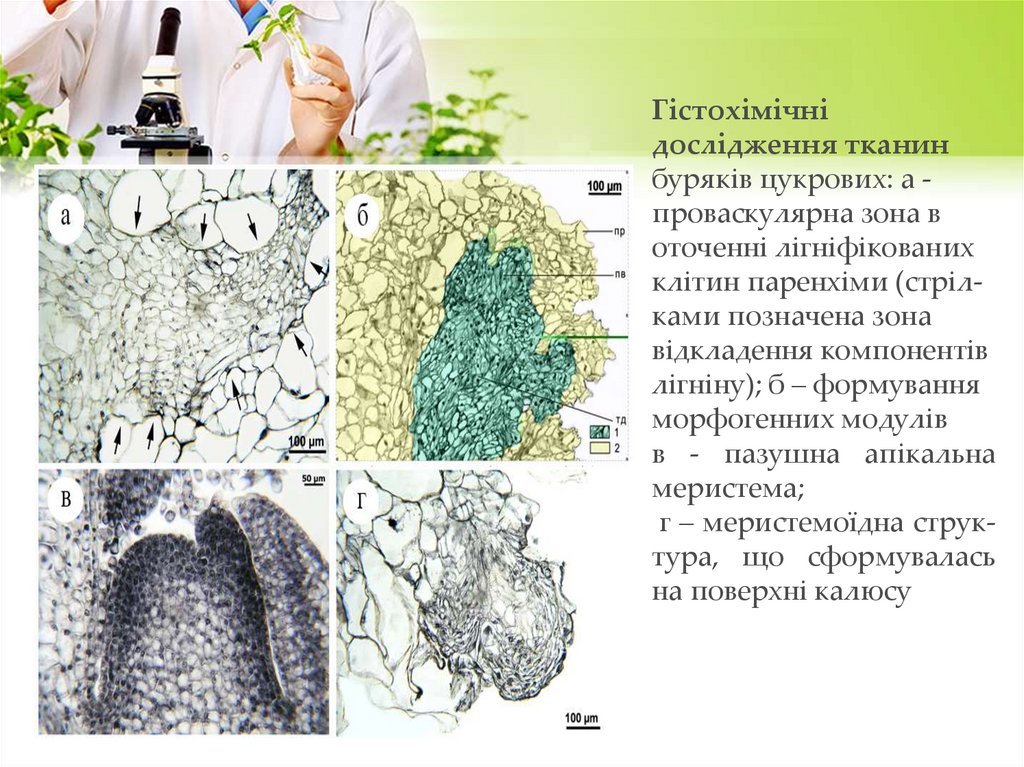
Гістохімічнідослідження тканин
буряків цукрових: а проваскулярна зона в
оточенні лігніфікованих
клітин паренхіми (стрілками позначена зона
відкладення компонентів
лігніну); б – формування
морфогенних модулів
в - пазушна апікальна
меристема;
г – меристемоїдна структура, що сформувалась
на поверхні калюсу
13.
• Меристемоїди - це морфогенетично компетентніклітини, які на індуктори диференціювання і склад
живильних середовищ відповідають утворенням
пагонів, бруньок, коренів, зародків. Морфологічно їх
виявляють у калюсних тканинах у компактних
осередках клітин, які діляться у вигляді мілких,
ізодіаметричних, тонкостінних клітин з великим
ядром, густою цитоплазмою і майже без вакуолей.
14.
Збільшення вмісту меристемоїдівВміст меристемоїдів можна збільшити завдяки
відбору. Крім того, для подальшого розвитку
меристемоїдів їх необхідно відділяти від
немеристемоїдних клітин, так як останні
подавляють ембріогенез компетентних клітин,
виділяючи інгібітори.
Необхідність відбору меристемоїдних клітин
також
обумовлюється
тим,
що
при
довготривалому культивуванні тканин знижується
здатність до регенерації рослин. Процес відбору
залежить від досвіду і здатності дослідника
визначати морфо генетичні компетентні клітини.
При цьому використовують «зелені осередки»
калусу, як маркери клітин, які регенерують
рослини. Інші по шукачі відбирають для
регенерації гладенькі, білі структури, що не
розпадаються. Відмічено, що у злакових, вони
найбільш легко дають початок ембріогенним
лініям.
15.
Основні етапи мікроклонального розмноження1. Пошук наукової літератури;
2. Вибір рослини донора,
ізолювання і стерилізація експланту,
створення умов для його росту на живильному
середовищі in vitro.
3. Власне розмноження шляхом:
• стимуляції розвитку всіх пазушних бруньок
екпланту в результаті пригнічення апікального
домінування як первинного пагону так і тих,
що виникли заново;
16.
Етапи мікроклональногорозмноження
• стимуляції розвитку всіх пазушних бруньок екпланту в
результаті пригнічення апікального домінування як
первинного пагону так і тих, що виникли заново;
• мікрочеренкування пагону, який зберігає апікальне
домінування;
• стимуляція утворення мікро бульб та мікро цибулин;
• індукція утворення адвентивних бруньок тканинами
листка, стебла, чешуйками, кореневищами, зачатками
суцвіть (без утворення калусних тканин);
17.
Етапи мікроклонального розмноження4. Укорінення розмножених пагонів і адаптація
пробірочних рослин до висадження в умови in
vivo.
5. Вирощування рослин і перенесення їх в умовах
теплиці в грунт або на штучний субстрат.
6. Підготовка до реалізації або висадження на
поля.
18.
Не існує технології мікроклонального розмноження, єдиної для всіхвидів рослин, тому для кожного виду (а часто - і сорту) оптимальні
умови кожного з етапів підбираються індивідуально .
При розробці протоколу розмноження слід
враховувати :
1
2
• Генотип рослини-донора
• Фізіологічний стан рослини-донора
Розмір і тип експлантату
3
4
5
• Склад живильного середовища
• Фізичні умови культивування
19.
Рослини-донори експлантатів повинні бутипротестовані на наявність вірусних,
мікоплазменних та бактеріальних інфекцій за
допомогою: ПЛР – діагностики,
імуноферментного
аналізу, молекулярної
ПЛР-діагностики
гібридизації нуклеїнових кислот
20.
Підбір екплантатів та введення їх в культуру in vitroНайкраще використовувати матеріал, вилучений із здорових
(неінфікованих) сильних рослин, що мали оптимальні умови
вирощування (площа живлення, забезпечення NPK, полив
тощо).
Розмір експлантату залежить від виду біоматеріалу і
коливається в межах від 0,1мм до 1,0 см.
Апікальну меристему – конус наростання клітин, що активно
діляться висотою 0,1мм і шириною 0,25мм важко відділити без
ушкоджень та індукувати 5 до росту
Вичленування меристем проводять у стерильному ламінарбоксі за використання бінокулярного мікроскопу зі
збільшенням в 20-40 разів.
21.
Живильні середовища для мікроклональногорозмноження
Мурасіге-Скуга
Гамборга
Уайта
Міллера
Као та Михайлюка
Мореля
22.
Активація розвитку меристем з експлантату• Живильне середовище для введення in vitro меристем збагачують
на 15 % вищими концентраціями регуляторів росту
• Висаджені на живильне середовище матеріали розміщують у
культуральних кімнатах і забезпечують оптимальними фізичними
умовами вирощування: температурний режим 22–26 °С;
• відносна вологість 75–80 %;
• 16-ти годинний фотоперіод за інтенсивності освітлення 3–5 клк .
Після 20–30 діб (що залежить від біотипу, генотипу, живильного
субстрату) утворені пагони звільняють від вихідних тканин і
переносять на середовище для розмноження
23.
Розмноження рослинного матеріалуЗа мікроклонального розмноження розрізняють два типи
клонування:
Вертикальне
Горизонтальне
Тип залежить від орієнтації розвитку і наростання
біоматеріалу та закладення вегетативних бруньок.
24.
Вертикальний тип клонування характерний длятканин ауксинової природи (картопля, спаржа,
гвоздика).
Для цього типу тканин у ростове живильне
середовище
додатково
вводять
високі
концентрації ауксинів, що стимулюють розвиток
апікальної меристеми і пригнічують формування
бокових пагонів. Матеріал швидко наростає,
формуючи одне центральне стебло з листочками
25.
У фазі 7–10 листків рослина здатна доклонування. ЇЇ виймають з пробірки і гострим
ланцетом ділять на клони. Кожен клон має
частину
стебла
з
одним
листочком.
Проклонований матеріал висаджують на свіже
(оновлене) ростове живильне середовище, що
стимулюватиме розвиток бокової бруньки, яка
знаходиться між стеблом і черенком листка. Такий
тип клонування дозволяє отримати з однієї
рослини 7–10 клонів.
26.
Горизонтальнийтип
клонування
характерний для тканин цитокінінової
природи (буряк цукровий, цикорій, суниця
тощо). Для розвитку та розмноження такі
рослини
потребують
введення
до
живильного субстрату високих концентрацій
цитокінинів (6-бензиламінопурин, кінетин,
аденін)
Висока брунькоутворююча здатність рослин
під впливом цих регуляторів росту дає змогу
з однієї рослини отримати 15–35 клонів.
Кожен клон має апікальну меристему і
вільно відокремлюється; від загальної
колонії.
27.
Коефіцієнт розмноження залежить• генотипу рослини-донора і її фізіологічного стану;
• складу живильного середовища та фізичних умов
в культуральній посудині і за її межами
(освітлення, вологість, газовий склад);
• рівня стабільності процесу розмноження при
субкультивуванні мериклонів, що утворилися;
• дотримання асептичних умов вирощування та
приділенні особливої уваги хронічним інфекціям,
яку викликають повільно ростучі патогени
(Pseudomonas, Erwinia, Bacillus).
28.
Укорінення рослин-регенерантівПісля отримання необхідної (запрограмованої) кількості клонів,
їх переносять на середовище для укорінення та отримання
повноцінних рослин. Основними індукторами коренеутворення
є ауксини.
Для формування коренів пагони розділяють і висаджують на
живильне середовище для ризогенезу, що містить підвищені
концентрації регуляторів росту ауксинивої природи. Це
основне правило коренеформування in vitro. Під впливом
ауксинів (нафтилоцтова кислота, гетероауксин) стимулюється
поділ клітин паренхіми пагона, що призводить до
диференціації клітин у базальній частині клону та утворення
кореневих зачатків. Найкраще укорінюються клони, висота
яких перевищує 7 мм.
29.
Через 15–25 діб після висадки рослин на середовищедля ризогенезу формується добре розвинена
коренева система і рослинний матеріал готовий для
адаптації та перенесення в природні умови
вирощування.
30.
Адаптація культурального матеріалу та перенесеннярослин у грунтові умови вирощування
Відомо два способи адаптації:
• адаптація
пробірочних рослин
у біотехнологічній
лабораторії;
• проміжне
укорінення рослин
за використання
фітотронів
(теплиці)
31.
Рослинний матеріал на початковому етапі ростуможе мати незначні морфологічні зміни листкового
апарату та стебла, проте до кінця вегетації рослини
набувають типового вигляду, що є характерним для
рослини-донору вихідного експланту.
Обовʼязкову ідентифікацію біоматеріалу проводять
за допомогою цитологічного методу досліджень.
32.
Параметри росту рослин-регенерантівСира та суха маса рослин-регенерантів
Кількість та довжина міжвузлів
Індекс росту
Площа листкової поверхні
Коефіцієнт розмноження
33.
Мікроклонування використовуєтьсядля отримання посадкового
матеріалу таких рослин
Ягідні культури – лохина, суниця, малина, ожина, жимолость
Кісточкові плодові рослини – вишня, слива, черешня, абрикос, персик, а
також підщепи для них
Горіхоплідні – лісовий горіх (фундук), волоський горіх
Деревні та хвойні рослини (павловнія, туя)
Енергетичні рослини (верба, міскантус)
Декоративні – троянди, орхідеї, хризантеми, бегонії тощо
Екзотичні – банани, цитрусові
Лікарські та ефіроолійні – лаванда, женьшень, душиця
34.
Мікроклональне розмноження дляукраїнських аграріїв уможливлює
• Прискорити селекційний процес, завдяки чому у 5-6 разів скорочуються
строки отримання товарної продукції;
• Отримувати посадковий матеріал, ідентичний вихідному, із збереженням
усіх властивостей сорту, очищений від вірусних та бактеріальних інфекцій;
• Забезпечити рослинам активний ріст протягом всього року та захист від
несприятливих абіотичних та біотичних факторів;
• Тиражувати посадковий матеріал рослин, які складно розмножуються
вегетативно, або втрачають свої властивості при генеративному
розмноженні;
• При вирощуванні рослин із тривалою ювенільною фазою можна
прискорювати перехід рослин від ювенільної до репродуктивної фази;
• Забезпечити тривале зберігання рослин в умовах in vitro, створювати
банки для зберігання цінних видів рослин та їх органів;
• Використовувати культивування рослинних тканин для отримання
вторинних метаболітів (антибіотики, ферменти тощо).

































 Биология
Биология








