Похожие презентации:
Назовите основные классы неорганических веществ
1. «Основания»
L/O/G/O2.
Назовите основные классынеорганических веществ
NaOH
Оксиды
Основания
Классы
веществ
Кислоты
Соли
KOH
Cu(OH)2
Основания – сложные
вещества, состоящие из
атомов металла и
гидроксильных групп.
+n
Ме (ОН)n
3.
Основания– это сложные вещества,
состоящие из атома
металла и одной или
нескольких
гидроксогрупп.
4. Состав оснований: Назовите составные части оснований.
Валентность гидроксогруппы (ОН) – IКоличество гидроксогрупп определяется
валентностью металла, образующего основание.
М(ОН)х
5. Основания
NaOH – гидроксид натрияCa(OH)2 – гидроксид кальция
Fe(OH)3 – гидроксид железа (III)
Cи(OH)2 – гидроксид меди (II)
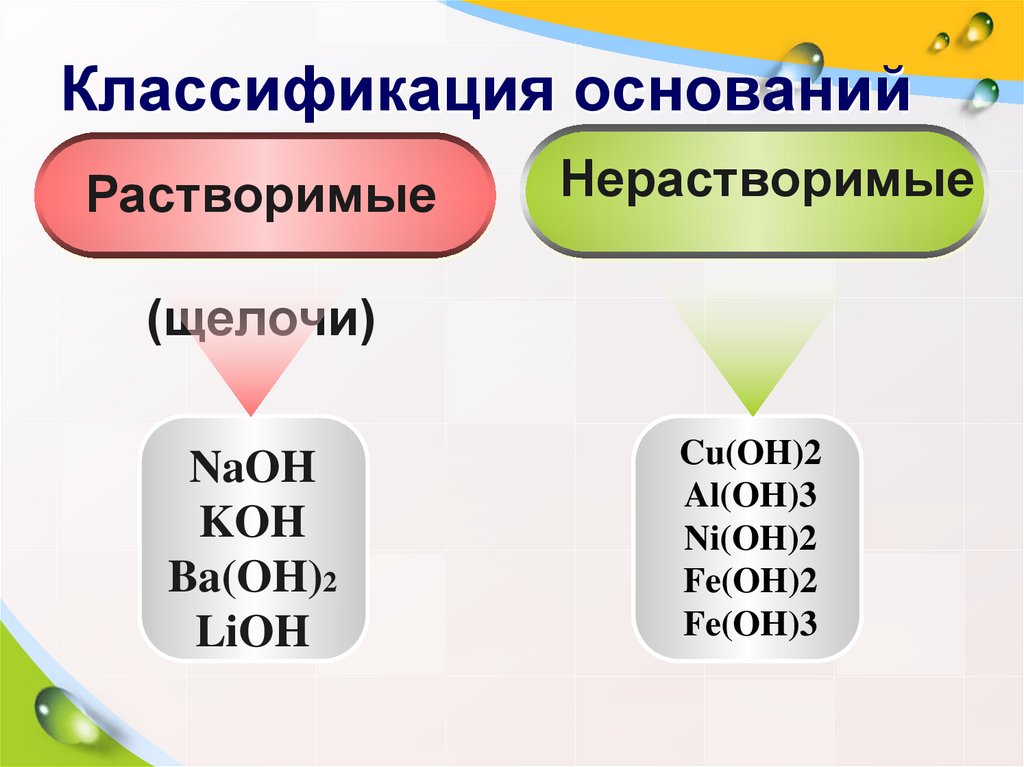
6. Классификация оснований
РастворимыеНерастворимые
(щелочи)
NaOH
KOH
Ba(OH)2
LiOH
Cu(OH)2
Al(OH)3
Ni(OH)2
Fe(OH)2
Fe(OH)3
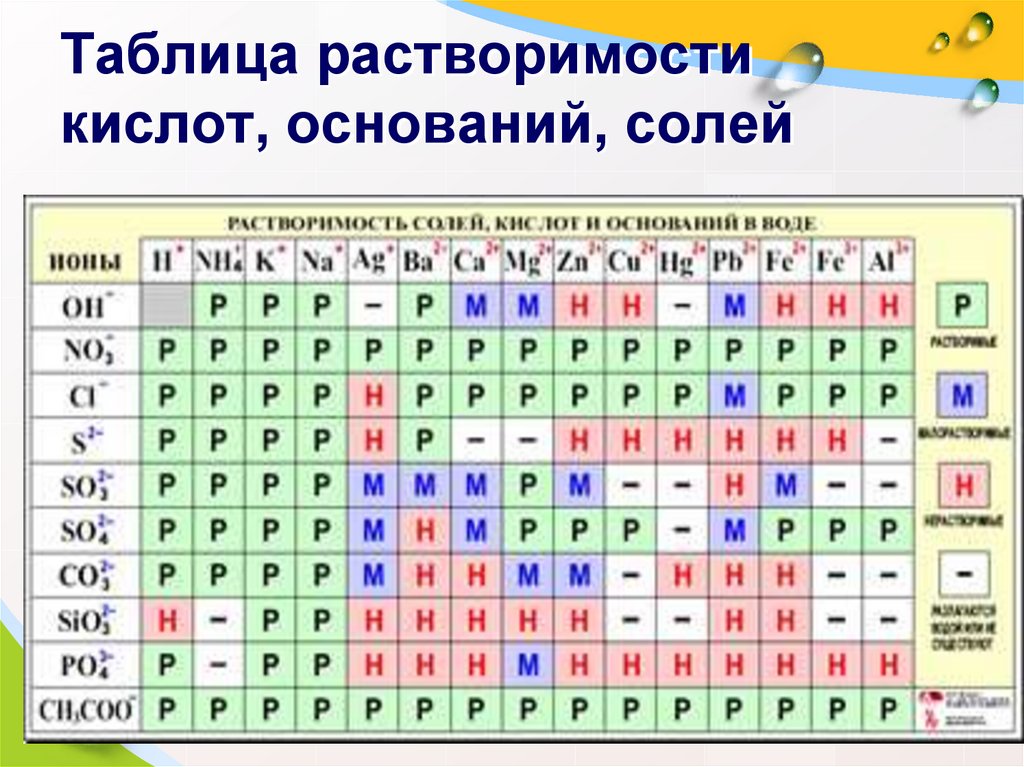
7. Таблица растворимости кислот, оснований, солей
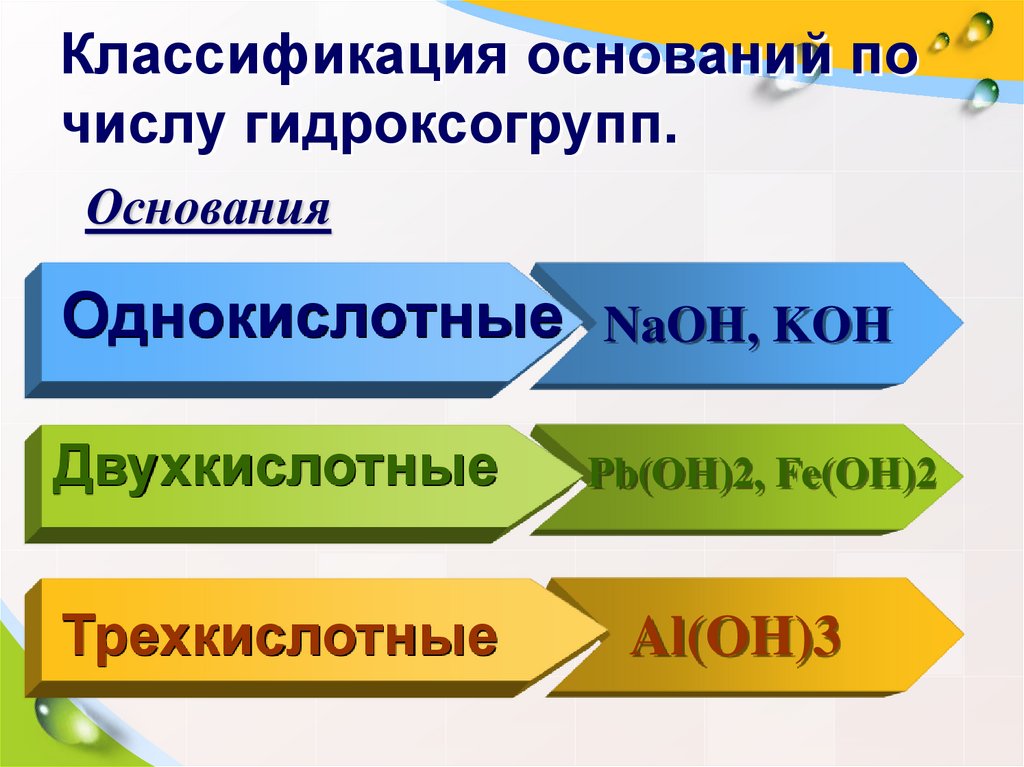
8. Классификация оснований по числу гидроксогрупп.
ОснованияОднокислотные NaOH, KOH
Двухкислотные
Pb(OH)2, Fe(OH)2
Трехкислотные
Al(OH)3
9.
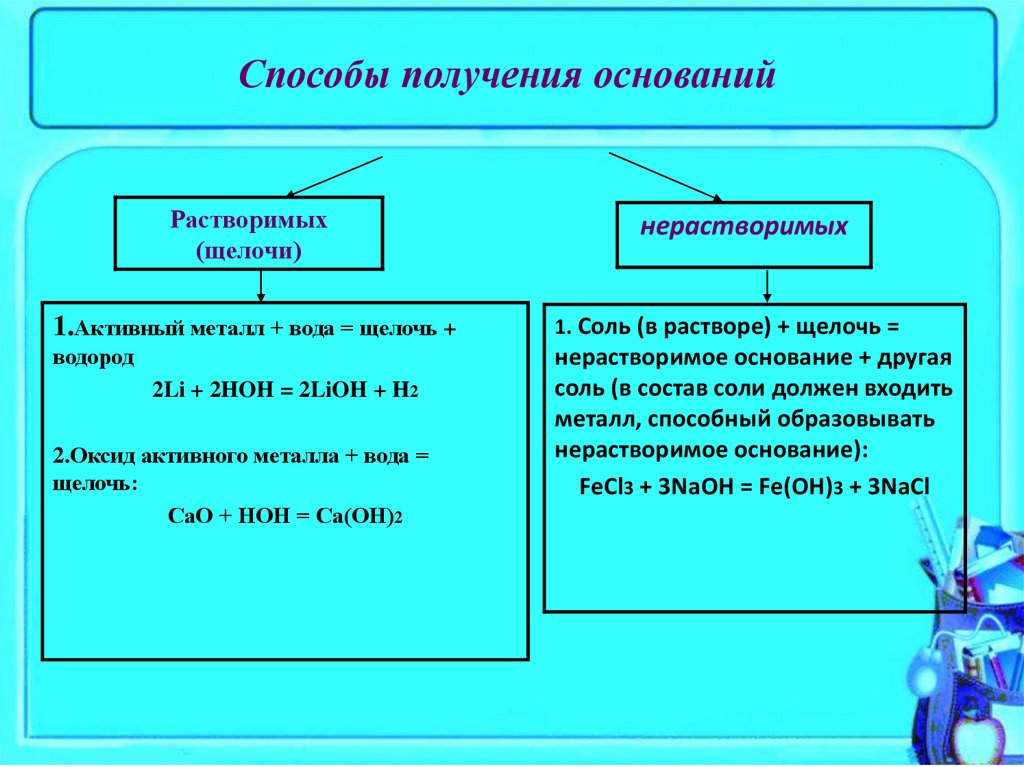
Способы получения основанийПолучение оснований
Растворимых
(щелочи)
нерастворимых
1.Активный металл + вода = щелочь +
1. Соль (в растворе) + щелочь =
водород
нерастворимое основание + другая
соль (в состав соли должен входить
металл, способный образовывать
нерастворимое основание):
FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl
2Li + 2HOH = 2LiOH + H2
2.Оксид активного металла + вода =
щелочь:
СаО + НОН = Са(ОН)2
10. Химические свойства нерастворимых оснований.
1). Разлагаются принагревании.
2). Взаимодействуют с
кислотами (реакция
нейтрализации).
11.
1. НЕРАСТВОРИМОЕ ОСНОВАНИЕ = ОКСИД +ВОДА
Fe(OH)2 = FeO + H2O
2. ОСНОВАНИЕ + КИСЛОТА = СОЛЬ + ВОДА
12. Химические свойства щелочей.
1). Изменяют окраскуиндикаторов.
Взаимодействуют с:
2). кислотами (реакция
нейтрализации),
3). кислотными оксидами,
4). солями.
13.
1). Щелочи изменяют окраску индикаторов.Индикаторы – от лат. «indication» - указатели
Лакмус
Метиловый
оранжевый
Фенолфталеин
NaOH
NaOH
NaOH
14.
2. ОСНОВАНИЕ + КИСЛОТА = СОЛЬ + ВОДА2KOH + H2SO4 → K2SO4 + 2H2O
15.
3. ЩЕЛОЧЬ+ КИСЛОТНЫЙ ОКСИД = СОЛЬ + ВОДА• 2NaOH + SO3 = Na2SO4+ H2O
16.
4. ЩЕЛОЧЬ+ РАСТВОРИМАЯ СОЛЬ =НОВОЕ ОСНОВАНИЕ↓ + НОВАЯ СОЛЬ
2KOH + CuSO3 = Cu(OH)↓ + K2SO4











 Химия
Химия








