Похожие презентации:
Щелочные металлы
1.
ЩЕЛОЧНЫЕ МЕТАЛЛЫ2.
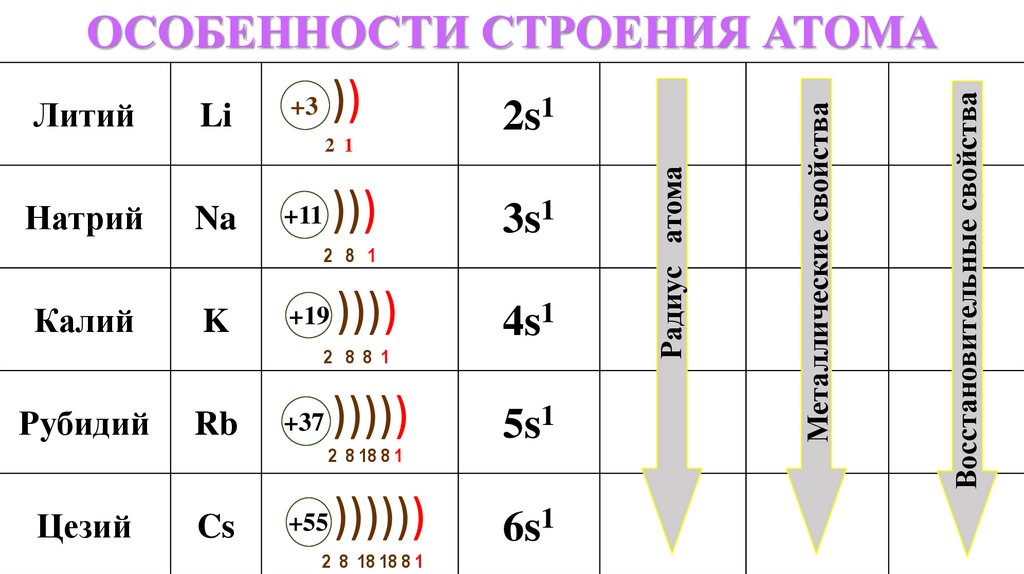
1. Расположение в периодической системе2. Особенности строения атома
3. Физические свойства
4. Химические свойства
5. Открытие
6. Получение
7. Na+ и K+ в организме человека
3.
))+3
2 1
Натрий
Na
)))
+11
2s1
3s1
2 8 1
Калий
K
+19
))))
4s1
2 8 8 1
Рубидий
Rb
)))))
+37
2 8 18 8 1
Цезий
Cs
+55
))))))
2 8 18 18 8 1
5s1
6s1
Восстановительные свойства
Li
Радиус атома
Литий
Металлические свойства
ОСОБЕННОСТИ СТРОЕНИЯ АТОМА
4.
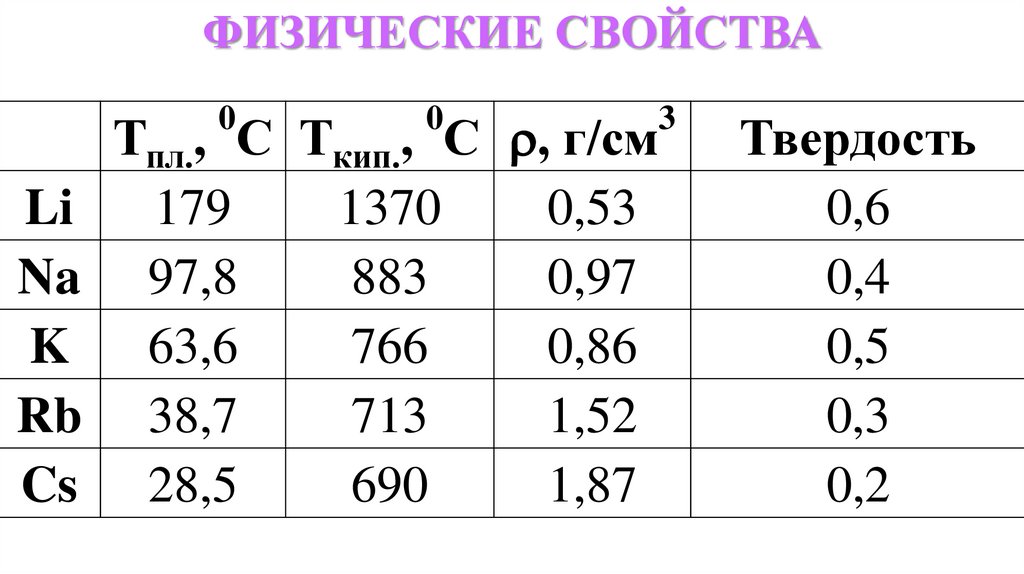
ФИЗИЧЕСКИЕ СВОЙСТВАТпл., С Ткип., С , г/см
Li
179
1370
0,53
Na 97,8
883
0,97
K
63,6
766
0,86
Rb 38,7
713
1,52
Cs 28,5
690
1,87
0
0
3
Твердость
0,6
0,4
0,5
0,3
0,2
5.
ХИМИЧЕСКИЕ СВОЙСТВАI. Реакции с неметаллами
1. Взаимодействие с галогенами:
2Na + Cl2 2NaCl
2. Взаимодействие с кислородом:
4Li + O2 2Li2O
оксид Li
2Na + O2 Na2O2
пероксид Na
2Na + Na2O2 2Na2O
оксид Na
6.
2K + 2O2 K2O4надпероксид K
6K + K2O4 4K2O
оксид K
0
3. Взаимодействие с водородом (при нагревании 200-400 С):
2Na + H2 2NaH
гидрид Na
4. Взаимодействие с азотом:
6Li + N2 2Li3N
нитрид Li
7.
II. Реакции со сложными веществами1. Взаимодействие с водой:
2Na + 2H2O 2NaOH + H2
2. Взаимодействие с кислотами:
2Na + 2HCl 2NaCl + H2
8.
КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕЩЕЛОЧНЫХ МЕТАЛЛОВ
Для распознавания соединений щелочных металлов по
окраске пламени исследуемое вещество вносится в пламя
горелки на кончике железной проволоки
+
Li
+
Na
+
K
+
Rb
+
Cs
Карминово-красный
Желтый
Фиолетовый
Красный
Фиолетово-синий
9.
10.
11.
ОТКРЫТИЕ ЩЕЛОЧНЫХ МЕТАЛЛО• 1807 г. в Англии Г. Деви открыл натрий и калий
•В 1817г. в Швеции А. Арфведсоном был открыт литий.
•В 1860 – 1861г.г. в Германии Р.Бунзен и Г.Кирхгоф открыли
рубидий «темно-красный» и цезий «небесно-голубой»
•В 1939г. во Франции М. Перей открыла радиоактивный
элемент франций, который назвала в честь своей страны –
Франции
12.
ПОЛУЧЕНИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ1. Электролиз расплавов соединений щелочных металлов:
2МеCl 2Ме + Cl2
4МеOH 4Ме + 2Н2О + О2
2. Восстановление оксидов и гидроксидов щелочных
металлов:
2Li2O + Si 4Li + SiO2↓
KOH + Na NаOH + K↓










 Химия
Химия








