Похожие презентации:
Оксиды
1. ОКСИДЫ
2. ОКСИДЫ -
ОКСИДЫ сложные вещества, состоящиеиз 2-х химических элементов,
один из которых кислород со
степенью окисления -2.
3. ФИЗИЧЕСКИЕ СВОЙСТВА ОКСИДОВ
ФИЗИЧЕСКИЕ СВОЙСТВА ОКСИДОВТВЕРДЫЕ
ЖИДКИЕ
ГАЗООБРАЗНЫЕ
4.
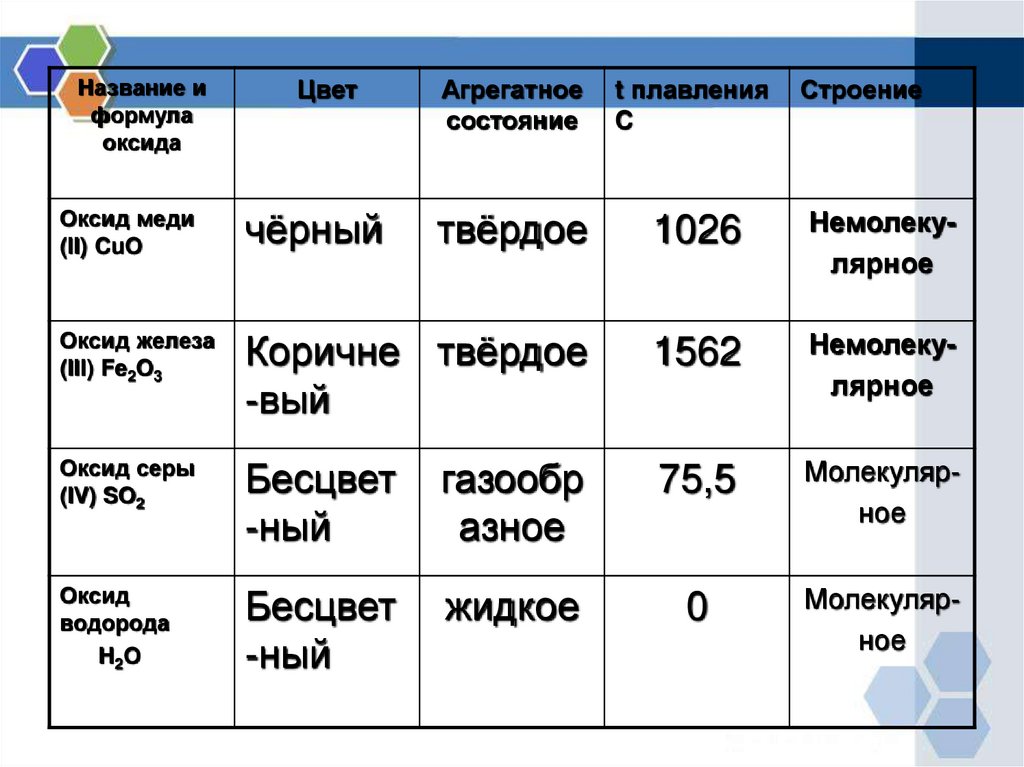
Название иформула
оксида
Цвет
Агрегатное
состояние
t плавления
C
Оксид меди
(II) CuO
чёрный
твёрдое
1026
Немолекулярное
Оксид железа
(III) Fe2O3
Коричне твёрдое
-вый
1562
Немолекулярное
Оксид серы
(IV) SO2
Бесцвет
-ный
газообр
азное
75,5
Молекулярное
Оксид
водорода
H2O
Бесцвет
-ный
жидкое
0
Молекулярное
Строение
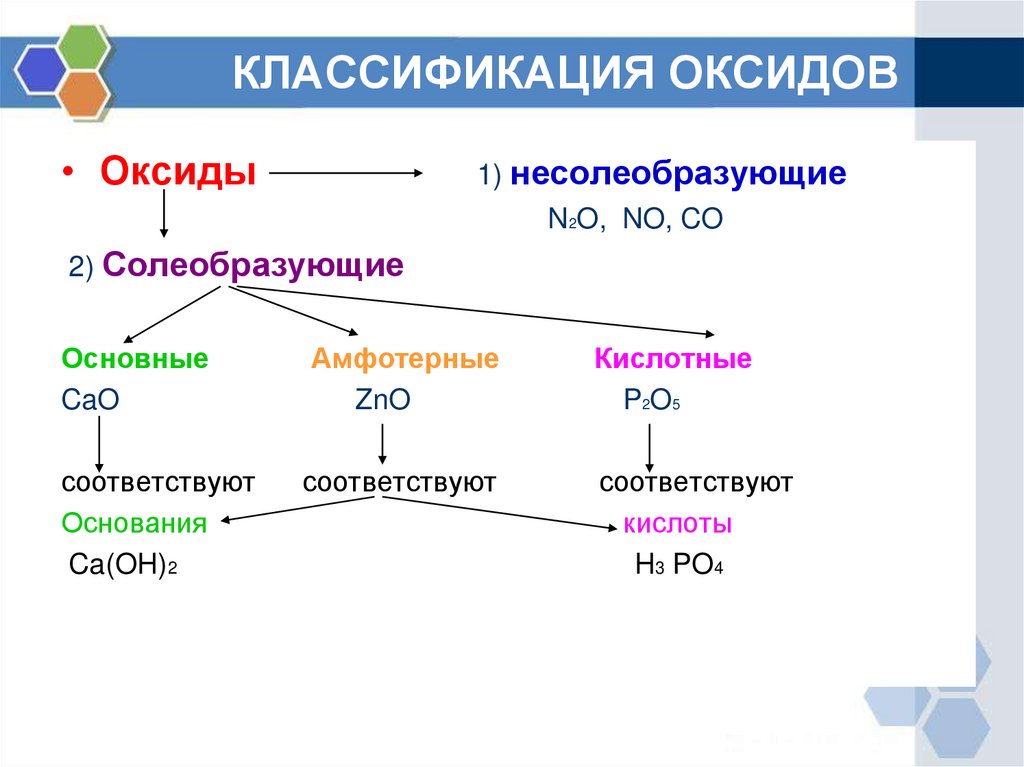
5. КЛАССИФИКАЦИЯ ОКСИДОВ
• Оксиды1) несолеобразующие
N2O, NO, CO
2) Солеобразующие
Основные
CaO
Амфотерные
ZnO
Кислотные
P2O5
соответствуют
Основания
Ca(OH)2
соответствуют
соответствуют
кислоты
H3 PO4
6. СХЕМА
ОксидыОсновные
металл и
кислород
CuO, Na2O
Кислотные
неметалл и
кислород
CO2, SO2
7. Образование оксидов
МеталлыНеметаллы
Образуют основные оксиды,
Степень окисления
(валентность) меньше 4
Образуют кислотные оксиды,
К
N
Na
S
Fe
P
Степень окисления
(валентность) больше четырех
8. ОПРЕДЕЛЕНИЕ ГРУПП ОКСИДОВ
• Основными называются оксиды, которымсоответствуют основания.
• Кислотными называются оксиды, которым
соответствуют кислоты.
• Амфотерными оксидами, называют
оксиды которые проявляют свойства как
кислот, так и оснований.
9. ФОРМУЛЫ ОКСИДОВ
1)Оксид серы(IV)2)Оксид азота(V)
3)Оксид калия (I)- основной оксид
4)Оксид железа(II) – основной оксид
5)Оксид фосфора(V)
6) оксид натрия (I)- основной оксид
10. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ (О.О.)
• 1) О.О. + кислота =соль + водаCaO + H2 SO4 →
• 2) О.О. + кислотный оксид = соль
СaO + SiO2 =
• 3) О.О.(раств) + вода = основание (щелочь)
Na2O + H2O →
11. Химические свойства кислотных оксидов (К.О.)
Химические свойства кислотных оксидов• 1) К.О. + основание = соль + вода
SO3 + NaOH →
• 2) К.О. +О.О. = СОЛЬ
SO3 + Na2O →
• 3) К.О. + вода = кислота (кроме SiO2 )
P2O5 + H2O →
(К.О.)
12. Получение оксидов:
1) Горение простых веществ2) Горение сложных веществ
3) Разложение нерастворимых оснований
4) Разложение солей
13. Домашнее задание
Составьте уравнения реакций, спомощью которых можно получить
следующие оксиды:
CO2 , Al2O3 , Li2 O , CaO , P2O5
14. Выпишите только формулы кислотных, основных, амфотерных оксидов
Домашнее задание № 1Выпишите только формулы кислотных,
основных, амфотерных оксидов
K2CO3 ; Li2O ; H2S ; Cr2 O3 ; LiOH ;
Сl2 O7 ; H3 PO4 ; MgO ; Al(OH) 3 ; SiO2 ;
NaNO3 ; CO2 ; Ca(NO3)2 ; SiO2 ; Na2S ;
HNO2 ; P2O5 ; HF ; H2S ; Fe (OH)2 ; СuO ;
SO2 ; Сr2O3 ; CuSO 4 ; N2 O5.
Дайте названия оксидам.
15. Домашнее задание № 2
Напишите уравнения возможных реакций:а) оксид натрия + вода =
б) оксид лития + серная кислота =
в) оксид бария + соляная кислота=
г) оксид меди (II) + оксид серы (IV) =
д) оксид калия + оксид серы (VI) =
е) Na2O + Ca(OH) 2 =
ж) CO2 + HCl =
16. Составьте уравнения реакций:
1) С +…= СO2
2) Al + … = Al2O3
3) PH3 + … = P2O5 + H2O
4) CuO + … = CuCl2 + H2O
5) P2O5 + … = H3PO4














 Химия
Химия








