Похожие презентации:
Соединения кальция: роль в природе и технике
1.
Соединения кальция, ихроль в природе и технике.
2.
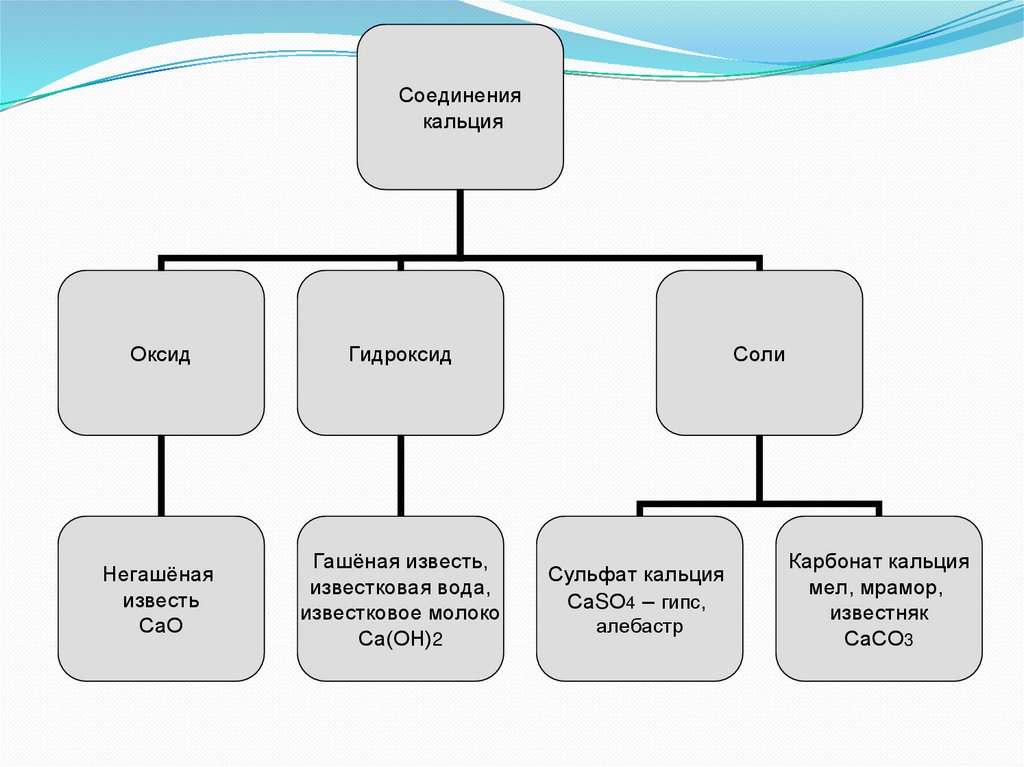
Соединениякальция
Оксид
Гидроксид
Негашёная
известь
СаО
Гашёная известь,
известковая вода,
известковое молоко
Са(ОН)2
Соли
Сульфат кальция
СаSО4 – гипс,
алебастр
Карбонат кальция
мел, мрамор,
известняк
СаСО3
3.
Гидроксидкальция
- гашёная известь
- пушонка
-известковое
молоко
4.
Оксид кальция – СаО – негашёнаяизвесть. Получают его в
промышленности путём обжига
известняка:
СаСO3 → СаО + СО2↑
Это тугоплавкое вещество белого
цвета, основной оксид, поэтому
обладает всеми свойствами
присущими основным оксидам.
5.
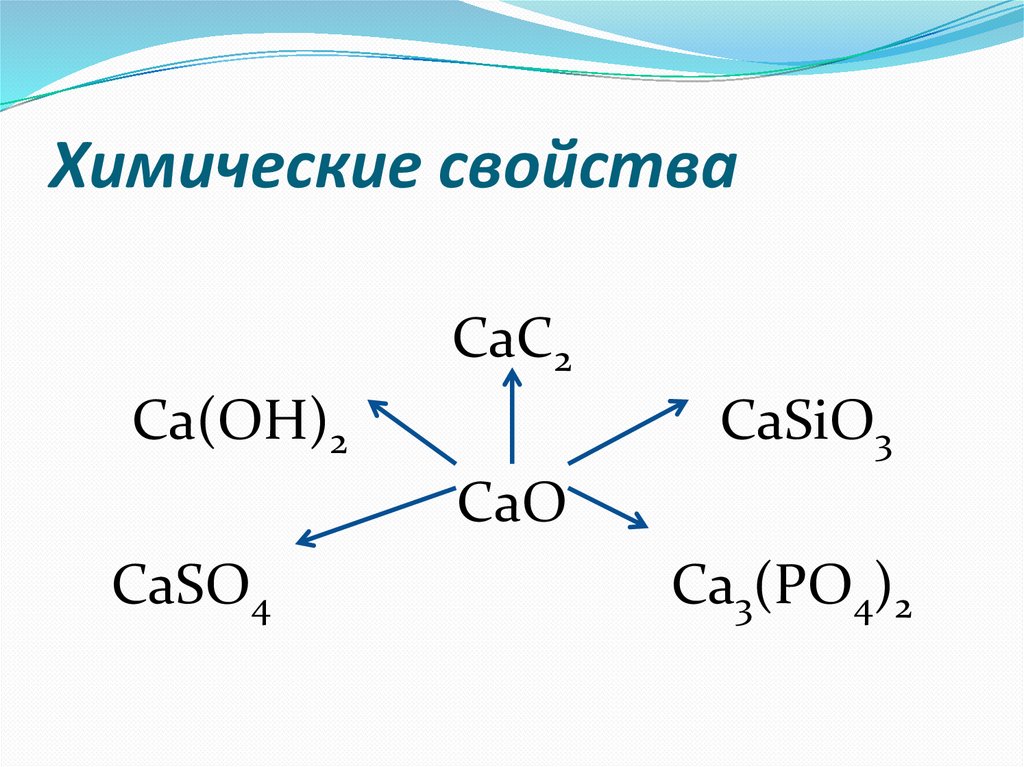
Химические свойстваСаС2
Са(ОН)2
СаSiО3
СаО
СаSО4
Са3(РО4)2
6.
Химические свойстваСаО + Н2О → Са(ОН)2
3СаО + Р2О5 → Са3(РО4)2
СаО + Н2SO4 → СаSO4 + Н2О
СаО + 3С → СаС2 + СО
СаО + SiО2 → СаSiО3
7.
8.
Са(ОН)2 – гидроксид кальция,известковая вода, гашёная известь.
Получают:
СаО + Н2О → Са(ОН)2
Диссоциирует
Са(ОН)2 → Са2+ + 2ОН-
9.
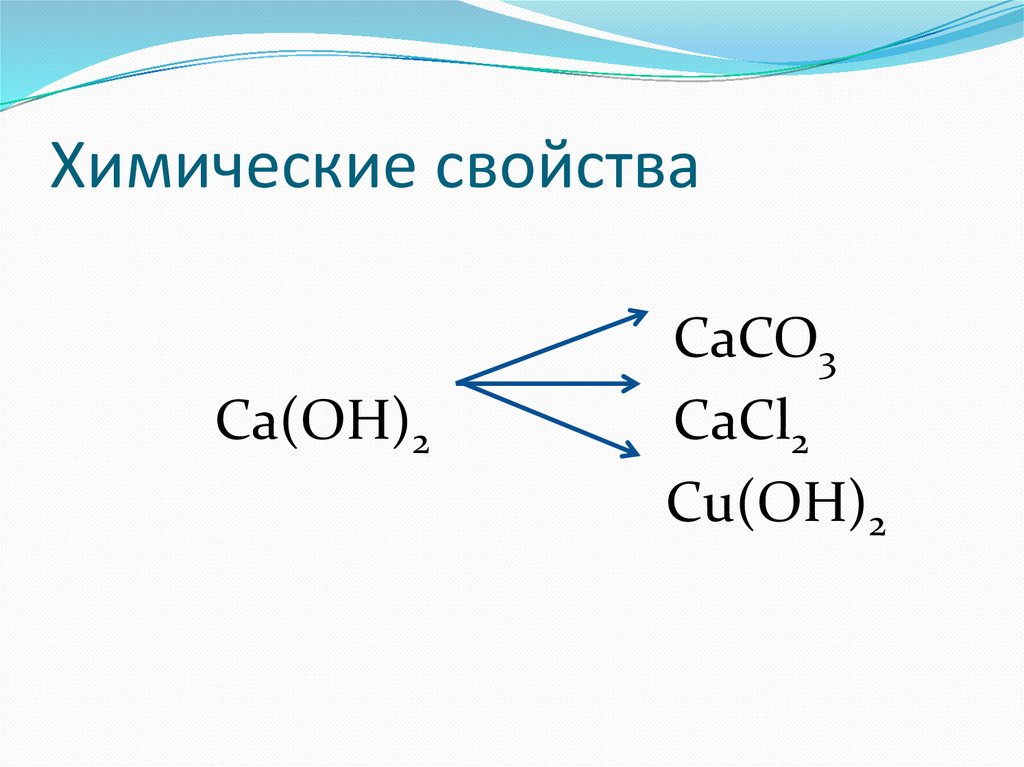
Химические свойстваСа(ОН)2
СаСО3
СаСl2
Сu(ОН)2
10.
Химические свойстваСа(ОН)2 + СО2 → СаСО3↓ + Н2О
В избытке СО2 осадок СаСО3
растворяется:
СаСО3 + СО2 + Н2О → Са(НСО3)2
Са(ОН)2 + 2НСl → СаСl2 + 2Н2О
Са(ОН)2 + СuСl2 → СаСl2 + Сu(ОН)2↓
11.
Качественная реакция на ионыСа2+:
Са(ОН)2 + СО2 → СаСО3↓ + Н2О
Наблюдается помутнение
известковой воды.
12.
Гашёная известь – тонкий рыхлый порошок,обычно серого цвета, немного растворим в воде.
Смесь гашёной извести с цементом, водой и
песком применяют в строительстве.
Известковое молоко – взвесь, похожая на молоко.
Она образуется при смешивании избытка гашёной
извести с водой. Применяют его для получения
хлорной извести, при производстве сахара и др.
Известковая вода – прозрачный раствор Са(ОН)2,
получаемый при фильтровании известкового
молока. Используют его в лаборатории для
обнаружения углекислого газа.
13.
Домашнее задание:Осуществить превращения:
I вариант
Ca→ CaO → Ca(OH)2 → CaCl2 → CaCO3
II вариант
Ca CaO Ca(OH)2 CaCO3 Ca(HCO3)2










 Химия
Химия








