Похожие презентации:
Лимфомы у детей
1.
Лимфомы у детейКозлов АВ 2022
2.
ЛимфомаЗлокачественное онкологическое заболевание клеток
иммунной системы (главным образом, лимфоцитов)
При некоторых вариантах тонкая грань между
лейкозом и лимфомой (>20% поражения КМ уже
лейкоз)
3.
Классификация лимфом (поВОЗ примерно 60 подтипов)
Лимфома Ходжкина
Неходжкинские лимфомы:
Диффузная крупноклеточная В-клеточная л-ма;
Фолликулярная л-ма;
Л-ма, поражающая ассоциированную со слизистыми оболочками лимфоткань (mucosa-associated lymphatic tissue - MALT);
Мелкоклеточная л-ма / хроническая лимфоцитарная лейкемия;
Мантийноклеточная л-ма;
Медиастинальная (тимическая) крупноклеточная В-клеточная л-ма;
Лимфопластическая л-ма и макроглобулинэмия Вальденстрема;
Узловая В-клеточная л-ма маргинальных зон;
Селезеночная л-ма маргинальных зон;
Экстранодальная В-клеточная л-ма маргинальной зоны;
Внутрисосудистая крупноклеточная В-клеточная л-ма;
Л-ма с первичным выпотом;
Л-ма Беркитта (лейкемия Беркитта);
Лимфатоидный грануломатоз.
Подтипы Т-клеточной и НК-клеточной л-м
периферическая Т-клеточная л-ма, которая ничем более не обусловлена;
кожная Т-клеточная л-ма (синдром Сезари и грибовидный микоз);
анапластическая крупноклеточная л-ма;
ангиоиммунобластическая Т-клеточная л-ма;
лимфобластная л-ма (иногда может быть B-клеточного подтипа);
л-ма с преобладанием естественных клеток-киллеров (НК-л-ма)
4.
Чаще всего только 6 видов лимфомЛимфома Ходжкина
И 5 видов НХЛ
Лимфобластная лимфома
Лимфома Беркитта (одна из самых частых НХЛ у детей,
относительно редко у взросых)
Анапластическая крупноклеточная лимфома
Диффузная крупноклеточная В-клеточная лимфома
Первичная медиастинальная В-крупноклеточная
Возможны и другие виды
5.
ЭпидемиологияНХЛ – чаще дети младшего
возраста
ЛХ – подростки
Лимфомы 3-ая по частоте
онкология у детей (те одна из
самых частых, в отличие от
взрослых)
6.
КлиникаПролиферативный синдром
Лимфаденопатия (лимфома Беркитта – брюшная
полость, Т-лимфобластная лимфома и ПМВККЛ –
средостение)
Спленомегалия.
Гепатомегалия.
Поражение различных органов и тканей (легкие,
кишечник) и др
Характерно более частое поражение ЦНС у детей с
НХЛ, чем у взрослых (почти все протоколы НХЛ
содержат профилактическое введение интратекальных
триплетов в отличие от взрослых)
Интоксикация ( В-симптомы).
7.
Клиника (отличия у детей)НХЛ почти всегда агрессивные (у взрослых часто
индолентные)
Характерно более частое поражение ЦНС у детей с
НХЛ, чем у взрослых (почти все протоколы НХЛ
содержат профилактическое введение интратекальных
триплетов в отличие от взрослых)
Клиническая картина ЛХ не отличается от таковой у
взрослых
8.
Неходжкинская лимфома споражением средостения
9.
Т-лимфобластная лимфома (в процесселечения)
10.
11.
Обследование больных сподозрением на лимфому
Обнаружение опухолевого поражения и
распостранения опухолевого процесса –
стадирование
(КТ, МРТ, ПЭТ-КТ, остеосцинтиграфия,
трепанобиопсия)
Цитологическая и гистологическая
верификация: инцизионная биопсия лимфоузла или
патологического очага, трепанобиопсия, асцитическая,
плевральная жидкость)
Световая микроскопия,
иммуногистохимия/цитофлуорометрия,
цитогенетика
Молекулярная биология (FISH, ПЦР)
Гуморальная активность (СОЭ, ЛДГ)
12.
Обследование больных с подозрением налимфому (особенности у детей)
Цитологическая и гистологическая
верификация: возможна поставновка
диагноза по выпотным жидкостям (у
взрослых в стандарт не входит)
В остальном обследование не
отличается от взрослых
13.
Роль генетических факторов(особенно у детей)
Семейная предрасположенность (однояйцевые
близнецы чаще болеют, чем разнояйцевые) при ЛХ
Консультация генетика при наличии семейных случаев
Обследование на первичные иммунодефициты у
пациентов с редкими лимфомами, нестандартным
течением
Нередко вторичный характер лимфом (на фоне ПИД,
после химиотерапии, наследственные синдромы и тд)
14.
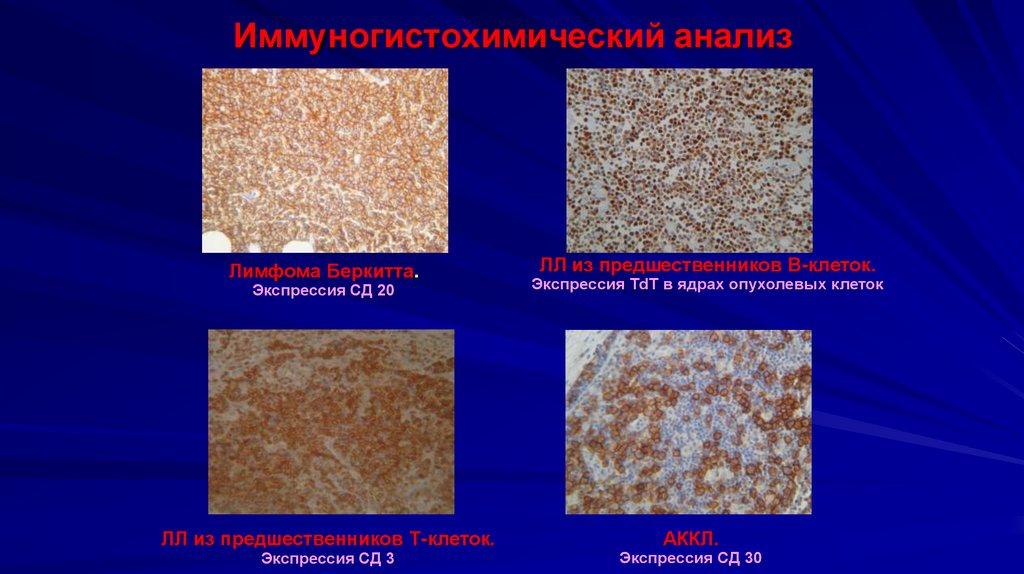
Иммуногистохимический анализЛимфома Беркитта.
Экспрессия СД 20
ЛЛ из предшественников Т-клеток.
Экспрессия СД 3
ЛЛ из предшественников В-клеток.
Экспрессия TdT в ядрах опухолевых клеток
АККЛ.
Экспрессия СД 30
15.
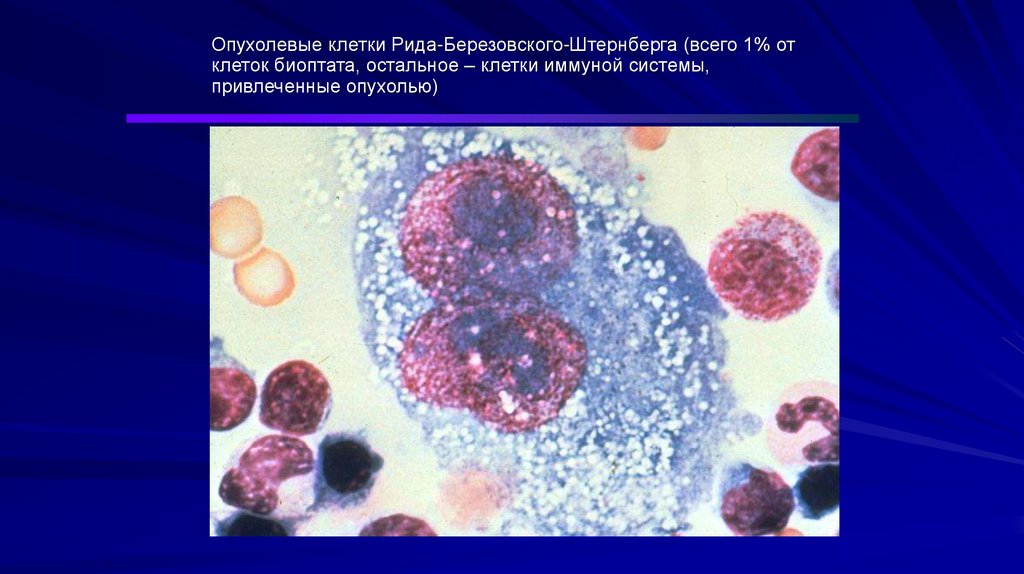
Опухолевые клетки Рида-Березовского-Штернберга (всего 1% отклеток биоптата, остальное – клетки иммуной системы,
привлеченные опухолью)
16.
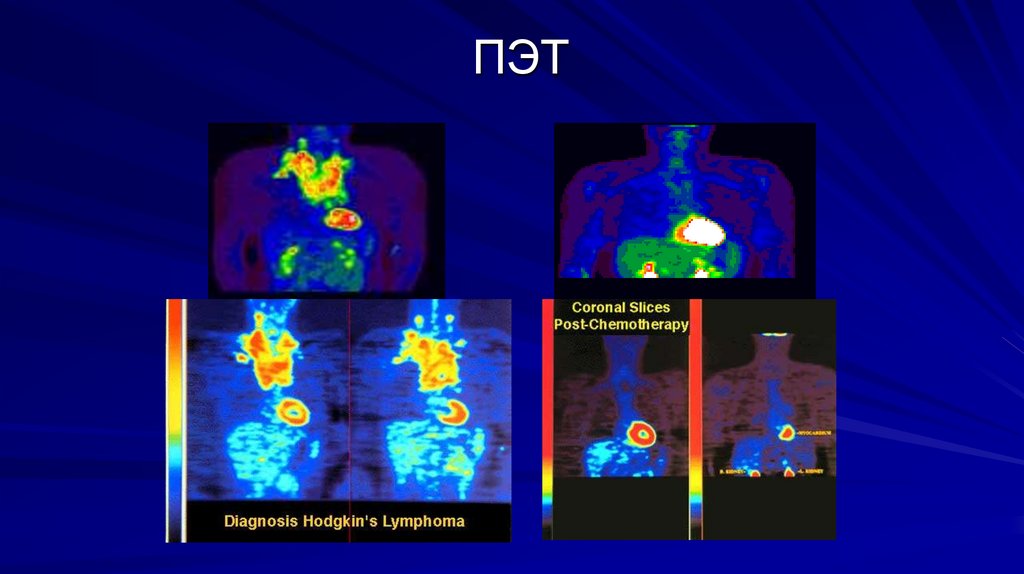
ПЭТ17.
18.
Лимфома ХоджкинаОсобенности:
Опухоль иммунной системы, из В-лимфоцитов
Характеризуется наличием клеток Рида-БерезовскогоШтернберга
Чаще медленное течение
Факторы риска: анемия, высокое СОЭ, большая
опухолевая масса, В-симптомы, продвинутая (III и IV)
стадии заболевания, лейкоцитоз, лимфопения, низкий
уровень албумина
Семейная предрасположенность (однояйцевые
близнецы чаще болеют, чем разнояйцевые)
19.
Эпидемиология и прогноз лимфомыХоджкина (ЛХ) у детей
ЛХ является относительно редким заболеванием (0,9 на 100 000
детского населения)
Одна из наиболее распространенных опухолей
Излечивается 80-90%
Еще совсем недавно возможности для терапии детей с
рецидивирующим и рефрактерным течением (Р-Р) ЛХ были
значительно ограничены
Считалось, что если в течение года от начала второй линии не
удавалось принципиально изменить течение Р-Р ЛХ, то прогноз
становился неблагоприятным
Развитие иммунотерапии улучшило шансы на излечение этих
пациентов, но ауто-ТГСК до сих пор остается очень важным
компонентом терапии[
20.
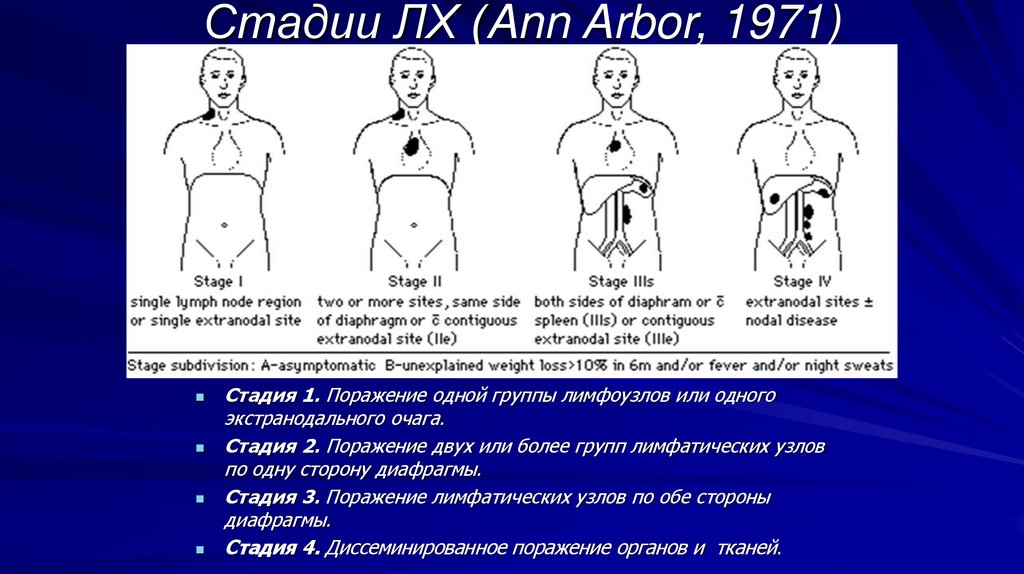
Стадии ЛХ (Ann Arbor, 1971)Стадия 1. Поражение одной группы лимфоузлов или одного
экстранодального очага.
Стадия 2. Поражение двух или более групп лимфатических узлов
по одну сторону диафрагмы.
Стадия 3. Поражение лимфатических узлов по обе стороны
диафрагмы.
Стадия 4. Диссеминированное поражение органов и тканей.
21.
Гистологические варианты лимфомыХоджкина (ЛХ)
Классическая ЛХ
Нодулярный склероз (НС), 40-60%,
нижнешейные, надключичные, лимфоузлы
средостения
Смешанноклеточный вариант (СК), 15-30%;
более запущенный вариант с экстранодальным
вовлечением.
Лимфоидное преобладание (ЛП), 5-15%,
проявляется как локальная форма
Лимфоидное истощение (ЛИ) (<5%);
распространенная форма заболевания
Не классическая
Нодулярная ЛХ с лимфоидным преобладанием
(5%)
22.
Зачем нужно знать гистологическиеварианты?
Терапия классической и неклассической ЛХ
отличается (при последней чаще применяют RCHOP- подобные схемы, в том числе у детей)
Нодулярный склероз – обычно остаточная опухоль
после окончания терапии (не должно настороживать
или пугать врача/пациента)
Смешанно-клеточный вариант (остаточная опухоль не
очень характерна)
23.
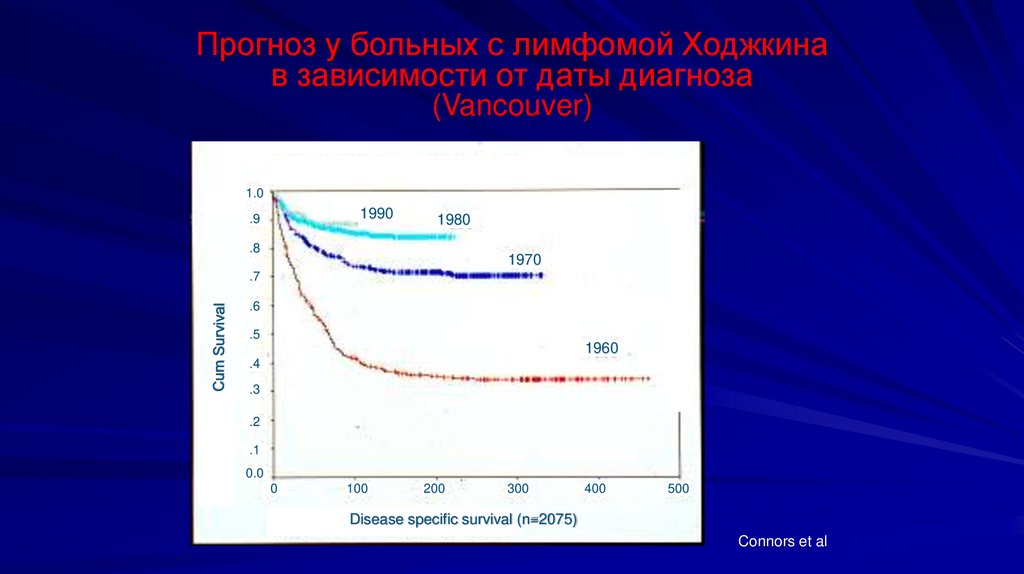
Прогноз у больных с лимфомой Ходжкинав зависимости от даты диагноза
(Vancouver)
1.0
1990
.9
1980
.8
1970
.7
.6
.5
1960
.4
.3
.2
.1
0.0
0
100
200
300
400
500
Disease specific survival (n=2075)
Connors et al
24.
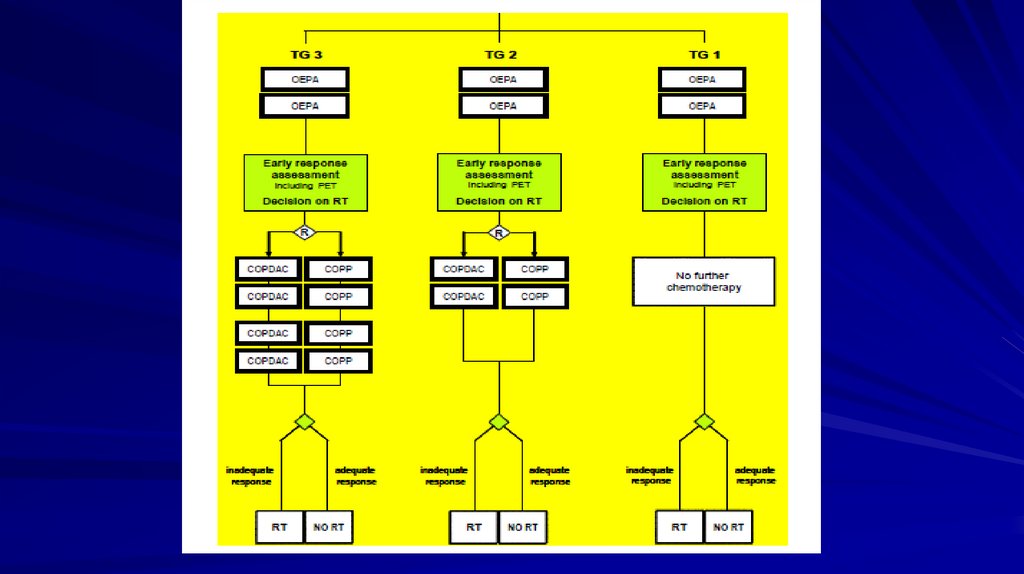
Программа лечения у детей с ЛХ (и в России)The German Society of Pediatric Oncology and
Hematology (GPOH), сейчас Euronet-HD
2 курса OEPA (винкристин, этопозид,
преднизолон, адриабластин)
2-4 курса COPDAC (циклофосфан,
винкрситин, преднизолон,
дакарбазин)
+ ЛТ 20 на вовлеченные области
Число курсов ПХТ зависит от стадии
заболевания (при I,IIA стадии-2
курса, при IIB, III-IV – 4-6 курсов).
25.
26.
США, Children's Oncology Group•-ABVE-PC (doxorubicin, bleomycin, vincristine,
etoposide, prednisone, cyclophosphamide)
-преимущества более низкие дозы, антрациклинов,
алкиляторов, блеомицина = меньше осложнений
(вторичных опухолей, сердечно-сосудистых и
легочных заболеваний, нарушений фертильности)
27.
Лучевая терапия- Children's Oncology Group (США) – ЛТ может не
проводится в группе промежуточного риска, включая
пациентов с bulky-disease, в случае адекватного
ответа после 2 курсов ПХТ.
- GPOH (Европа) – ЛТ не проводится у 30% пациентов
низкого риска при адекватном ответе после 2-х блоков
OEPA (сохраняется в группе промежуточного и
высокого риска)
- В целом, ЛТ у детей используют более низкие дозы
(15-25 Гр) и как можно меньшую площадь облучения
(лучевая терапия по методике «вовлеченных» полей)
- Исследование роли протонной терапии
28.
Эффективны ли «взрослые протоколы удетей?
- Отсутствие проспективных исследования по
сравнению «детских» и «взрослых»
протоколов у подростков и молодых
взрослых
- В крупном ретроспективном исследовании
(245 пациентов в возрасте 14-21 год) лучшая
бессобытийная выживаемость при
применении педиатрических схем
29.
Токсичность протоколов• Детские протоколы менее токсичны (специально
разработаны так, чтобы отдаленных осложнений было
меньше)
• Не снижает фертильность (GPOH-DAL)
• Без веских на то оснований будет ошибкой
использование взрослых протоколов у детей именно изза токсичности
• Нестандартно большая опухолевая масса может быть,
на мой взгляд, показанием для использования более
интенсивных схем терапии (взрослых)
30.
СТАДИИ НХЛ у детей по S. Murphy(St. Jude, 1980)
I Одно экстранодальное новообразование или поражение лимфоузлов
одной анатомической области (за исключением средостения, живота и
эпидуральной локализации).
II Одно экстранодальное новообразование с поражением регионарных
лимфоузлов.
Поражение л/у двух и более анатомических областей по одну сторону
диафрагмы.
Два одиночных экстранодальных новообразований с наличием или с
отсутствием поражения регионарных л/у на одной стороне диафрагмы.
Первичная опухоль желудочно-кишечного тракта обычно в
илеоцекальной области с наличием или отсутствием поражения только
регионарных брыжеечных л/у и при этом по большей части полностью
резецированная
III Два одиночных экстранодальных новообразования по разные
стороны диафрагмы.
Две и более области л/у выше и ниже диафрагмы
Все первичные внутригрудные опухоли (средостение, плевра, тимус).
Все распространенные первичные внутрибрюшные опухоли.
Все новообразования около позвоночника и в эпидуральной области.
IV Все поражения ЦНС и костного мозга.
31.
СТАДИИ НХЛ у детей по S. Murphy (St.Jude)
• Поражение органов брюшной полости
и грудной клетки – всегда III стадия
• IV стадия – только поражение костного
мозга и ЦНС
• Изолированное поражение костей,
кожи – I стадия
• В остальном похоже на Ann-Arbour
32.
Неходжкинскиелимфомы у детей
Злокачественная, быстро пролиферирующая
опухоль
Характеризуется агрессивным
диссеминированным течением, вовлечение
костного мозга, ЦНС, других органов (в
целом, в противоположность взрослым НХЛ)
Быстрый ответ на химиотерапию с
развитием синдрома острого лизиса
опухоли.
7% от всех детских опухолей (вместе с ЛХ –
3-ья по встречаемости детская опухоль)
Одна из самых частых онкопатологий у
подростков
33.
Эпидемиология НХЛ7% опухолей у детей
60% всех детских лимфом
Возраст 5-15; M:F - 2.5:1
Факторы риска
ТКИН, ВИЧ, ЭБВ
ТКМ с Т-деплецией
Трансплантация органов
Географические, вирусные,
генетические и иммунологические
факторы
34.
Анапластическая крупно-клеточная лимфома (1025%)Характерен генерализованный процесс в дебюте
(70-80%), составляет 10-15% всех лимфом.
B-симптомы (75%), частое экстранодальное
поражение(25%), легкие (10%), кости(17%) и
печень(8%)
ЦНС редко
Экпрессия CD 30+
ALK + (чаще у детей, лучше прогноз), ALK- (чаще
у взрослых, хуже прогноз). Морфологически не
отличимы, только наличие ALK
Часто t (2;5)
Неблагоприятные прогностические факторы:
Поражение средостения, легких, печени, селезенки,
кожи
-
35.
АККЛАнапластические крупноклеточные лимфомы (АККЛ) –
группа злокачественных опухолей лимфоидного
происхождения, которые составляют 10–15% у детей
и 2—3% у молодых взрослых от всех неходжкинских
Экспрессия киназы анапластической лимфомы (АЛК)
носит вариабельный характер и обнаруживается у
детей и взрослых с АККЛ в 55-85%
После стандартной химиотерапии первой линии у 2540% пациентов с АККЛ, экспрессирующей АЛК
(АЛК+АККЛ) развивается рецидив
36.
АККЛГистологически выделяют 2 морфологических типа – общий (common type)
(встречается в 65% случаев) и редкий (non common type),
Редкий представлен несколькими гистологическими вариантами: гистиоцитарный,
мелкоклеточный, смешанно-клеточный (в одной пораженной зоне сочетает несколько
вариантов), гигантский (напоминающий лимфому Ходжкина), саркомоподобный.
Редкие гистологические варианты АЛК+АККЛ ассоциированы с худшим прогнозом
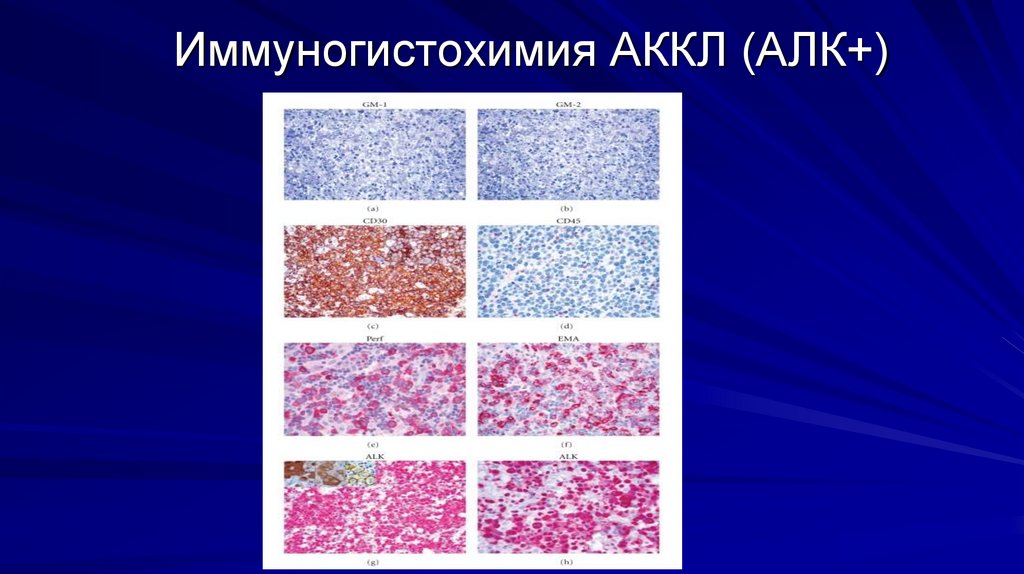
Отличительными иммуногистохимическими особенностями АККЛ является экспрессия
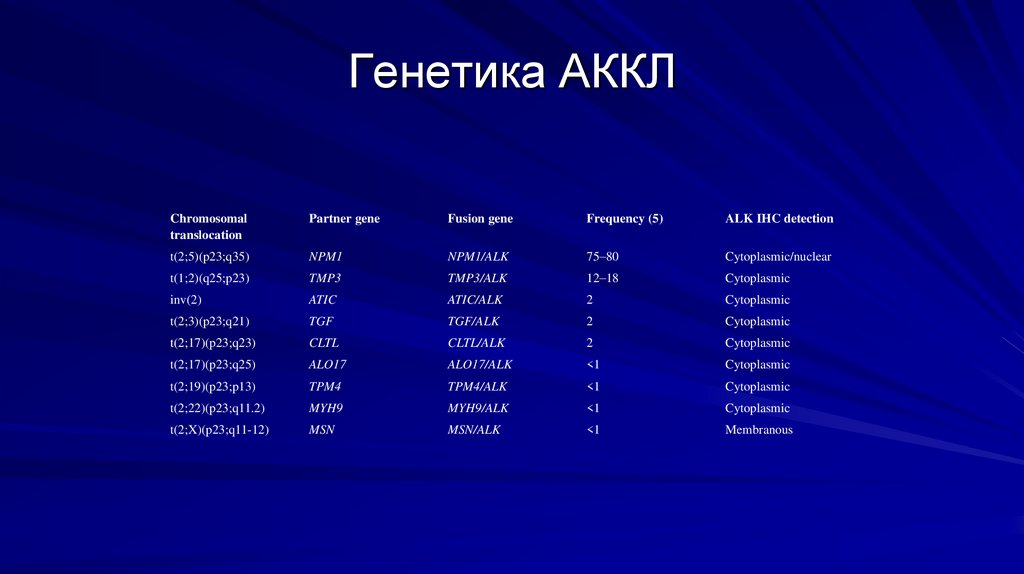
CD30, CD2, CD3, CD4, CD7, EMA. АЛК+АККЛ ассоциированы с транслокациями: t(2;5) в
75–80 % случаев и t(1;2)— в 12–18 %, а также inv(2), t(2;3), t(2;17). При t(2;5)
происходит образование химерного гена NPM1-ALK, а при t(1;2) — химерного гена
TPM3-ALK, которые способствуют активации клеточных сигнальных путей, в частности
Jak/STAT3/pSTAT3tyr705
37.
АККЛМониторинг химерного белка NPM-ALK позволяет оценивать
минимальную диссеминированную болезнь (МДБ) в крови и/или костном
мозге больных.
Общая выживаемость (ОВ) у больных без МДБ выше в 1,5 раза
Менее благоприятный прогноз отмечается при экспрессии Т-клеточного
маркера CD3, СD8, активации пути pSTAT3tyr705, активация которого
коррелирует с неблагоприятным прогнозом
38.
Иммуногистохимия АККЛ (АЛК+)39.
Патогенез АККЛ40.
Генетика АККЛChromosomal
translocation
Partner gene
Fusion gene
Frequency (5)
ALK IHC detection
t(2;5)(p23;q35)
NPM1
NPM1/ALK
75–80
Cytoplasmic/nuclear
t(1;2)(q25;p23)
TMP3
TMP3/ALK
12–18
Cytoplasmic
inv(2)
ATIC
ATIC/ALK
2
Cytoplasmic
t(2;3)(p23;q21)
TGF
TGF/ALK
2
Cytoplasmic
t(2;17)(p23;q23)
CLTL
CLTL/ALK
2
Cytoplasmic
t(2;17)(p23;q25)
ALO17
ALO17/ALK
<1
Cytoplasmic
t(2;19)(p23;p13)
TPM4
TPM4/ALK
<1
Cytoplasmic
t(2;22)(p23;q11.2)
MYH9
MYH9/ALK
<1
Cytoplasmic
t(2;X)(p23;q11-12)
MSN
MSN/ALK
<1
Membranous
41.
Периферическая Т-клеточная лимфома42.
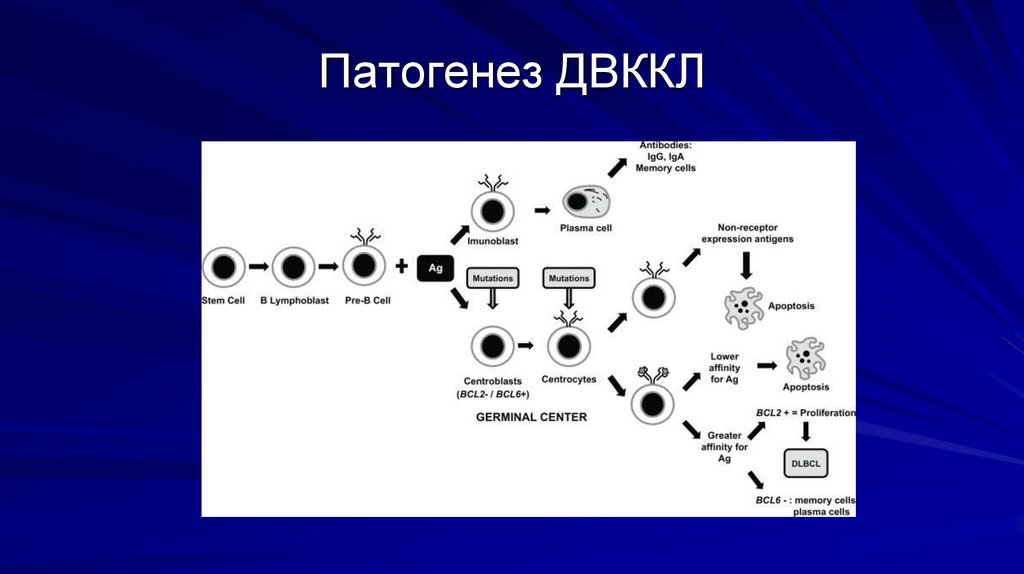
Диффузная В клеточная крупноклеточнаялимфома (DLBCL)
- Часто вовлечение средостение, легкие, ЦНС, ЖКТ
- У взрослых более благоприятный прогноз при ДBККЛ из
клеток зародышевого центра (молекулярнобиологическая классификация), у детей разницы в
прогнозе не отмечено (germinal center vs non-germinal
center).
- У детей чаще ДВККЛ из герминогенного центра
43.
Патогенез ДВККЛ44.
Лимфома БеркиттаСамая частая неходжкинская лимфома у детей
Типичная локализация – илеоцекальный угол
Типичная клиническая картина – острый живот
Роль хирургии – диагностическая (биопсия), иногда
резекция опухоли в дебюте (если резектабельна)
Лечение – химиотерапия
Прогноз благоприятная (>80% излечиваются)
Для подтверждения диагноза – c myc необходим
(стандарт)
45.
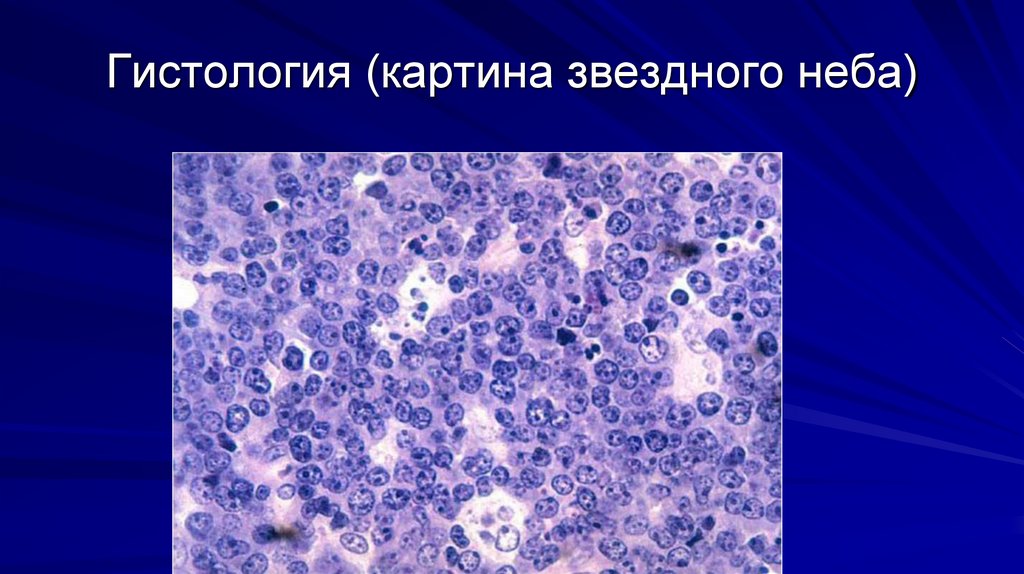
Гистология (картина звездного неба)46.
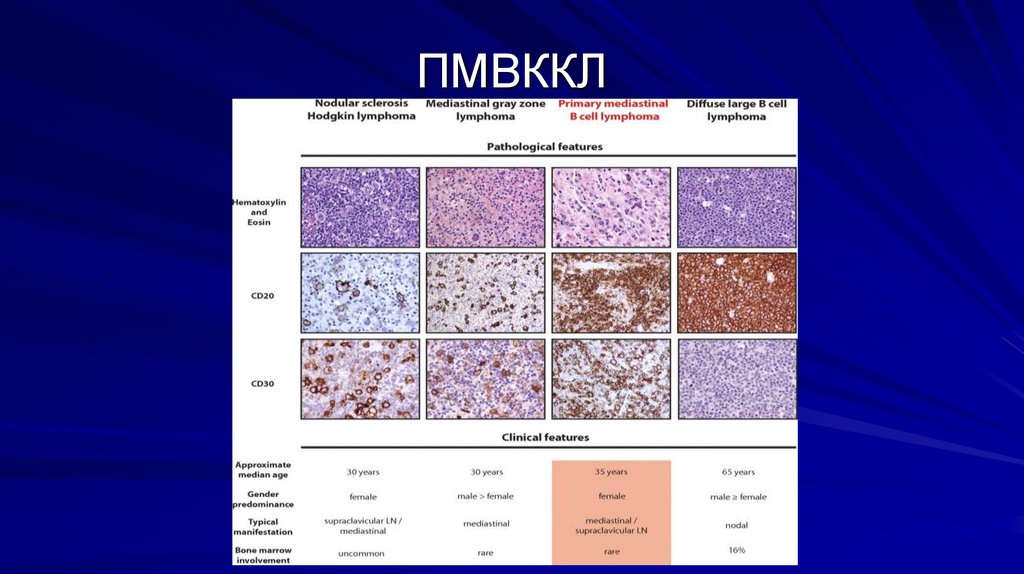
ПМВККЛ47.
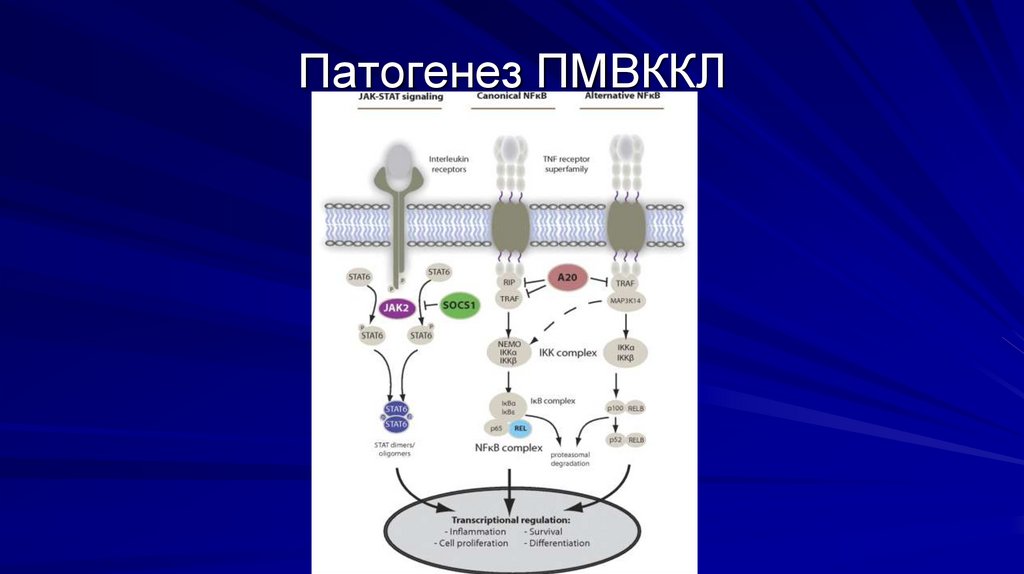
Патогенез ПМВККЛ48.
Принципы стратегии лечения НХЛ иззрелых В-клеток у детей, подростков и
молодых взрослых:
1. Адаптированность интенсивности лечения к
распространенности опухоли (стадия и активность
лактатдегидрогеназы (ЛДГ);
2. Важность сопроводительной терапии с акцентом на
профилактику и лечение инфекций, мукозита и
синдрома лизиса опухоли (СЛО)
3. Необходимость короткой «плотно упакованной»
интенсивной курсовой терапии
4. Профилактика поражения ЦНС
49.
Лечение НХЛОсновное лечение: химиотерапия, общая
выживаемость; высокий риск СОЛО
В отличие от взрослых СТАНДАРТНО
проведение интратекального введение
цитостатиков для профилактики
поражения ЦНС
Лучевая терапия (у детей в нстоящее
время редко): может быть использована
для локального контроля остаточной
опухоли
Хирургия: для проведения
диагностической биопсии
Рецидив: ПХТ, с последующей ТКМ
50.
Принципы стратегии лечения НХЛ иззрелых В-клеток у детей
Интенсивность и длительность лечения зависят от стадии, уровня ЛДГ и
полноты резекции
1. Группа риска 1 (R1): полная резекция опухоли
2. Группа риска 2 (R2): неполная резекция + стадии I + II или стадия III и LDH <
500 U/l
3. Группа риска 3 (R3): неполная резекция, стадия III и ЛДГ 500-1000 Ед/л или
стадия IV/B-ОЛЛ и ЛДГ < 1.000 U/l
4. Группа риска 4 (R4): неполная резекция, стадия III и ЛДГ≥ 1.000 или стадия
IV/B-ОЛЛ и ЛДГ ≥ 1.000 или поражение ЦНС
51.
ТЕРАПЕВТИЧЕСКИЙ ПЛАН В-NHL-BFM 200452.
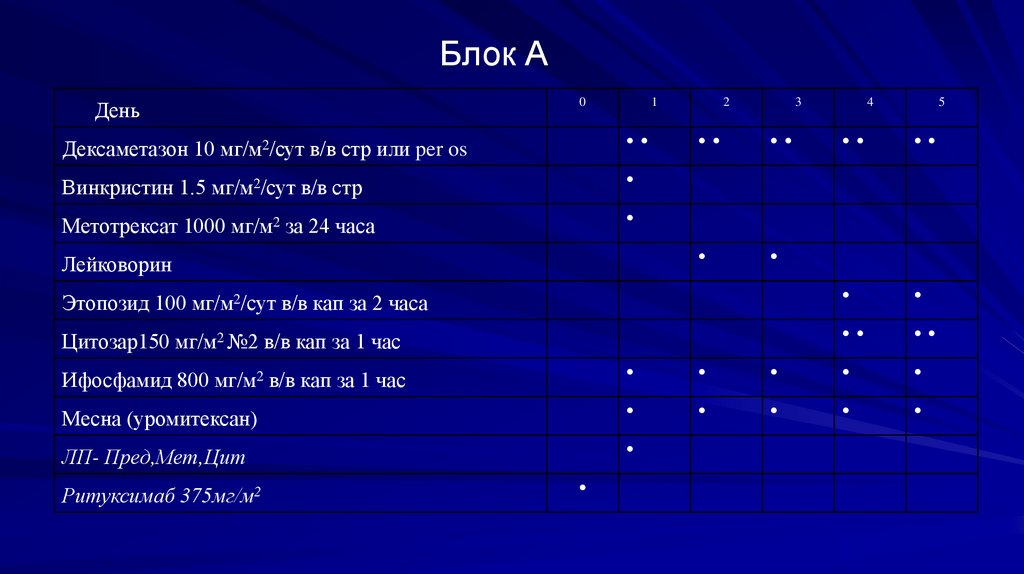
Блок АДень
0
1
Дексаметазон 10 мг/м2/сут в/в стр или per os
●
Винкристин 1.5 мг/м2/сут в/в стр
Метотрексат 1000 мг/м2 за 24 часа
2
3
●
5
●
●
Этопозид 100 мг/м2/сут в/в кап за 2 часа
Цитозар150 мг/м2 №2 в/в кап за 1 час
●
●
Лейковорин
●
4
Ифосфамид 800 мг/м2 в/в кап за 1 час
Месна (уромитексан)
ЛП- Пред,Мет,Цит
Ритуксимаб 375мг/м2
53.
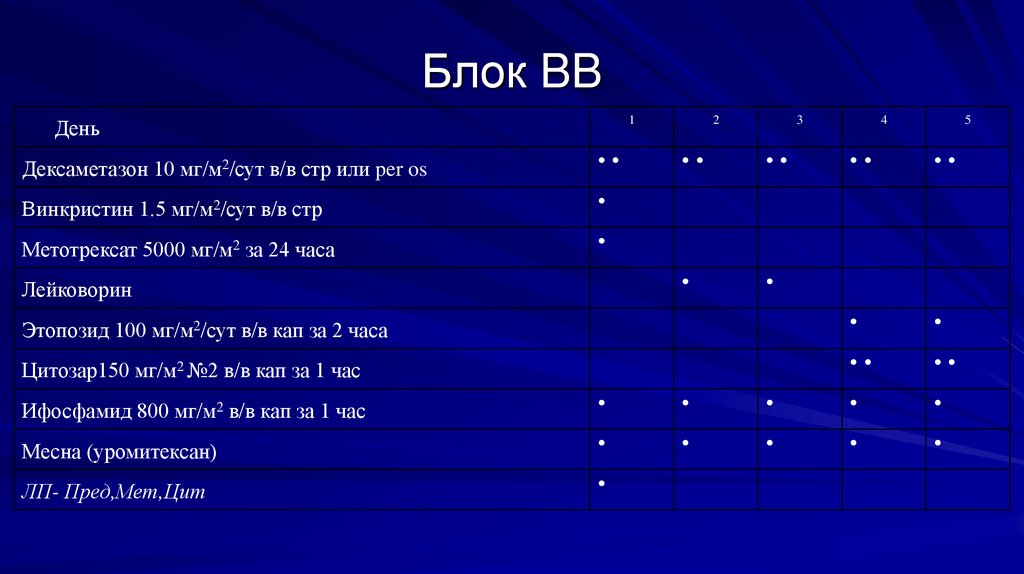
Блок BB1
День
Дексаметазон 10 мг/м2/сут в/в стр или per os
●
Винкристин 1.5 мг/м2/сут в/в стр
Метотрексат 5000 мг/м2 за 24 часа
2
3
●
5
●
●
Этопозид 100 мг/м2/сут в/в кап за 2 часа
Цитозар150 мг/м2 №2 в/в кап за 1 час
●
●
Лейковорин
●
4
Ифосфамид 800 мг/м2 в/в кап за 1 час
Месна (уромитексан)
ЛП- Пред,Мет,Цит
54.
Особенность терапии у детей с НХЛВ отличие от взрослых – более интенсивная
(высокодозная терапия) Так у пациентов высокой группы риска используется
метотрексат 5 г/м2
Всегда профилактика поражения ЦНС (в отличие от
взрослых)
Лучевая терапия (у детей в настоящее время не
используется): может быть использована для
локального контроля остаточной опухоли
55.
Таргетная и иммунотерапия в педиатрии(почти все off label)
Добавление ритуксимба к протоколу НХЛ
Снижение дозы МТХ в первых 2-х блоках
Сохранение эффективности
56.
Ритуксимаб в педиатриииспользование ритуксимаба (анти CD20) с 1998 года
наличие крупных исследований БСВ при добавлении к терапии В-клеточных НХЛ в
старшей возрастной группе
В 2016года в крупной работе показана эффективность применения ритуксимаба в
педиатрии (Veronique Minard-Colin, Anne Auperin, Marta Pillon, Amos Burke, James Robert Anderson, Donald A. Barkauskas, et al. Results of the randomized Intergroup trial Inter-B-NHL Ritux 2010
for children and adolescents with high-risk B-cell non-Hodgkin lymphoma (B-NHL) and mature acute leukemia (B-AL): Evaluation of rituximab (R) efficacy in addition to standard LMB chemotherapy (CT) regimen.
Journal of Clinical Oncology 34, no. 15_suppl (May 2016) 10507-10507)
Работа проф.Самочатовой ЕВ по добавлению ритуксимба к протоколу BFM-NHL и
снижению интенсивности первых циклов ПХТ в группе выоского риска – не привело к
снижению эффективности
(Kobos R et al, 2015).
57.
Ингибиторы иммунных контрольныхточек
Одобрен пембролизумаб у детей с ЛХ в качестве 3-ей
линии терапии
Единственный иммунный препарат на сегодня
одобренный для использования у детей
58.
Прогноз при лимфоме у детейЛимфома Беркитта, ДВККЛ – ОВ до 90%
ПМВКК – ОВ до 70%
ОЛЛ- ОВ до 90%
АККЛ - - ОВ 75%
Лимфома Ходжкина ОВ 90%
В случае Р-Р лимфомы ОВ в среднем 50%
59.
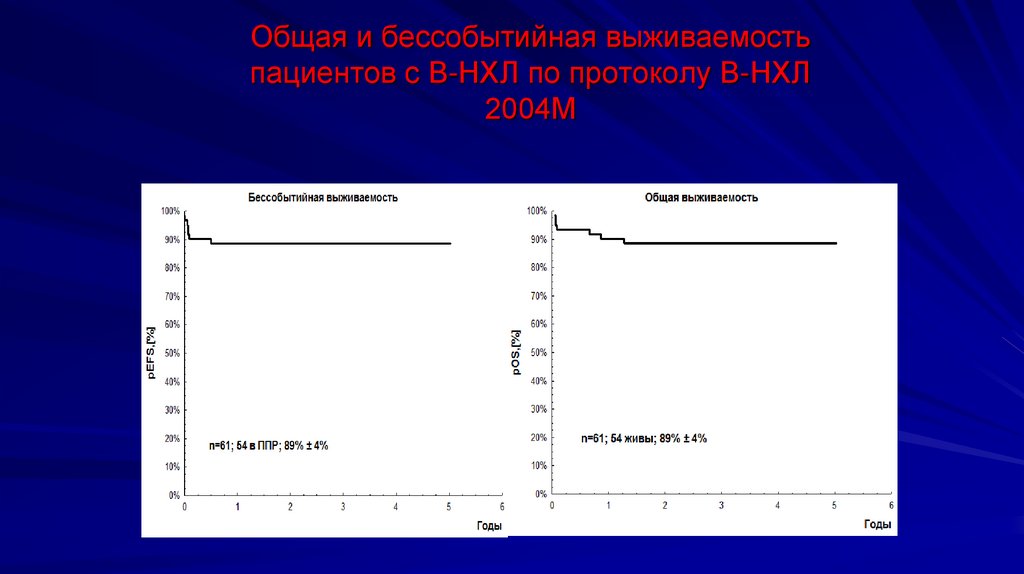
Общая и бессобытийная выживаемостьпациентов с В-НХЛ по протоколу В-НХЛ
2004М
60.
Лечение лимфобластных лимфом(протоколы близкие к острым лейкозам)
(Blood. 2000;95:416-421)
61.
Бессобытийная выживаемость детей с Тлимфобластной лимфомой(Blood. 2000;95:416-421)
62.
Прогноз при НХЛЛимфома Беркитта,
ДВККЛ – ОВ до 90%
ПМВКК – ОВ до 70%
ОЛЛ- ОВ до 90%
АККЛ - - ОВ 75%
63.
Лечение резистентных и рефрактерныхлимфом у детей
64.
РезистентностьПричины резистентности:
1. Биология опухоли
-иммунологические механизмы – избегание опухолью
иммунного надзора (контрольные точки-PDL1, PD1,
CD80-CTLA4)
- нарушение механизмов апоптоза: double hit ДBККЛ
(myc+, bcl2+)
- и др.
2. Неадекватная терапия первой линии
65.
Способы преодоления резистентности ЛПЗ1) Изменение химиотерапии (стандартные дозы)
2) Высокодозная химиотерапия (ауто-ТГСК)
3) Иммунотерапия:
-аллогенная ТГСК (1957)
-донорские лимфоциты (1990)
-CAR Т-клеточная терапия (модицификация рецепторов лимфоцитов)
-ингибиторы контрольных точек (активация резервов собственной иммунной
системы)
-брентуксимаб ведотин (иммунологической способ доставки цитостатика)
4) Таргетная терапия:
-ибрутиниб (ДBККЛ)
-кризотиниб (АККЛ)
и др.
66.
Прогноз Р-Р ЛХ у детей≥ 3-х линий терапии = неблагоприятный прогноз
Даже современная иммунотерапия не изменила
принципиально ситуацию
Ингибиторы контрольных точек (ИКТ) и брентуксимаб
ведотина (БВ) - высокая частота достижения ответа,
но низкая БСВ
Долгосрочный прогноз после алло-ТГСК лучше
67.
История алло-ТКМ при ЛХПервая алло-ТКМ - 1970
Первая у ребенка – 1980
Более чем 30-летний опыт использования алло-ТКМ у
детей с кЛХ
Последняя крупная публикация, посвященная этому
вопросу у детей, относится к 2009 году
68.
Ауто-ТГСК у детей с ЛХ«Золотой стандарт» у взрослых для консолидации ремиссии Р-Р ЛХ
Попытки лечения детей с ранним рецидивом или рефрактерным течением ЛХ
без ауто-ТГСК не эффективны
У детей с поздними рецидивами ЛХ отмечается более благоприятное течение
заболевания, и трансплантация нередко не проводится
У детей с Р-Р ЛХ важен дифференцированный, риск-адаптированный
подход к использованию ВДПХТ с ауто-ТГСК
Этот подход связан со стремлением повысить долгосрочные результаты за
счет снижения частоты отдаленных осложнений
Появление ингибиторов иммунных контрольных точек (ИКТ) и брентуксимаба
ведотина (БВ) улучшило прогноз в этой группе, но не решило проблему и
использование ауто-ТГСК остается важным методом лечения
Необходимо переосмыслить место ауто-ТГСК в детской онкологии с учетом
появления новых методов терапии
69.
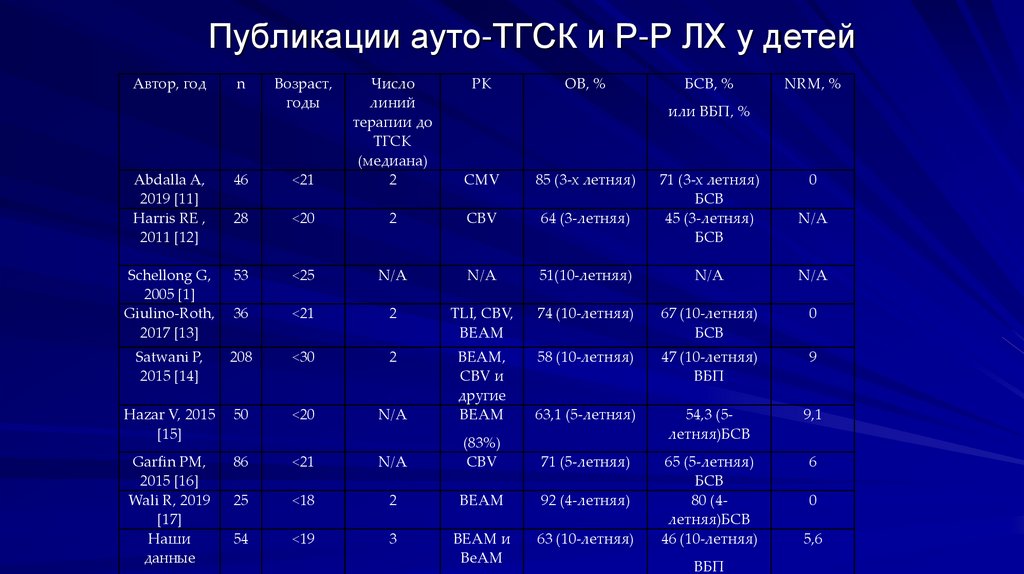
Публикации ауто-ТГСК и Р-Р ЛХ у детейАвтор, год
n
Возраст,
годы
Abdalla A,
2019 [11]
Harris RE ,
2011 [12]
46
<21
Число
линий
терапии до
ТГСК
(медиана)
2
РК
ОВ, %
БСВ, %
NRM, %
28
<20
2
CBV
64 (3-летняя)
Schellong G,
2005 [1]
Giulino-Roth,
2017 [13]
53
<25
N/A
N/A
51(10-летняя)
N/A
N/A
36
<21
2
TLI, CBV,
BEAM
74 (10-летняя)
67 (10-летняя)
БСВ
0
Satwani P,
2015 [14]
208
<30
2
58 (10-летняя)
47 (10-летняя)
ВБП
9
Hazar V, 2015
[15]
50
<20
N/A
BEAM,
CBV и
другие
BEAM
63,1 (5-летняя)
9,1
Garfin PM,
2015 [16]
Wali R, 2019
[17]
Наши
данные
86
<21
N/A
(83%)
CBV
54,3 (5летняя)БСВ
71 (5-летняя)
6
25
<18
2
BEAM
92 (4-летняя)
54
<19
3
BEAM и
BeAM
63 (10-летняя)
65 (5-летняя)
БСВ
80 (4летняя)БСВ
46 (10-летняя)
или ВБП, %
CMV
85 (3-х летняя)
71 (3-х летняя)
БСВ
45 (3-летняя)
БСВ
ВБП
0
N/A
0
5,6
70.
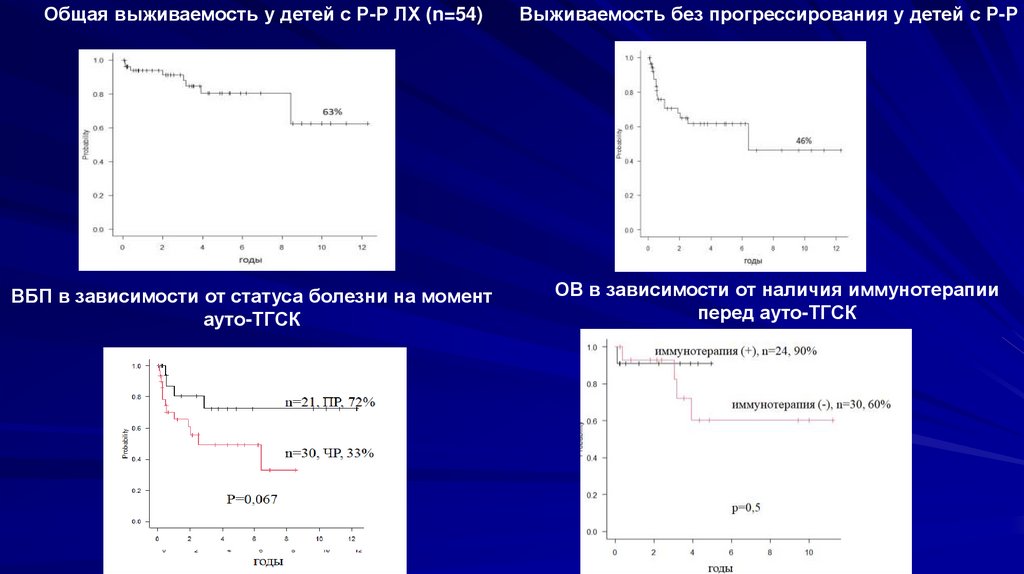
Общая выживаемость у детей с Р-Р ЛХ (n=54)Выживаемость без прогрессирования у детей с Р-Р
ВБП в зависимости от статуса болезни на момент
ауто-ТГСК
ОВ в зависимости от наличия иммунотерапии
перед ауто-ТГСК
71.
Режимы кондиционированияСамыми популярными режимами кондиционирования
при ЛХ являются BEAM и BeEAM.
Отличаются только заменой используемого в BEAM
кармустина на бендамустин (BeEAM)
Бендамустин 160 мг/м2 однократно
Дни
-8, -7
Этопозид 100 мг/м2 каждые 12 часов
Цитарабин 200 мг/м2 каждые 12 часов
Мелфалан 140 мг/м2
Инфузия ауто-ПСКК
-6,-5,-4,-3
-6,-5,-4,-3
-2
0
72.
Ауто-ТГСКДля оценки отдаленных результатов ВДПХТ с ауто-ТГСК у
пациентов с Р-Р ЛХ в качестве основной конечной точки
исследования чаще используют бессобытийную
выживаемость.
Это связано с возможным развитием таких осложнений, как
вторичные опухоли или иные проявления отсроченной
токсичности.
Критически важно отслеживать именно долгосрочную
выживаемость у детей с Р-Р ЛХ
Выживаемость может значительно отличаться от результатов,
полученных в первые годы наблюдения, за счет поздних
рецидивов заболевания и осложнений проведенной терапии
73.
Статус перед ауто-ТГСКЛучшие показатели выживаемости достигают у пациентов,
которые находились в полной ремиссии (ПР)
Важность достижения ПР перед трансплантацией с
использованием в том числе возможностей современной
иммунной терапии
Несмотря на снижение эффективности ауто-ТГСК после
каждой дополнительной линии терапии, считается, что
наличие >2 линий терапии в анамнезе следует рассматривать
не как противопоказание, а, скорее наоборот, как показание
для ауто-ТГСК, так как эти пациенты относятся к группе
высокого риска.
74.
Ингибиторы контрольных точек (ИКТ) иР-Р ЛХ
ИКТ эффективны у взрослых (общий ответ до 70%)
Продолжительность ответа ограничена во времени и
без консолидации с помощью ТГСК обычно
развиваются рецидив или прогрессия (выживаемость
без прогрессии (ВБП) <30%)
Прогноз в долгосрочной перспективе без
консолидации остается неблагоприятным
Роль у детей изучена до настоящего времени
недостаточно
75.
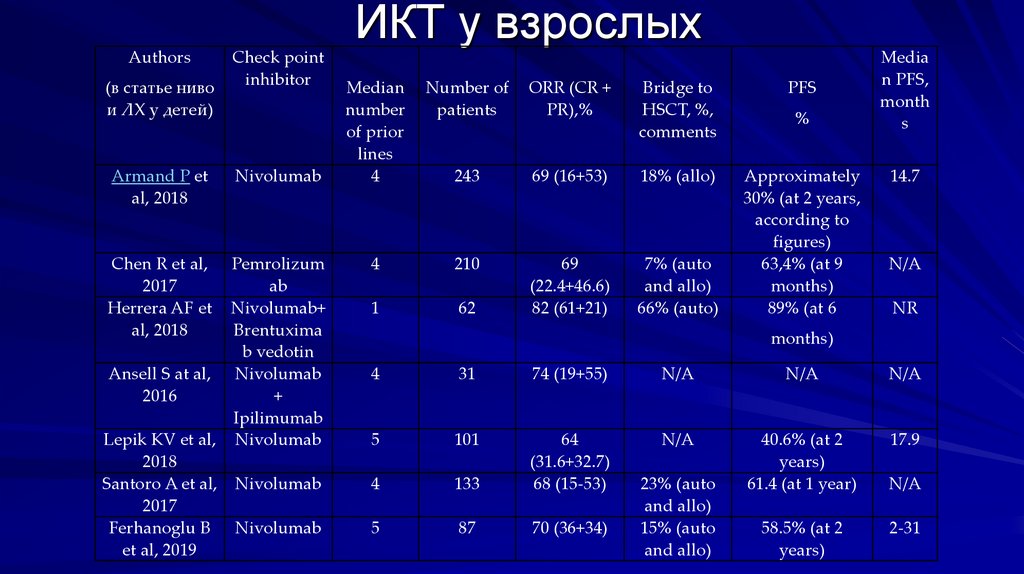
ИКТ у взрослыхAuthors
(в статье ниво
и ЛХ у детей)
Armand P et
al, 2018
Chen R et al,
2017
Herrera AF et
al, 2018
Check point
inhibitor
Nivolumab
Pemrolizum
ab
Nivolumab+
Brentuxima
b vedotin
Ansell S at al, Nivolumab
2016
+
Ipilimumab
Lepik KV et al, Nivolumab
2018
Santoro A et al, Nivolumab
2017
Ferhanoglu B Nivolumab
et al, 2019
Median
number
of prior
lines
4
Number of
patients
ORR (CR +
PR),%
Bridge to
HSCT, %,
comments
PFS
243
69 (16+53)
18% (allo)
4
210
1
62
69
(22.4+46.6)
82 (61+21)
7% (auto
and allo)
66% (auto)
Approximately
30% (at 2 years,
according to
figures)
63,4% (at 9
months)
89% (at 6
%
Media
n PFS,
month
s
14.7
N/A
NR
months)
4
31
74 (19+55)
N/A
N/A
N/A
5
101
N/A
133
40.6% (at 2
years)
61.4 (at 1 year)
17.9
4
64
(31.6+32.7)
68 (15-53)
5
87
70 (36+34)
23% (auto
and allo)
15% (auto
and allo)
58.5% (at 2
years)
N/A
2-31
76.
ИКТ у детей c ЛХ(данные литературы, многоцентровые исследования)
автор
ИКТ
Geoerger B,
2020
Пембро
Davis KL, 2020
Ниво
Количество пациентов
Общий ответ
(полный+частичный)
10
6
(1+5)
10
3 (1+2)
77.
Осложнения у детей (ниво, n=85)(данные литературы, Davis et al 2020, Lancet Oncology)
CTCAE v5 term
Избранная
токсичность
Всего пациетов No. (%)
Число
N пациентов (%)
событий
Степень
Grade 3
Grade 4
АСТ
32
22 (32)
1
0
АЛТ
25
18 (26)
1
0
Гипотиреоз
Сыпь
Диарея
Гипертиреоз
Амилазы
Плевральный
выпот
12
9
9
7
5
10 (14)
8 (12)
6 (9)
6 (9)
3 (4)
0
0
0
0
0
0
0
0
0
0
4
4 (6)
2
0
3
3 (4)
0
0
Перикардиальный
выпот
78.
Осложнения у детей после пембро (n=155)(Данные литературы, Geoerger B, 2020, Lancet Oncology,)
Анемия 9%
Лимфопения 6%
Побочные эффекты 3-5 степени – 8%
2 пациента (1%) погибли (плевральный выпот (n=1) и
отек легких (n=1)
У 4 пациентов (3%) терапии была остановлена из-за
осложнений
79.
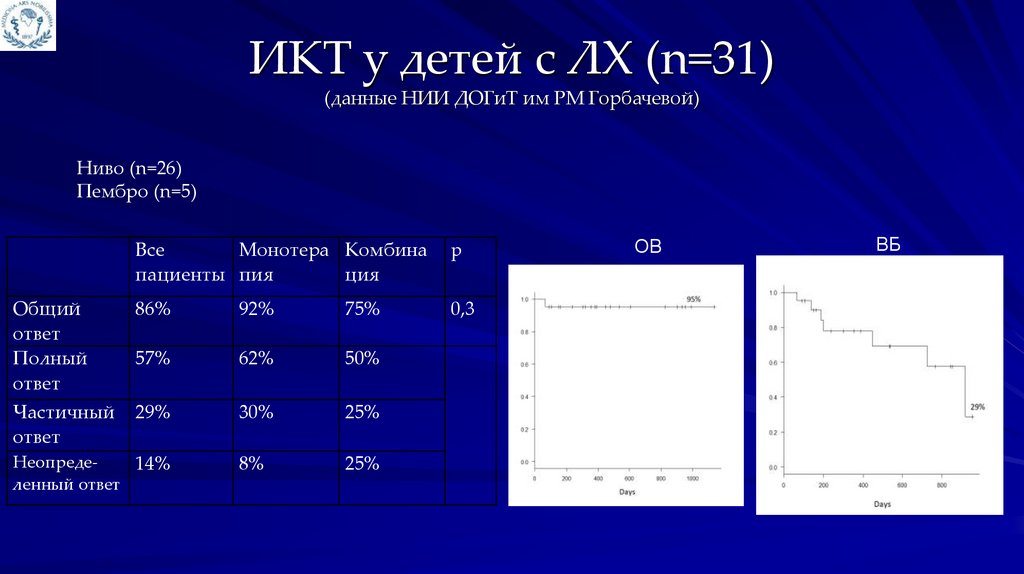
ИКТ у детей с ЛХ (n=31)(данные НИИ ДОГиТ им РМ Горбачевой)
Ниво (n=26)
Пембро (n=5)
Все
Монотера Комбина
пациенты пия
ция
p
Общий
ответ
Полный
ответ
86%
92%
75%
0,3
57%
62%
50%
Частичный
ответ
29%
30%
25%
Неопреде14%
ленный ответ
8%
25%
ОВ
ВБ
П
80.
Осложнения терапии ИКТ у детей(данные НИИ ДОГиТ им РМ Горбачевой)
Цитопения (n=2, 6%),
Сыпь(n=2, 6%)
Аутоиммуный тиреодит (n=1, 3%)
Реактивация туберкулеза (n=1, 3%)
Летальных случаев не было
81.
ИКТ и ТГСКБез консолидации с помощью трансплантации
гемопоэтических стволовых клеток (ТГСК) обычно
развивается рецидив
Вопрос о проведении аутологичной ТГСК (ауто-ТГСК)
после ИКТ изучен плохо
По данным у взрослых ауто-ТГСК после ИКТ является
эффективным и безопасным методом для
консолидации ремиссии (Advani RH, 2021).
82.
Ауто-ТГСК у взрослых послеИКТ
Advani RH, Blood. 2021
83.
ТГСК после ИКТ у детей (n=14)(НИИ ДОГиТ им РМ Горбачевой)
Из 14 пациентов, у которых
для индукции ремиссии
перед ауто-ТГСК
использовали ИКТ, живы 13
человек при медиане
наблюдения 431 день (57–
1944). При этом у 10
сохраняется ПР
84.
Брентуксимаб ведотинVaklavas c, forero-torres a. safety and efficacy of brentuximab vedotin in patients with hodgkin lymphoma OR systemic anaplastic large cell lymphoma. ther adv dermatol 2012; 3 209-225.. Search instead for Vaklavas C, Forero-Torres A. Safety and efficacy of
brentuximab vedotin in patients with Hodgkin lymphoma or systemic anaplastic large cell lymphoma. Ther Adv Hematol 2012; 3: 209-225.
85.
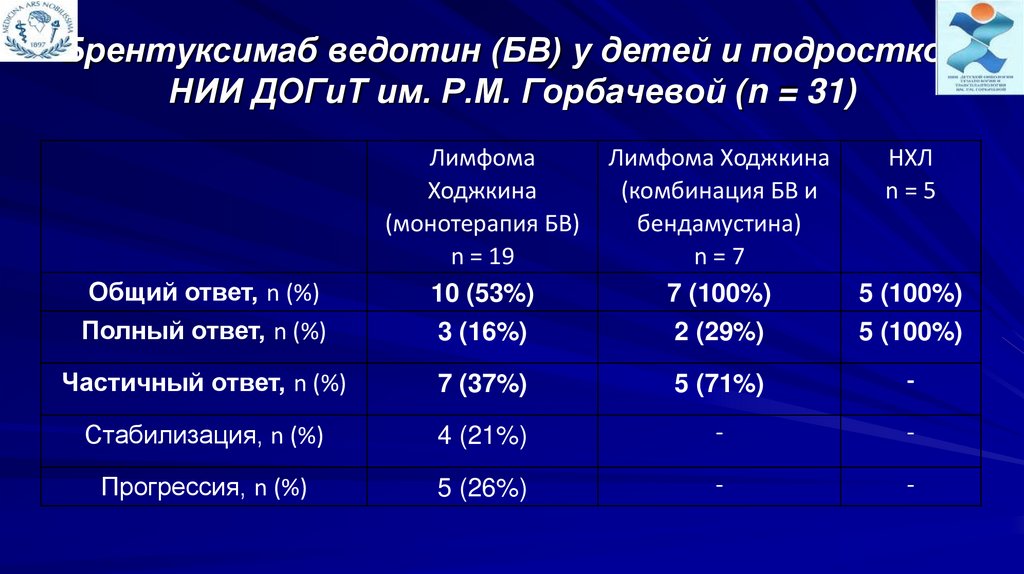
Брентуксимаб ведотин (БВ) у детей и подростковНИИ ДОГиТ им. Р.М. Горбачевой (n = 31)
Общий ответ, n (%)
Полный ответ, n (%)
Лимфома
Ходжкина
(монотерапия БВ)
n = 19
10 (53%)
3 (16%)
Лимфома Ходжкина
(комбинация БВ и
бендамустина)
n=7
7 (100%)
2 (29%)
НХЛ
n=5
5 (100%)
5 (100%)
Частичный ответ, n (%)
7 (37%)
5 (71%)
-
Стабилизация, n (%)
4 (21%)
-
-
Прогрессия, n (%)
5 (26%)
-
-
86.
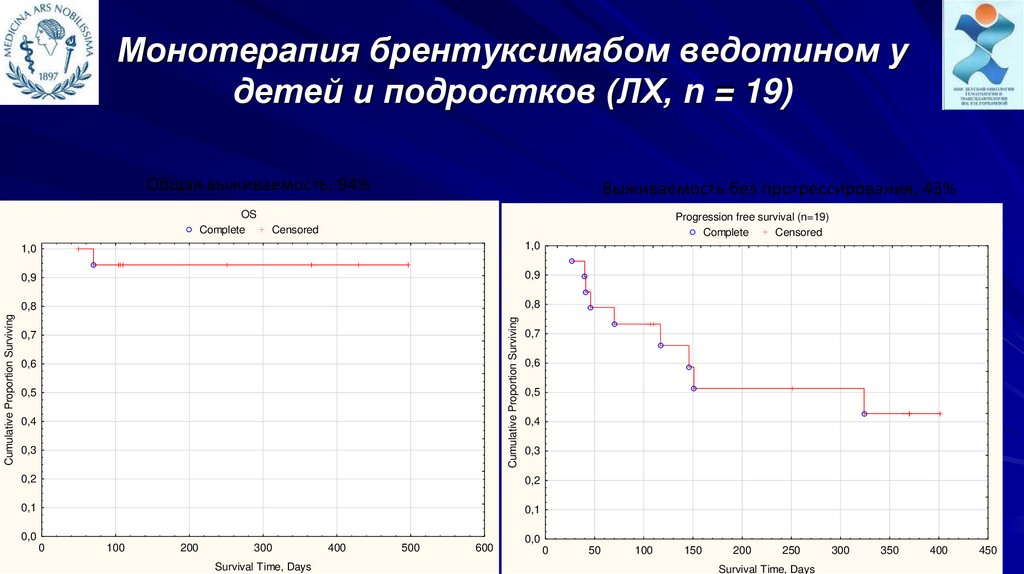
Монотерапия брентуксимабом ведотином удетей и подростков (ЛХ, n = 19)
Общая выживаемость, 94%
OS
Complete
Выживаемость без прогрессирования, 43%
Progression free survival (n=19)
Complete
Censored
Censored
1,0
1,0
0,9
0,9
Cumulative Proportion Surviving
Cumulative Proportion Surviving
0,8
94%
0,8
43%
0,7
0,6
0,5
0,4
0,3
0,7
0,6
0,5
0,4
0,3
0,2
0,2
0,1
0,1
0,0
0
100
200
300
Survival Time, Days
400
500
600
0,0
0
50
100
150
200
250
Survival Time, Days
300
350
400
450
87.
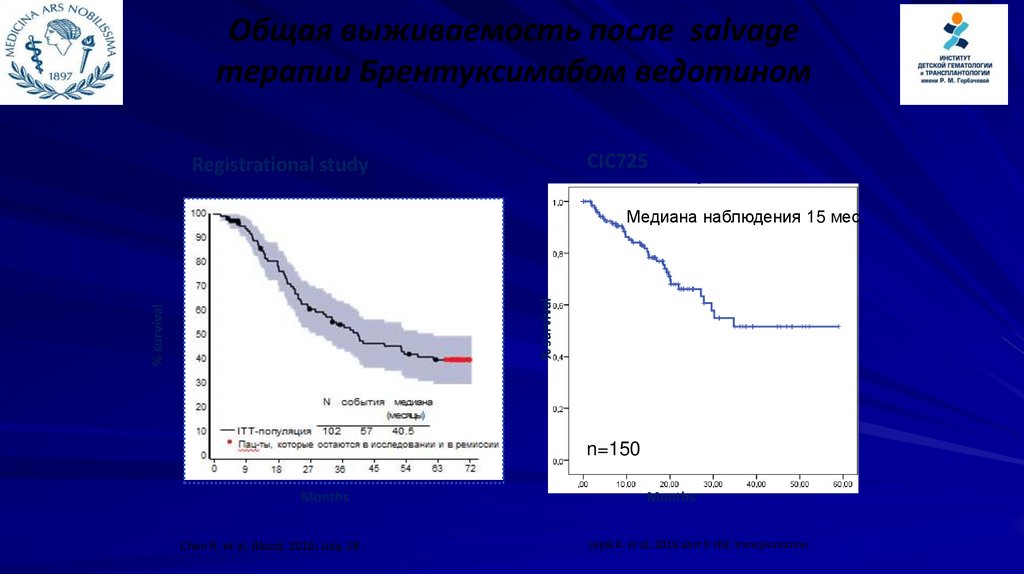
Общая выживаемость после salvageтерапии Брентуксимабом ведотином
CIC725
Registrational study
% survival
% survival
Медиана наблюдения 15 мес.
n=150
Months
Chen R. et al, Blood, 2016; July, 18
Months
Lepik K. et al, 2016 abst Х HSC transplantation
88.
Побочные эффекты БВПолинейропатия (n = 1, 3 %)
Острый панреатит (n = 1, 3 %)
Анафилактический шок (n = 1, 3 %)
Ни один пациент не погиб из-за осложнений БВ
89.
Лимфома Ходжкина и алло-ТГСК90.
Алло-ТГСК у детей с ЛХ = стандарт!?Рекомендована ASBMT (American Society of Blood and
Marrow Transplantation) при прогрессии после аутоТКМ
Рекомендована EBMT (European Society for Blood and
Marrow Transplantation) у детей с Р-Р ЛХ
Алло-ТГСК при ЛХ часто недооценивается детскими
онкологами
91.
Алло-ТГСК показана при Р-Р ЛХ у детейАлло-ТГСК рекомендована Американским обществом по
трансплантации периферических гемопоэтических стволовых
клеток крови и костного мозга (American Society of Blood and
Marrow Transplantation) у пациентов, страдающих
классической лимфомой Ходжкина (кЛХ), в случае рецидива
после аутологичной трансплантации гемопоэтических
стволовых клеток (ауто-ТГСК)
Европейское общество по трансплантации периферических
гемопоэтических стволовых клеток крови и костного мозга
(European Society for Blood and Marrow Transplantation,
EBMT) считает, что алло-ТГСК также может использоваться у
детей с рецидивирующим или рефрактерным течением (Р-Р)
кЛХ
Несмотря на наличие общепризнанных рекомендаций роль
алло-ТГСК при Р-Р кЛХ часто недооценивается детскими
92.
Сколько детей с ЛХ требует алло в РФ?Приблизительно 10 детей с ЛХ в год в РФ нуждаются в
алло-ТГСК
93.
Место алло-ТГСК удетей в «эру иммунотерапии»
Требуется переосмысление роли алло-ТГСК у детей с
учетом активного использования эффективных
методов иммунотерапии
94.
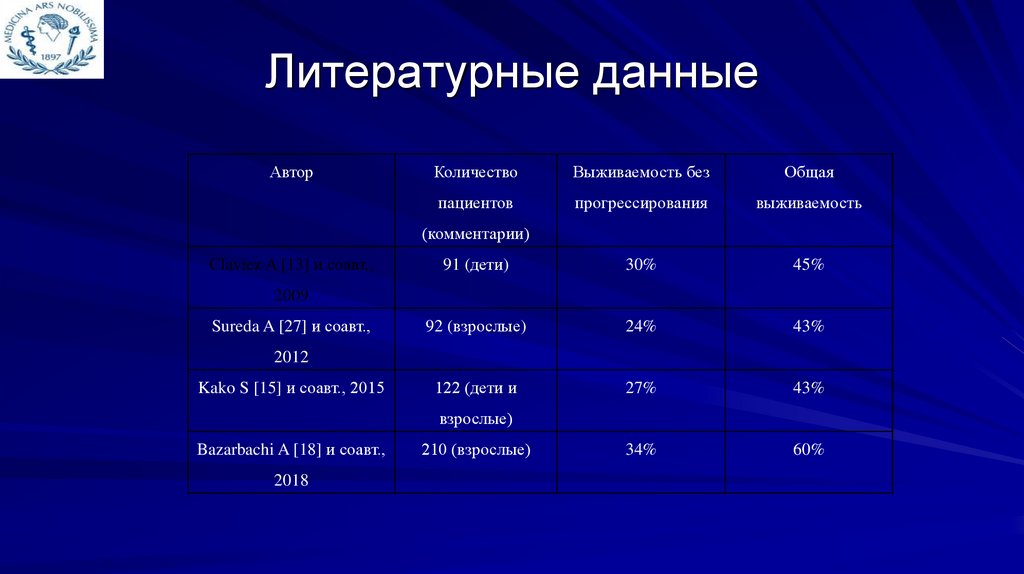
Литературные данныеАвтор
Количество
Выживаемость без
Общая
пациентов
прогрессирования
выживаемость
91 (дети)
30%
45%
92 (взрослые)
24%
43%
122 (дети и
27%
43%
34%
60%
(комментарии)
Claviez A [13] и соавт.,
2009
Sureda A [27] и соавт.,
2012
Kako S [15] и соавт., 2015
взрослые)
Bazarbachi A [18] и соавт.,
2018
210 (взрослые)
95.
Алло-ТКМ у детей с ЛХВ НИИ ДОГиТ им. Р.М. Горбачевой с 2003 по 2019
годы алло-ТГСК была проведена 14 пациентам
детского возраста с Р-Р ЛХ
96.
Характеристика пациентовМедиана возраста - 17 (14-18)
Ранние стадии - 2 (14%), продвинутые - у 12 (86%)
Большая опухолевая масса - 7 (50%) и экстранодальные очаги
поражения - в11 (79%)
Нодулярный склероз (n=10, 71%)
Статус Карновского 90-100% (n=13, 93%)
Медиана времени от диагноза до алло-ТГСК была 2,5 года (1,8-5)
Медиана времени между ауто-ТГСК и алло-ТГСК - 1,5 года (0,9-2,5).
Медиана предшествующих линий терапии составляла 5 (1-6)
и ауто-ТГСК в анамнезе была в 6 случаях (43%)
97.
Характеристика пациентовРецидивирующее течение (n=7, 50%), рефрактерное
(n=6, 43%), а также у 1 (7%) ЛХ+ПИД
Ремиссия перед алло-ТГСК – (n=10, 71%) случаев
Иммунотерапия (n=10, 71%): Брентуксимаб ведотин
(n=6) или комбинации БВ с ниволумабом (n=4)
98.
Донор и режим кондиционированияПолностью HLA-совместимый донор - у 12 (86%) и
гаплоидентичный донор - у 2 (14%).
Режим кондиционирования: флударабин 90 мг/м2+
бендамустин 390 мг/м2 (n=10, 71%),
Немиелоаблативный режим кондиционирования
(n=13, 93%)
99.
Профилактика РТПХПосттрансплантационный циклофосфан (n=12,
86%)
Антитимоцитарный глобулин (n=1, 7%)
Комбинации с такролимусом (n=11, 79%), селл-септом
(n=4, 29%), сиролимусом (n=4, 29%) и ритуксимабом
(n=1, 7%).
100.
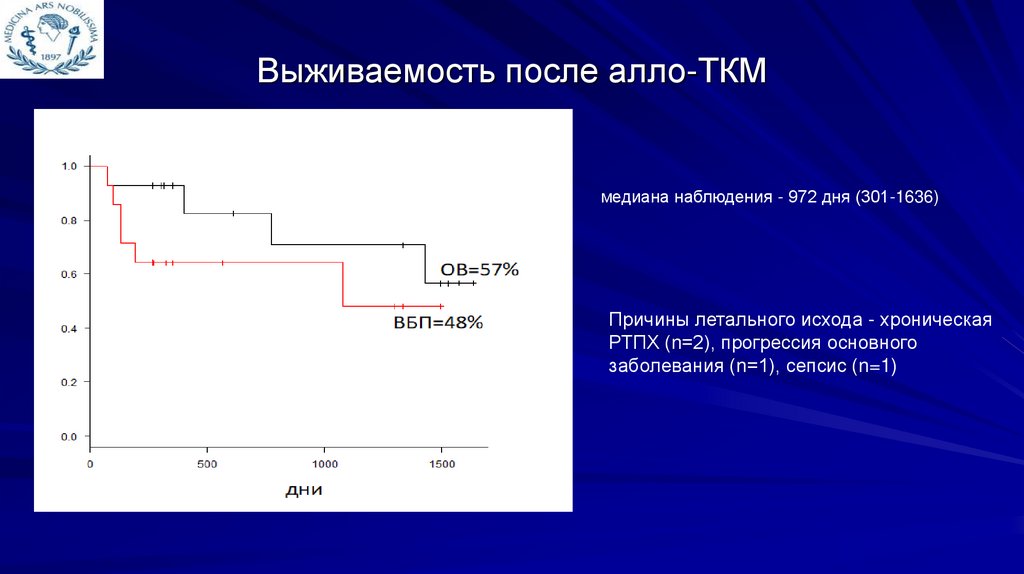
Выживаемость после алло-ТКМмедиана наблюдения - 972 дня (301-1636)
Причины летального исхода - хроническая
РТПХ (n=2), прогрессия основного
заболевания (n=1), сепсис (n=1)
101.
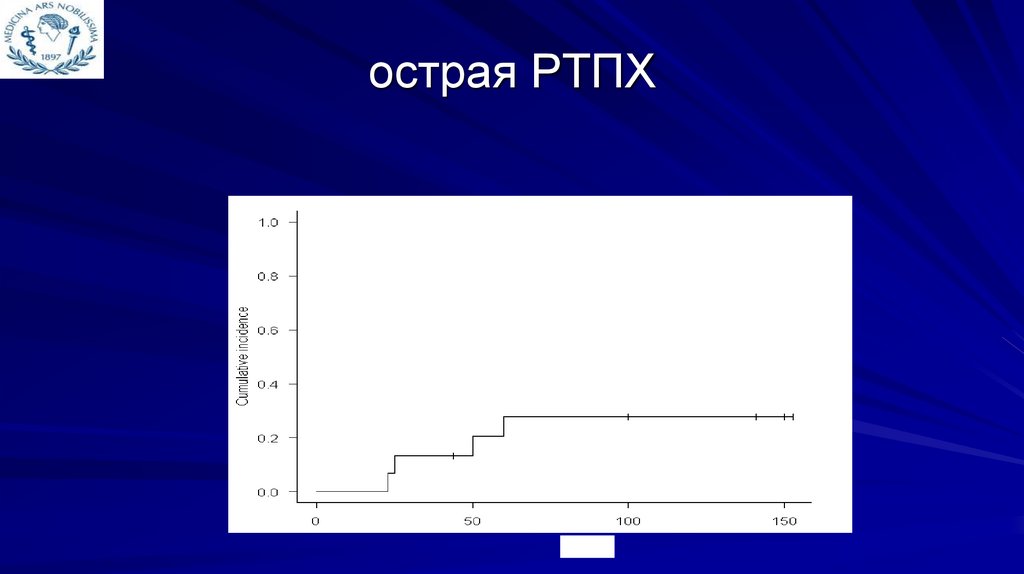
TRM и рецидивы102.
РТПХОстрая РТПХ (I стадия)
наблюдалась только у 1-го
пациента (7%).
Стероид-резистентная
форма хРТПХ развилась в
4-х случаях (80%)
103.
Неприживление транплантатаПервичное неприживление трансплантата (n=2, 14%)
Смешанный химеризм (n=1, 7%)
Требуется модификация режима кондиционирования?
104.
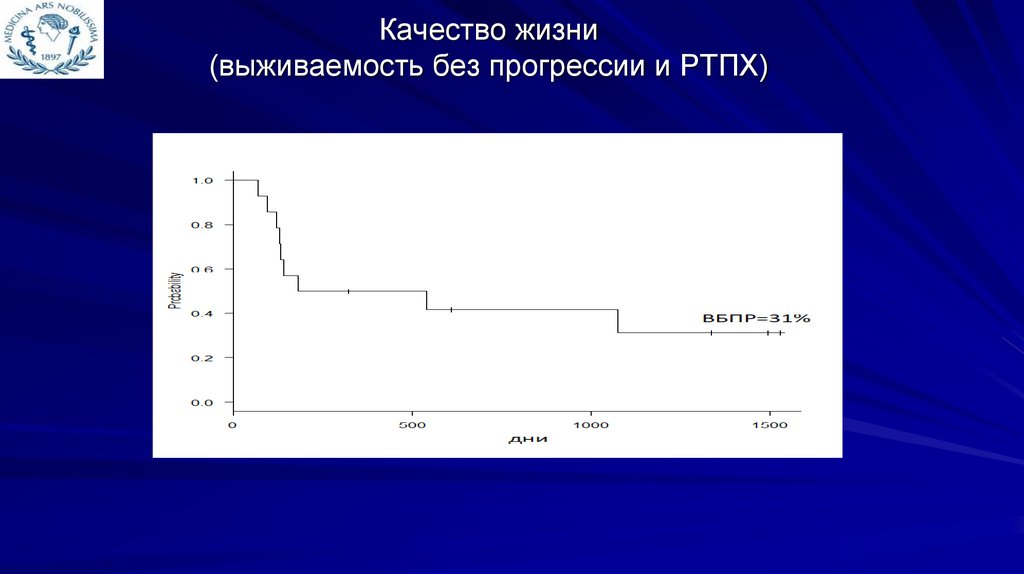
Качество жизни(выживаемость без прогрессии и РТПХ)
105.
Лимфобластная лимфома (ЛЛ)Вторая по частоте среди НХЛ у детей
Т-клеточный вариант – до 90%
Частый переход в ОЛЛ
Редкое использование молекулярно-биологических
маркеров в клинической практике(в отличие от ОЛЛ)
106.
ЛЛ и ТКМ10% рецидив или первично рефрактерное течение
заболевания (Р-Р)
Лечение Р-Р ЛЛ остаётся не решённой проблемой
при достижении ремиссии Р-Р ЛЛ показано
проведение алло-ТГСК
ауто-ТГСК - возможная опция
107.
ЛЛ и ТКМВыбор в пользу алло-ТГСК преимущественно
основывается на опыте терапии взрослых пациентов
Аналогичные результаты по данным CIBMTR
получены и в педиатрической практике
Количество публикаций посвященных данной
проблеме в целом не велико
Вопрос требует дальнейшего изучения
•Levine JE, Harris RE, Loberiza FR Jr, Armitage JO, Vose JM, Van Besien K et al. A comparison of allogeneic and autologous bone marrow transplantation for lymphoblastic lymphoma. Blood 2003 Apr;101(7):2476-2482.
108.
Эффективность терапии Р-Р ЛЛ(литературные данные)
Автор
Число
пациентов
Вариант НХЛ
Дети/
взрослые
Терапия
TRM, %
ОВ,%
БСВ,%
Bureo E, 1995
46
ЛЛ (21)+другие НХЛ
дети
ауто и алло
13
N/A
58
Levine JE, 2002
204
ЛЛ
дети и
взрослые
ауто и алло
ауто-3,
алло-18
ауто-44,
алло-39
ауто-39,
алло-36
Burkhardt B, 2009
34
ЛЛ
дети
ХТ, ауто,
алло
N/A
все- 14,
алло-44
N/A
Gross TG, 2010
53
ЛЛ
дети
ауто и алло
ауто-24,
алло-25
N/A
ауто-4,
алло-40
Michaux K, 2016
23
ЛЛ
дети
ХТ, ауто и
алло
N/A
8,7
8,7
Naik S, 2019
36
ЛЛ (9)+другие НХЛ
дети
алло
6
67
68
Burkhardt B, 2021
89
ЛЛ
дети
алло
44
109.
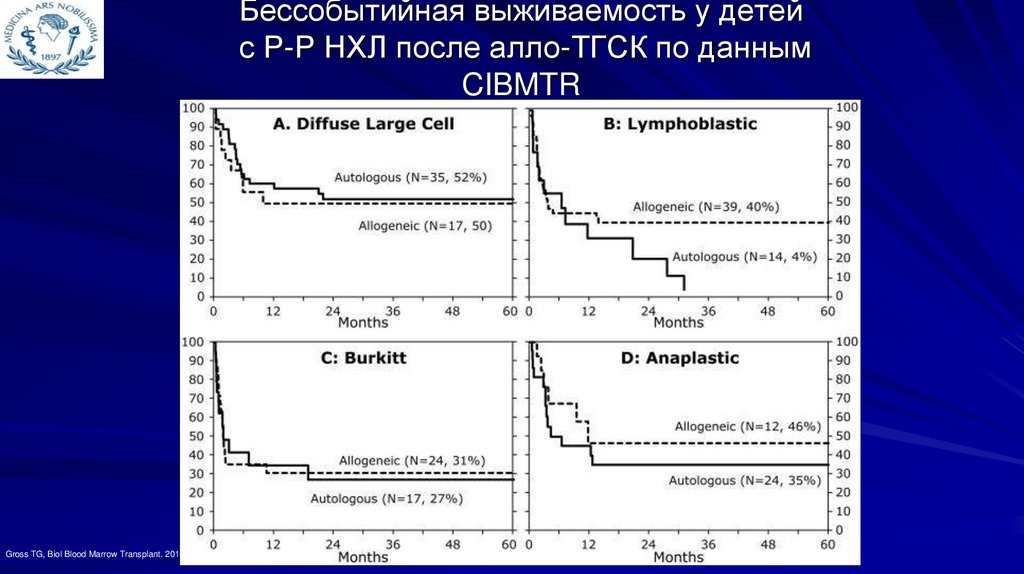
Бессобытийная выживаемость у детейс Р-Р НХЛ после алло-ТГСК по данным
CIBMTR
Gross TG, Biol Blood Marrow Transplant. 2010 Feb;16(2):223-30
110.
ЛЛ и ТКМ у детейОграниченность данных объясняется малым числом
пациентов
Группа BFM: 34 ребенка за 13 лет
Прогноз - крайне неблагоприятный
111.
Рандомизированные исследования?Требуются другие способы доказательной медицины
в области алло-ТГСК
Достижение высоких показателей выживаемости в
рамках нерандомизированных исследований может
быть достаточным аргументом в пользу ТКМ
112.
ОЛЛ и ЛЛ (одинаков ли прогноз после аллоТГСК?)Возможен ли простой перенос опыта применения
алло-ТГСК при ОЛЛ на ЛЛ?
Долгосрочная выживаемость после алло-ТГСК при
ОЛЛ 40 -70% в зависимости от различных
прогностических факторов
Объективные сомнения в возможности такого
механического подхода (разная молекулярная
биология, клиническая картина)
113.
Совершенствование терапии Р-Р ЛЛОптимизация использования алло-ТГСК
Углублением молекулярно-биологического понимания
опухоли
Внедрением эффективных методов таргетной и
иммунотерапии
114.
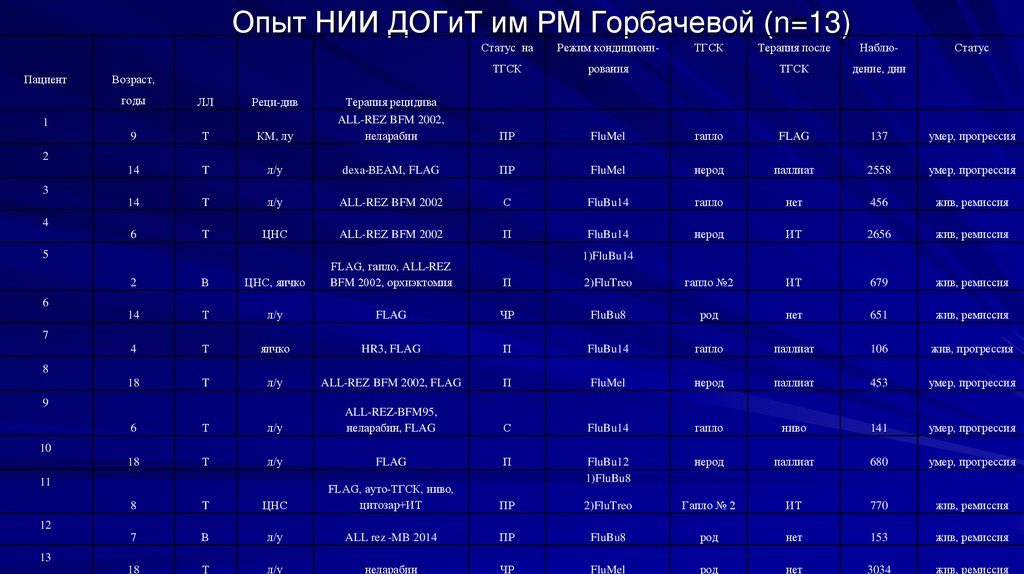
Опыт НИИ ДОГиТ им РМ Горбачевой (n=13)Пациент
Возраст,
Статус на
Режим кондициони-
ТГСК
рования
ПР
FluMel
ТГСК
Терапия после
Наблю-
Статус
ТГСК
дение, дни
гапло
FLAG
137
умер, прогрессия
годы
ЛЛ
Реци-див
9
Т
КМ, лу
Терапия рецидива
ALL-REZ BFM 2002,
неларабин
14
T
л/у
dexa-ВЕАМ, FLAG
ПР
FluMel
нерод
паллиат
2558
умер, прогрессия
14
T
л/у
ALL-REZ BFM 2002
С
FluBu14
гапло
нет
456
жив, ремиссия
6
T
ЦНС
ALL-REZ BFM 2002
П
FluBu14
нерод
ИТ
2656
жив, ремиссия
П
2)FluTreo
гапло №2
ИТ
679
жив, ремиссия
1
2
3
4
5
1)FluBu14
2
В
ЦНС, яичко
FLAG, гапло, ALL-REZ
BFM 2002, орхиэктомия
14
Т
л/у
FLAG
ЧР
FluBu8
род
нет
651
жив, ремиссия
4
Т
яичко
HR3, FLAG
П
FluBu14
гапло
паллиат
106
жив, прогрессия
18
T
л/у
ALL-REZ BFM 2002, FLAG
П
FluMel
нерод
паллиат
453
умер, прогрессия
С
FluBu14
гапло
ниво
141
умер, прогрессия
6
7
8
9
6
Т
л/у
ALL-REZ-BFM95,
неларабин, FLAG
18
Т
л/у
FLAG
П
FluBu12
1)FluBu8
нерод
паллиат
680
умер, прогрессия
ПР
2)FluTreo
Гапло № 2
ИТ
770
жив, ремиссия
10
11
8
T
ЦНС
FLAG, ауто-ТГСК, ниво,
цитозар+ИТ
7
В
л/у
ALL rez -МВ 2014
ПР
FluBu8
род
нет
153
жив, ремиссия
18
Т
л/у
неларабин
ЧР
FluMel
род
нет
3034
жив, ремиссия
12
13
115.
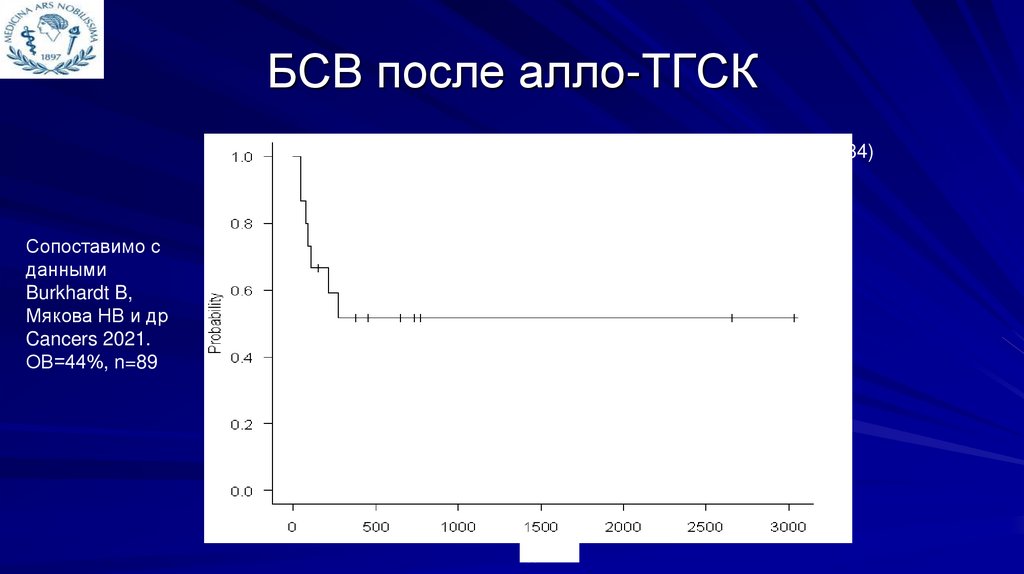
БСВ после алло-ТГСКмедиане наблюдения 651 день (106-3034)
Сопоставимо с
данными
Burkhardt B,
Мякова НВ и др
Cancers 2021.
ОВ=44%, n=89
52%
дни
116.
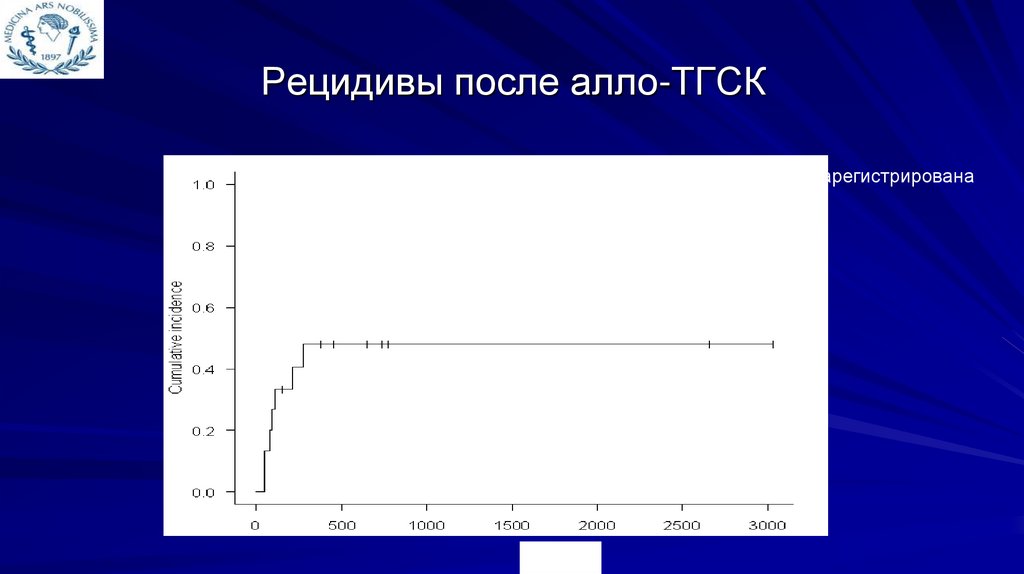
Рецидивы после алло-ТГСКTRM не зарегистрирована
48%
дни
117.
острая РТПХ28%
дни
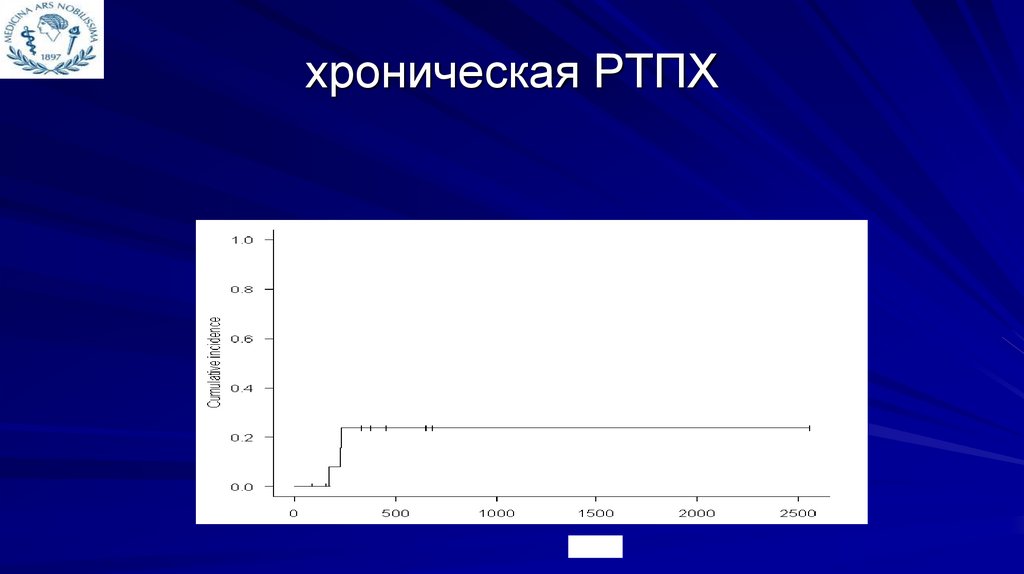
118.
хроническая РТПХ24%
дни
119.
Можно ли трансплантировать вне ремиссии?В целом проведение трансплантации в
стабилизации или прогрессии ЛЛ не показано.
Общепризнанной и рекомендованной тактикой в таких
ситуациях должно быть проведение паллиативной
терапии.
На Западе нет значительного опыта ТКМ вне
ремиссии у детей с ЛБЛ (из 76 пациентов вне
ремиссии после второй линии у 69 (91%) не
проводиласть алло-ТГСК)*.
Но…
Burkhardt B, Мякова НВ и др, Cancers 2021*
120.
Данные НИИ ДОГиТ им РМ Горбачевой7 пациентов с прогрессией или стабилизацией на
момент алло-ТГСК
у 3-х сохраняется ремиссия в течение значительного
временного интервала (1, 2 и 5 лет)
Этично ли у всех детей вне ремиссии ЛЛ
отказываться от алло-ТКМ?
121.
Паллиативная терапияУ 3-х пациентов с рецидивом или прогрессией после
алло-ТГСК удалось добиться относительно
длительной выживаемости (>1 года) на фоне
различных схем паллиативной терапии
У части пациентов позволит значимо увеличить
продолжительность жизни при сохранении качества
122.
Анапластическая крупноклеточная лимфома(АЛК+)
и ТКМ
Предпочтительнее использовать алло-ТГСК (БСВ
80%)*
Возможна ауто-ТГСК, но часто рецидивы, однако ОВ
остается высокой
У всех пациентов с АККЛ, АЛК+ (n=4) сохраняется
ремиссия после алло-ТГСК (собственные данные)
Благоприятный прогноз!
*Knörr F, Brugières L, Pillon M, Zimmermann M, Ruf S, Attarbaschi A et al; European Inter-Group for Childhood Non-Hodgkin Lymphoma. Stem Cell Transplantation and Vinblastine Monotherapy for Relapsed Pediatric Anaplastic Large Cell
Lymphoma: Results of the International, Prospective ALCL-Relapse Trial. J Clin Oncol. 2020 Dec 1;38(34):3999-4009.
123.
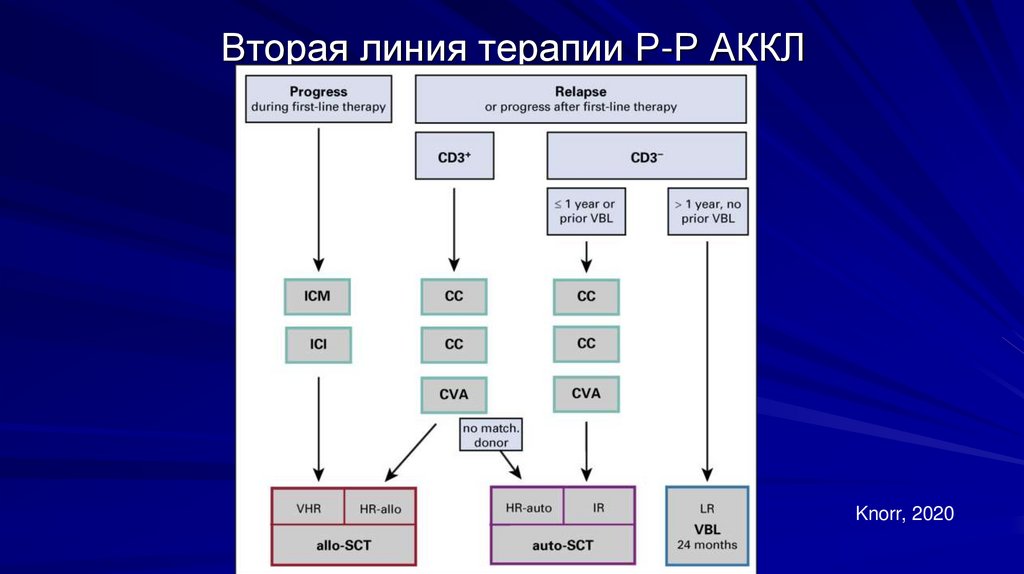
Р-Р АККЛВ отличие от других вариантов НХЛ, при развитии Р-Р АЛК+АККЛ
прогноз остается относительно благоприятным, ввиду высокой
эффективности таргетной терапии и аллогенной ТГСК (алло-ТГСК)
В качестве терапии второй линии Р-Р АККЛ может применяться рискадаптированная стратегия химиотерапии с использованием ТГСК для
консолидации ремиссии (или без нее в группе низкого риска)
Важной особенностью АЛК+АККЛ является то, что в отличие от всех
других видов лимфом, алло-ТГСК может рассматриваться у пациентов
вне ремиссии, так как эта опция эффективна у части пациентов с
активным заболеванием
Особую роль в лечении Р-Р АЛК+АККЛ играет таргетная терапия:
брентуксимаб ведотин (анти-CD30) и ингибиторы АЛК.
124.
Вторая линия терапии Р-Р АККЛKnorr, 2020
125.
ДниСтатус
Алло-ТГСК
78
жив, ремиссия
2
3
ALCL-99, ALCL-relapse 2004, аутоТГСК
2
ПО
Ауто-ТГСК
6
жив, ремиссия
3
7
3
ПО
Ауто-ТГСК
152
жив, ремиссия
3
ЧО
Алло-ТГСК
18
жив, ремиссия
3
ПО
Алло-ТГСК
59
жив, ремиссия
4
ПЗ
Алло-ТГСК
11
жив, ремиссия
4
8
NHL-BFM-95, NHL-BFM-90, ICE, аутоТГСК + MTX+V+NK-клетки, EURO LB2002, CHOP, MTX +AraC+Dexa+ЛТ, CNOP
NHL-BFM, ALCL-Rez-2016+Кризотиниб, СС+Кризотиниб, аллоТГСК,
ЛТ+Кризотиниб
NHL-BFM-95, NHL-BFM 95 +ICE, аутоТГСК, БВ, аллоТГСК, ЛТ
ии
ПО
терап
4
линий
NHL-BFM-90, NHL-BFM-90, COP, аутоТГСК, БВ, аллоТГСК
Терапия
№
11 мес
ст
1
Возра
ТГСК
Р-Р АККЛ Опыт НИИ ДОГиТ им РМ Горбачевой
5
11
6
12
7
24
CHOEP, GDP, Be+кризотиниб, аллоТКМ
3
ПО
аллоТГСК
3
жив, ремиссия
8
26
R-CHOP, R-DexaBEAM, аутоТГСК+Кризотиниб
2
ЧО
Ауто-ТГСК
174
жив, ремиссия
9
28
3
ПЗ
Алло-ТГСК
108
жив, ремиссия
10
34
CHOEP, NHL-BFM-90, аутоТГСК
2
ПО
Ауто-ТГСК
38
жив, ремиссия
11
35
CHOEP, NHL-BFM-90, аутоТГСК
2
ПО
Ауто-ТГСК
79
жив, ремиссия
12
36
CHOEP, БВ+GDP, аутоТГСК+ БВ
2
ПО
Ауто-ТГСК
10
жив, ремиссия
13
36
NHL-BFM-90, TL-REZ-2008+ ALL-2009, БВ, БВ+Be, аллоТГСК
4
ЧО
Алло-ТГСК
17
умер, прогрессия
14
36
HyperCVAD, Ве, GVP, БВ, аллоТГСК, IDL
4
ПО
Алло-ТГСК
89
жив, ремиссия
NHL-BFM-2012, MTX+V, ICE+БВ, аутоТГСК+ Кризотиниб, ViGePP
+БВ+Кризотиниб, аллоТГСК
NHL-BFM-90, GDP, GIFOX, аллоТКМ, DLI, Гемцитабин+DLI+ЛТ, БВ+DLI,
Церитиниб
126.
Ответ на терапию Р-Р АККЛБрентуксимаб
2-линия
терапии
ведотин±ХТ
Ингибиторы
АЛК±ХТ
Оценка ответа независимо
от линии терапии
Количество пациентов, n
15
7
5
Полный ответ, n
7
5
4
Частичный ответ, n
3
0
0
Прогрессия, n
5
2
1
Частота общего ответа, n
10
5
4
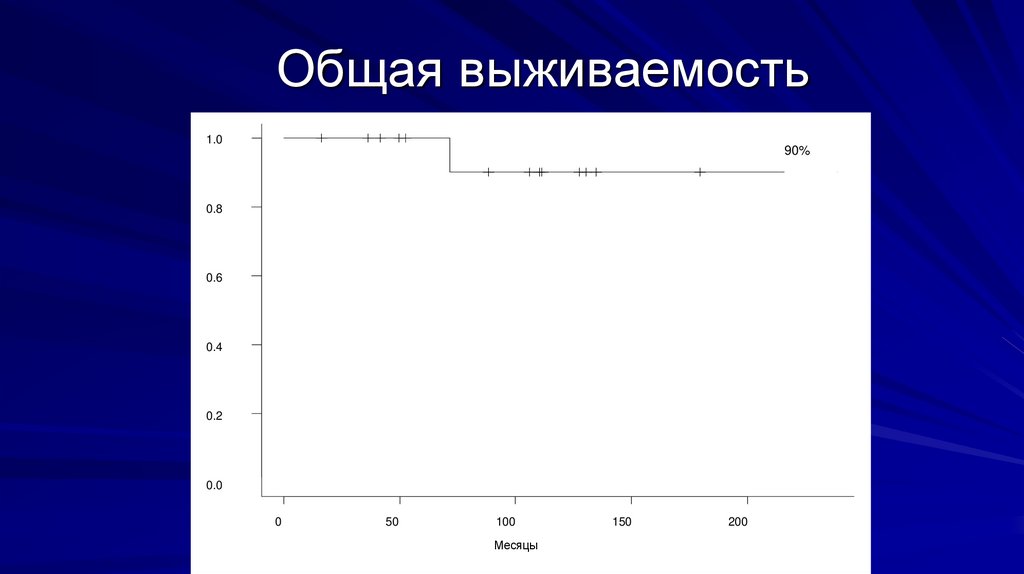
127.
Общая выживаемость1.0
90%
0.8
0.6
0.4
0.2
0.0
0
50
100
Месяцы
150
200
128.
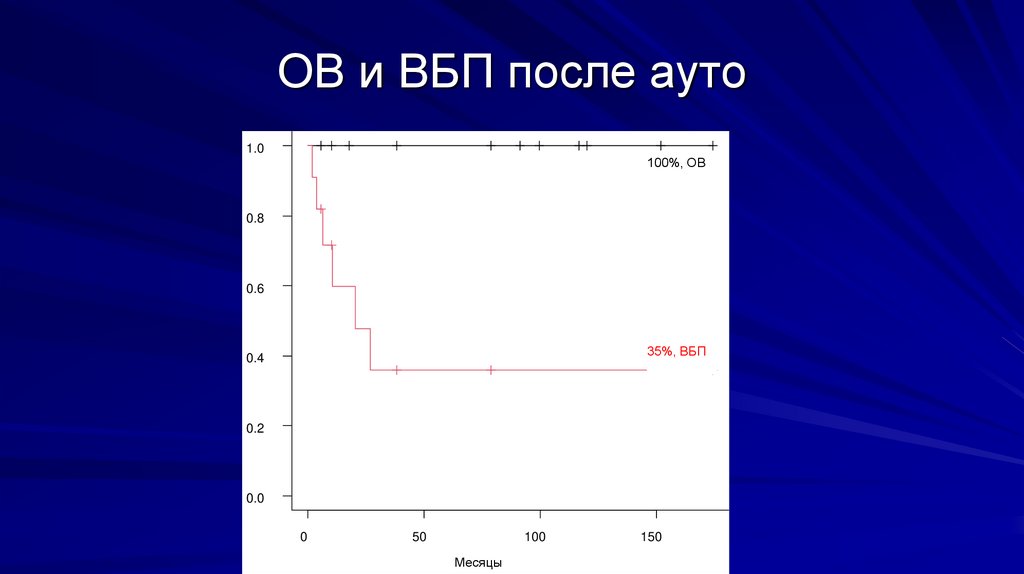
ОВ и ВБП после ауто1.0
100%, ОВ
0.8
0.6
35%, ВБП
0.4
0.2
0.0
0
50
100
Месяцы
150
129.
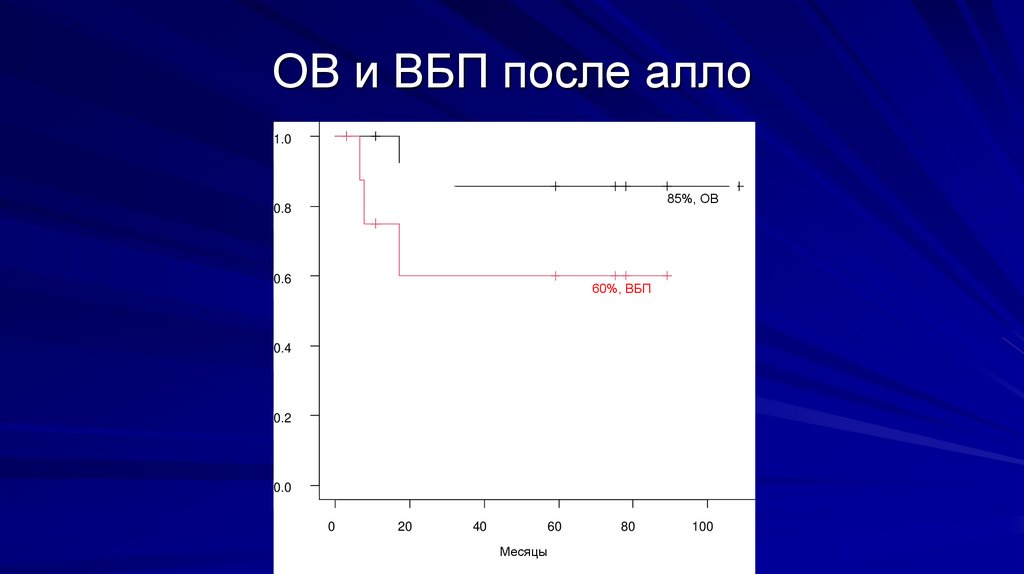
ОВ и ВБП после алло1.0
85%, ОВ
0.8
0.6
60%, ВБП
0.4
0.2
0.0
0
20
40
60
Месяцы
80
100
130.
Р-Р АККЛ, АЛК+Р-Р АЛК+ АККЛ является заболеванием с
относительно благоприятным прогнозом даже у
значительно предлеченных пациентов ( у наших
пациентов медиана линий терапии была 4)
131.
Лимфома Беркитта и алло-ТГСК?!Группа BFM (Woessmann W, Blood, 2020)
Рецидив/рефрактерное течение лимфомы Беркитта
Вторая линия R-VICI (ритуксимаб, винкристин,
ифосфамид, карбоплатин, идарубицин, дексаметазон)
Консолидация алло-ТГСК
10 из 15 живы и в длительной ремиссии (ОВ 67%)
Не относится к пациентам с прогрессией на фоне
терапии первой линии
132.
Ауто-ТГСК у детей и подростков с НХЛНИИ ДОГиТ им. Р.М. Горбачевой (n = 31)
Общая выживаемость
Выживаемость без прогрессирования
ОВ=79%
ВБП=50%
Дни после ауто-ТГСК
Дни после ауто-ТГСК
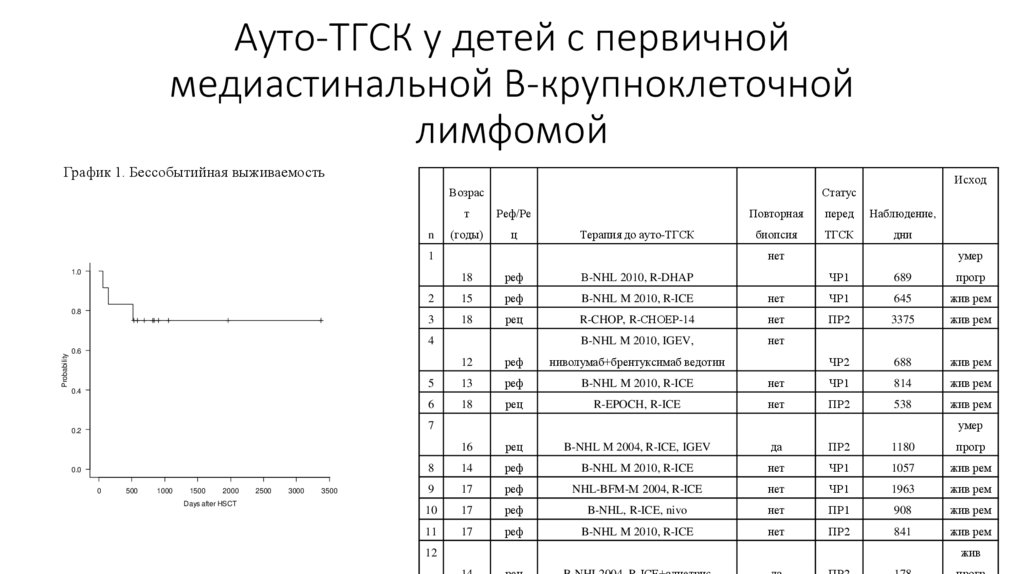
133.
Ауто-ТГСК у детей с первичноймедиастинальной В-крупноклеточной
лимфомой
График 1. Бессобытийная выживаемость
Возрас
n
т
Реф/Ре
(годы)
ц
Терапия до ауто-ТГСК
0.8
18
реф
В-NHL 2010, R-DHAP
2
15
реф
B-NHL M 2010, R-ICE
3
18
рец
4
Probability
Повторная
перед
Наблюдение,
биопсия
ТГСК
дни
нет
1
1.0
Исход
Статус
умер
ЧР1
689
прогр
нет
ЧР1
645
жив рем
R-CHOP, R-СHOEP-14
нет
ПР2
3375
жив рем
B-NHL M 2010, IGEV,
нет
ЧР2
688
жив рем
0.6
0.4
12
реф
ниволумаб+брентуксимаб ведотин
5
13
реф
B-NHL M 2010, R-ICE
нет
ЧР1
814
жив рем
6
18
рец
R-EPOCH, R-ICE
нет
ПР2
538
жив рем
умер
7
0.2
0.0
0
500
1000
1500
2000
Days after HSCT
2500
3000
3500
16
рец
B-NHL M 2004, R-ICE, IGEV
да
ПР2
1180
прогр
8
14
реф
B-NHL M 2010, R-ICE
нет
ЧР1
1057
жив рем
9
17
реф
NHL-BFM-М 2004, R-ICE
нет
ЧР1
1963
жив рем
10
17
реф
B-NHL, R-ICE, nivo
нет
ПР1
908
жив рем
11
17
реф
B-NHL M 2010, R-ICE
нет
ПР2
841
жив рем
12
жив
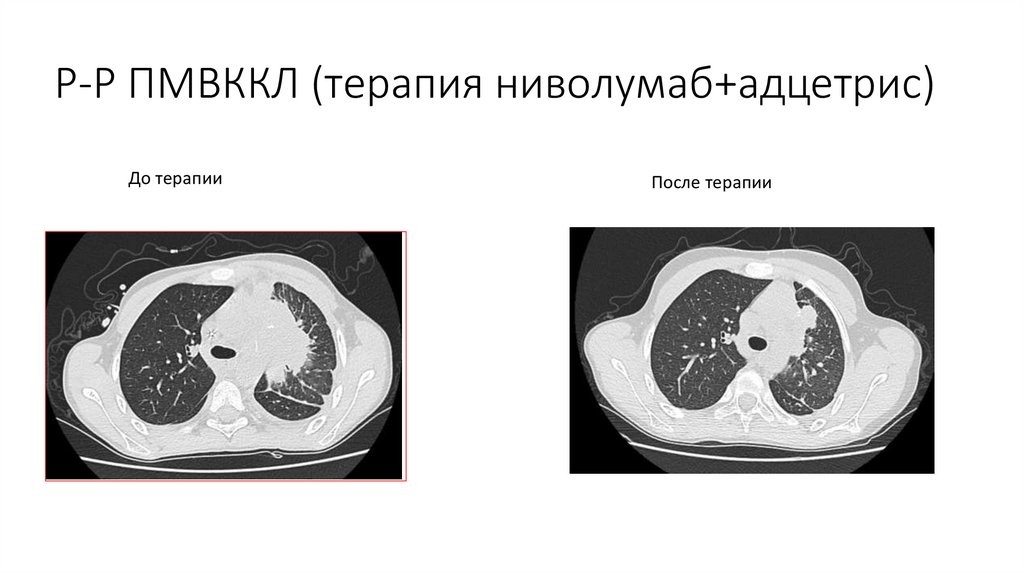
134.
Р-Р ПМВККЛ (терапия ниволумаб+адцетрис)До терапии
После терапии
135.
Пациент Алексей Ж.,Диагноз
Лимфома Ходжкина, нодулярный склероз, gr I, IVЕБ стадия с поражением
внутригрудных, шейных, надключичных лимфатических узлов, легочной ткани
правого легкого, лимфатических узлов брюшной полости и забрюшинных
лимфатических узлов. Состояние после комбинированного лечения 11.2011г.06.2012г., (включающего 8 BEACOPP-esc, лучевую терапию).
Прогрессия(ноябрь 2012г) с поражением правых шейно-надключичных л/у,
средостенных л/у. Состояние после 2-ой линии ПХТ (4 ViGEPP).
Метаболическая ремиссия по данным ПЭТ (04.2013). ВДПХТ с ауто-ТКМ от
20.05.2013. Рецидив (сентябрь 2014г.) с поражением забрюшинных л/у с
распространением на заднее средостение, правых поднижнечелюстных,
заднешейных л/у, надключичных л/у с 2х сторон. Состояние после терапии
адцетрисом (№4) ПЭТ-ремиссия (24.03.2015). Гапло-ТКМ от брата
(06.07.2015). Отрицательная ПЭТ динамика? Сохраняющаяся Ремиссия?.
Терапия Адцетрисом №5, DLI №3. Ремиссия?
136.
Анамнеззаболевания.
• Заболел в 16 лет (февраль 2010): лихорадка, расширение
средостения по рентгенограмме органов грудной клетки,
заподозрено лимфопролиферативное заболеваниеи (детская
Одинцовская больница).
• От дальнейшего обследования и терапии родители пациента на тот
момент отказались
• Обратились за мед.помощью только в ноябре 2011: появление
одышки, увеличение шейных лимфоузлов (конгломераты до 6 см).
• НИИ ДОГ (РОНЦ) открытая биопсия л/узла шеи справа
(гистологическое исследование и ИГХ): классическая лимфома
Ходжкина, вариант нодулярного склероза, grade I.
• КТ ОГК : в средостении конгломерат л/узлов: 9,1х8,9см х12,0см, в
правом легком множественные очаговоподобные уплотнения
легочной ткани до 0,5см
• КТ+АГ органов брюшной полости от множественные л/узлы,
сливающиеся в конгломераты до 18,0см.
137.
Первая линиятерапии
• С 24.11.2011 по 23.01.2012 проведено 4 курса BEACOPP-esc.
• Рестадирование по КТ: сокращение опухолевой масса на
50%.
14.02.2012-5.03.12 BEACOPP esc №5-8
КТ ОГК и брюшной полости: без динамики
ПЭТ всего тела: метаболически активные л/у средостения
С 21.05.12 по 19.06.12 проведена лучевая терапия на области
шеи с двух сторон и забрюшинного пространства РОД 2 Гр,
СОД 20 Гр, средостения + корня правого легкого РОД 2Гр,
СОД 30 Гр
138.
Прогрессия (через 11 месяцев отначала терапии)
• Увеличение шейных л/справа
• Биопсия шейных л/у: подтверждена
прогрессия
139.
2-ая линия терапииViGEPP №1-2 с 14/12/2012 по 17/02/2013
КТ ОГК от 18.01.2013: положительная
динамика.
С 18.02.2013 по 26.04.2013 ViGEPP №3-4
КТ ОГК от 24.04.2013. Без динамики.
ПЭТ всего тела: Метаболическая
ремиссия.
140.
ВДПХТ с ауто-ТГСКВДПХТ с ауто-ТГСК от 20.05.2013. Бендамустин 160
мг\м2\сут Д. 5,-4, Мелфалан 80 мг\м2\сут Д. -3,-2
ПЭТ всего тела после ауто-ТГСКм (через 3
месяца).Сохраняется метаболическая ремиссия.
141.
Рецидив (через 1,5 года)По данным ПЭТ всего тела (04.09.2014): метаболически
активный конгломерат л/у в забрюшинном пространстве (до 83
мм).
Данные подтверждены по МРТ.
142.
Терапия рецидиваПроведено 4 курса Адцетриса 1,8 мг/кг
По данным ПЭТ от 07.05.15. метаболическая
ремиссия
143.
Гапло-ТГСК от братаРежим кондиционирования: 02.07.04.07.15. Флюдарабин 30 мг/м2/д №3,
бендамустин 130 мг/м2/д №3.
Профилактика РТПХ: такролимус,
селлсепт, циклофосфан.
144.
ПЭТ КТ (через 3 мес после гапло-ТГСК)ПЭТ КТ всего тела: рецидив? Неспецифические изменения?
метаболически активные л/у (по Deauville 4): единичные мелкие
шейные л/у от 0,7 до 1,6 см),единичные мелкие забрюшинные л/у
максимально 0, 9 см.
Учитывая высокий риск рецидива, принято решение о проведении
посттрансплантационной терапии
145.
Посттрансплантионная терапия5 введений адцетриса 1,8 мг/кг (итого 9 введений) (последнее 06.2016)
3 введения донорских лимфоцитов:
02.12.15. 1 введение DLI в дозе 1х10/5/кг.
21.01.16. 2 введение DLI в дозе 2,5х10/5/кг.
25.03.16. 3е введение DLI по CD3+ 2,5х10/5/кг.
146.
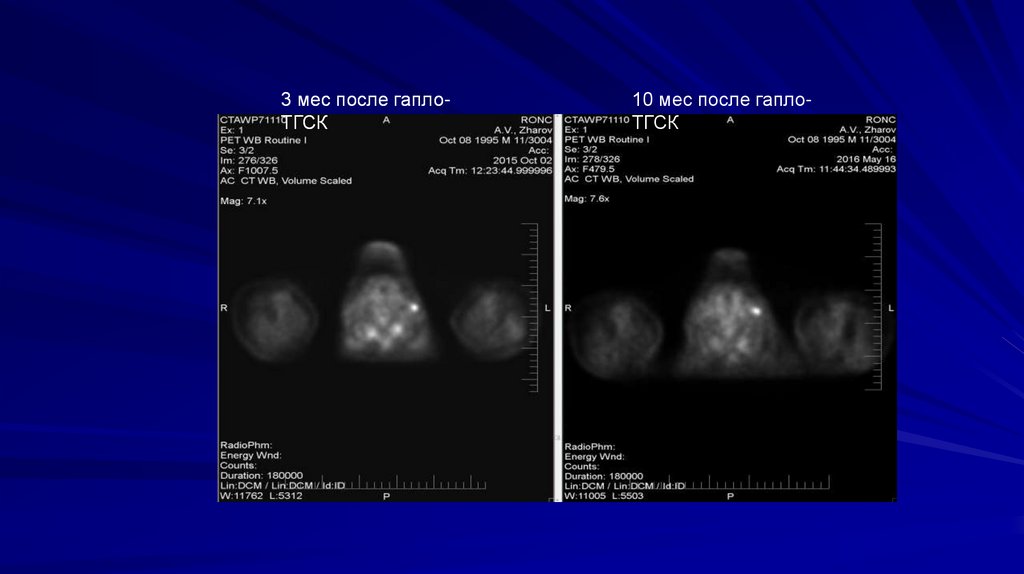
ПЭТ КТ после 10 мес от гапло-ТГСК ипосттранплантационной терапии
Единичные мелкие метаболически активные шейные и
внутрибрюшные л/у.
шейные л/у от 0,4 до 1,6 см (макс по Deuaville 4).
Внутрибрюшные л/у (макс по Deauville 4) : единичные
прекавальные л/у на уровне L5 до 1,0 см, наружный
подвздошный л/у до 0,7 см.
В целом, без динамики по сравнению с 10.2015.
Ремиссия? Сохранение активной опухолевой ткани?
147.
3 мес после гаплоТГСК10 мес после гаплоТГСК










































































































 Медицина
Медицина








