Похожие презентации:
Феррум. Железо
1.
2.
3.
2 место среди металлов (после алюминия)На него приходится 5,1% массы земной коры.
Встречается только в виде соединений.
Свободное железо находят только в
метеоритах.
4.
Fe2+Fe3+
5.
Процесс ржавления железа можнозаписать так:
2Fe + O2 + 2Н2О = 2Fe(OH)2
4Fe(OH)2 + O2 + 2Н2О = 4Fe(OH)3
Fe(OH)2 = FeO + H2O
2Fe(OH)3 = Fe2O3 + 3H2O
6.
При високой температуресоединяется с кислородом, образуя
окалину
Fe3O4 ( FeO • Fe2O3 )
7.
При нагревании железоможет легко реагировать с
хлором, серой и другими
неметаллами:
2Fe + 3Cl2 = 2FeCl3
Fe + S = FeS
8.
Железо легко реагирует соляной иразбавленной серной кислотами:
Fe + 2HCl = FeCl2 + Н2 ↑
Fe + H2SO4 = FeSO4 + H2 ↑
С разбавленной азотной кислотой:
Fe + HNO3 + 3HNO3 = Fe (NO3)3 + 2H2O + NO ↑
9.
З концентрованными серной и азотнойкислотами без нагревания железо не
реагирует.
Оно становится «пассивным»,
покрываясь тонкой оксидной пленкой,
которая не растворяется в кислотах и
защищает металл от действия кислоты.
Благодаря этому концентрованную
азотную и серную кислоты можно
хранить и транспортировать в железной
10. Домашнее задание
Напишите отрасли применениясоединений железа.
2. Осуществите превращения: железо _
оксид железа (II) – хлорид железа (II) –
гидроксид железа (II) – гидроксид
железа (III) – оксид железа (III) железо - сульфат железа (II)
3. Рассчитайте, сколько граммов чистого
железа содержится в образце
легированной стали массой 50 г?
1.

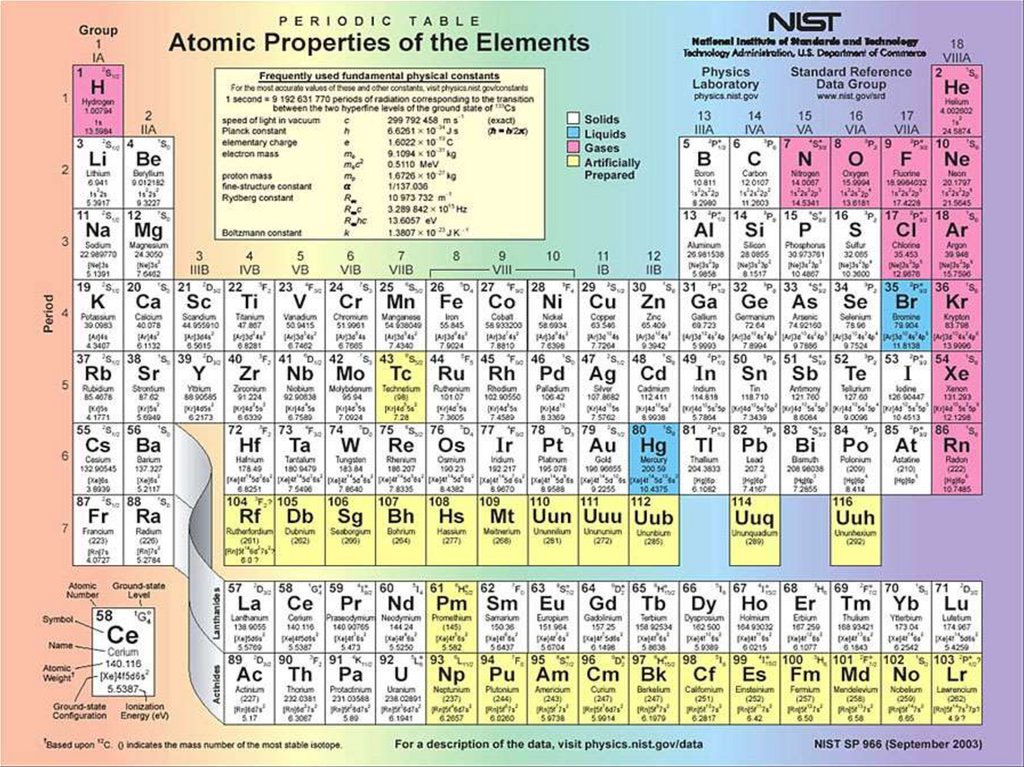








 Химия
Химия