Похожие презентации:
Химические свойства оксидов
1. Химические свойства оксидов».
2. Типичные реакции кислотных оксидов
1.Взаимодействие с основаниямиSO2+2KOH→K2SO3+H2O
2. Взаимодействие с основными
оксидами
CO2+CaО→CaCO3
3. Взаимодействие с водой
(исключение SiO2)
SO3 +H2O→H2SO4
3. Типичные реакции основных оксидов
1.Взаимодействие с кислотойCuO + H2SO4→CuSO4 + H2O
2. 1.Взаимодействие с кислотным
оксидом
K2O +СО2→K2СО3 + H2O
1.Взаимодействие с водой
Ca O + H2O→Ca(OH)2
4. Типичные реакции амфотерных оксидов
1.Взаимодействие соснованиями
ZnO + NaOH → Na2ZnO2+ H2O
2. Взаимодействие с
основными оксидами
BeO + MgO → MgBeO2
5. Типичные реакции амфотерных оксидов
3.Взаимодействие с кислотамиAl2O3 + 6HCl → 2AlCl3 + 3H2O
4. Взаимодействие с кислотными
оксидами
Fe2O3 + CO2 → Fe2(CO3)3
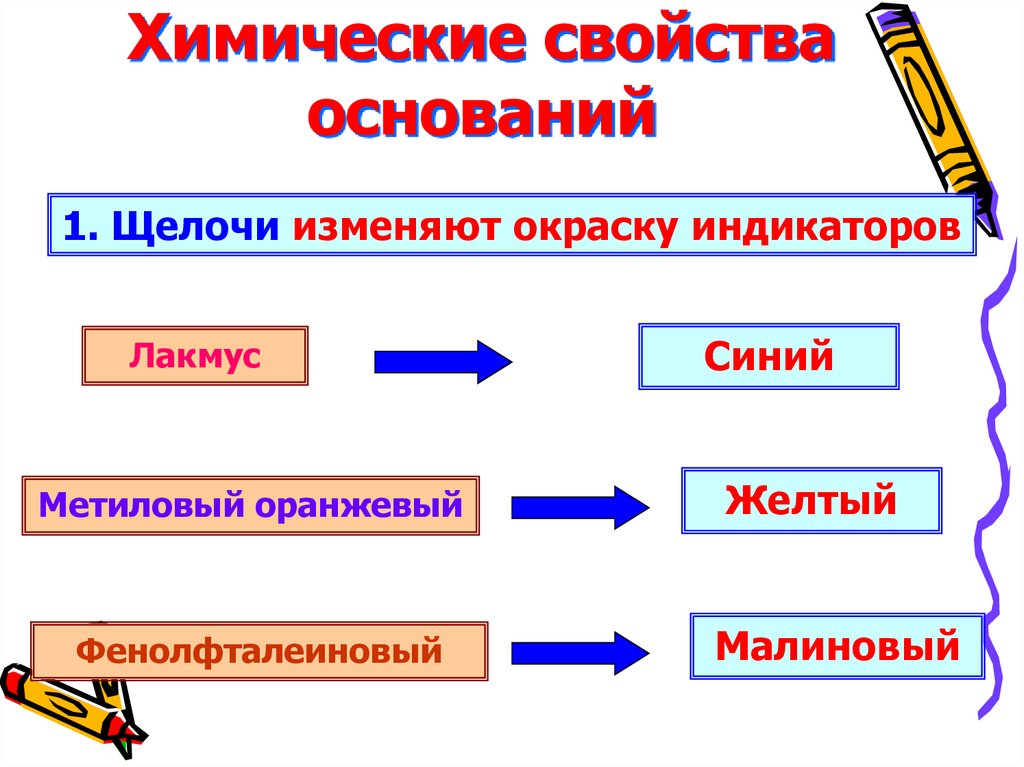
6. Химические свойства оснований
1. Щелочи изменяют окраску индикаторовЛакмус
Метиловый оранжевый
Фенолфталеиновый
Синий
Желтый
Малиновый
7.
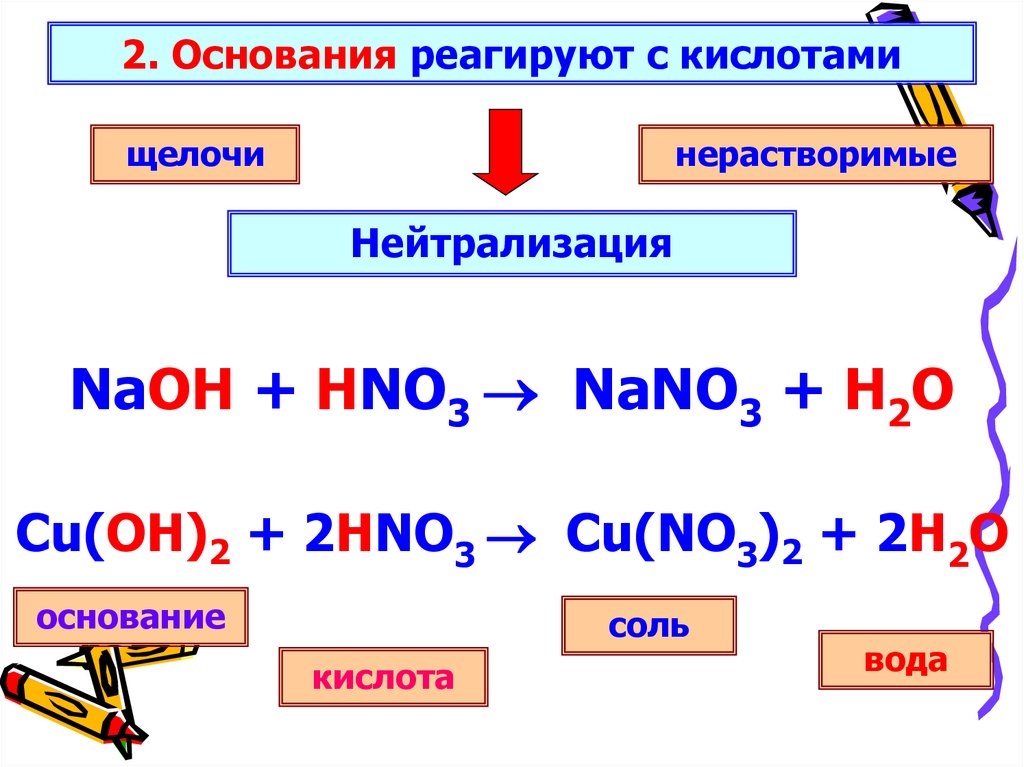
2. Основания реагируют с кислотамищелочи
нерастворимые
Нейтрализация
NaOH + HNO3 NaNO3 + H2O
Cu(OH)2 + 2HNO3 Cu(NO3)2 + 2H2O
основание
соль
кислота
вода
8.
3. Взаимодействие с кислотнымиоксидами
6NaOH + P2O5 2Na3PO4 + 3H2O
4. Взаимодействие с солями
2KOH + CuSO4 K2SO4 +Cu(OH)2
9.
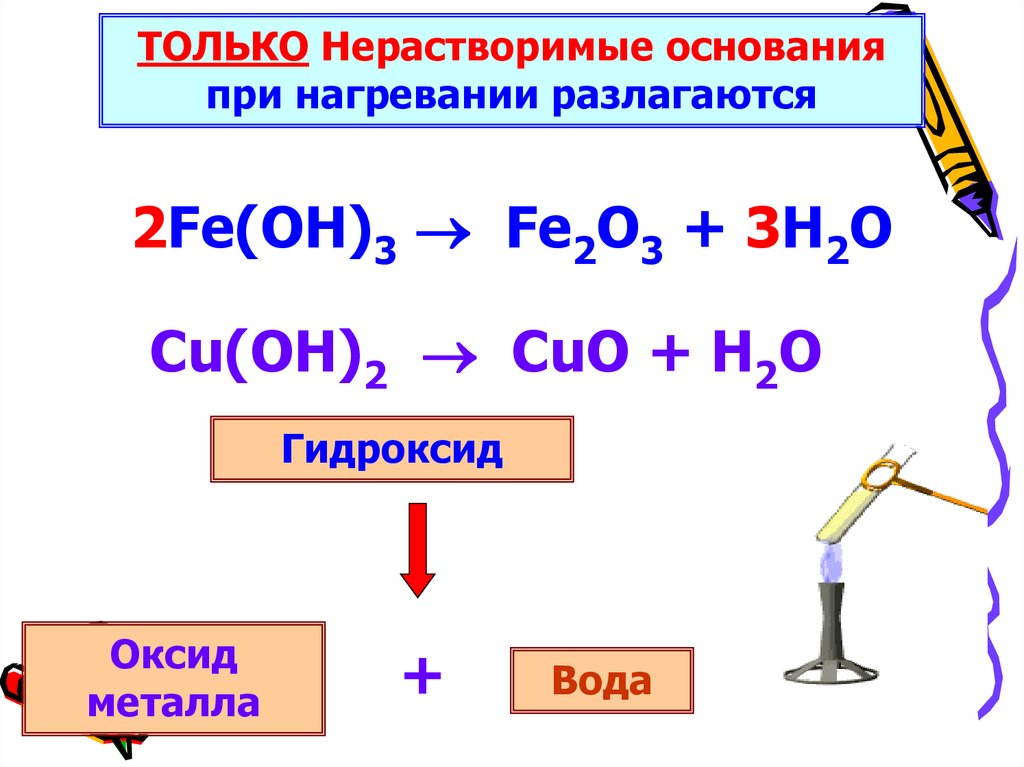
ТОЛЬКО Нерастворимые основанияпри нагревании разлагаются
2Fe(OH)3 Fe2O3 + 3H2O
Cu(OH)2 CuO + H2O
Гидроксид
Оксид
металла
+
Вода
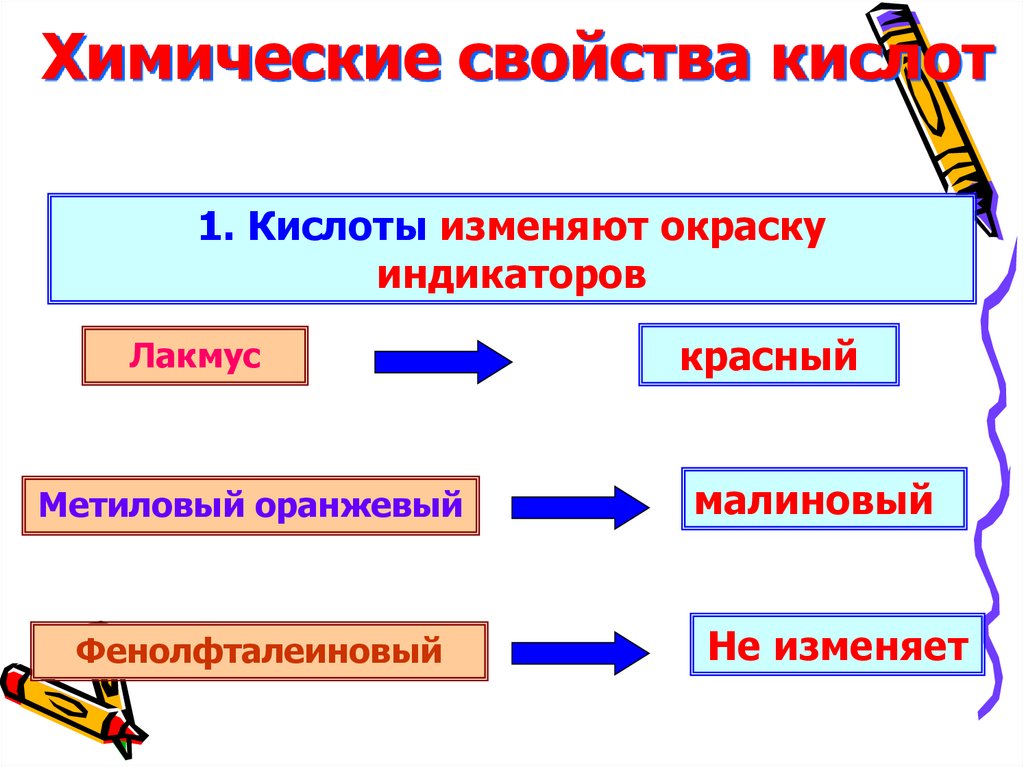
10. Химические свойства кислот
1. Кислоты изменяют окраскуиндикаторов
Лакмус
красный
Метиловый оранжевый
малиновый
Фенолфталеиновый
Не изменяет
11.
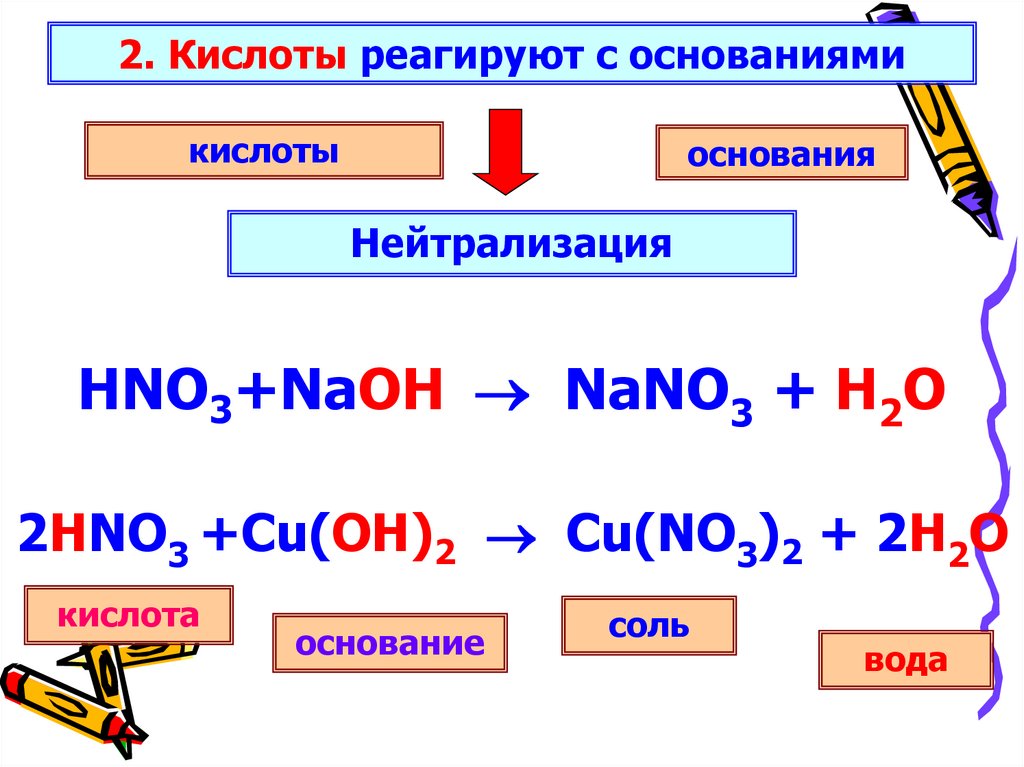
2. Кислоты реагируют с основаниямикислоты
основания
Нейтрализация
HNO3+NaOH NaNO3 + H2O
2HNO3 +Cu(OH)2 Cu(NO3)2 + 2H2O
кислота
основание
соль
вода
12.
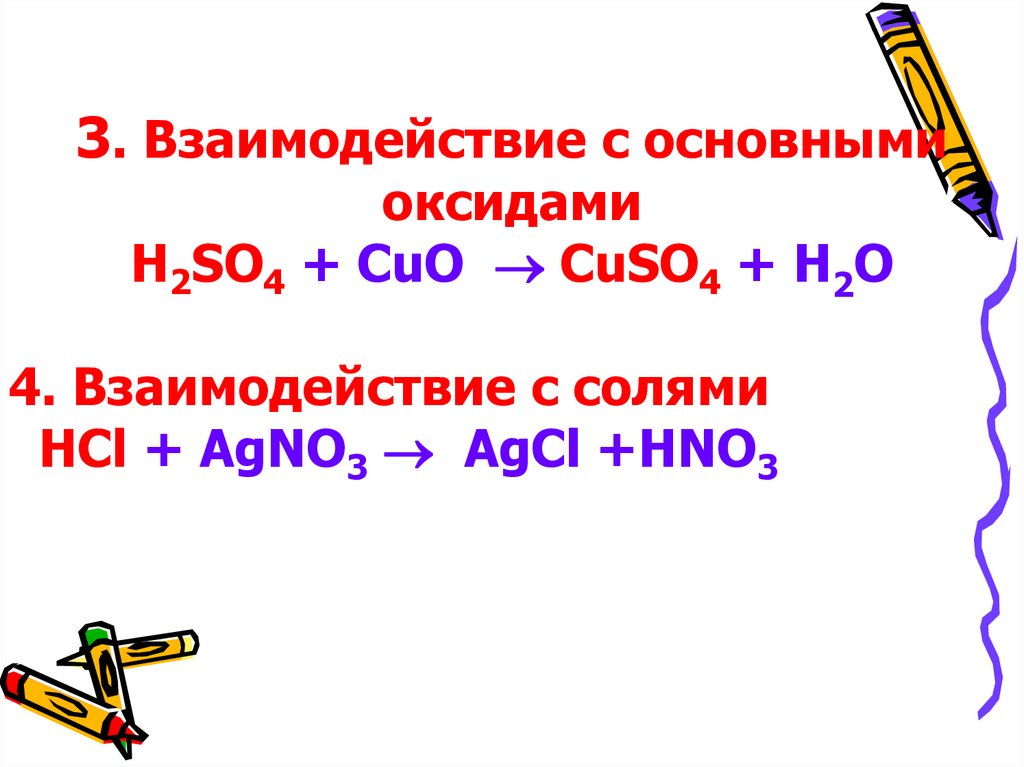
3. Взаимодействие с основнымиоксидами
H2SO4 + CuO CuSO4 + H2O
4. Взаимодействие с солями
HCl + AgNO3 AgCl +HNO3
13.
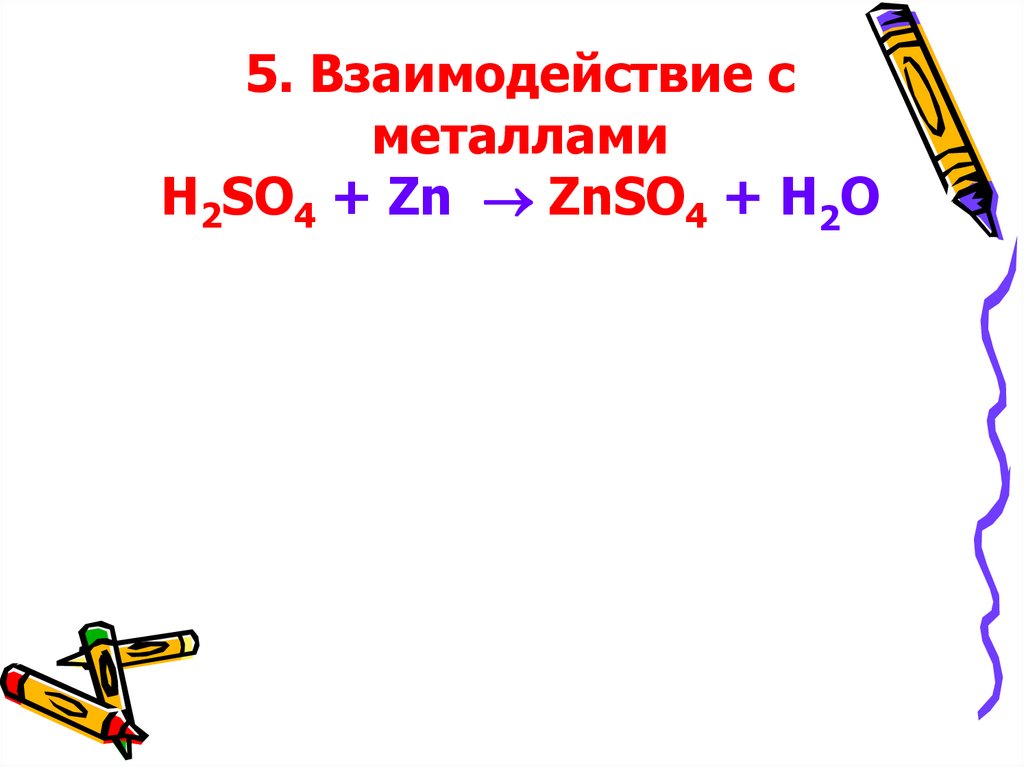
5. Взаимодействие сметаллами
H2SO4 + Zn ZnSO4 + H2O
14. Химические свойства солей
• 1. Взаимодействие с основаниямиCuSO4 +2KOH K2SO4 +Cu(OH)2
2. Взаимодействие с кислотами
AgNO3 +HCl AgCl +HNO3
3. Взаимодействие с друг c другом
NaCl + AgNO3 NaNO3 + AgCl
4. С металлами
Zn + CuSO4
ZnSO4 + Cu
15.
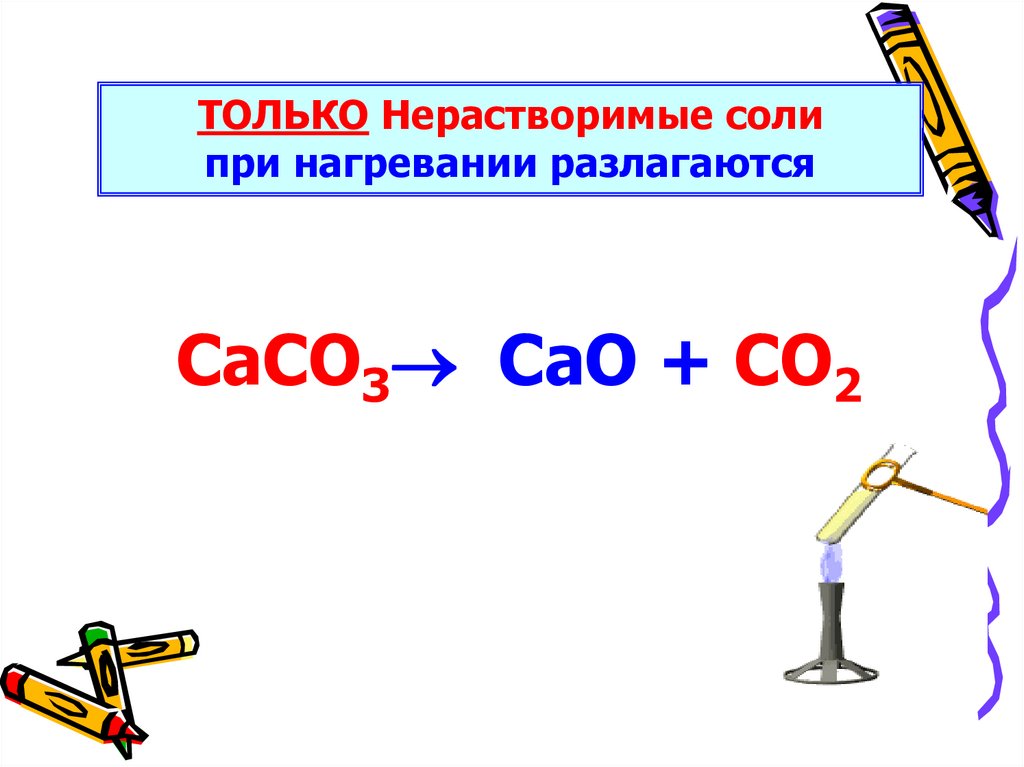
ТОЛЬКО Нерастворимые cолипри нагревании разлагаются
CaCO3 CaO + CO2







 Химия
Химия








