Похожие презентации:
Концентраційні межі поширення полум'я. Лекція 7
1. Розділ II. ВИНИКНЕННЯ ПРОЦЕСУ ГОРІННЯ
Тема 3. ГОРЮЧІ СИСТЕМИ.Лекція 7
КОНЦЕНТРАЦІЙНІ МЕЖІ
ПОШИРЕННЯ ПОЛУМ'Я.
2. План лекції
1. Умови виникнення горіння2. Умови утворення горючого середовища.
3. Чинники, що впливають на КМПП
4. Практичне значення КМПП
3. 1. Умови виникнення горіння
Виникнення горіння - це швидкий перехід відповільної реакції до миттєвої у наслідок її
самоприскорення реакції зі спалахом та звуковим
ефектом.
Для виникнення горіння необхідна наявність
горючої системи – суміші горючої речовини та
окисника у певному співвідношенні. За умови
накопичення в такій системі тепла або активних
центрів і виникає горіння (тепловий або
ланцюговийм механізм виникнення горіння).
4.
Особливістю горіння є те, що швидкість хімічноїреакції збільшується не зважаючи на зменшення
концентрації реагуючих речовин.
Це має місце тому, що прискорення реакції
внаслідок підвищення температури може дати
більший вплив ніж зменшення в ході реакції
концентрацій реагентів (за законом Арреніуса).
хр = jгрnjокm kоexp (-Eакт/RT).
Ланцюгова теорія пояснює прискорення реакції
горіння лавиноподібним накопиченням активних
центрів.
5.
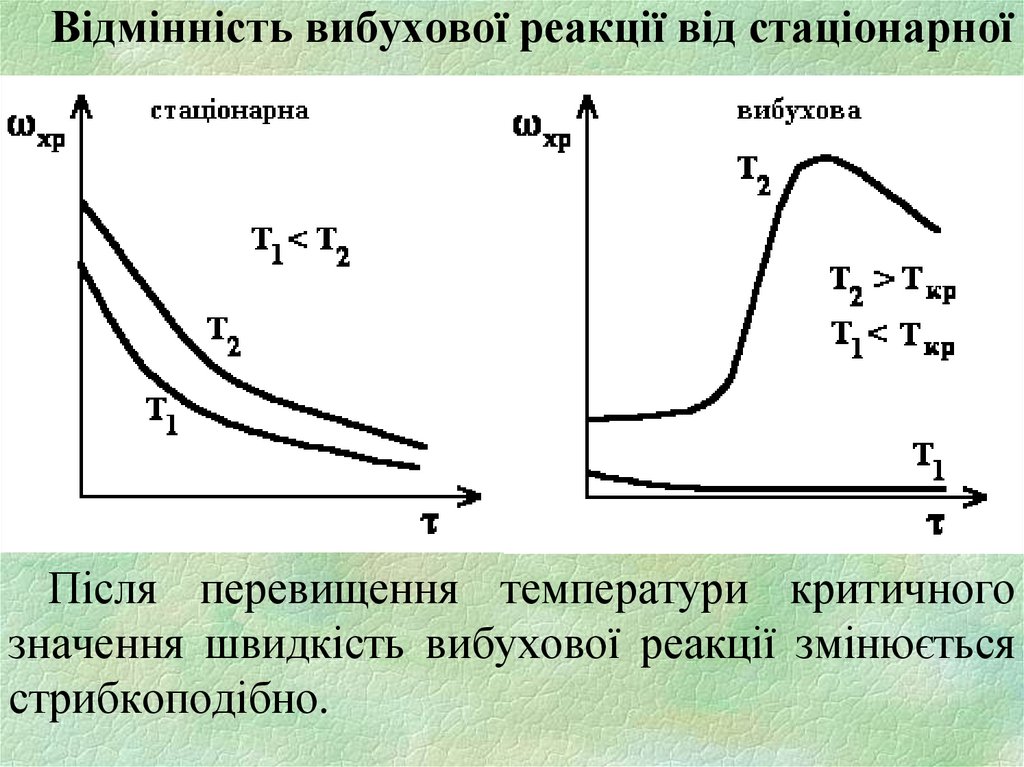
Відмінність вибухової реакції від стаціонарноїПісля перевищення температури критичного
значення швидкість вибухової реакції змінюється
стрибкоподібно.
6.
Інтенсивність тепловиділення реакції:q(+) =QгVгс хр
Поява різниці температур між системою та
навколишнім середовищем викликає віддачу тепла
шляхом конвекції з інтенсивністю:
q(–) = S (Т – То).
Якщо q(–)>q(+) - зона реакції охолоджується, реакція
окиснення гальмується;
q(–)<q(+) - зона реакції нагрівається, реакція
окиснення прискорюється.
Період часу з початку самовільного зростання
температури горючої системи до моменту виникнення
горіння називається періодом або часом індукції.
7.
Розрізняють три вида виникнення горіння:Самоспалахування – виникнення горіння всієї
горючої системи водночас під впливом зовнішнього
нагріву до критичної температури.
Самозаймання – виникнення горіння внаслідок
накопичення тепла внутрішніх екзотермічних
процесів в горючій системі.
Вимушене запалювання – виникнення горіння
внаслідок дії високотемпературного джерела
запалювання на малу частку горючої системи.
8.
Загальні ознаки процесу виникнення горіння:наявність горючої системи: горючої речовини та
окисника у певному співвідношенні;
температура системи більша за критичну;
тепловиділення в горючій системі q(+) перевищує
тепловіддачу q(–) в навколишнє середовище;
перехід від повільної реакції до вибухоподібної
відбувається за період індукції.
9. 2. Умови утворення горючого середовища
Горючим є середовище, здатне самостійно горітипісля усунення джерела запалювання.
2.1. Поняття концентраційних меж поширення
полум'я (КМПП)
За законом Ареніуса, якщо концентрація одного з
компонентів горючої суміші (jгр або jок) стане менше
критичного значення, швидкість реакції зменшується
на стільки, що інтенсивність тепловиділення q(+)
стане меншою, ніж інтенсивність тепловтрат q(-), зона
реакції охолоджується, горіння не виникає або
припиняється. Тобто умова q(–)=q(+) є критичною для
виникнення горіння.
10.
НКМПП (jн) - найменша концентрація горючоїречовини в суміші з повітрям, при якій вже
можливе виникнення та поширення горіння.
ВКМПП (jв) - найбільша концентрація горючої
речовини в суміші з повітрям, при якій ще
можливе виникнення та поширення горіння.
11.
2.2. Методи визначення КМПП1. НКМПП розраховують, виходячи з нижчої
теплоти згоряння ГР:
//
Qкр 183000
Qн - 100%
о
jн 100
,%
Qкр - φн %
Qн//
Qн//
2. НКМПП розраховують, виходячи зі складу ГР:
100
о
jн
,%
o
1 hf H f h jm j
j
де hf = 0,0246 - параметр теплоти утворення ГР;
Hof - стандартна теплота утворення ГР;
hj - параметр j-го елемента в молекулі ГР;
mj - число атомів j-го елемента в молекулі ГР.
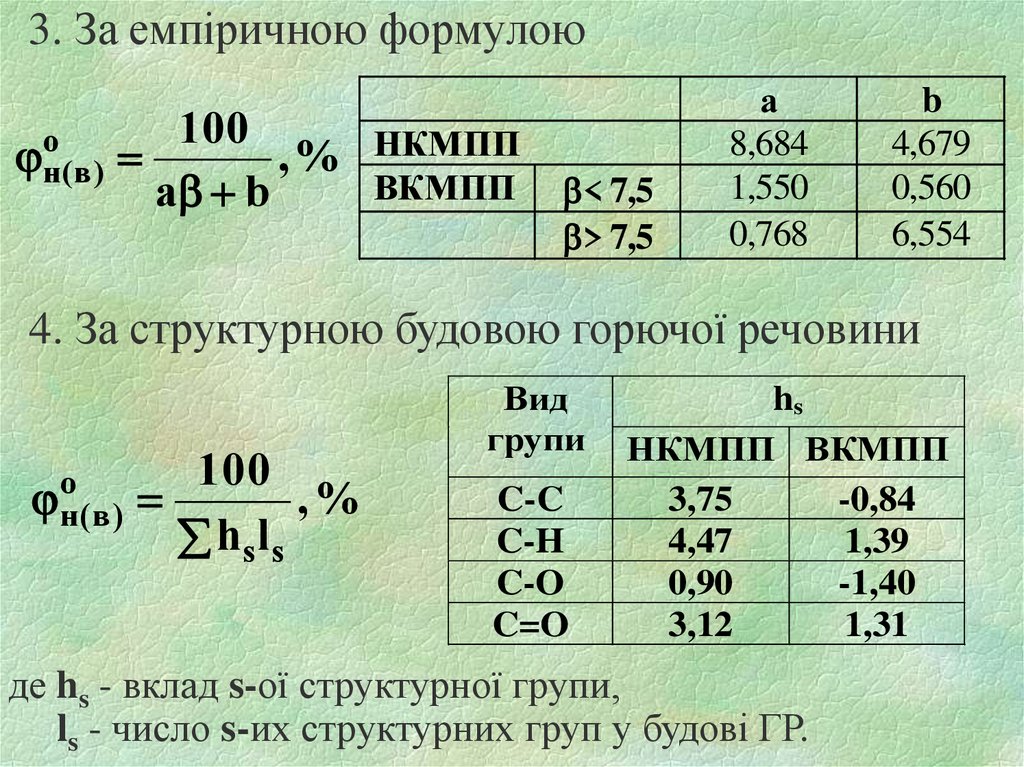
12. 3. За емпіричною формулою
оjн(в )
100
, % НКМПП
ВКМПП < 7,5
a b
> 7,5
а
8,684
1,550
0,768
b
4,679
0,560
6,554
4. За структурною будовою горючої речовини
о
jн ( в )
100
,%
hs l s
Вид
групи
C-C
C-H
C-O
C=O
hs
НКМПП ВКМПП
3,75
-0,84
4,47
1,39
0,90
-1,40
3,12
1,31
де hs - вклад s-ої структурної групи,
ls - число s-их структурних груп у будові ГР.
13. 5. КМПП суміші горючих газів
Правило Ле-Шательє: багатокомпонентна система, яка складається із декількох бінарних сумішейграничного складу, взятих у довільному
співвідношенні, також є граничною.
о
j н( в )сум
o
ji
,%
о
ji
o
j н( в ) i
де jон(в)I - нижня або верхня КМПП i-го горючого
компоненту,
jоi - процентний вміст i-го компоненту в суміші.
14.
Склад суміші: СН4 – 30%; С2Н4 – 70%.jно СН4 = 5,3%;
jно С2Н4 = 2,7%
30 70
о
jн
3,16%
30 70
сум
5, 3
2 ,7
Для перерахунку об'ємної концентрації jо у
масову j/ та назад можна користуватися
формулою:
/
о
j 10j
, г 3
V
м
15. 3. Чинники, що впливають на КМПП
Чинники, які збільшують тепловиділення в системіq(+) , розширюють КМПП (φн , φв ), а чинники, які
збільшують тепловтрати від системи в навколишнє
середовище q(-) , звужують область запалювання
(φн , φв ) аж до неможливості горіння.
Найбільший вплив на зміну КМПП мають:
1) вид горючої речовини;
2) склад горючої суміші:
концентрації кисню в окислювальному середовищі;
домішки негорючих газів;
добавки каталізаторів або інгібіторів.
3) умови, в яких знаходиться суміш:
температура і тиск системи;
міра турбулізації газового потоку;
потужність впливу ДЗ.
16.
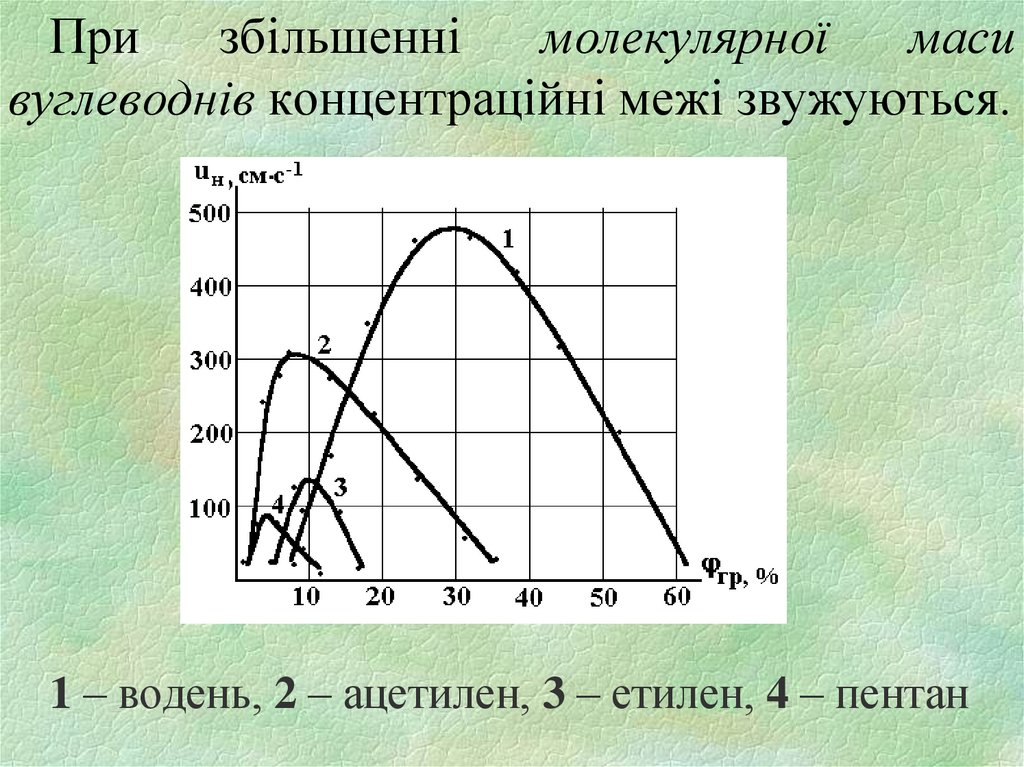
Призбільшенні
молекулярної
маси
вуглеводнів концентраційні межі звужуються.
1 – водень, 2 – ацетилен, 3 – етилен, 4 – пентан
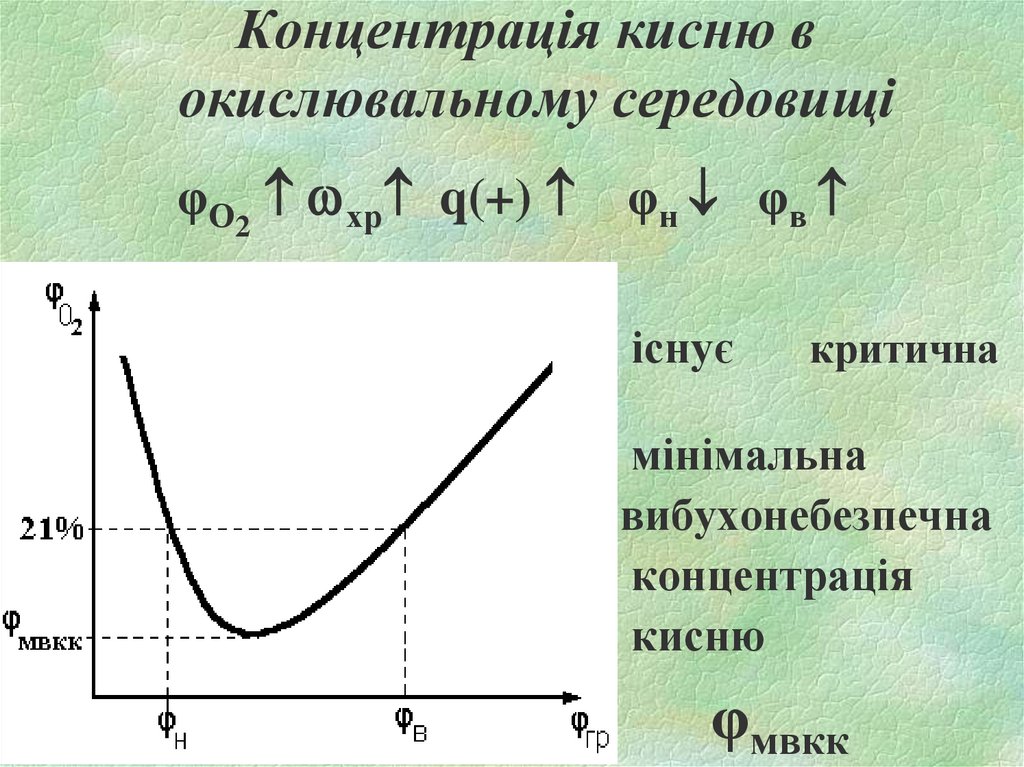
17. Концентрація кисню в окислювальному середовищі
φО2 хр q(+) φн φвзначення
існує
критична
мінімальна
вибухонебезпечна
концентрація
кисню
φмвкк
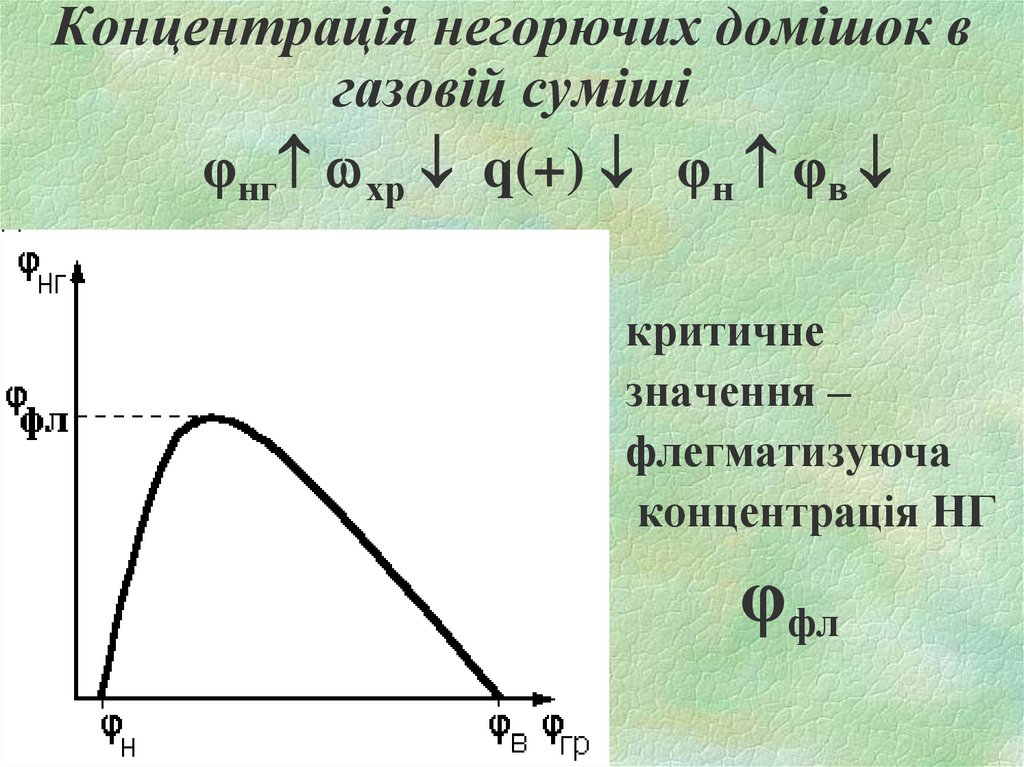
18. Концентрація негорючих домішок в газовій суміші
φнг хр q(+) φн φвкритичне
значення –
флегматизуюча
концентрація НГ
φфл
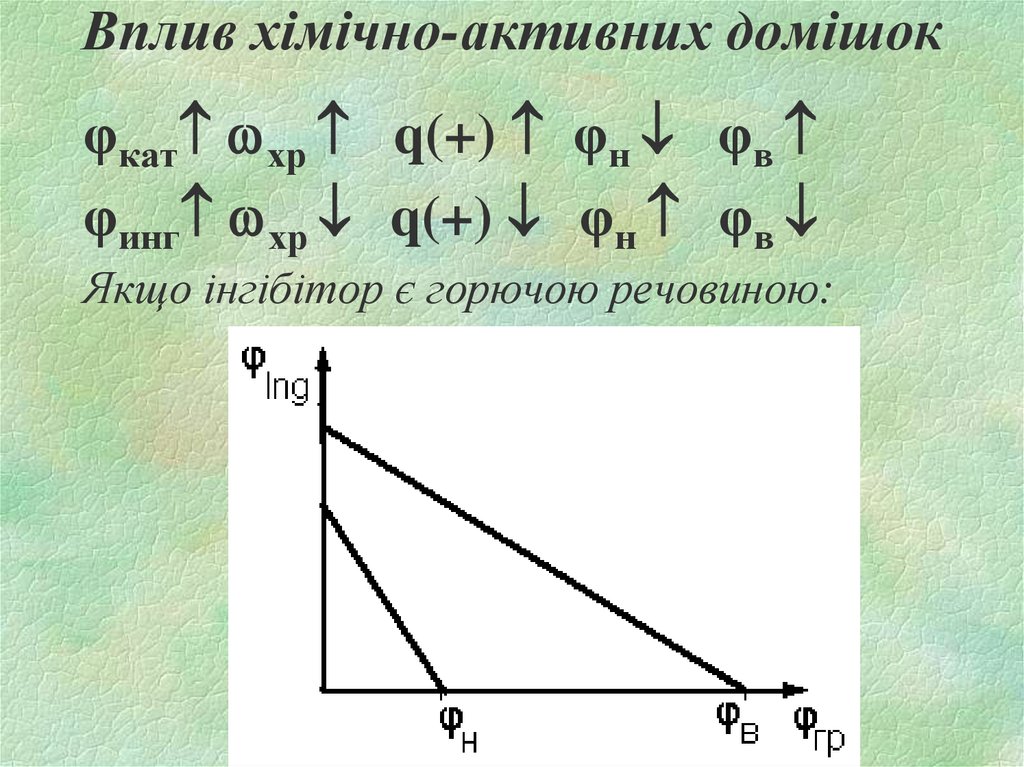
19. Вплив хімічно-активних домішок
φкат хр q(+) φн φвφинг хр q(+) φн φв
Якщо інгібітор є горючою речовиною:
20.
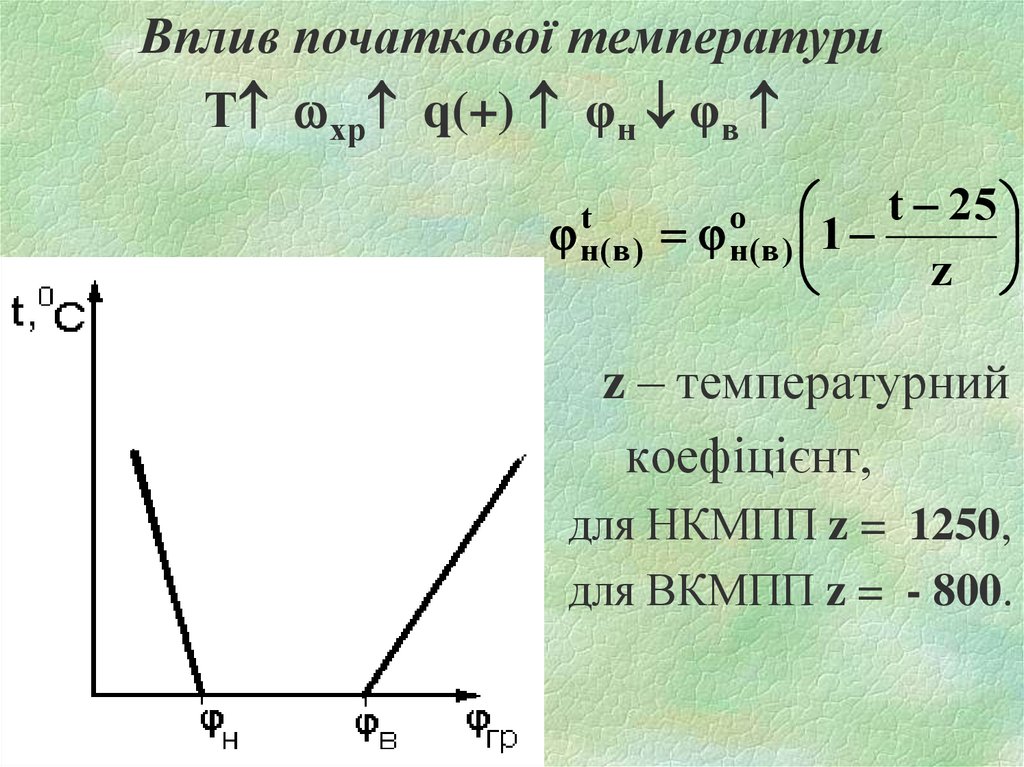
Вплив початкової температуриТ хр q(+) φн φв
t 25
t
o
j н( в ) j н( в ) 1
z
z – температурний
коефіцієнт,
для НКМПП z = 1250,
для ВКМПП z = - 800.
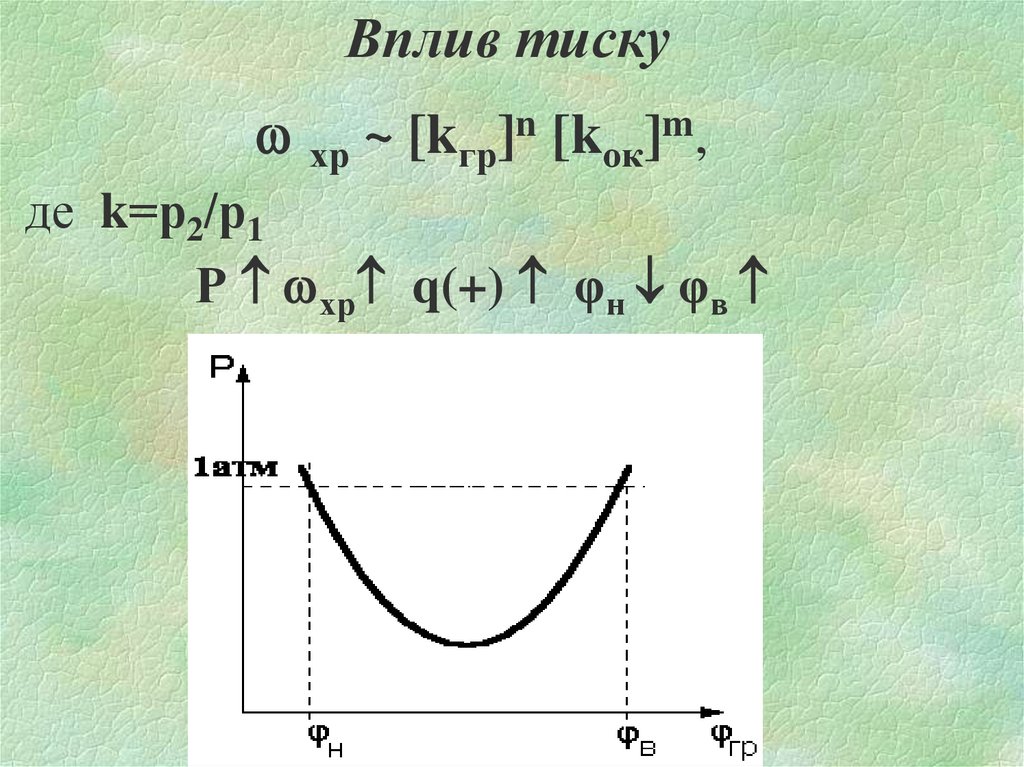
21. Вплив тиску
хр ~ [kгр]n [kок]m,де k=р2/р1
Р хр q(+) φн φв
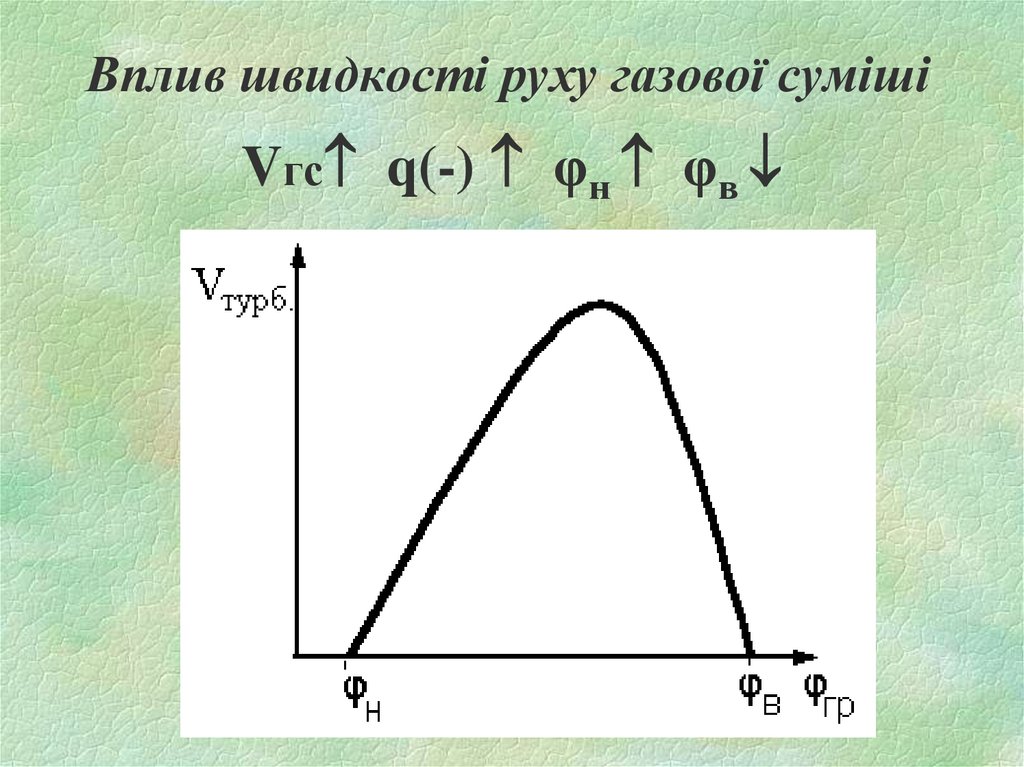
22. Вплив швидкості руху газової суміші
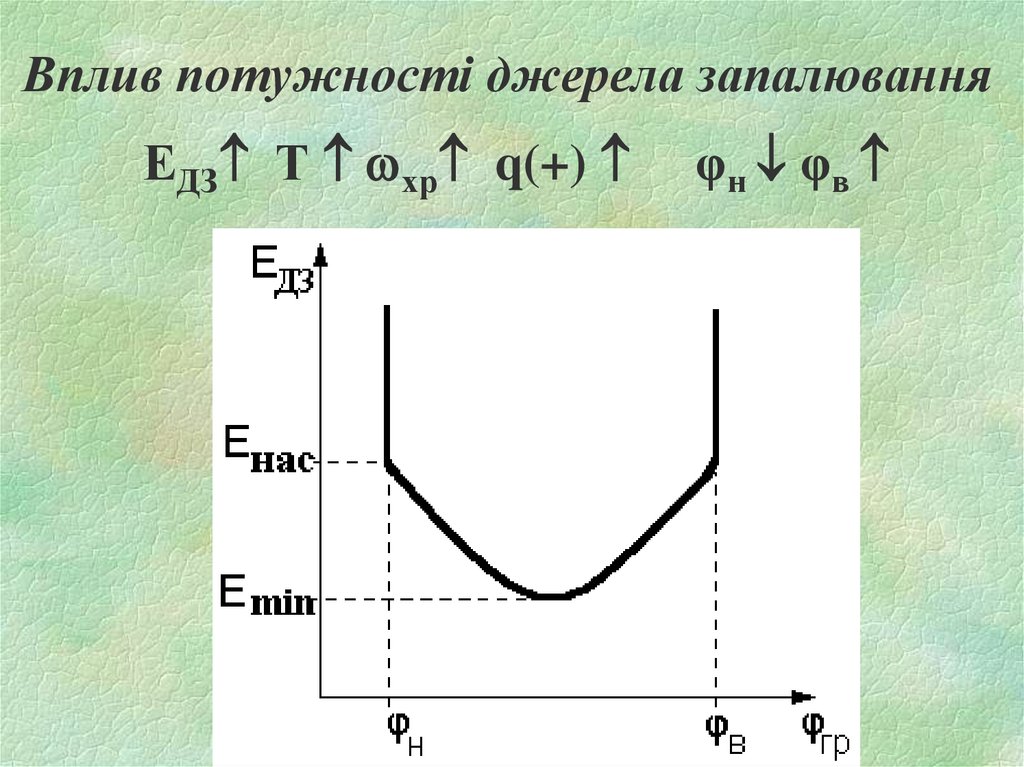
Vгс q(-) φн φв23. Вплив потужності джерела запалювання
ЕДЗ Т хр q(+)φн φв
24. Безпечні концентраційні межі поширення полум'я: φонб < 0,9(φон - 0,21), % φовб >1,1(φов + 0,42), %
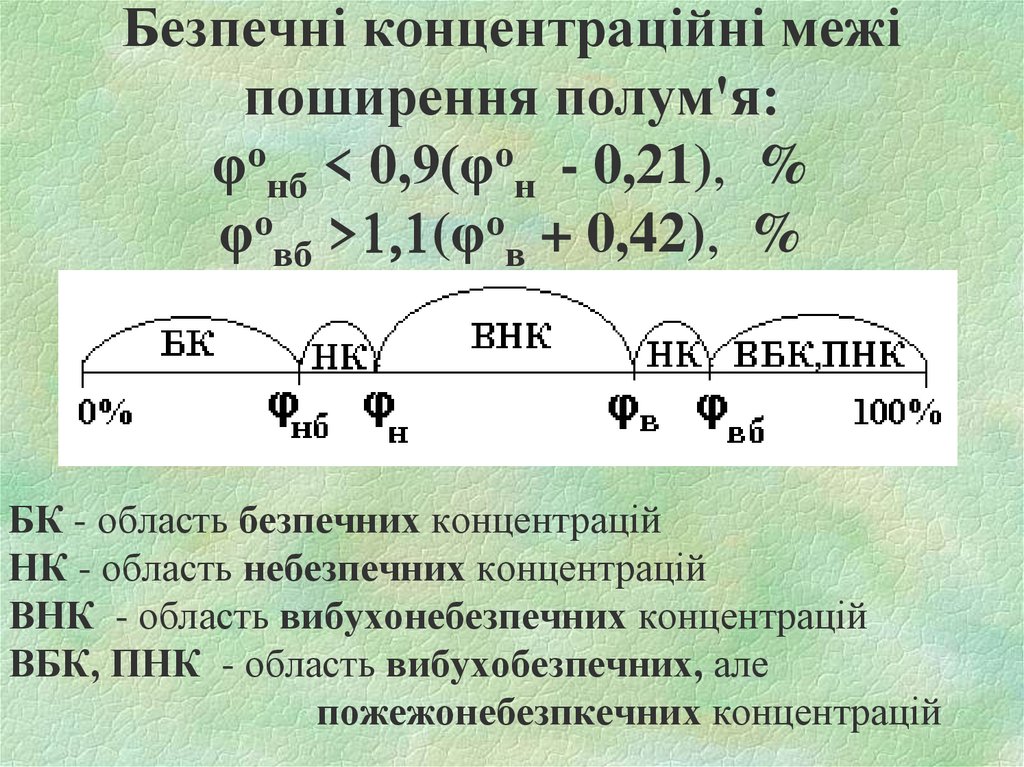
Безпечні концентраційні межіпоширення полум'я:
φонб < 0,9(φон - 0,21), %
φовб >1,1(φов + 0,42), %
БК - область безпечних концентрацій
НК - область небезпечних концентрацій
ВНК - область вибухонебезпечних концентрацій
ВБК, ПНК - область вибухобезпечних, але
пожежонебезпкечних концентрацій
25. 4. Практичне значення КМПП
1. Для порівняльної оцінки пожежної небезпекидекількох речовин.
Найбільш пожежо- та вибухонебезпечними є
речовини з більш широким діапазоном
вибухонебезпечних концентрацій.
2. Для оцінки пожежної небезпеки фактичної
концентрації горючої речовини.
φфакт< φнб
- безпечна концентрація
φнб< φфакт< φн - небезпечна концентрація за зміни
умов
φн< φфакт< φв - вибухонебезпечна конц-ція
φв< φфакт< φвб - небезпечна концентрація за зм. умов
φфакт > φв
- вибухобезпечна, але
пожежонебезпечна концентрація
26.
3. Для визначення вибухобезпечних умовзнаходження
горючої
речовини
всередині
технологічного обладнання:
φфакт< φнб,
φфакт > φв .
4. Для встановлення безпечних концентрацій
речовин у повітрі, що визначають можливість дії
безумовних джерел запалювання без виникнення
горіння (відкриті вогневі роботи, вентиляційні
системи та ін.):
φобез< φонб.
27. Завдання на самопідготовку:
Вивчити матеріал1. Демидов, Шандыба, Щеглов. - Горение и
свойства горючих веществ, стор. 85-104.
2. Демидов, Саушев. - Горение и свойства
горючих веществ, стор. 152-181.
















 Химия
Химия








