Похожие презентации:
Строение атома и атомного ядра
1.
2.
Демокрит(460-370 до н.э)
М.В.Ломоносов
( 1711-1765)
3.
АТОМ –НАИМЕНЬШАЯ ЧАСТИЦАХИМИЧЕСКОГО ЭЛЕМЕНТА,
ЯВЛЯЮЩАЯСЯ НОСИТЕЛЕМ ЕГО
СВОЙСТВ.
4.
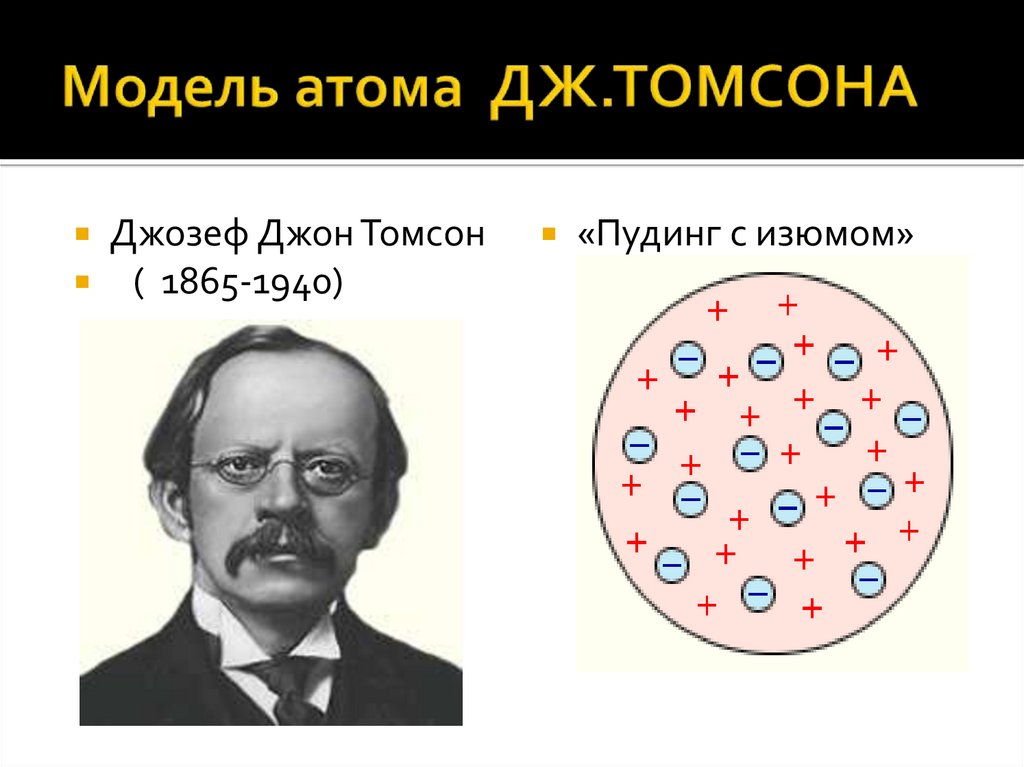
Джозеф Джон Томсон( 1865-1940)
«Пудинг с изюмом»
5.
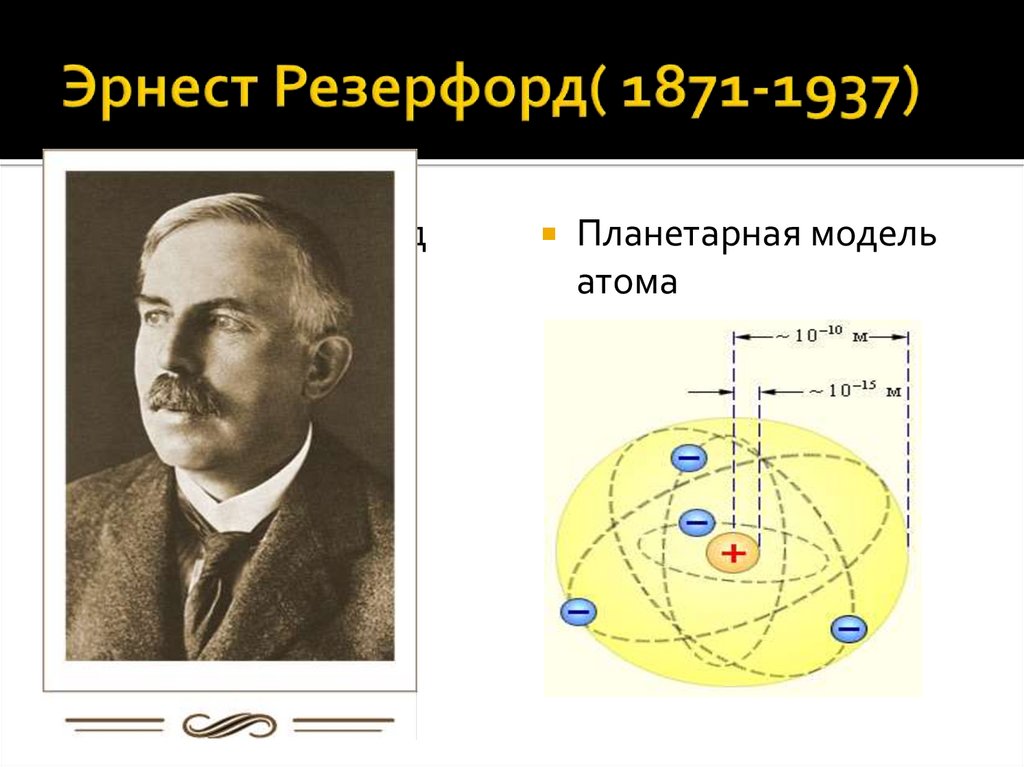
Эрнест Резерфорд(1871—1937)
Планетарная модель
атома
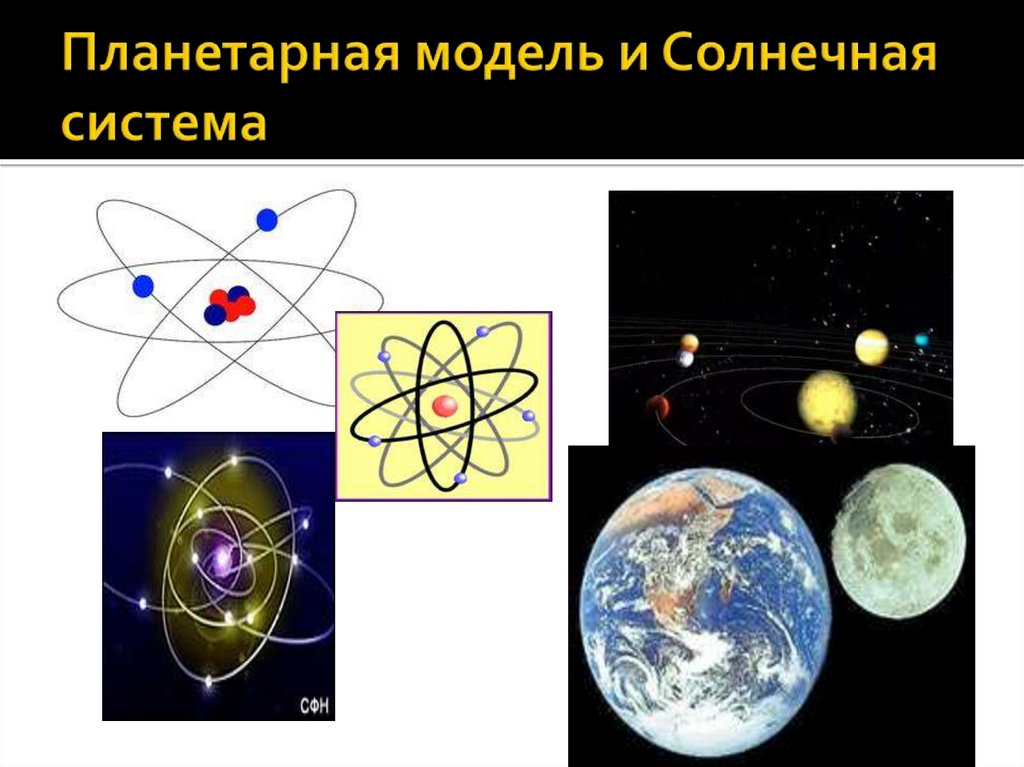
6.
7.
Видел Модель атома8.
Название частицыОбозначение
Заряд ( Кл)
Масса ( кг)
Электрон
e
-1,60219* 10-19
9,1095*10-31
Протон
p
-1,60219*10-19
1,6726*10-27
Нейтрон
n
нет
1,6749*10-27
9.
Z-зарядовое число - порядковый номер, заряд
ядра, количество протонов, количество
электронов
М
МАССОВОЕ ЧИСЛО, МАССА ЯДРА
N
- число нейтронов
=М-Z
м
z
Х
10.
11.
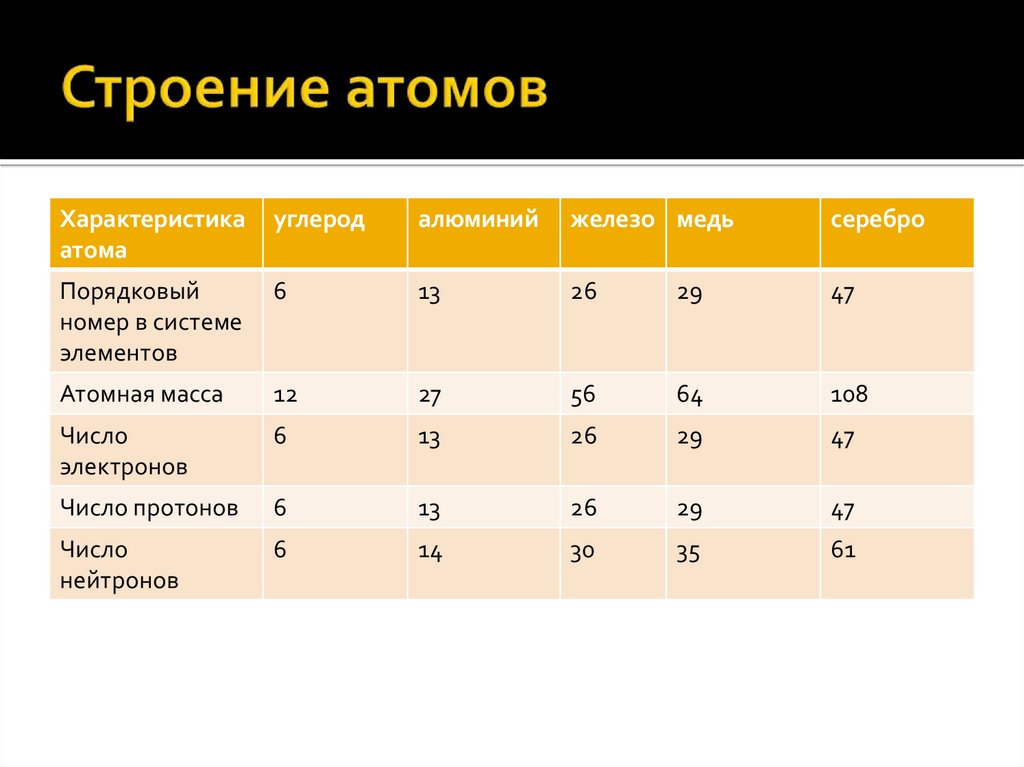
Характеристикаатома
углерод
алюминий
железо медь
серебро
Порядковый
номер в системе
элементов
6
13
26
29
47
Атомная масса
12
27
56
64
108
Число
электронов
6
13
26
29
47
Число протонов
6
13
26
29
47
Число
нейтронов
6
14
30
35
61
12.
1.Что изображено на рисунках?2 Каково строение атомов водорода,
гелия, лития?
3Если атом потерял один или несколько
электронов, то что произойдет ? Можно ли
считать его нейтральным?
4 Если атом приобрел один или несколько
электронов, как называют этот атом?
13.
1 В центре атома находитсяположительное ядро, состоящее из
положительных протонов и нейтральных
частиц нейтронов, а вокруг него движутся
отрицательные электроны;
2Атом в целом не имеет заряда, он
нейтральный, т.к.положительный заряд
ядра равен отрицательному заряду всех
его электронов или ( число протонов равно
числу электронов).
14.
1Чем отличаются друг от друга атомыразличных химических элементов?
2. Что является главной характеристикой
данного химического элемента? Почему?
3.Какие физические понятия вы встретили
в тексте?
4.Назовите отличие электрона от протона?
Протона от нейтрона.
5.Что можно сказать о массах протона и
нейтрона?
15.
16.
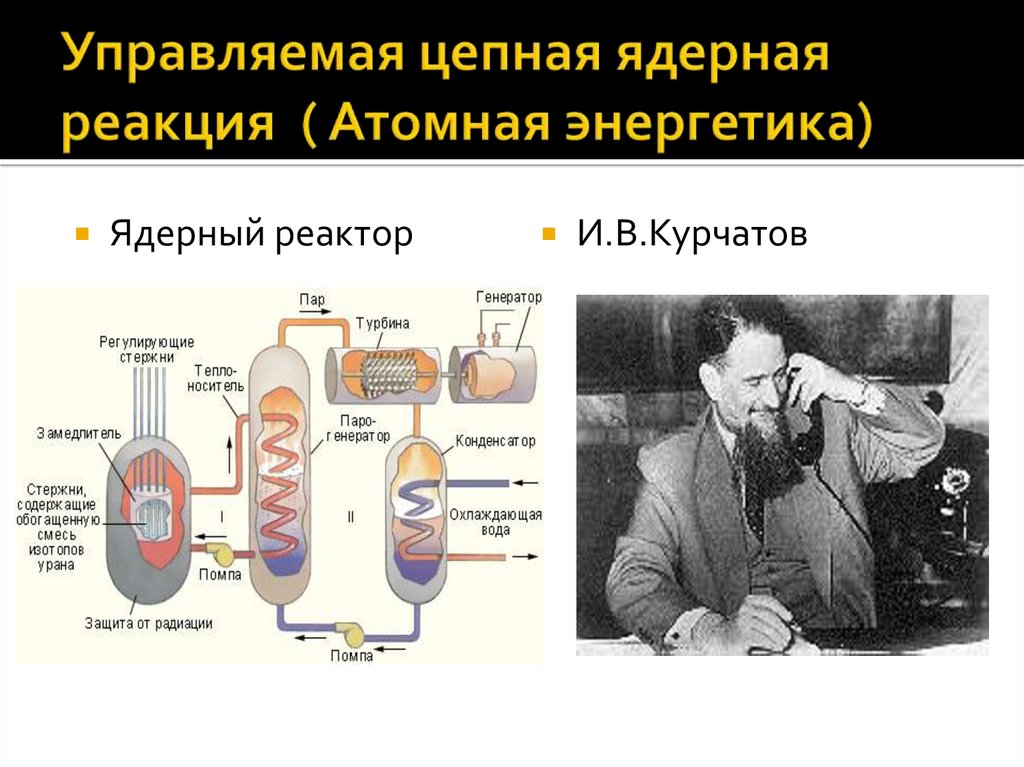
Ядерный реакторИ.В.Курчатов
17.
18.
19.
1 Параграф № 302 Упражнение № 11















 Химия
Химия








