Похожие презентации:
Изменение свойств соединений в периодической системе
1.
2.
11
2
2
Сходство в строении атомов химических
элементов одной А-группы обусловлено
одинаковыми
одинаковыми
зарядами
3
размерами атомов
ядер атомов
одинаковым
одинаковым
числом валентных 4 числом электронэлектронов
ных слоев
В одной подгруппе периодической системы
находятся химические элементы, имеющие
электронные схемы
1
2,8,4 и 2,8,5
3
2,8,6 и 2,8,7
2
2,8,3 и 2,3
4
2,8,1 и 2,8
3.
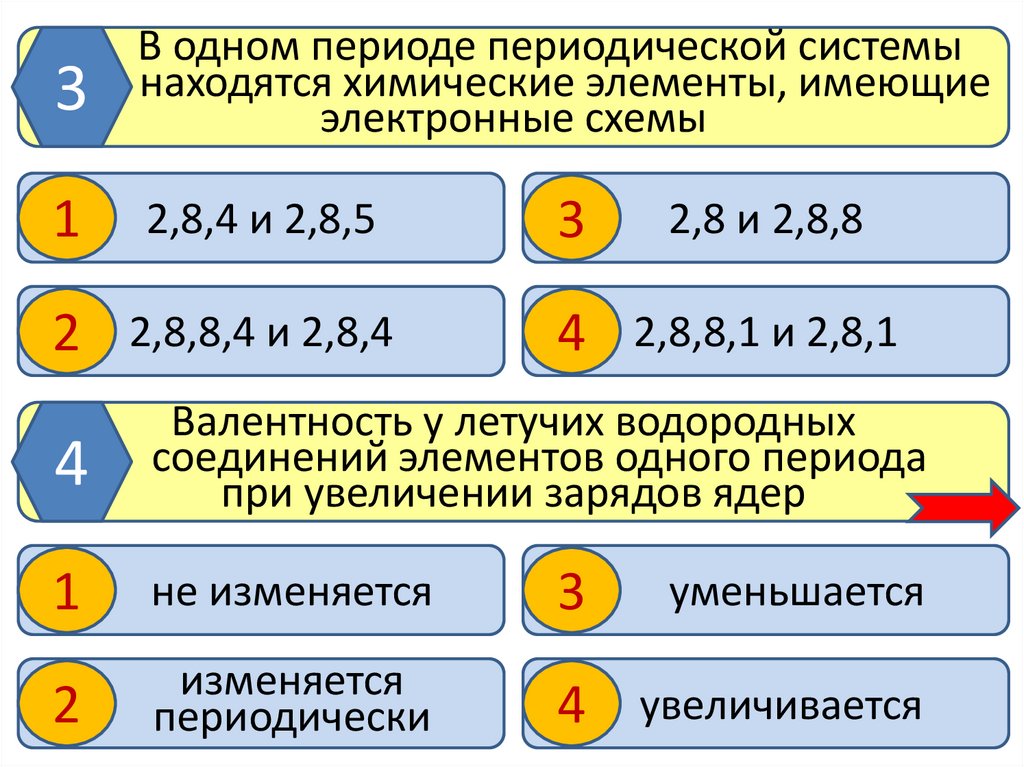
3В одном периоде периодической системы
находятся химические элементы, имеющие
электронные схемы
1
2,8,4 и 2,8,5
2 2,8,8,4 и 2,8,4
3
2,8 и 2,8,8
4 2,8,8,1 и 2,8,1
4
Валентность у летучих водородных
соединений элементов одного периода
при увеличении зарядов ядер
1
не изменяется
3
2
изменяется
периодически
4 увеличивается
уменьшается
4.
5Валентность у оксидов элементов одного
периода при увеличении зарядов ядер
1
увеличивается
2
6
1
2
уменьшается
3
не изменяется
4
изменяется
периодически
При увеличении заряда ядра атомов
свойства гидроксидов, образованных
элементами подгруппы IVA изменяются,
соответственно
щелочь→амфотерный гидроксид
амфотерный гидроксид → кислота
3
4
кислота → амфотерный гидроксид
нерастворимое основание →кислота
5.
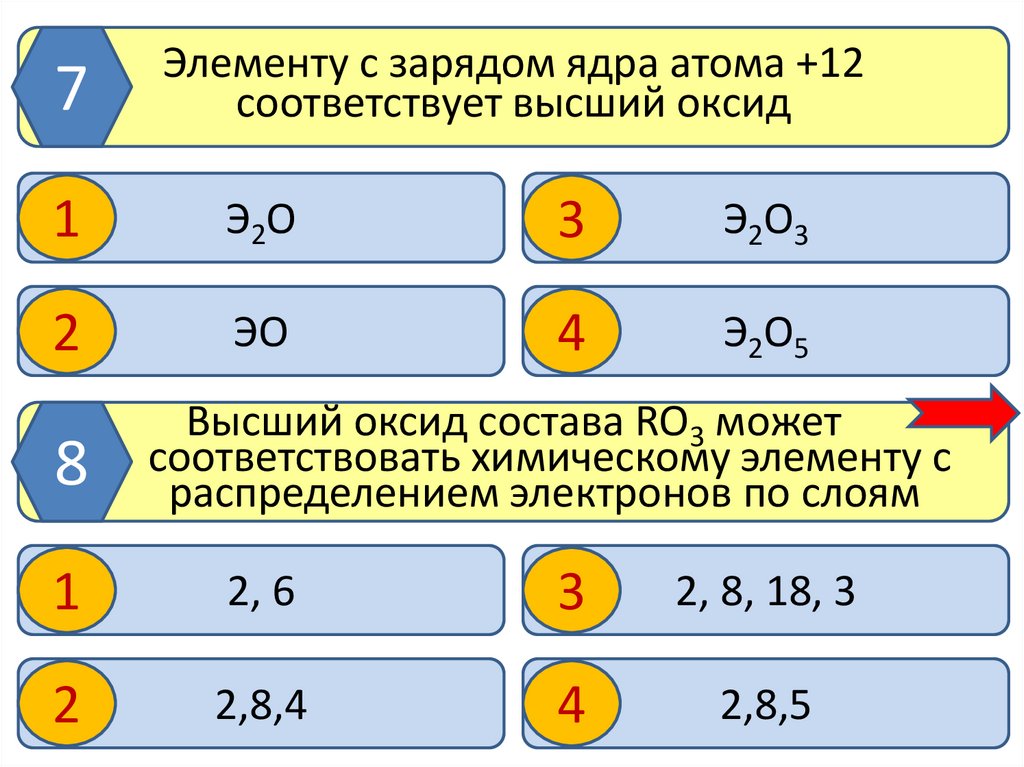
7Элементу с зарядом ядра атома +12
соответствует высший оксид
1
Э2О
3
Э2О3
2
ЭО
4
Э2О5
8
Высший оксид состава RO3 может
соответствовать химическому элементу с
распределением электронов по слоям
1
2, 6
3
2, 8, 18, 3
2
2,8,4
4
2,8,5
6.
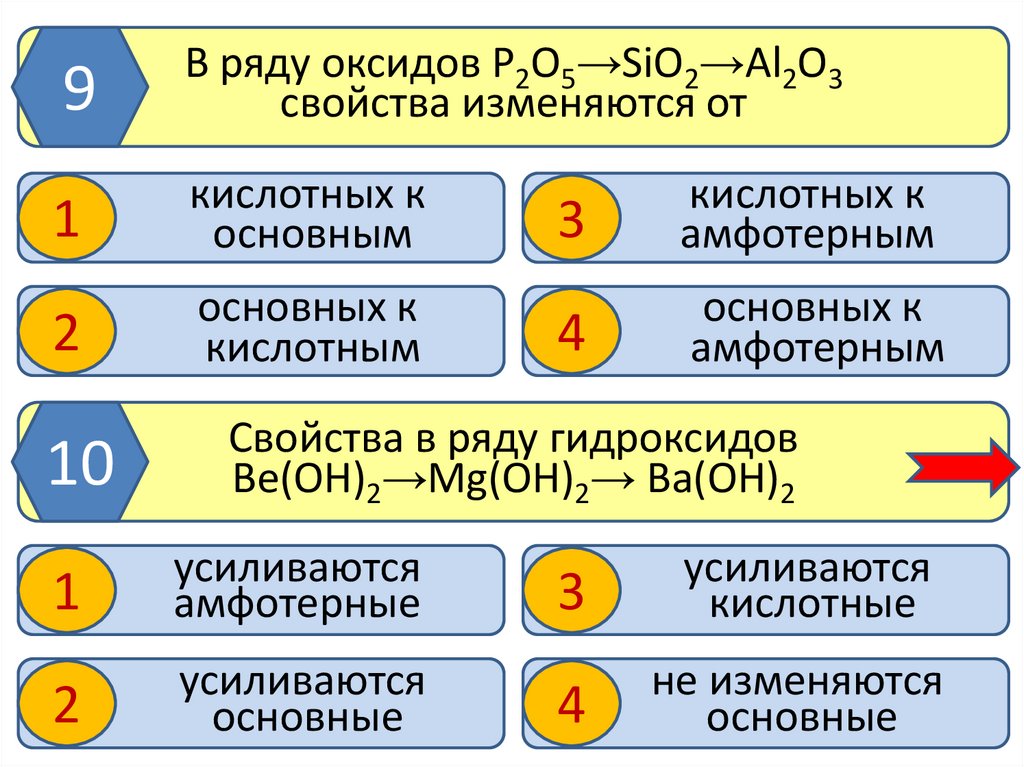
9В ряду оксидов P2O5→SiO2→Al2O3
свойства изменяются от
1
кислотных к
основным
2
основных к
кислотным
10
3
кислотных к
амфотерным
4
основных к
амфотерным
Свойства в ряду гидроксидов
Be(OH)2→Mg(OH)2→ Ba(OH)2
1
усиливаются
амфотерные
2
усиливаются
основные
3
усиливаются
кислотные
4
не изменяются
основные
7.
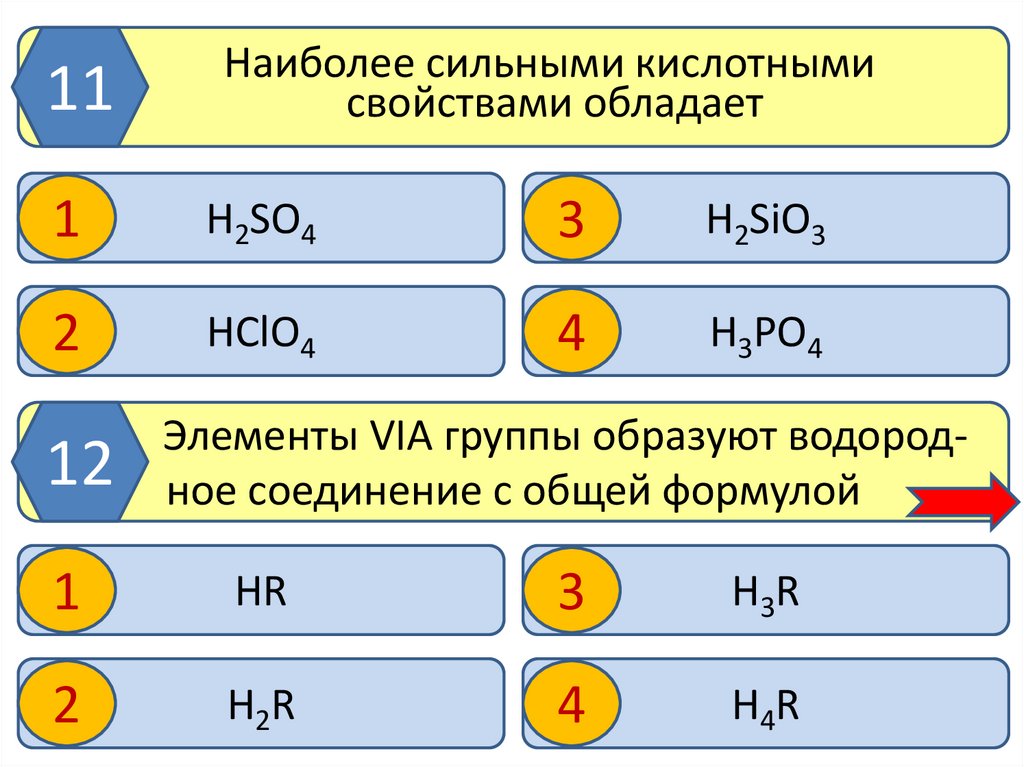
11Наиболее сильными кислотными
свойствами обладает
1
H2SO4
3
H2SiO3
2
HClO4
4
H3PO4
12
Элементы VIА группы образуют водородное соединение с общей формулой
1
HR
3
H3R
2
H2R
4
H4R
8.
131
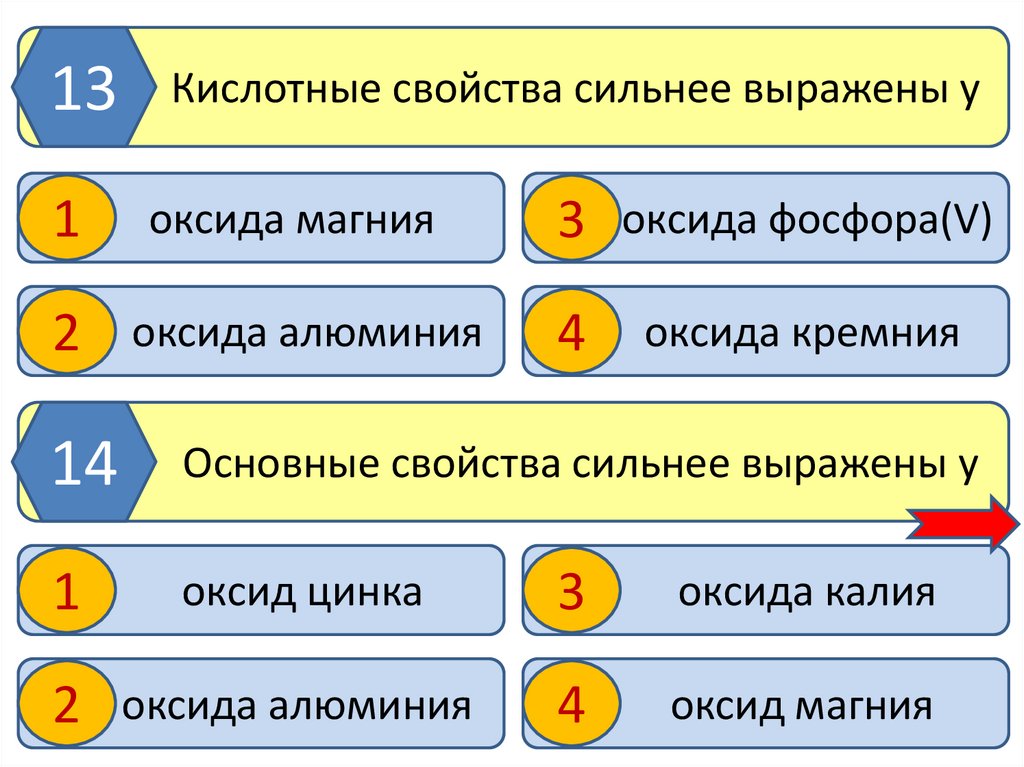
Кислотные свойства сильнее выражены у
оксида магния
2 оксида алюминия
3 оксида фосфора(V)
4
оксида кремния
14
Основные свойства сильнее выражены у
1
оксид цинка
2 оксида алюминия
3
оксида калия
4
оксид магния
9.
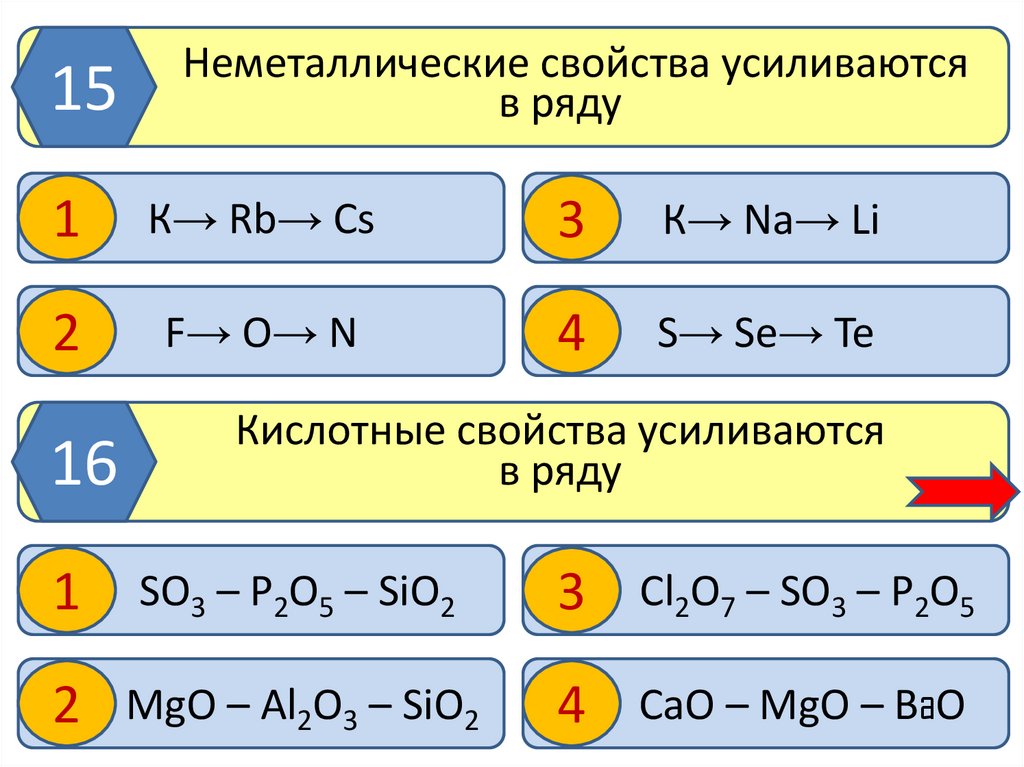
15Неметаллические свойства усиливаются
в ряду
1
К→ Rb→ Cs
3
К→ Na→ Li
2
F→ O→ N
4
S→ Se→ Te
16
1
Кислотные свойства усиливаются
в ряду
SO3 – P2O5 – SiO2
2 MgO – Al2O3 – SiO2
3 Cl2O7 – SO3 – P2O5
4 СaO – MgO – ВaO
10.
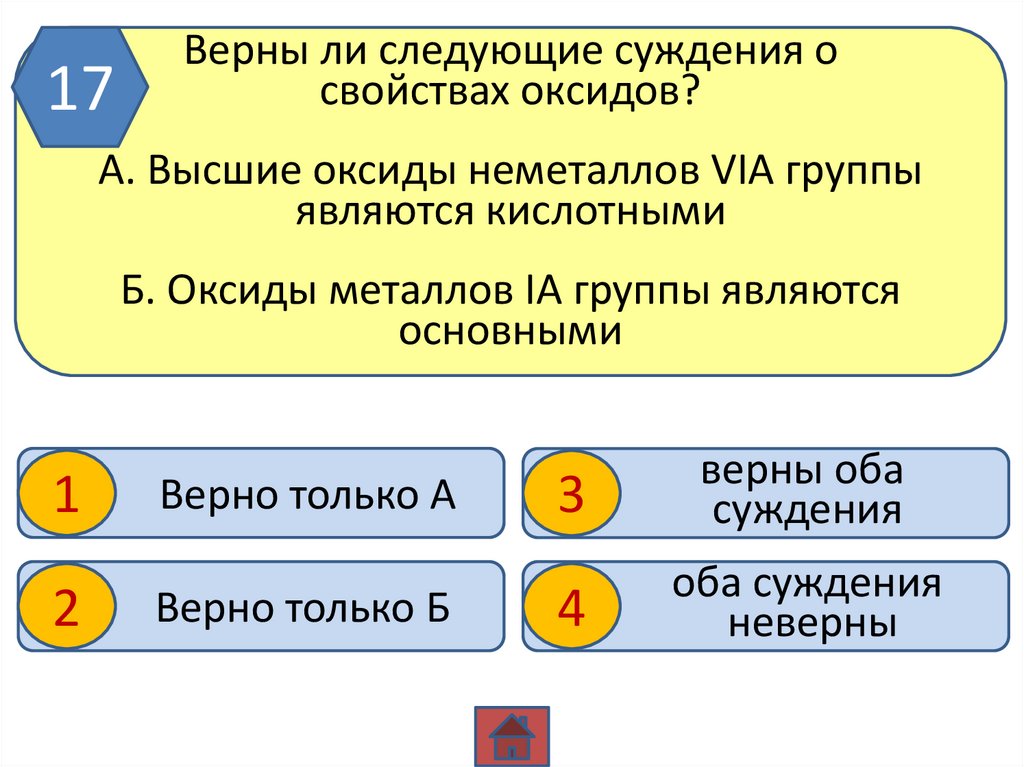
17Верны ли следующие суждения о
свойствах оксидов?
А. Высшие оксиды неметаллов VIА группы
являются кислотными
Б. Оксиды металлов IA группы являются
основными
1
2
Верно только А
Верно только Б
3
верны оба
суждения
4
оба суждения
неверны



 Химия
Химия